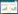文章信息
- 程启明, 黄青, 刘英杰, 廖祯妮
- CHENG Qi-ming, HUANG Qing, LIU Ying-jie, LIAO Zhen-ni
- 花生壳与花生壳生物炭对镉离子吸附性能研究
- Adsorption of Cadmium(Ⅱ) on Peanut Shell and Its Biochar
- 农业环境科学学报, 2014, 33(10): 2022-2029
- Journal of Agro-Environment Science, 2014, 33(10): 2022-2029
- http://dx.doi.org/10.11654/jaes.2014.10.020
-
文章历史
- 收稿日期:2014-5-9
2. 同济大学环境科学与工程学院, 上海 200092;
3. 广西大学农学院, 南宁 530004
2. College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China;
3. Guangxi University, Nanning 530004, China
镉是一种具有金属光泽的非典型过渡性重金属,镉污染主要源于矿山开采、化工、电镀等行业的“三废”,通过水和食物链进入生物系统逐级放大进而对相关生物甚至人造成难以逆转的伤害。镉的生物蓄积性强、毒性持久、具有致畸、致癌、致突变(“三致”)作用;摄入过量的镉通常导致肝、肾、骨、睾丸、脑屏障等免疫系统、心血管系统、中枢神经系统损伤,进而引发记忆力衰退、智力低下以及其他多种疾病[1,2].然而,通常镉污染水体治理主要基于物理或化学原理采用如离子交换法[3]、化学沉淀法[4]、电化学法[5]、反渗透法[6]、膜分离法[7]等,这些方法通常存在成本高或适用范围窄,或容易造成二次污染等问题。
近年来,生物质及生物质基高性能吸附材料用于废水的处理成为国内外研究的热点。由于生物质基材料来源广泛、品种多、成本低,吸附设备简单易操作、见效快、吸附量大,尤其适宜低浓度重金属废水的处理[8,9],近年已有不少利用工农业生物质废弃物或其改性材料进行相关的开发研究,如稻秆[10]、茶叶[11]、改性豆杆[12]、改性玉米芯[13]、改性稻壳[14]等。
花生壳为一种很容易大量获得的廉价工农业生物质废弃物。除少部分花生壳作为粗饲料外,大量的花生壳被当作燃料或是废弃物处置,造成极大的资源浪费。有学者[15,16,17,18]对花生壳或花生壳生物质基作为吸附材料处理废水开展过探讨,但由于吸附容量小或花生壳改性材料成本较高,实际推广应用很少。然而重金属离子废水的治理一直期待吸附容量更大以及成本更低的吸附材料,在重金属废水中的应用范围及其机理还有待进一步研究[19].因此,本研究通过简单经济高效的改性方式获得性能优良的花生壳生物质基吸附材料,并进一步全面及定量化地研究花生壳与花生壳生物炭对废水中Cd2+的吸附性能,探究其吸附作用机理,从反应时间、吸附材料剂量、pH值、吸附质Cd2+浓度的响应等方面,通过模型拟合、场发扫描电镜(SEM)、傅里叶红外(FTIR)和比表面积分析对其吸附机理进行探讨,以期为工农业生物质基废弃物材料的资源高值化利用提供参考或借鉴,同时为Cd污染水体与场地的治理或修复提供一种备选方案。 1 材料与方法 1.1 供试材料
花生壳购自厦门本地花生油加工厂。将花生壳用超纯水清洗3次,于80 ℃烘箱中烘干,用中药粉碎机粉碎过10目尼龙网筛,得到灰黄色颗粒状花生壳粉末(PS)备用。另外,将足够的花生壳置于马沸炉中,通氮气20 min,然后以20 ℃·min-1的速率升温至500 ℃,于500 ℃厌氧条件下保持4 h;待碳化结束自然冷却至室温,制得花生壳生物炭,将其粉碎过10目筛后得花生壳生物质基改性吸附材料(PSB)备用。 1.2 供试试剂
用Cd(NO3)2与2%的稀硝酸溶液配制成10 g·L-1 Cd2+储备液,4 ℃保存备用;将储备液逐级稀释成不同浓度的Cd2+工作溶液浓度。Cd(NO3)2、NaOH、36%的HCl为国药集团分析纯;68%的HNO3为德国Merck公司优级纯,所有试剂配置用水均为 Mili-Q 18.0 MΩ超纯水。 1.3 实验仪器
安捷伦7500C型电感耦合等离子体发射质谱仪(ICP-MS),M6型原子吸收光谱仪(AAS),Thermo Scientific Nicolet IS10傅立叶变换红外光谱仪(FTIR),日立S-4800型场发射扫描电子显微镜(SEM),美国ASAP 2020比表面积与孔隙度吸附仪;超纯水系统,电子天平,高速中药粉碎机,PB-10型pH计,恒温鼓风干燥箱,振荡培养箱。 1.4 实验设计 1.4.1 时间对吸附效果影响分析
分别称取0.2 g PS和PSB,置于100 mL离心管中,加入pH为5.0浓度为200 mg·L-1的Cd2+溶液50 mL,于室温条件下在振荡器中以200 r·min-1分别振荡10、20、40、60、90、120、180、360、720、1440、2880、5760 min后过滤,每个梯度3个平行。 1.4.2 吸附剂用量对去除效率分析
分别称取0.1、0.2、0.5、0.8、1.0、2.0、5.0 g PS和PSB,置于100 mL离心管中,加入pH为5.0浓度为200 mg·L-1的Cd2+溶液50 mL,于室温条件下在振荡器中以200 r·min-1振荡24 h后过滤,每个梯度3个平行。 1.4.3 pH值对吸附效率影响分析
分别称取0.2 g制备好的PS和PSB,置于100 mL离心管中,加入pH分别为1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0浓度为200 mg·L-1的Cd2+溶液50 mL,于室温条件下在振荡器中以200 r·min-1振荡24 h后过滤,每个梯度3个平行。 1.4.4 吸附等温实验
分别称取0.2 g PS和PSB,置于100 mL离心管中,加入pH为5.0浓度分别为10、20、50、100、200、500、800 mg·L-1的Cd2+溶液50 mL,于室温条件下在振荡器中以200 r·min-1振荡24 h后过滤,每个梯度3个平行。 1.4.5 镉离子检测
将经过PS和PSB吸附前后的Cd2+溶液过滤,用AAS或ICP-MS测定溶液中Cd2+的浓度。 1.4.6 吸附材料表面结构与吸附基团分析
将吸附前后的PS和PSB经恒温干燥后,均匀粘在含导电胶的样品台上,喷金处理后使用扫描电镜进行扫描,对比二者表面的微观结构差异;同时,对干燥吸附前后的PS和PSB采用KBr压片法进行FTIR光谱分析(波数为4000~500 cm-1);最后,将干燥的PS和PSB利用ASAP 2020比表面积与孔隙度吸附仪分析其比表面积。 1.5 数据处理 1.5.1 吸附数值计算
实验数据应用Office 2007和SigmaPlot 10.0 进行分析及图表处理。 吸附材料的吸附效果分别用去除效率和吸附量来衡量,其计算公式如下:
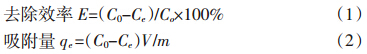
基于吸附学科应用广泛的单分子吸附Langmuir模型与多分子层吸附Freundlich模型对PS和PSB 材料的等温吸附过程分别进行拟合分析,以无量纲参数分离因子来分析PS与PSB 材料的吸附性能,其公式如下:
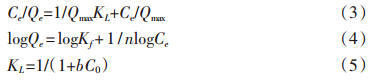
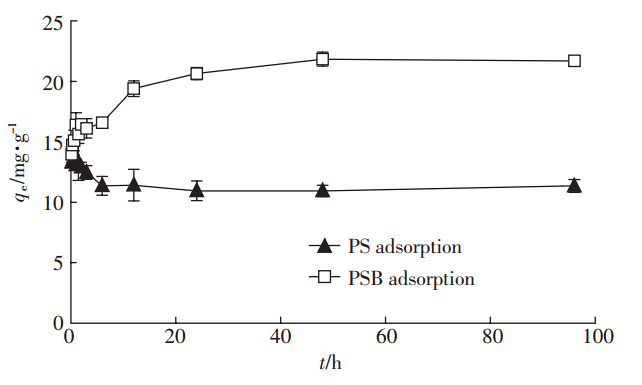
PSB在吸附48 h达到最高21.84 mg·g-1,在吸附10 min时其吸附量为13.97 mg·g-1,为最大吸附量的63.96%,吸附12 h达到最大吸附量的88.83%,吸附24 h达到最大吸附量的94.51%,吸附96 h比48 h略有下降,即PSB随着吸附时间延长而增加,最后趋于稳定;PS则随着吸附时间的增加吸附量则逐步下降,PS最大吸附量为13.59 mg·g-1,表明PSB对于溶液中Cd2+的去除能力比PS要强1.6倍(图 1).推测PS吸附这种情况是表面的物理化学吸附过程,在吸附初期,PS表面的酚羟基、氨基等与水溶液中的Cd2+离子具有较好的交换、结合能力,交换结合位点较多,PS吸附处于动态吸附的正向吸附;随着时间的推移,正向吸附速率减小,同时PS表面带负电基团如-C=O、-CHO等与Cd2+结合较弱,在后期随着被交换下来的H+增多,导致原来弱吸附的Cd2+逐渐被解吸下来。因此,PS随着时间的延长吸附量下降,直到解吸速率与吸附速率相等即达到动态平衡。李光林等[20]研究认为胡敏酸在特定时间吸附量达最大后有所下降,是由于反应初期Cd2+与H+竞争结合相同位点,溶液中H+浓度处于上升,直至最后趋于稳定与本研究结果一致。PSB随时间延长吸附量逐渐升高并于12 h开始稳定,推测PSB吸附机理与PS一样是表面的物理化学吸附,24 h后吸附容量逐步升高是由于Cd2+从表面进入到微孔中,Cd2+在其中移动较慢,吸附容量相应地随时间缓慢增加直至饱和。
|
| 图 1 吸附时间对Cd2+吸附效果的影响 Figure 1 Adsorption of Cd2+ as function of time |
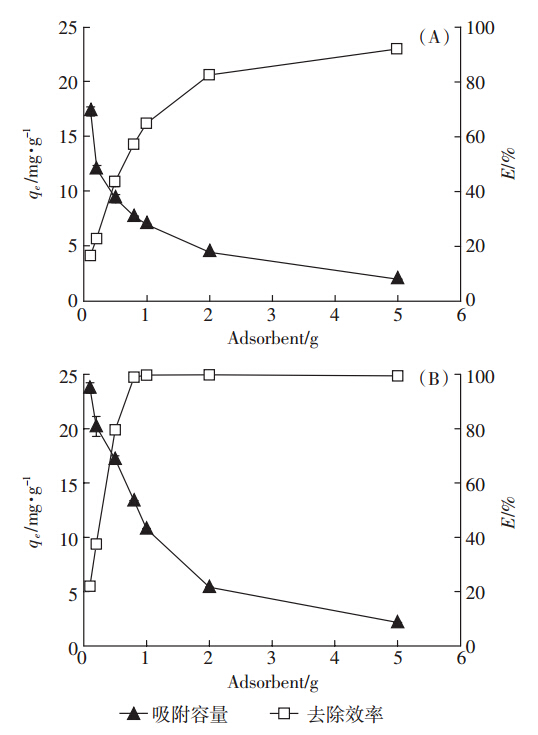
PS在实验剂量为100 mg·mL-1时对溶液中Cd2+的去除效率为91.83%;PSB剂量为16 mg·mL-1时去除效率为98.96%,PSB剂量在40 mg·mL-1去除效率为99.85%,即可将200 mg·L-1的镉离子溶液降低到0.3 mg·L-1(图 2). 去除效率随着PS和PSB吸附剂量增加而上升,推测是源于吸附剂量的增加总比表面积和总官能团数的增加所致。实验结果还显示,吸附材料吸附容量大时对单位体积Cd2+溶液中去除效率较低,去除效率较高时吸附材料的吸附容量相对较小。丁洋等[21]在研究板栗内皮对镉的去除时观测到与本研究类似的结论。最后结果显示,PSB比PS的吸附去除效率更高,推测除PSB比PS在总比表面积和总官能团数更大外,还在于PSB改性后呈碱性,部分[OH]-与之发生了沉淀反应,进而促进了溶液中Cd2+的去除。
|
|
A-花生壳;B-花生壳生物炭 A-PS; B-PSB 图 2 吸附剂投加量对Cd2+吸附的影响 Figure 2 Adsorption of Cd2+ as function of adsorbent doses |
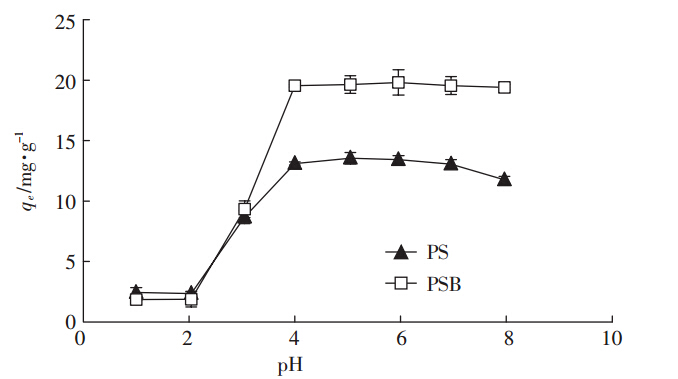
pH处于1.0~2.0之间时,吸附量与pH值无关,PS与PSB对Cd2+吸附差异不明显;当pH处于2.0~4.0时,随着初始溶液pH的增加吸附效率急剧增加;pH为4.0~8.0时,吸附去除效率几乎无变化,表明该吸附反应适应的pH范围较宽(图 3).推测在低pH条件下,溶液中大量存在的H+竞争有限的结合位点,使得吸附量减少;随着pH上升,H+量减少,吸附剂表面结合位点暴露,负电荷密度增大,吸附容量也随之增加;当pH>8.0时,基于溶液中[OH]-会与Cd2+反应产生沉淀而去除一部分,故在本研究中未进行相关研究。在初始浓度、生物量、时间等其他条件不变的情况下,溶液pH对PS和PSB吸附去除Cd2+有较大影响,因此溶液pH值是影响PS和PSB吸附Cd2+的最重要因素之一。李力等[22]与谭光群等[23]分别在对小麦秸秆和玉米秸秆的Cd2+吸附性能中观测到类似的趋势,他们认为pH升高,溶液中H+含量减少,H+竞争作用减弱,使更多带负电荷的官能团暴露出来而有利于金属离子结合。即表明PS和PSB吸附Cd2+的最佳pH在4.0~8.0之间,故本研究中后续实验pH控制为5.0.
|
| 图 3 溶液初始pH值对吸附的影响 Figure 3 Effects of initial pH values on Cd2+ adsorption |
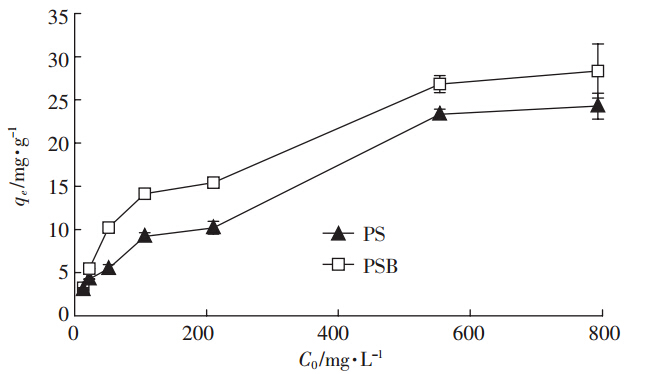
PS与PSB吸附容量随溶液中Cd2+浓度的升高而增加(图 4).初始浓度为10 mg·L-1时,PS的去除效率为93.33%,PSB的去除效率为99.51%,Cd2+的浓度达到800 mg·L-1时,PS的去除效率为12.46%,PSB的去除效率为14.43%,表明溶液中Cd2+浓度低时去除效率较高,Cd2+浓度高时去除效率降低,PS与PSB适合低浓度Cd2+离子的吸附去除。张再利等[16]在Pb2+、Cu2+、Ni2+ 等金属离子去除研究中得到与本研究相似的结论。
|
| (A)花生壳;(B)花生壳生物炭 图 5 Langmir吸附等温线 Figure 5 Langmuir isotherm plot of Cd2+ adsorption |
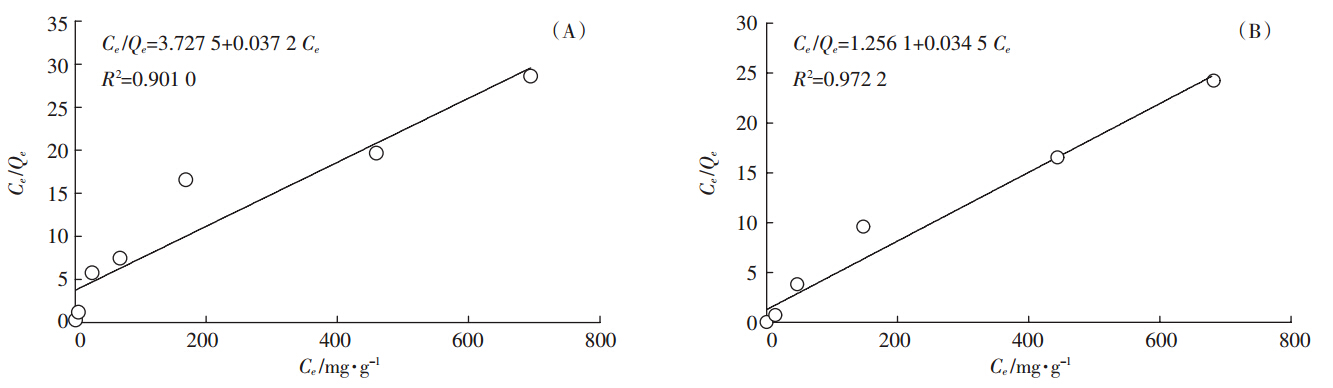
采用Langmuir吸附模型和Freundlich模型[24,25,26]对Cd2+吸附平衡浓度与PS或PSB的吸附容量拟合结果表明:Langmuir和Freundlich模型均能较好地表征拟合PS与PSB对Cd2+吸附性能,对Cd2+的最大吸附量分别为26.88、28.99 mg·g-1(表 1及图 5、6),PS与PSB能较好地吸附Cd2+.在不同材料间,当n值接近时,Kf值与吸附剂吸附容量正相关,PSB的Kf值大于PS,表明PSB对Cd2+吸附容量大于PS,与本实验结果一致。
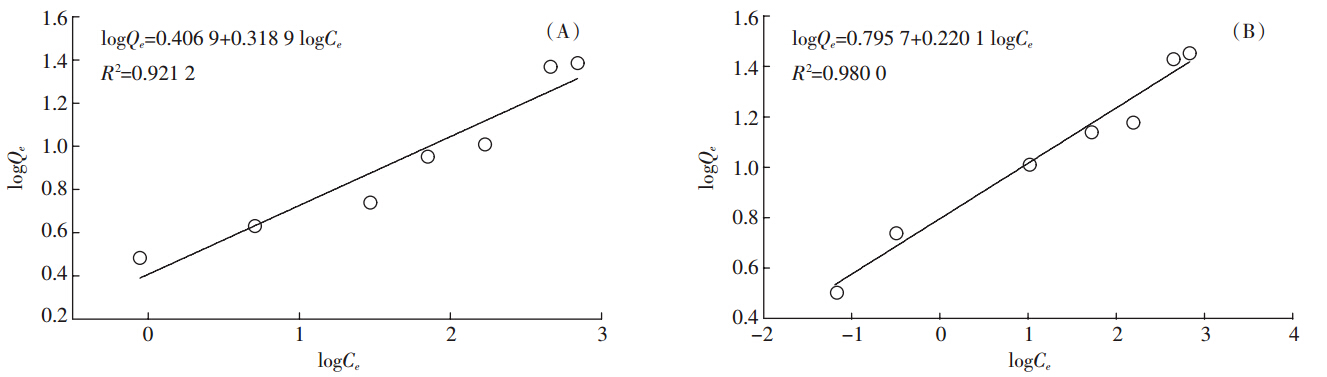
|
| (A)花生壳;(B)花生壳生物炭 图 6 Freundlich吸附等温线 Figure 6 Freundlich isotherm plot of Cd2+ adsorption |
Freundlich模型的R2与Langmuir模型的R2相比略高,表明Freundlich等温线方程模型相当或略优于Langmuir等温线方程模型,即PS与PSB存在着多分子层吸附,但是Langmuir模型的Qmax与实验值更接近(图 4).通过与此前报道的生物质基吸附剂对比发现,PS与PSB的吸附容量远高于板栗内皮、稻壳、稻壳生物炭、HNO3(或NaOH)改性稻壳、甲醛改性豆壳、吡啶改性豆壳、香蕉皮(表 2).
|
| 图 4 Cd2+初始浓度对吸附剂的影响 Figure 4 Effects of initial Cd2+ concentrations on adsorption of Cd2+ |
根据无量纲参数分离因子KL进行分析[16].PS和PSB的KL均在0~1之间,表明PS和PSB对Cd2+有较好的吸附性; PS的KL为0.0100,表明PS的大多吸附位点为不可逆吸附;而PSB的KL为0.7961,表明为接近线性的可逆吸附,且PSB的吸附性能优于PS. 2.5 场发射扫描电镜分析
通过SEM观察表明,PS和PSB的微观结构在吸附Cd2+前表面平整,颗粒附着物少;吸附后PS与PSB材料表面聚集着众多颗粒附着物,大量颗粒物或粉状物聚集在表层(图 7).王宁等[32]研究认为生物炭吸附能力优于其母体材料与本文的现象一致。丁洋等[21]研究板栗内皮对镉的吸附机理,认为生物质材料或生物炭对重金属离子的吸附能力与材料疏水性、比表面积、孔隙结构、表面官能团组成等相关。

|
|
花生壳(A-吸附前;B-吸附后);花生壳生物炭(C-吸附前;D-吸附后) PS(A-Before; B-After); PSB(C-Before; D-After) 图 7 吸附剂对Cd2+吸附前后场发扫描电镜图(×20 000倍) Figure 7 SEM images of adsorbents before and after Cd2+ adsorption(×20 000) |
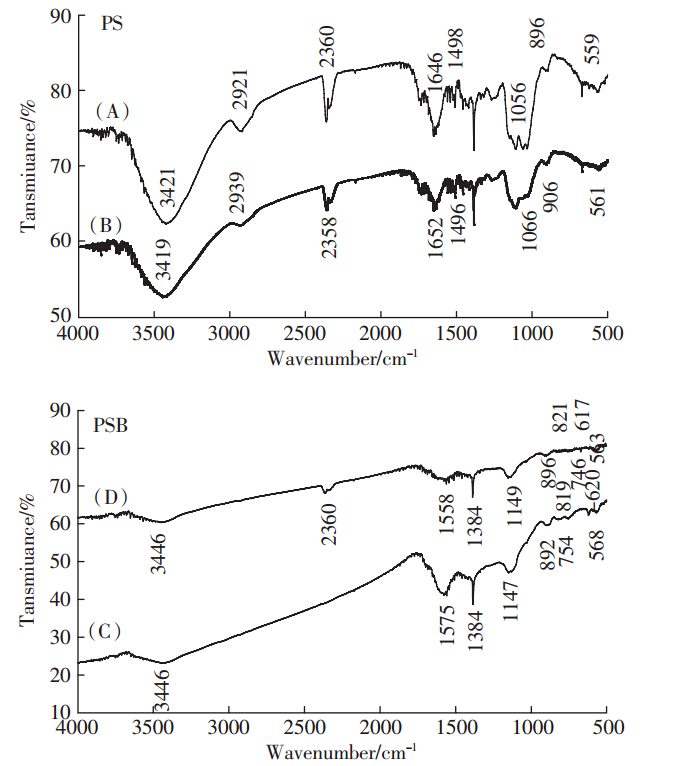
PS和PSB吸附前后材料经FTIR分析结果显示,有多处谱带发生明显位移,进一步分析显示多种官能团参与了Cd2+的络合反应。PS吸附Cd2+后谱带发生较为明显位移的主要有2921 cm-1移到2939 cm-1、1646 cm-1移到1652 cm-1、1056 cm-1移到1066 cm-1和896 cm-1移到906 cm-1;与之对应的烷烃和醛类中的-C-H与-CHO基团、 -C=O基、-P=O基。PSB吸附Cd2+后有多处谱带发生位移,较为明显的2360 cm-1峰出现有双键、三键类中的-C=C-、-C≡C-和-C≡N的伸缩振动,-N-H的伸缩振动峰由1575 cm-1移到1558 cm-1,-P=O的反对称伸缩振动峰由892 cm-1移到896 cm-1,醇、酚类和卤素类伸缩振动峰由754 cm-1移到746 cm-1,620 cm-1移到617 cm-1,568 cm-1移到563 cm-1(图 8).丁洋等[21]研究板栗内皮得出的官能团变化与本文观测到的PS结果类似,李力等[22]在研究玉米秸秆生物炭对镉的吸附前后官能团变化与本文的PSB结果类似,即Cd2+分别与PS材料中的-CHO、-C=O、-OH和-P=O官能团络合,PSB吸附镉主要与-C=C-、-C≡C-和-C≡N、-OH、-R等官能团络合相关。通常-CHO、-C=O、-OH和-P=O相对于C=C-、-C≡C-和-C≡N、-OH、-R等官能团络合能力要强,而与本文实验结果PSB比PS 的去除效率和吸附容量都要高似乎相矛盾。我们推测这种情况除PSB比PS比表面积大与PSB材料呈碱性之外,可能还与单位质量材料表面的官能团密度相关,即影响生物质或生物质基材料对重金属离子的吸附量取决于材料的官能团种类外,还与官能团的密度、比表面积等综合因素相关。
|
|
花生壳(A-吸附前;B-吸附后);花生壳生物炭(C-吸附前;D-吸附后) PS(A-Before; B-After); PSB(C-Before; D-After) 图 8 吸附剂吸附镉前后的红外光谱图 Figure 8 FTIR spectra of adsorbents before(b)and after(a) Cd2+ adsorption |
(1)PS和PSB对Cd2+有良好的吸附去除性能。最佳吸附去除的pH范围为4.0~8.0;在pH为5.0、Cd2+溶液浓度为10 mg·L-1、吸附剂为4 mg·mL-1时,PS的去除效率为93.33%,PSB的去除效率为99.51%.等温吸附模型拟合结果表明,最大理论吸附量分别为26.88、28.99 mg·g-1.
(2)Freundlich吸附模型与Langmuir吸附模型均能较好地描述PS和PSB对Cd2+的等温吸附过程。SEM电镜扫描和FTIR图谱分析表明,PS和PSB对镉的吸附主要为多分子层的表层络合吸附去除,PS参与络合反应的主要官能团为-CHO、-C=O、-OH、 -P=O,PSB参与络合反应的主要官能团为-C=C-、-C≡C-、-C≡N和-OH等。
| [1] | Nawrot T S, Staessen J A, Roels H A, et al. Cadmium exposure in the population:From health risks to strategies of prevention[J]. Biometals, 2010, 23 (5):769-782. |
| [2] | Satarug S, Baker J R, Urbenjapol S, et al. A global perspective on cadmium pollution and toxicity in non-occupationally exposed population[J]. Toxicology Letters, 2003, 137(1):65-83. |
| [3] | 尔丽珠, 秦晓丹, 张惠源. 离子交换法移动处理重金属废水[J]. 电镀与精饰, 2007, 29(2):48-51. ER Li-zhu, QIN Xiao-dan, ZHANG Hui-yuan. Mobile treatment of waste water containing heavy metal by ion exchange method[J]. Plating & Finishing, 2007, 29 (2):48-51. |
| [4] | 郭燕妮, 方增坤, 胡杰华, 等. 化学沉淀法处理含重金属废水的研究进展[J]. 工业水处理, 2012, 31(12):9-13. GUO Yan-ni, FANG Zeng-kun, HU Jie-hua, et al. Research development of treating wastewater containing heavy metals by chemical precipitation process[J]. Industrial Water Treatment, 2012, 31(12):9-13. |
| [5] | 黄其祥, 胡衍华, 徐凑友, 等. 电镀废水处理技术研究现状及展望[J]. 广东化工, 2010, 4(37):128-130. HUANG Qi-xiang, HU Yan-hua, XU Cou-you, et al. Electroplating wastewater treatment technology research situation and prospect[J]. Guangdong Chemical Industry, 2010, 4(37):128-130. |
| [6] | 黄万抚, 徐 洁. 反渗透法处理矿山含重金属离子废水的试验研究[J]. 矿业工程, 2005, 3(4):36-37. HUANG Wan-fu, XU Jie. Experimental research of treating exmine wastewater containing heavy metal ions by means of hyperfiltration[J]. Mining Engineering, 2005, 3(4):36-37. |
| [7] | 徐德志, 相 波, 邵建颖, 等. 膜技术在工业废水处理中的应用研究进展[J]. 工业水处理, 2006, 26(4):1-4. XU De-zhi, XIANG Bo, SHAO Jian-ying, et al. Application of membrane technology to the industrial wastewater treatment[J]. Industrial Water Treatment, 2006, 26 (4):1-4. |
| [8] | Li D, Ke Y, Meng F. Research progress on heavy metal pollution control and remediation[J]. Research Journal of Chemistry and Environment, 2013, 17(2):76 -83. |
| [9] | Shao H, Chu L, Xu G, et al. Progress in phytoremediating heavy-metal contaminated soils[M]//Detoxification of Heavy Metals. Springer Berlin Heidelberg, 2011:73-90. |
| [10] | Rocha C G, Zaia D A M, Alfaya R V S, et al. Use of rice straw as biosorbent for removal of Cu(Ⅱ), Zn(Ⅱ), Cd(Ⅱ) and Hg(Ⅱ) ions in industrial effluents[J]. Journal of Hazardous Materials, 2009, 166(1):383-388. |
| [11] | Ahluwalia S S, Goyal D. Removal of heavy metals by waste tea leaves from aqueous solution[J]. Engineering in life Sciences, 2005, 5(2):158-162. |
| [12] | Zhu B, Fan T, Zhang D. Adsorption of copper ions from aqueous solution by citric acid modified soybean straw[J]. Journal of Hazardous Materials, 2008, 153 (1):300-308. |
| [13] | Leyva-Ramos R, Bernal-Jacome L A, Acosta-Rodriguez I. Adsorption of cadmium(Ⅱ) from aqueous solution on natural and oxidized corncob[J]. Separation and Purification Technology, 2005, 45(1):41-49. |
| [14] | Luo X, Deng Z, Lin X, et al. Fixed-bed column study for Cu2+ removal from solution using expanding rice husk[J]. Journal of Hazardous Materials, 2011, 187 (1):182-189. |
| [15] | 黄 翔, 宗 浩, 陈文祥, 等. 花生壳对水溶液中铜离子的吸附特性[J]. 四川师范大学学报:自然科学版, 2007, 30(3):380-383. HUANG Xiang, ZONG Hao, CHEN Wen-xiang, et al. Biosorption of copper(Ⅱ) in aqueons solution by peanut-shuck[J]. Journal of Sichuan Normal University(Natural Science), 2007, 30(3):380-383. |
| [16] | 张再利, 况 群, 贾晓珊. 花生壳吸附Pb2+, Cu2+, Cr3+, Cd2+, Ni2+的动力学和热力学研究[J]. 生态环境学报, 2010, 19(12):2973-2977. ZHANG Zai-li, KUANG Qun, JIA Xiao-shan. Study on the kinetics and thermodynamics of Pb2+, Cu2+, Cr3+, Cd2+, Ni2+ adsorption onto peanut hull[J]. Ecology and Environment, 2010, 19(12):2973-2977. |
| [17] | Xiang G, Huang Y, Luo Y. Solid phase extraction of trace cadmium and lead in food samples using modified peanut shell prior to determination by flame atomic absorption spectrometry[J]. Microchimica Acta, 2009, 165(1-2):237-242. |
| [18] | Li Q, Zhai J, Zhang W, et al. Kinetic studies of adsorption of Pb(Ⅱ), Cr(Ⅲ) and Cu(Ⅱ) from aqueous solution by sawdust and modified peanut husk[J]. Journal of Hazardous Materials, 2007, 141(1):163-167. |
| [19] | Wilson K, Yang H, Seo C W, et al. Select metal adsorption by activated carbon made from peanut shells[J]. Bioresource Technology, 2006, 97(18):2266- 2270. |
| [20] | 李光林, 魏世强, 青长乐. 镉在胡敏酸上的吸附动力学和热力学研究[J]. 土壤学报, 2004, 41(1):74-80. LI Guang-lin, WEI Shi-qiang, QING Chang-le. Kinetics and thermodynamics of cadmium adsorption on humic acid[J]. Acta Pedologica Sinica, 2004, 41(1):74-80. |
| [21] | 丁 洋, 靖德兵, 周连碧, 等. 板栗内皮对水溶液中镉的吸附研究[J]. 环境科学学报, 2011, 31(9):1933-1941. DING Yang, JING De-bing, ZHOU Lian-bi, et al. The adsorption of aquatic cadmium(Ⅱ) by chestnut inner shell[J]. Acta Scientiae Circumstantiae, 2011, 31 (9):1933-1941. |
| [22] | 李 力, 陆宇超, 刘 娅, 等. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2012, 31(11):2277-2283. LI Li, LU Yu-chao, LIU Ya, et al. Adsorption mechanisms of cadmium(Ⅱ) on biochars derived from corn straw[J]. Journal of Agro-Environment Science, 2012, 31 (11):2277-2283. |
| [23] | 谭光群, 袁红雁, 刘 勇, 等. 小麦秸秆对水中Pb2+和Cd2+的吸附特性[J]. 环境科学, 2011, 32(8):2298-2304. TAN Guang-qun, YUAN Hong-yan, LIU Yong, et al. Characteristics of Pb2+ and Cd2+ sorption in aqueous solution by wheat straw[J]. Chinese Journal of Environmental Science, 2011, 32(8):2298-2304. |
| [24] | Li Q, Chai L, Qin W. Cadmium(Ⅱ) adsorption on esterified spent grain:Equilibrium modeling and possible mechanisms[J]. Chemical Engineering Journal, 2012, 197:173-180. |
| [25] | 苏 峰, 罗胜联, 曾光明, 等. 海带对镉的吸附动力学与热力学研究[J]. 环境工程学报, 2009, 3(5):857-860. SU Feng, LUO Sheng-lian, ZENG Guang-ming, et al. Kinetics and thermodynamics of Cd(Ⅱ) biosorption onto Laminaria japonica[J]. Chinese Journal of Environmental Engineering, 2009, 3(5):857-860. |
| [26] | Vargas A M M, Cazetta A L, Kunita M H, et al. Adsorption of methylene blue on activated carbon produced from flamboyant pods(Delonix regia):Study of adsorption isotherms and kinetic models[J]. Chemical Engineering Journal, 2011, 168(2):722-730. |
| [27] | Ding Y, Jing D, Gong H, et al. Biosorption of aquatic cadmium(Ⅱ) by unmodified rice straw[J]. Bioresource technology, 2012, 114:20-25. |
| [28] | Kumar U, Bandyopadhyay M. Sorption of cadmium from aqueous solution using pretreated rice husk[J]. Bioresource technology, 2006, 97(1):104-109. |
| [29] | Rocha C G, Zaia D A M, Alfaya R V S, et al. Use of rice straw as biosorbent for removal of Cu(Ⅱ), Zn(Ⅱ), Cd(Ⅱ) and Hg(Ⅱ) ions in industrial effluents[J]. Journal of Hazardous Materials, 2009, 166(1):383-388. |
| [30] | Adediran G O, Tella A C, Mohammed H A. Adsorption of Pb, Cd, Zn, Cu and Hg ions on formaldehyde and pyridine modified bean husks[J]. Journal of Applied Sciences and Environmental Management, 2007, 11(2):153-158. |
| [31] | Anwar J, Shafique U, Salman M, et al. Removal of Pb(Ⅱ) and Cd(Ⅱ)from water by adsorption on peels of banana[J]. Bioresource Technology, 2010, 101(6 ):1752-1755. |
| [32] | 王 宁, 侯艳伟, 彭静静, 等. 生物炭吸附有机污染物的研究进展[J]. 环境化学, 2012, 31(3):287-295. WANG Ning, HOU Yan-wei, PENG Jing-jing, et al. Research progress on sorption of orgnic contaminants to biochar[J]. Environmental Chemistry, 2012, 31(3):287- 295. |
 2014, Vol. 33
2014, Vol. 33