文章信息
- 吴群, 施艳红, 操海群, 李学德, 花日茂, 汤锋, 岳永德
- WU Qun, SHI Yan-hong, CAO Hai-qun, LI Xue-de, HUA Ri-mao, TANG Feng, YUE Yong-de
- 氯虫苯甲酰胺在水溶液中光解的影响因素研究
- Photodegradation of Chlorantraniliprole in Aqueous Solution
- 农业环境科学学报, 2014, 33(11): 2242-2246
- Journal of Agro-Environment Science, 2014, 33(11): 2242-2246
- http://dx.doi.org/10.11654/jaes.2014.11.024
-
文章历史
- 收稿日期:2014-5-8
2. 安徽农业大学植物保护学院, 安徽省农产品安全重点实验室, 合肥 230036;
3. 国际竹藤中心, 北京 100080
2. School of Plant Protection, Anhui Agricultural University, Key Laboratory of Agri-Food Safety of Anhui Province, Hefei 230036, China;
3. International Centre for Bamboo & Rattan, Beijing 100080, China
化学农药在使用过程中,不可避免地通过多种途径进入水体环境中,危害水生生物安全及人类健康。农药在水环境中的降解主要有生物降解、水解和光化学降解等,其中光化学降解(以下简写为光解)是农药在水环境中降解的重要途径之一,其过程和产物对农药药效、代谢、毒性及环境的影响很大。研究农药在水环境中的光解一直是环境化学及环境毒理学的热点之一[1,2,3],该研究对指导农药的合理使用和探索农药污染环境的修复技术等具有重要的意义[4]。
氯虫苯甲酰胺(Chlorantraniliprole),化学名称为3-溴-N-{4-氯-2-甲基-6-[(甲氨基)羰基]苯基}-1-(3-氯-2-吡啶基)-1-H-吡唑-5-酰胺,是一种高效、低毒和作用机制独特的新型邻甲酰氨基苯甲酰胺类杀虫剂,对危害水稻、果树、蔬菜等作物的大部分鳞翅目、鞘翅目害虫具有快速、长效、广谱的防治作用[5]。目前,国内外有关氯虫苯甲酰胺的研究主要集中在合成工艺、剂型和应用技术方面[6,7,8],而关于其在环境介质中的光解动态的报道较少[9]。作为一种具有良好发展前景的农药,氯虫苯甲酰胺在应用过程中难免会进入水体而造成环境污染和生态效应。本文采用紫外灯作为光源,探索了不同因素对水体中氯虫苯甲酰胺光解的影响,为氯虫苯甲酰胺的正确使用及其在水环境中的安全性提供科学依据。 1 材料与方法 1.1 药品与试剂
氯虫苯甲酰胺标准品(纯度94.5%),Dr. Ehrenstorfer GmbH;乙腈为色谱纯;冰乙酸、氢氧化钠、磷酸、硼酸、30%过氧化氢等均为分析纯;超纯水(由实验室超纯水系统制得),自来水(取自实验室自来水管网出水口),池塘水(采自安徽农业大学校园内池塘),河水(采自合肥地区董浦水库),湖水(采自巢湖水质检测点),所有水样(除超纯水外)在试验前用孔径0.22 μm滤膜过滤灭菌,各水样的理化性质见表 1。
试验使用仪器有Agilent1200型高效液相色谱仪配可变波长紫外检测器(美国安捷伦科技有限公司),AUX120型电子分析天平(日本岛津公司),UV-1800型紫外分光光度计(日本岛津公司),TES-1332型照度计(泰仕电子工业股份有限公司),AYJ1-1002-U型超纯水系统(重庆艾科浦),PHS-25型酸度计(上海雷磁仪器厂),78-1型磁力搅拌器(江苏姜堰市分析仪器厂),KQ5200 型超声波清洗器(江苏昆山仪器有限公司),DDS-307型电导率仪(上海雷磁仪器厂),COD-507型化学需氧量分析仪(上海雷磁仪器厂),石英试管(可见光透过率≥93%,紫外光谱区透过率≥80%)等。试验光源为20 W紫外灯,光强180~240 lx。 1.3 试验方法 1.3.1 母液及缓冲溶液的配制
以乙腈为溶剂将氯虫苯甲酰胺配成700 mg·L-1的标准母液,以超纯水为溶剂将30% H2O2试剂配成 9.7 mmoL·L -1的母液;参照文献[10]的方法,用超纯水配制0.2 mol·L-1氢氧化钠溶液以及含0.04 mol·L-1冰乙酸、0.04 mol·L-1磷酸、0.04 mol·L-1硼酸的储备液,使用时将氢氧化钠溶液与储备液以不同比例混合配制成pH为5、7、9的缓冲溶液。 1.3.2 氯虫苯甲酰胺在水溶液中的光解试验 1.3.2.1 氯虫苯甲酰胺不同初始浓度的影响
用超纯水分别配制不同浓度氯虫苯甲酰胺的光解反应液,经磁力搅拌器充分混匀。移取反应液15 mL于具塞石英试管中,置于紫外灯下照光,照光时石英试管距光源15 cm,控制反应温度为(25±1)℃,同时以锡箔纸包裹的处理为黑暗对照。每处理设3次重复,不同时间间隔取样,样品经0.45 μm滤膜过滤后用高效液相色谱仪直接进样分析。 1.3.2.2 pH和水质对氯虫苯甲酰胺光解的影响
光解试验操作同1.3.2.1。用不同pH值的缓冲溶液和制备好的超纯水、自来水、塘水、河水和湖水,分别配制浓度为0.7 mg·L-1的氯虫苯甲酰胺光解反应液。在常温下避光保存70 h,不同时间间隔分别取样,样品经0.45 μm滤膜过滤后用高效液相色谱仪直接进样分析,探讨氯虫苯甲酰胺在不同pH值缓冲溶液中的储存稳定性。 1.3.2.3 H2O2对氯虫苯甲酰胺光解的影响
用超纯水分别配制含不同浓度过氧化氢和0.7 mg·L-1氯虫苯甲酰胺的光解反应液。光解试验操作同1.3.2.1。 1.4 分析条件
Agilent1200型高效液相色谱仪,ZORBA-ODS色谱柱(250 mm×4.6 mm,5 μm),可变波长紫外检测器(VWD),检测波长230 nm,流动相为乙腈/水=55/45(体积比),流速1.0 mL·min-1,柱温40 ℃,进样量20 μL。此条件下氯虫苯甲酰胺的保留时间为6.80 min左右。
水中添加0.02、0.7、5 mg·L-1氯虫苯甲酰胺母液时,其平均回收率分别为99.6%、100.1%、100.7%,变异系数分别为0.12%、0.25%和0.31%。该方法的准确性、精确性均满足农药残留分析的要求。 1.5 统计方法和计算公式
所有试验数据的统计分析均采用唐启义和冯明光[11]的DPS 统计软件,一级动力学方程采用文献[12]的方法。其计算公式如下:
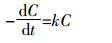
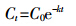
研究结果表明(表 2),在设置的0.3、0.7、1.5、3、5 mg·L-15个不同试验浓度下,水溶液中氯虫苯甲酰胺的光解速率常数与初始浓度呈负相关性,半衰期分别为3.726、4.091、4.485、4.901、5.602 min。郑和辉等、邹雅竹等研究乙草胺、咪鲜胺在水体中的光化学降解也发现了类似规律[13,14]。这可能是由于在光能一定的条件下,增大氯虫苯甲酰胺的初始浓度,水溶液中氯虫苯甲酰胺分子数增多,其对光子的吸收竞争增强,单位分子平均接受的光能减少,从而发生降解的机会相应减少,光解速率降低。
 |
为研究氯虫苯甲酰胺在不同pH缓冲溶液中的光解,首先考察其在黑暗条件下的水解情况。结果表明,室温下放置70 h后,氯虫苯甲酰胺在pH5和pH7的缓冲溶液中没有降解,在pH9的碱性溶液中的降解率不超过10%。由此可知在试验光照期间,氯虫苯甲酰胺在三种不同pH的缓冲溶液中是相对稳定的,可以排除pH影响其水解的可能性。
不同缓冲溶液中氯虫苯甲酰胺的光化学降解试验结果表明(表 3),在pH9的缓冲溶液中,氯虫苯甲酰胺光解速率最慢,其光解半衰期为4.559 min,而在pH5和pH7的缓冲溶液中分别为4.127、4.177 min。有报道认为不同缓冲溶液的吸收光谱差异是造成农药光解动态变化的原因之一[15]。但对于本实验来说,通过紫外分光光度计对试验溶液进行了吸收光谱扫描(图 1),其吸收光谱基本一致,氯虫苯甲酰胺的最大吸收峰均在201 nm左右,MacDonald通过用同位素14C分别标记苯甲酰胺和吡唑上的羰基追踪实验发现在氙灯的照射下,氯虫苯甲酰胺在pH7的TRIS-马来酸缓冲液中主要有三种光解产物[6]。因此,推测导致本试验不同缓冲溶液中氯虫苯甲酰胺光解速率差异可能与其解离方式以及其对应的光解速率常数不同有关,有待进一步研究。
 |

|
| 图 1 氯虫苯甲酰胺在不同pH中的紫外-可见吸收光谱 Figure 1 UV-Visible spectra of chlorantraniliprole in different pH buffer solution |
从表 4可以看出,氯虫苯甲酰胺在5种不同类型水中的光解速率为超纯水>自来水>池塘水>湖水>河水,光解半衰期分别为3.835、4.239、4.506、4.580、4.592 min。农药在天然水中的光解速度差异与水的理化性质有关[16,17],不同类型水中所含的溶解性物质对光能的吸收与传导,以及对水中其他物质的光化学反应有着不同的影响[18,19]。由表 1可知,超纯水的pH值和电导率最小,其中溶解性物质最少,对光的吸收和传导阻碍作用小,光解表现最快。由于河水等其他水体的pH值较大,且都不同程度地含有一定的离子和可溶性物质,这些物质一方面可能与氯虫苯甲酰胺发生螯合作用,减少氯虫苯甲酰胺参与光化学降解反应的量从而阻碍其光解进程,另一方面在一定波长范围内,对光的吸收和传导产生了遮蔽效应,抑制了氯虫苯甲酰胺在水体中的光解。
从表 5可以看出,在添加不同浓度H2O2的水溶液中,氯虫苯甲酰胺的光解反应明显加快,光解速率比氯虫苯甲酰胺单独光解时快3.11~1.08倍,H2O2对其光敏作用显著。当H2O2的添加浓度小于3.88 mmol·L-1时,氯虫苯甲酰胺的光解速率随着H2O2添加浓度的增高而加快,光解半衰期从4.218 min缩短到1.358 min。但当H2O2添加浓度达到7.76 mmol·L-1时,氯虫苯甲酰胺光解速率反而下降。
H2O2在光辐射下发生光解产生羟基,反应式如下:H2O2+hν→2·OH,·OH可以使有机物氧化分解;同时H2O2本身对·OH也具有捕获能力(·OH+H2O2→H2O2+H2O·)[20,21,22]。从本试验结果来看,H2O2光敏化降解氯虫苯甲酰胺的原因可能在于H2O2光解产生的·OH攻靶标农药分子并使之发生解离,所以H2O2在一定浓度范围内提高了氯虫苯甲酰胺在其水溶液中光解速率。但由于H2O2在光辐射下既可提供羟基又可自身捕获羟基的两面性,使得水溶液中的H2O2非线性促进氯虫苯甲酰胺的光解,即当H2O2浓度达到7.76 mmol·L-1时,H2O2与氯虫苯甲酰胺之间发生了·OH的竞争反应,使氯虫苯甲酰胺的光解速率常数明显减小。 3 结论
(1)相同条件下,氯虫苯甲酰胺的光解速率随自身浓度的升高而减慢。
(2)在试验光照期间,氯虫苯甲酰胺在三种缓冲溶液中是相对稳定的,在碱性条件下比在酸性和中性条件下光解较慢。
(3)不同水质中氯虫苯甲酰胺的光解速率不同,其在超纯水中的降解速率最快,在其他水质中降解速率较慢,造成这种差异性一方面与不同可溶性物质、不同离子的种类与含量有关,另一方面与不同水质的pH有关。
(4)H2O2促进了氯虫苯甲酰胺在其水溶液中的光解,且H2O2的添加浓度对其光解速率影响较大,H2O2浓度在3.88 mmol·L-1以下时,氯虫苯甲酰胺的光解速率随着H2O2添加浓度的增加迅速加快,但当H2O2浓度达到7.78 mmol·L-1时,氯虫苯甲酰胺的光解速率反而下降。本试验结果可为含氯虫苯甲酰胺的农药废水处理提供一定的技术支撑。
| [1] | 汤 锋, 岳永德, 花日茂, 等. 增效磷在液相中的光化学降解研究[J]. 农药学学报, 2000, 2(2):71-76. TANG Feng, YUE Yong-de, HUA Ri-mao, et al. Photodegradation of SV1 in various solvents[J]. Chinese Journal of Pesticide Science, 2000, 2(2):71-76. |
| [2] | 钟明洁, 陈 勇, 胡 春. 水溶液中嗪草酮的光化学行为研究[J]. 环境科学学报, 2009, 29(7):1470-1474. ZHONG Ming-jie, CHEN Yong, HU Chun. Photochemical fate of Metribuzin in aqueous solution under simulated sunlight irradiation[J]. Acta Scientiae Circumstantiae, 2009, 29(7):1470-1474. |
| [3] | 贾 娜, 施海燕, 王鸣华. 2, 4-D丁酯的水解与光解特性研究[J]. 农业环境科学学报, 2011, 30(6):1082-1086. JIA Na, SHI Hai-yan, WANG Ming-hua. Hydrolysis and photolysis of 2, 4-D butylate[J]. Journal of Agro-Environment Science, 2011, 30(6):1082-1086. |
| [4] | 郑立庆, 方 娜, 刘国光, 等. 农药在环境中的光化学降解研究进展[J]. 安徽农业科学, 2006, 34(19):5012-5014. ZHENG Li-qing, FANG Na, LIU Guo-guang, et al. The progress in the research of pesticides degradation in the environment[J]. Journal of Anhui Agricultural Sciences, 2006, 34(19):5012-5014. |
| [5] | 张绍明, 吴永芳, 奚本贵. 氯虫苯甲酰胺(康宽TM200SC)和茚虫威(凯恩TM150EC)防治水稻稻纵卷叶螟田间试验示范报告[C]//任 露, 李永平, 梁桂梅. 氯虫苯甲酰胺和茚虫威应用技术手册. 北京:中国农业科学技术出版社, 2009:47-51. ZHANG Shao-ming, WU Yong-fang, XI Ben-gui. The report of combating rice leafroller by Chlorantraniliprole(TM200SC) and Indoxacarb(TM150EC) in field trials[C]// REN Lu, LI Yong-ping, LIANG Gui-mei. Technical manual about the application of chlorantraniliprole and Indoxacarb. Beijing:China Agricultural Science and Technology Press, 2009:47- 51. |
| [6] | US EPA. Pesticide Fact Sheet [EB/OL]. http://www.epa.gov/opprd001/factsheets/chloran.pdf. |
| [7] | 欧晓明, 唐德秀, 林雪梅. 新型邻甲酰氨基苯甲酰胺类农药氯虫酰胺的研究概述[J]. 世界农药, 2007, 29(5):6-10. OU Xiao-ming, TANG De-xiu, LIN Xue-mei. A review on research and development of new pesticide chlorantraniliprole[J]. World Pesticides, 2007, 29(5):6-10. |
| [8] | 姜干明. 氯虫苯甲酰胺20%悬浮剂防治水稻害虫药效试验[J]. 农药科学与管理, 2009, 30(4):36-37. JIANG Gan-ming. Field control efficacy of chlorantraniliprole 20% SC against rice pest insects[J]. Pesticide Science and Administration, 2009, 30(4):36-37. |
| [9] | 付启明, 欧晓明, 刘红玉, 等. 新农药氯虫酰胺在醇液中的光解[J]. 生态环境学报, 2010, 19(3):532-536. FU Qi-ming, OU Xiao-ming, LIU Hong-yu, et al. Photolysis of new insecticide chlorantraniliprole in methanol and ethanol[J]. Ecology and Environmental Sciences, 2010, 19(3):532-536. |
| [10] | 楼书聪. 化学试剂配制手册[M]. 南京:江苏科学技术出版社, 1993:1024. LOU Shu-cong. Handbook of chemical reagents preparation[M]. Nanjing:Jiangsu Science and Technology Press, 1993:1024. |
| [11] | 唐启义, 冯明光. 实用统计分析及其DPS 数据处理系统[M]. 北京:科学出版社, 2000:418-449. TANG Qi-yi, FENG Ming-guang. DPS data processing system for practical statistics[M]. Beijing:Science Press, 2000:418-449. |
| [12] | 花日茂, 徐 利, 吴祥为. 表面活性剂对水中乙草胺光解的影响[J]. 农业环境科学学报, 2007, 26(3):1049-1053. HUA Ri-mao, XU Li, WU Xiang-wei, et al. Effect of surfactants on the photo-degradation of acetochlor in water[J]. Journal of Agro-Environment Science, 2007, 26(3):1049-1053. |
| [13] | 郑和辉, 叶常明. 乙草胺在水中的光化学降解动态研究[J]. 农药科学与管理, 2001, 22(6):12-13. ZHENG He-hui, YE Chang-ming. Study on photolysis kinetics of acetochlor in sater[J]. Pesticide Science and Administration, 2001, 22(6):12-13. |
| [14] | 邹雅竹, 龚道新. 咪鲜胺在水中的光化学降解研究[J]. 农药科学与管理, 2006, 27(2):27-30. ZOU Ya-zhu, GONG Dao-xin. Photo-degradation of prochloraz in water[J]. Pesticide Science and Administration, 2006, 27(2):27-30. |
| [15] | 吴祥为, 花日茂, 汤 锋, 等. 毒死蜱在水溶液中的光化学降解[J]. 应用生态学报, 2006, 17(7):1303-1304. WU Xiang-wei, HUA Ri-mao, TANG Feng, et al. Photochemical degradation of chlorpyrifos in water[J]. Chinese Journal of Applied Ecology, 2006, 17(7):1301-1304. |
| [16] | 花日茂, 李湘琼, 李学德, 等. 丁草胺在不同类型水中的光化学降解[J]. 应用生态学报, 1999, 10(1):57-59. HUA Ri-mao, LI Xiang-qiong, LI Xue-de, et al. Photochemical degradation of butachlor in different water[J]. Chinese Journal of Applied Ecology, 1999, 10(1):57-59. |
| [17] | 花日茂, 岳永德, 樊德方. 乙草胺在水中的光化学降解[J]. 农药学学报, 2000, 2(1):71-74. HUA Ri-mao, YUE Yong-de, FAN De-fang. The photodegradation of acetochlor in water[J]. Chinese Journal of Pesticide Science, 2000, 2(1):71-74. |
| [18] | Sakkas V A, Lambropoulou D A, Albanis T A. Photochemical degradation study of irgarol 1051 in natural waters:Influence of humic and fulvic substances on the reaction[J]. Journal of Photochemistry and Photobiology A:Chemistry, 2002, 147(2):135-141. |
| [19] | Sakkas V A, Lambropoulou D A, Albanis T A. Study of chlorothalonil photodegradation in natural waters and in the presence of humic substances[J]. Chemosphere, 2002, 48(9):939-945. |
| [20] | Mack J, Bolton J R. Photochemistry of nitrite and nitrate in aqueous solution:A review[J]. Journal of Photochemistry and Photobiology A:Chemistry, 1999, 128(1):1-13. |
| [21] | 李学德, 花日茂, 汤 锋, 等. 几种化学物质对水中百菌清光解的影响[J]. 安徽农业科学, 2009, 37(11):5097-5099, 5220. LI Xue-de, HUA Ri-mao, TANG Feng, et al. Effect of several chemical materials on photolysis of chlorothalonil in water[J]. Journal of Anhui Agricultural Sciences, 2009, 37(11):5097-5099, 5220. |
| [22] | Sook M K, Sven U G, Alfons V. Landfill leachate treatment by a photoassisted fenton reaction[J]. Wat Sci Tech, 1997, 35(4):239-248. |
 2014, Vol. 33
2014, Vol. 33







