文章信息
- 甘信宏, 郭书海, 徐文迪, 李刚, 李凤梅
- GAN Xin-hong, GUO Shu-hai, XU Wen-di, LI Gang, LI Feng-mei
- 电芬顿泥浆反应器中羟基自由基生成影响因素分析
- Analysis of Factors Influencing Hydroxyl Radical Formation in Electro-Fenton Slurry Reactor
- 农业环境科学学报, 2015, 34(1): 44-49
- Journal of Agro-Environment Science, 2015, 34(1): 44-49
- http://dx.doi.org/10.11654/jaes.2015.01.007
-
文章历史
- 收稿日期:2014-08-25
2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
近年来,污染土壤修复越来越受到重视与关注,特别是难降解有机物污染土壤修复需求迫切[1]。有机污染土壤的修复难度大,最主要的原因就是土壤为非流动态,传质效果不佳。泥浆化处理可以很好地解决土壤传质慢、非均相问题。井欣[2]将泥浆化法同微生物处理法结合制成生物泥浆反应器,修复多环芳烃污染土壤,经15 d后PAHs各环平均去除效率在50%以上。但研究结果表明,即使将土壤泥浆化后,传统的物化及生物修复方法仍存在处理效率低、修复周期长等缺点,很难达到处理要求[3,4]。高级氧化技术能够弥补上述不足,其主要原理是利用各种光、声、电、磁等物理化学过程产生具有强氧化性的·OH,使大分子难降解有机物快速矿化或提高其可生化性[5]。电芬顿法(Electro-Fenton Process,EFP)作为高级氧化技术的一种,其实质就是在电解过程中直接生成芬顿试剂[6],进而生成·OH,作为反应中间产物的·OH会诱发一系列的链反应,并且基本上可以无选择性地直接与有机污染物反应,生成CO2、H2O及无害的盐[7],很好地解决了传统芬顿法中H2O2难运输、难保存等问题[8]。
目前在处理废水、废液、垃圾渗滤液等方面已开展了大量的电芬顿法研究[9],但尚未在污染土壤修复方面见到相关报道。Wang等[10]研究了应用活性炭纤维毡为阴极的电芬顿处理染料废水的反应机制,2 h后检测到118.7 μmol·L-1·OH,表明电芬顿过程·OH产生量较高。Lin等[11]将电芬顿技术与SBR反应器结合处理垃圾渗滤液,取得了良好效果,为垃圾渗滤液的处理提供了技术支持。本研究中,将供试土按一定的水土比制成泥浆,建立多相集成的一体化反应器——电芬顿泥浆反应器,将泥浆化方法同电化学技术结合,具有高传质、快氧化、低消耗等特征,为有机污染土壤修复提供了新思路。然而在电芬顿法中,决定性的因素是·OH的生成量,因此检测·OH生成量及其影响因素的研究至关重要。
有·OH参与的化学反应基本属于游离基反应[12],在水相反应体系中·OH存在的时间仅约为10-9 s [13],因而直接测定它的浓度几乎是不可能的,一般采用捕获剂捕获的方法来进行间接定量分析。目前测定·OH的方法以自旋捕捉-ESR法[14]、高效液相色谱法[15]、分光光度法为主[16]。在高效液相色谱法中可以选择不同的·OH捕获剂,对捕获产物进行定量分析。Fukui等[17]用二甲基亚砜捕捉·OH后生成的甲基亚磺酸和重氮盐坚牢黄GC盐反应,生成邻-氯苯重氮甲基砜,经乙酸乙酯萃取后用HPLC定量地测定了Fenton反应体系中产生的·OH。Halliwell等[18]以水杨酸(2-HBA)作为捕获剂,用高效液相色谱仪检测分析2,3-二羟基苯甲酸(2,3-DHBA)和2,5-二羟基苯甲酸(2,5-DHBA)的浓度变化来分析·OH的瞬时浓度的变化。本实验以水杨酸为捕获剂,对生成的·OH进行定量检测,但在检测过程中没有检测到2,3-DHBA,可能是因为电芬顿作为电化学氧化的一种,在处理过程中没有或者很少产生2,3-DHBA[19],故以水杨酸作为捕获剂,用高效液相色谱仪检测分析2,5-DHBA浓度变化,间接地表征·OH的瞬时浓度,研究·OH在电芬顿泥浆反应器中生成的影响因素。 1 材料与方法 1.1 仪器与试剂
KQ-300DE型数控超声波清洗器(江苏昆山超声仪器有限公司),JJ-4A六联电动搅拌器(江苏金坛荣华电器制造有限公司),TGL-16M高速台式冷冻离心机(湖南湘仪实验仪器开发有限公司),雷磁pH仪(上海仪电科学仪器股份有限公司),美国Waters高效液相色谱仪[沃特世科技(上海)有限公司,2707进样器,2475荧光检测器]。
水杨酸(天津福晨化学试剂工厂),二氯甲烷/丙酮等(天津科密欧化学药剂有限公司)。 1.2 供试土壤
实验所用土壤采自沈阳生态站,自然晾干,研磨过60目筛备用。其理化性质参数见表 1[20]。
实验装置如图 1 所示。在一个1 L的烧杯中,阴极和阳极分别为长17 cm、直径10 mm的石墨电极与铁电极,外加12 V的直流电以及相应的曝气装置。在烧杯中加入600 mL水和200 g供试土壤(即水土比为3∶1)制成泥浆,控制阴极附近曝气的速度为1 L·min-1,投加电解质Na2SO4浓度为10 g·L-1,电极间距为5 cm,一次性加入捕获剂的浓度控制在240 μmol·L-1。以上为参考基准实验,以此为基准来研究不同的单个因素变化对·OH生成的影响。

|
| 图 1 电芬顿泥浆反应器装置示意图 Figure 1 Schematic diagram of Electro-Fenton slurry reactor |
C18反相柱,流动相为30 mmol·L-1醋酸-醋酸钠缓冲溶液(pH为4.9),流速为0.8 mL·min-1,色谱柱柱温为25 ℃[21]。 2 结果与讨论 2.1 标准工作曲线
配制0.5、2.0、5.0、8.0、10 μmol·L-1系列浓度的2,5-DHBA标准溶液,用液相色谱进行分析,以不同浓度(X,μmoI·L-1)及其对应的色谱峰面积(Y)进行线性回归,得到标准曲线方程:
Y=5.89×104X-1.44 ×104(R2=0.999 8)
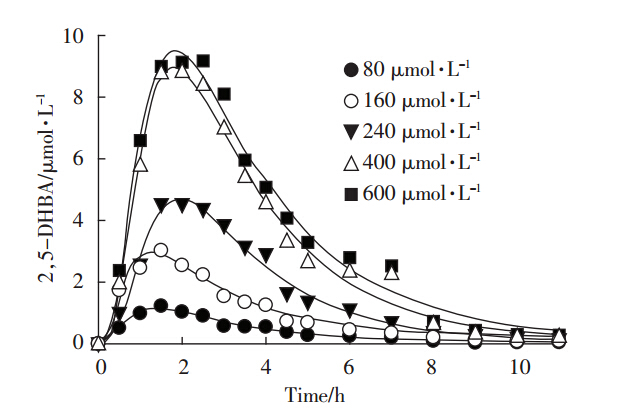
2.2 水杨酸初始浓度对·OH测定的影响为获得捕获剂最佳初始浓度参数,在保持实验其他因素不变情况下,一次性加入一定浓度水杨酸溶液作为捕获剂,使反应器内初始水杨酸浓度分别控制在80、160、240、400、600 μmol·L-1,处理9 h后结果见图 2。投加的水杨酸浓度越大,反应器内2,5-DHBA的浓度越高,约2 h后基本达到最高水平。可能原因在于,增大捕获剂水杨酸的浓度,可以使·OH同反应器内捕获剂碰撞几率增大,从而减少·OH自身的淬灭,故捕获剂初始浓度越高,生成的2,5-DHBA浓度越大。此外,在初始浓度400 μmoI·L-1时,捕获剂表征·OH的量在最高水平附近几乎是240 μmol·L-1时的2倍,但捕获剂初始浓度600 μmol·L-1与400 μmol·L-1相比,生成的2,5-DHBA没有明显增加。由此可以看出,捕获剂量在600 μmoI·L-1左右接近饱和,加入更多捕获剂,也不会使2,5-DHBA生成量有明显的增加。此捕获剂浓度下生成2,5-DHBA的量能够接近表征反应器内瞬时·OH的浓度。同时,2 h后生成的2,5-DHBA量开始下降,直到9 h浓度接近为0。原因可能是随着反应的进行,反应器内游离离子减少,大量的铁泥沉淀或附着在两电极上,造成阴、阳极钝化,电流效率下降,·OH的产生量减小。
|
|
电极间距5 cm;初始pH7;电解质浓度10 g·L-1;曝气量1 L·min-1 Electrode spacing=5 cm;initial pH=7;electrolyte concentration=10 g·L-1;aeration rate=1 L·min-1 图 2 水杨酸初始浓度对·OH测定的影响 Figure 2 Effect of different initial concentrations of salicylic acid on hydroxyl radical generation |
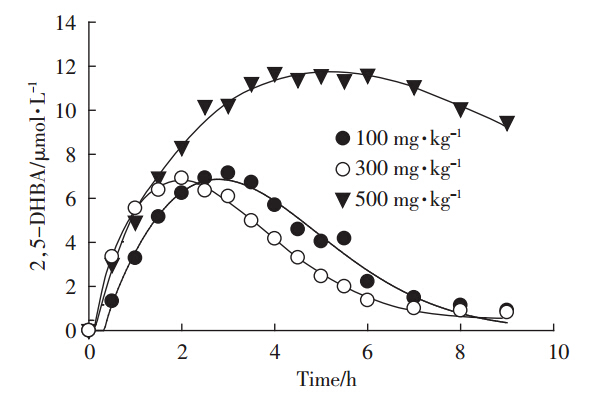
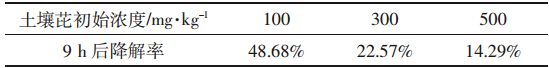
在供试土壤中均匀添加芘来模拟芘污染土壤,控制芘浓度分别为100、300、500 mg·kg-1,保持其他影响因素不变,在电芬顿处理9 h后,生成的2,5-DHBA随时间的变化见图 3。初始芘的浓度越高,生成的2,5-DHBA越多。可能原因在于,增大反应器内·OH有机物受体浓度,可以使·OH在反应器内同有机物接触几率增大,从而减少·OH自身的淬灭;再者,反应器内芘的浓度增大,减少了自由基与其他杂质的反应机会,从而使·OH引发链反应并继续传递链反应的可能性增大,这样会增加电流的效率[17],所以2,5-DHBA生成量亦增加,相应表征·OH生成量增加,与实验结果相吻合。9 h后芘的削减结果见表 2,可以看出土壤中初始芘浓度越小降解率越大,但总的去除量随芘初始浓度的增加而提高。
|
|
电极间距5 cm;初始pH7;电解质浓度10 g·L-1;曝气量1 L·min-1;初始捕获剂浓度240 μmol·L-1 Electrode spacing=5 cm;initial pH=7;electrolyte concentration=10 g·L-1;aeration rate=1 L·min-1;initial capture agent concentration=240 μmol·L-1图 3 土壤中芘初始浓度对·OH测定的影响 Figure 3 Effect of initial concentrations of pyrene in soil on hydroxyl radical generation |
 |
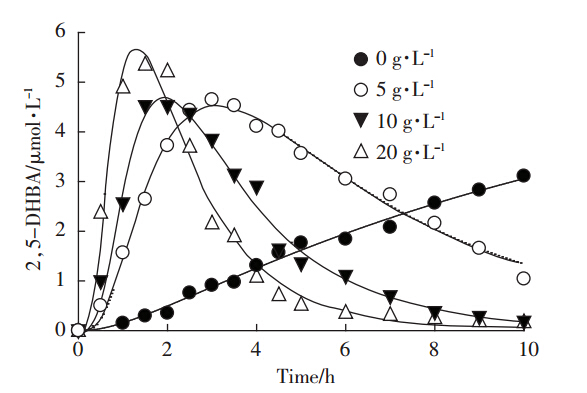
为了考察电解质浓度对·OH生成量的影响,在其他条件不变的情况下设置电解质(Na2SO4)浓度依次为0、5、10、20 g·L-1,处理9 h后,其·OH浓度随时间变化见图 4。在处理2 h内,电解质浓度越大,·OH浓度升高得越快;电解质浓度为20 g·L-1时达到最高水平,所用的时间是5 g·L-1时的一半。这表明电解质浓度越高,两电极间的电流越大,阴阳极分别产生的H2O2和Fe2+越多,·OH生成量的增长速率越快。但在处理3 h后,由于铁泥增加、阳极钝化等因素造成的电流下降,加入电解质的实验中·OH的生成量也在下降,且电解质浓度越大,·OH生成量减少的速率越大。这进一步证明:高浓度电解质造成铁泥产生的速率过快,阳极钝化严重,电流效率下降明显。此外,当不加电解质时,依靠供试土壤本身的离子在反应器内进行电子传递,电流效率低,·OH生成量的增长速率慢。由此可看出,往反应器内加入适量的电解质(浓度在5~10 g·L-1)可增大·OH的生成速度,在4~6 h里能够维持·OH的瞬时生成量在较高水平。
|
|
电极间距5 cm;初始pH7;曝气量1 L·min-1;初始捕获剂浓度240 μmol·L-1 Electrode spacing=5 cm;initial pH=7;aeration rate=1 L·min-1;initial capture agent concentration=240 μmol·L-1 图 4 电解质(Na2SO4)浓度对·OH生成的影响 Figure 4 Effect of electrolyte concentrations on hydroxyl radical generation |
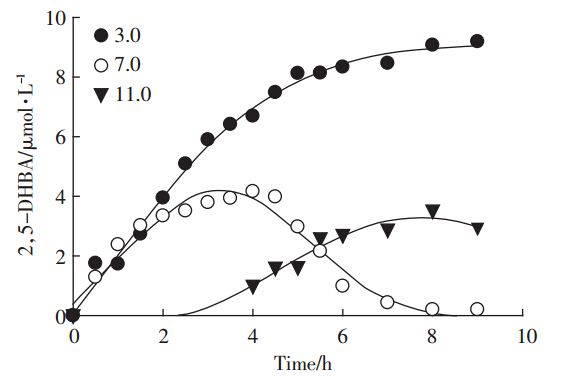
为研究初始pH对·OH生成量的影响,用H2SO4和NaOH将反应器的初始pH分别调至3、7和11,处理9 h,结果如图 5所示。生成·OH的量与速率在pH为3时最大,pH为11时最小。低pH条件下有利于·OH生成,是由于pH值不仅对阴极反应电位和槽电压有影响,还将决定生成H2O2的电流效率,进而影响随后生成·OH的效率。pH 值低的酸性条件下,还原性越好,越有利于H2O2的生成,这一结果同陈震等[22]的观点相符。在初始pH为11的实验中,前4 h未检测到·OH,说明碱性条件不利于H2O2的生成,同时Fe2+不容易存在于碱性条件,故·OH的产生量比较小,且有延迟。
|
|
电极间距5 cm;电解质浓度10 g·L-1;曝气量1 L·min-1;初始捕获剂浓度240 μmol·L-1 Electrode spacing=5 cm;electrolyte concentration=10 g·L-1;aeration rate=1 L·min-1;initial capture agent concentration=240 μmol·L-1 图 5 初始pH对·OH生成的影响 Figure 5 Effect of initial pH on hydroxyl radical generation |
为探究电极间距对·OH产生量的影响,调节阴阳两极间距分别为3、5、8 cm,各自处理9 h,结果如图 6所示。电极间距3 cm时,·OH浓度升高较快,在2 h左右就达到了最高值,但在电极间距5 cm时,产生·OH的量最大,同时发现在·OH生成量最高水平附近,电极间距为5 cm时生成量接近为8 cm时的2倍,比间距为3 cm时高约35%,同时瞬间生成量维持较高水平。因此,电极间距在5 cm左右时产生·OH的效果最好。原因在于电极相距太近,阳极干扰阴极H2O2的生成,进而影响·OH的生成;电极相距太远则影响电压梯度,会使电流效率下降,阳极解离的Fe2+和阴极产生的H2O2也会减少,使生成的·OH减少。

|
|
初始pH7;电解质浓度10 g·L-1;曝气量1 L·min-1;初始捕获剂浓度240 μmol·L-1 Initial pH=7;electrolyte concentration=10 g·L-1;aeration rate=1 L·min-1;initial capture agent concentration=240 μmol·L-1 图 6 电极间距对·OH生成的影响 Figure 6 Effect of electrode space on hydroxyl radical generation |
(1)在本实验反应体系中,控制初始pH为3左右,加入适量的Na2SO4,控制浓度在5 g·L-1左右,保持电极间距5 cm左右,可以增加·OH生成量且在较长时间段内使·OH瞬时浓度维持在较高水平;当加入适量水杨酸溶液使反应器内初始浓度为400 μmol·L-1时,生成的2,5-DHBA浓度最大,接近9 μmol·L-1,可以间接表征瞬时·OH的生成量。
(2)由芘的初始浓度对·OH测定影响来看,有机物的存在减少·OH自身淬灭,且有机污染物含量越大,削减的总量越大,提高了·OH利用率。
(3)相比于传统修复方法,电芬顿技术可以更加经济方便地生成大量的·OH,快速削减有机污染物;泥浆反应器能极大地提高土壤的均质化程度,有利于传质过程。二者的协同模式有望形成土壤有机污染高效修复方法。
| [1] | 李法云, 臧树良, 罗 义. 污染土壤生物修复技术研究[J]. 生态学杂志, 2003, 22(1):35-39. LI Fa-yun, ZANG Shu-liang, LUO Yi. Bioremediation of contaminated soils:A review[J]. Chinese Journal of Ecology, 2003, 22(1):35-39. |
| [2] | 井 欣. 多环芳烃污染土壤的生物泥浆反应器处理技术研究[D]. 沈阳:中国科学院沈阳应用生态研究所, 1999. JING Xin. Bioremediation of soil contaminated with Polynuclear Aromatic Hydrocarbons(PAHs) in a bioslurry reactor[D]. Shenyang:Institute of Applied Ecology, Chinese Academy of Sciences, Shenyang, 1999. |
| [3] | 张 旋, 王启山. 高级氧化技术在废水处理中的应用[J]. 水处理技术, 2009, 35(3):18-22. ZHANG Xuan, WANG Qi-shan. Application of advanced oxidation technologies in wastewater treatment[J]. Technology of Water Treatment, 2009, 35(3):18-22. |
| [4] | 卢晓霞, 李秀利, 马 杰, 等. 焦化厂多环芳烃污染土壤的强化微生物修复研究[J]. 环境科学, 2011, 32(3):864-869. LU Xiao-xia, LI Xiu-li, MA Jie, et al. Enhanced bioremediation of coking plant soils contaminated with polycyclic aromatic hydrocarbons[J]. Environmental Science, 2011, 32(3):864-869. |
| [5] | 江传春, 肖蓉蓉, 杨 平. 高级氧化技术在水处理中的研究进展[J]. 水处理技术, 2011, 37(7):12-16, 33. JIANG Chuan-chun, XIAO Rong-rong, YANG Ping. Research process of advanced oxidation processes in wastewater treatment[J]. Technology of Water Treatment, 2011, 37(7):12-16, 33. |
| [6] | 肖 华, 周荣丰. 电芬顿法的研究现状与发展[J]. 上海环境科学, 2004, 23(6):253-256. XIAO Hua, ZHOU Rong-feng. Current research and development of Electric-Fenton[J]. Shanghai Environmental Sciences, 2004, 23(6):253-256. |
| [7] | 钟 理, 陈建军. 高级氧化处理有机污水技术进展[J]. 工业水处理, 2002, 22(1):1-4. ZHONG Li, CHEN Jian-jun. Technical progress in organic effluent water treatment by advanced oxidationprocesses[J]. Industrial Water Treatment, 2002, 22(1):1-4. |
| [8] | 周 蕾, 电芬顿阴极材料的制备与转盘工艺的研究[D]. 天津:南开大学, 2013. ZHOU Lei, Preparation of cathodic materials and investigation of rotating disk reactor for Electro-Fenton system[D]. Tianjin:Nankai University, 2013. |
| [9] | 赵豫北. 电芬顿在废水处理方面的发展现状和研究[J]. 科技传播, 2013(12):44-45. ZHAO Yu-bei. The development status and research of the Electro-Fenton in effluent treatment[J]. Public Communication of Science & Technlogy, 2013(12):44-45. |
| [10] | Wang A M, Li Y Y, Ru J. The mechanism and application of the Electro-Fenton process for azo dyeAcid Red 14 degradation using an activated carbon fibre felt cathode[J]. Journal of Chemical Technology andBiotechnology, 2010, 85(11):1463-1470. |
| [11] | Lin S H, Chang C C. Treatment of landfill leachate by combined Electro-Fenton oxidation and sequencingbatch reactor method[J]. Water Research, 2000, 34(17):4243-4249. |
| [12] | 余双菊. 羟基自由基的特性及检测方法比较[J]. 广东化工, 2010, 37(9):141-143. YU Shuang-ju. The Specifity of hydroxyl free radical and the methods to detect it[J]. GuangdongChemical Industry, 2010, 37(9):141-143. |
| [13] | Janzen E G, Kotake Y, Hinton R D. Stabilities of hydroxyl radical spin adducts of PBN-type spin traps[J]. Free Radical Biology & Medicine, 1992, 12(2):169-173. |
| [14] | Stokes N J, Tabner B J, Hewitt C N. The Determination of hydroxyl radical concentrations in environmental chambers using Electron Spin Resonance[J]. Chemosphere, 1994, 28(5):999-1008. |
| [15] | Tai C, Peng J F, Liu J F, et al. Determination of hydroxyl radicals in advanced oxidation processeswith dimethyl sulfoxide trapping and liquid chromatography[J]. Analytica Chimica Acta, 2004, 527(1):73-80. |
| [16] | 王仕良, 张 曾, 黄干强. 羟基自由基的产生与测定[J]. 造纸科学与技术, 2003, 22(6):45-47, 75. WANG Shi-liang, ZHANG Zeng, HUANG Gan-qiang. The Generation and determination of hydroxyl radicals[J]. Paper Science & Technology, 2003, 22(6):45-47, 75. |
| [17] | Fukui S, Hanasaki Y, Ogawa S. High-performance liquid chromatographic determination of methanesulphinic acid as a method for the determination of hydroxyl radicals[J]. Journal of Chromatography A, 1993, 630(1):187-193. |
| [18] | Halliwell B, Grootveld M. The measurement of free radical reactions in humans:Some thoughts for futureexperimentation[J]. FEBS letters, 1987, 213(1):9-14. |
| [19] | 吴 迪. 羟基自由基在电催化氧化体系中的形成规律及其在废水处理中的应用研究[D]. 长春:吉林大学, 2007. WU Di. Study on the rules of hydroxyl radicals generation in electrochemical catalytic oxidation system and its applications in wastewater treatment[D]. Changchun:Jilin University, 2007. |
| [20] | 鲁如坤. 土壤农化分析[M]. 北京:中国农业科技出版社, 2000. LU Ru-kun. Analytical methods of soil and agro-chemistry[M]. Beijing:China Agricultural Science and Technology Press, 2000. |
| [21] | 任信荣, 邵可声, 唐孝炎. 高效液相色谱法测定水杨酸及其羟基化产物[J]. 色谱, 2001, 19(2):191-192. REN Xin-rong, SHAO Ke-sheng, TANG Xiao-yan. Determination of salicylic acid and its hydroxylated products using high performance liquid chromatography and fluorescence detection[J]. Chinese Journal of Chromatography, 2001, 19(2):191-192. |
| [22] | 陈 震, 陈 晓, 郑 曦, 等. 溶液pH及电流浓度对电化学法生成羟基自由基降解机制的影响[J]. 环境科学研究, 2002, 15(3):42-44, 52. CHEN Zhen, CHEN Xiao, ZHENG Xi, et al. Influence of pH and current concentration on electrochemical-generated hydroxyl radical for degradation and decolorization of dye wastewater[J]. Research of Environmental Sciences, 2002, 15(3):42-44, 52. |
 2015, Vol. 34
2015, Vol. 34