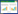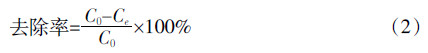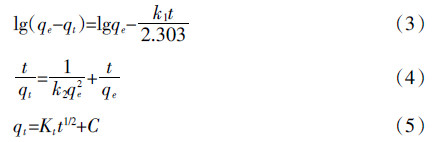文章信息
- 冯彦房, 薛利红, 杨梖, 刘杨, 段婧婧, 何世颖, 杨林章
- FENG Yan-fang, XUE Li-hong, YANG Bei, LIU Yang, DUAN Jing-jing, HE Shi-ying, YANG Lin-zhang
- 载镧生物质炭吸附水体中As(Ⅴ)的过程与机制
- Adsorption of As(Ⅴ) from Aqueous Solution by Lanthanum Oxide-loaded Biochar:Process and Mechanisms
- 农业环境科学学报, 2015, 34(11): 2190-2197
- Journal of Agro-Environment Science, 2015, 34(11): 2190-2197
- http://dx.doi.org/10.11654/jaes.2015.11.022
-
文章历史
- 收稿日期: 2015-06-05
2. 中国科学院南京土壤研究所, 土壤与农业可持续发展国家重点实验室, 南京 210008;
3. 江苏省农业科学院农业经济与信息研究所, 南京 210014
2. Institute of Soil Science, State Key Laboratory of Soil and Sustainable Agriculture, Chinese Academy of Sciences, Nanjing 210008, China;
3. Institute of Agricultural Economics and Information, Jiangsu Academy of Agriculture Sciences, Nanjing 210014, China
砷是众所周知的有毒元素,即使低浓度的含砷污水也会威胁水生动植物和人类的健康[1, 2]。砷广泛分布在环境中,特别是砷黄铁矿或金属砷酸,并且砷连同其他一些重金属进入水体的方式多样,包括通过自然来源如火山喷发、天然矿物、大气沉积、暴雨冲刷等以及通过人为来源如有色冶炼、化石燃料发电厂等[3, 4]。无机砷在水体中一般形态有三价(主要存在于地下水)或五价(主要存在于溶氧量高的水中)[5]。自1993年以来,世界卫生组织(WHO)建议最大污染水平饮用水中砷含量为10 μg·L-1[6]。因此,降低水体中砷的浓度一直是研究和关注的焦点。现在除砷技术主要包括电絮凝、化学沉淀、过滤、反渗透、离子交换、膜处理、生物法等[6, 7, 8, 9, 10, 11, 12, 13],其中吸附法以其操作简便、成本低廉等优点,引起了广泛的关注[14, 15, 16]。
稀土元素镧的氧化物已被证明有较高的阴离子吸附能力,并被应用于水体的吸附净化研究[17, 18, 19]。然而,直接投加使用镧的氧化物,不易进行回收,且在加大使用成本同时易造成资源的浪费和二次污染。此外,细小的氧化物颗粒易堆积产生传质阻力,阻碍吸附质进入到堆积体内部,限制了吸附能力[20, 21]。因此,有必要设计一种新型的吸附剂材料,将镧的纳米颗粒负载分布在适宜的载体上,以提升吸附性能,降低吸附成本和环境风险。
农业废弃物材料,如秸秆、谷物、米糠皮、锯末等近年来常被作为一类低成本的吸附剂用于去除水体污染物的试验研究[22, 23, 24]。然而,由于原生态的农业废弃物稳定性较差,直接用于水体污染物吸附会释放出化感物质,腐烂后更会导致水体污染[25]。利用农作物(秸秆类)等植物材料在缺氧或绝氧,低于700 ℃的条件下热解制备出的生物炭,容重小,且具有大量的表面负电荷以及高电荷密度的特征,构成了生物炭良好的吸附特性,能吸附水、土壤或沉积物中的一些无机阳离子及极性或非极性有机化合物[26, 27],而且生物炭施入土壤后更可控制温室气体释放,提高土壤肥力等,是一种成本低、来源广泛、环境友好的新兴炭基材料[28, 29]。生物炭表面的性质决定了其对阴离子的吸附能力较差,因此需要生物炭进行改性修饰,以增加其对阴离子污染物的去除能力[30, 31, 32, 33]。
本研究将生物炭材料和稀土元素镧的氧化物纳米颗粒结合起来,用于砷酸根离子吸附和砷污染水体的净化系统。将镧的氧化物负载到以玉米秸秆为原材料烧制的生物炭上,制备成一种成本低廉且具有高效除砷性能的载镧生物炭(La-biochar)。本研究考察了La-biochar对砷酸根的吸附动力学、吸附等温线以及主要操作参数(如La-biochar投加量和初始溶液pH值)对吸附砷酸根离子的影响,探讨了La-biochar对As(Ⅴ)的吸附机制,以期为秸秆废弃物资源化提供一种方法,也为水体中砷污染治理提供一种新的技术手段。
1 材料与方法 1.1 试剂与仪器氯化镧(LaCl3·7H2O)、氢氧化钠(NaOH)、盐酸(HCl)、95%乙醇、硝酸银(AgNO3)、砷酸二氢钠(Na2HAsO4)等均为分析纯(国药集团化学试剂有限公司),实验用水为去离子水。主要仪器:紫外可见分光光度计(日本岛津UV-2450);pH计(中国精密科学仪器PHS-3C);离心机(英国SciQuip Sigma 3-16);水浴恒温振荡器(中国科析仪器SHA-3C);马弗炉(中国上海精宏SXL-120);电热恒温鼓风干燥箱(中国华伟DGG-9070B)。
负载镧生物炭表面特征的测定:表面分析采用扫描电子显微镜(日本Hitachi S-4300);X射线光电子能谱仪(美国EDAX GENESIS XM2 60S);比表面及孔性结构分析采用全自动比表面和孔隙度分析仪(美国Quantachrome- NOVA4000e)。
水样中AsO43-浓度采用电感耦合等离子体原子发射光谱仪(美国Thermo 6300 ICP)测定,进行水样测定前使用0.45 μm微孔滤膜过滤。
1.2 载镧生物炭的制备实验选用采自江苏省农科院的玉米秸秆为原材料,洗净并去除杂质,风干后破碎,过2 mm筛。
取20 g过筛的玉米秸秆加入到200 mL 1 mol·L-1 La3+溶液中,边搅拌边向上述混合溶液中逐滴加入6 mol·L-1 NaOH溶液至pH值为10,继续搅拌1 h;搅拌得到的产物离心后倒掉上清液,将剩余固体用95%乙醇清洗至淋洗液中,用0.1 mol·L-1 AgNO3检测不到Cl-;清洗过后烘干至恒重,置于马弗炉中绝氧焙烧,以20 ℃·min-1升温至400 ℃,并在此温度条件下保持一定时间,待冷却至室温后取出炭化产物,使用去离子水反复清洗至淋洗液的pH值为中性;最后于105 ℃条件下烘干,过0.25 mm筛,即获得载镧生物炭(La-biochar),装瓶备用。
1.3 La-biochar吸附As(Ⅴ)实验静态吸附试验处理均设三个平行。
1.3.1 吸附动力学分别取0.05 g La-biochar加入到50 mL含AsO43- 50、100 mg·L-1的溶液中,置于水浴恒温振荡器中,振荡速率为200 r·min-1,保持温度为25 ℃。分别在固定的时间采样测定溶液中残余砷含量,其中t时刻La-biochar对As(Ⅴ)的吸附量计算式如下:
式中:C0和Ct分别为溶液中砷酸根离子的初始浓度和t时刻的浓度,mg·L-1;V为溶液体积,L;m是吸附剂质量,g。 1.3.2 等温吸附研究各取0.05 g La-biochar分别加入到50 mL含有10、50、75、100、125 mg·L-1的AsO43-溶液中,在 25 ℃于恒温振荡器中200 r·min-1振荡24 h以确保达到吸附平衡。La-biochar对不同浓度的砷酸根离子的平衡吸附量计算如式(1)。
1.3.3 La-biochar剂量对吸附As(Ⅴ)的影响分别取0.025、0.05、0.075、0.1、0.2 g La-biochar加入到50 mL含50 mg·L-1 AsO43-的溶液中,置于水浴恒温振荡器中振荡24 h,转速为200 r·min-1,保持温度为25 ℃。不同La-biochar添加量对As(Ⅴ)的去除率计算式如下:
式中:C0和Ce分别为溶液中As(Ⅴ)的初始浓度和24 h后砷酸根的浓度,mg·L-1。 1.3.4 pH值对吸附砷酸根离子的影响各取0.05 g La-biochar加入到50 mL含50 mg·L-1 AsO43-的溶液中,用0.1 mol·L-1 NaOH或HCl分别将溶液的pH调节为不同值,置于水浴恒温振荡器中振荡24 h,转速为200 r·min-1,保持温度为25 ℃。不同pH条件下La-biochar对砷酸根的去除率计算如式(2)。
2 结果与讨论 2.1 La-biochar的表征 2.1.1 扫面电子显微镜(SEM)分析通过扫描电子显微镜(SEM)观察La-biochar吸附砷酸根离子前后形态(图1)。总的来说,La-biochar整体呈片状堆积,在较高放大倍数下观察吸附前后载镧生物炭,可以发现表面较为均匀的分布着白色颗粒,可能被负载上镧的纳米颗粒。另外,热解产生的腐蚀性气体可能刻蚀生物炭表面,造成表面粗糙不平,经比表面积分析测试,得到生物炭比表面积由对照的27.98 m2·g-1增加到128.95 m2·g-1,证实了制备过程对微孔起到扩增效应,同时,微孔增加也利于更多纳米级镧氧化物的附着,进一步提高了载镧生物炭的吸附能力。

|
| 图 1 吸附As(V)前后La-biaochar的扫描电子显微镜图 Figure 1 SEMimages of La-biochar before (a,b) and after (c,d) As (V) adsorption |
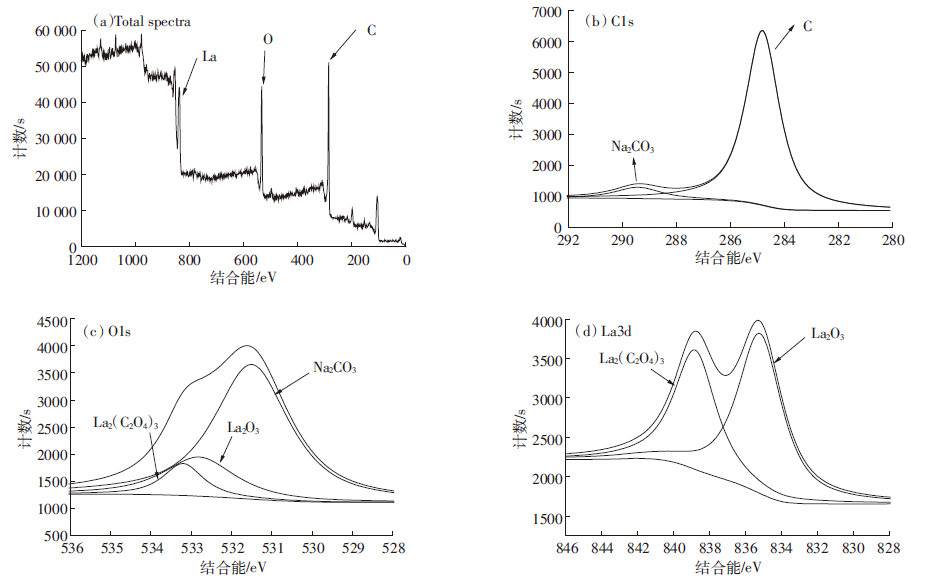
从图2a可见,通过X射线光电子能谱(XPS)分析,La-biochar的XPS总谱图有三个较明显的峰,分别对应着碳元素、氧元素和镧元素,说明经过本试验制备的生物炭表面成功负载了较多量的镧元素,这也为提升其对砷酸根的吸附能力打下了良好基础。
|
| 图 2 La-biochar表面的X射线光电子能谱(XPS) Figure 2 X ray photoelectron spectra of La-biochar |
La-biochar的C1s光谱(图2b)由两个峰组成,Na2CO3(峰1,289.4 eV)和C(峰2,284.8 eV)。峰2说明该物质的主要组成是碳元素,峰2的出现是因为材料制备过程中使用NaOH溶液调节pH值,引入了钠元素。O1s光谱(图2c)组成如下:Na2CO3(峰1,533.2 eV),La2O3(峰2,532.8 eV)和La2(C2O4)3(峰3,531.5 eV)。La3d光谱(图2d)由La2O3(峰2,835.3 eV)和La2(C2O4)3(峰3,838.8 eV)组成。O1s光谱和La3d光谱都表明镧元素被成功负载在La-biochar的表面上,并且镧元素的主要存在形式为La2O3和La2(C2O4)3。
2.2 La-biochar吸附As(Ⅴ)的过程 2.2.1 吸附动力学La-biochar接触时间对吸附As(Ⅴ)的影响如图3所示。在最初的几分钟,吸附非常快,是因为刚开始La-biochar上有丰富的可利用的吸附位点,然后吸附位点逐渐被As(Ⅴ)填满,吸附速度放缓最后达到平衡饱和。本实验条件下La-biochar吸附As(Ⅴ)的平衡时间为60~90 min。未修饰的生物炭对As(Ⅴ)的吸附量只有0.15 mg·g-1,本实验制备的载镧生物炭对As(Ⅴ)的吸附量达到38.02 mg·g-1,吸附能力明显高于修饰前。

|
| 图 3 接触时间对吸附As(V)的影响 Figure 3 Effect of contact time on As (V) adsorption |
本实验采用准一级动力学模型、准二级动力学模型和内扩散模型对La-biochar吸附As(Ⅴ)的动力学过程进行拟合[32, 33, 34, 35]。初始浓度为50、100 mg·L-1,平衡时浓度分别为34.59、46.60 mg·L-1,准一级动力学模型、准二级动力学模型和内扩散模型可以表示如下:
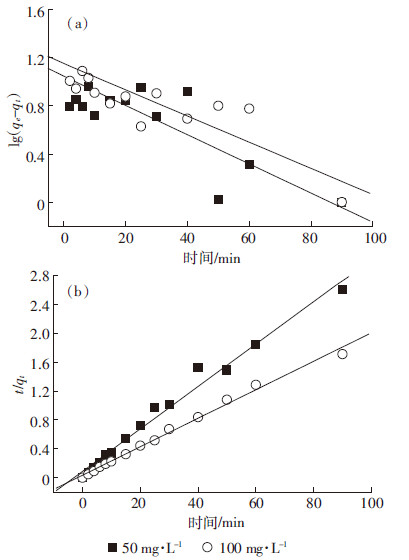
式中:qt和qe分别为t时刻和吸附平衡时La-biochar对As(Ⅴ)的吸附容量,mg·L-1;k1(min)、k2(mg·g-1·min-1)分别为准一级动力学和准二级动力学模型的速率常数;Kt为粒内扩散速率常数,mg·g-1·min-1/2;C为与边界层厚度有关的常数。线性拟合结果如图4和表1所示,相比准一级动力学相关系数,准二级动力相关系数更接近1.000,表明准二级动力学模型更适合描述La-biochar对As(Ⅴ)吸附。
|
| 图 4 La-biochar吸附As(V)的一级动力学(a)和二级动力学(b)线性图 Figure 4 Pseudo-first-order (a) and pseudo-second-order (b) kinetic plots for As (V) adsorption on La-biochar |
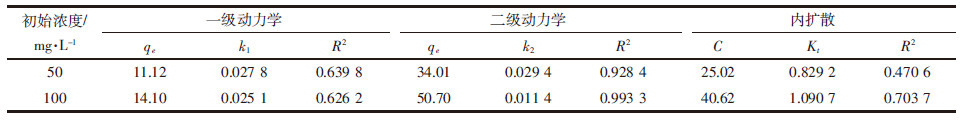 |
大量的研究表明,准二级动力学模型往往更符合对吸附过程的描述。而准二级动力学模型的速率常数则与吸附材料本身的一些性质(如粒径)以及吸附体系中的环境要素(如温度、吸附剂添加量、吸附质浓度等)有关联。如表1所示,较高初始浓度条件下,准二级动力学速率常数k2低于较低初始浓度的试验处理,说明La-biochar在较高As(Ⅴ)浓度条件下需要更长的时间达到吸附平衡。
准一级动力学模型基于如下假设:吸附质占据吸附位点的速率与未被占据的位点数目成正比。该模型往往不适合描述整个吸附过程,但这符合对物理吸附过程的描述。如图4a所示,对于整个吸附过程而言,准一级动力学对吸附过程数据的符合程度并不好,拟合参数R2不超过0.640 0(表1)。但对于吸附开始的很短时间内准一级动力学模型与试验数据符合程度较好,只是限于试验技术手段,无法在吸附刚开始的很短时间内采集足够样品。本研究使用的准二级动力学模型的基本假设为吸附质在吸附剂上的吸附过程为化学吸附,而准二级动力学模型对整个吸附过程都有较好的拟合参数,其R2不低于0.920 0(表1)。通过对准一级和准二级动力学模型的讨论可以推测,在吸附过程刚开始的阶段,可能同时存在物理吸附(如静电作用)和化学吸附(如离子交换)过程,随着吸附过程的进一步进行,化学吸附开始占主导,而这与后文中对吸附机制的讨论相呼应。
从整个吸附过程来看,初始浓度为50 mg·L-1和100 mg·L-1时用内扩散模型拟合得到一次线性相关系数分别0.470 6和0.703 7,其线性相关性不高,表明吸附过程中存在颗粒间扩散现象。但是该过程只发生在吸附开始阶段,并不是速率控制阶段,并且吸附过程由两个甚至多个步骤控制。
2.2.2 等温吸附研究应用Freundlich和Langmuir吸附等温线模型对La-biochar吸附As(Ⅴ)的等温吸附过程进行拟合[36, 37]。二者的线性表达式如下:
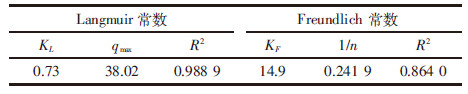
式中:qe和qmax分别为吸附剂平衡时的吸附量和理论最大吸附量,mg·g-1;KL为Langmuir常数,L·mg-1;KF和n分别都为Freundlich模型的常数。在Langmuir模型的吸附研究中常使用分离常数(RL)来衡量吸附过程是不是良性的,是不是有利于吸附进行的[38]。分离常数RL是对Langmuir模型本质的另一种表达:
当RL=0时,该吸附过程是不可逆的;当0<RL<1时,该吸附过程是良性的;当RL=1时,意为线性吸附;当RL>1时,表示不利于吸附。
由表2所见,La-biochar对As(Ⅴ)的吸附过程更适合用Langmuir吸附等温方程描述,说明其对As(Ⅴ)的吸附为单层吸附,计算得RL 的值为0.964 8(0<RL<1),该吸附过程是良性的[39]。
 |
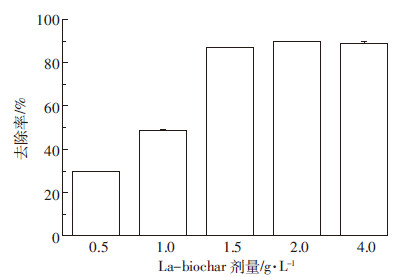
La-biochar剂量对As(Ⅴ)的去除率如图5所示,正如预期,As(Ⅴ)去除率随着吸附剂剂量的增大而增大,在吸附剂剂量达到2.0 g·L-1时趋于平衡。
|
| 图 5 不同吸附剂剂量对吸附As(V)的影响 Figure 5 Effect of adsorbent rates on As(V) adsorption |
随着pH值的不同,砷酸根可以在溶液中电解成不同形式[12, 40],其电离式如下(pKa1=2.24,pKa2=6.76,pKa3=11.60):
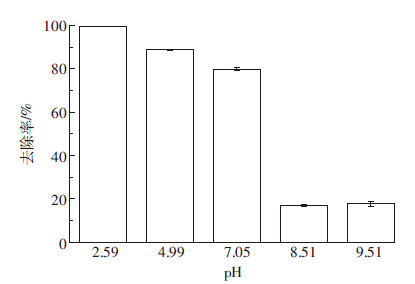
从图6可以看到,La-biochar对砷酸根离子的去除率随着pH值的变化有较大的浮动。随着pH值的增大,对As(Ⅴ)的吸附能力减小。整体上来说,酸性条件下La-biochar对As(Ⅴ)的去除率要显著高于碱性条件。这是因为酸性条件下La-biochar容易被质子化而带更多的正电,吸附带负电的H2AsO-4和HAsO2-4;而且,碱性条件下较高浓度的OH-会与砷酸水解产生的阴离子竞争La-biochar表面的吸附点位,阻碍了对As(Ⅴ)的吸附。
|
| 图 6 初始pH 值对As(V)去除率的影响 Figure 6 Effect of initial pH on As(V) removal efficiency |
经过对La-biochar初步的表征分析,可以发现,镧的氧化物纳米颗粒成功负载到了生物炭表面。基于XPS数据分析和SEM观察,推测镧氧化物纳米颗粒负载到生物炭表面的过程可能由以下步骤组成:
(1)将生物质材料粉末置于含有La3+的溶液中,由于生物质材料表面含有大量的羧基、羟基等含氧官能团,对于阳离子的La3+具有良好的静电吸附作用;同时生物质材料因纤维素木质素等形成的粗糙表面,为吸附前述的La3+离子提供了较多的吸附位点[32]。
(2)经过充分的吸附反应和传质过程,生物质表面和微孔中负载了大量的La3+,为后续的热解以及进一步的负载镧的氧化物提供了前提条件。
(3)负载了La3+的生物质材料在较高温度条件下灼烧,发生脱水过程,稀土氯化物将会首先生成LaOCl,进而分解成为镧的氧化物(图2),与此同时产生腐蚀性气体HCl(相关反应式:LaCl3+ H2O=LaOCl+2HCl),进而发生如下反应:2LaOCl+H2O=La2O3+2HCl。
(4)生物炭的烧制过程中,易分解和易挥发的成分随着温度升高而烧失;同时,反应过程中由于产生腐蚀性的HCl气体,在高温烧制过程中会对生物炭表面的微孔形成刻蚀,使炭表面易于被酸腐蚀的有机物质和矿物质脱离表面,微孔增多,孔径增大,接着上述有机物质和矿物质被随后制作过程中的洗涤等过程清洗。该过程结束后留下的是相对稳定的炭骨架,同时形成较大的比表面积和孔容孔径(比表面积增大4.6倍)为镧氧化物提供附着的载体,进而为提高载镧生物炭对砷酸根的吸附性能提供了条件。
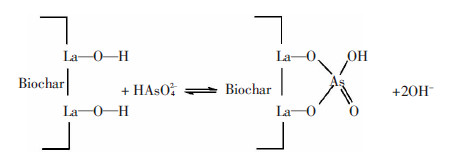
2.4.2 La-biochar对As(Ⅴ)的吸附机制根据以上实验结果分析,La-biochar吸附As(Ⅴ)的机制可以归因于负载到生物炭上的纳米镧氧化物和氧酸之间的吸附。水和氧化物具有活跃的核心,可以吸附阴离子。当镧纳米颗粒和砷酸根离子之间存在静电吸附,其水和氢氧化键被砷酸根离子所取代便形成新的复杂的化合物。因此,这个过程可以有效地去除阴离子[22, 41]。La-biochar对As(Ⅴ)的吸附过程可归结为复杂的离子交换吸附过程,该吸附机制可使用图7进行描述。
|
| 图 7 La-biochar 吸附砷酸根机制 Figure 7 Mechanism of As(V) adsorption by La-biochar |
此外,如前文所述,制备La-biochar过程中会显著增加生物炭比表面积,一方面利于更多的纳米镧氧化物的负载,另一方面由于生物炭表面存在丰富的官能团,也会在一定程度上增强生物炭对砷酸根的吸附作用。
3 结论(1)镧的氧化物纳米颗粒被负载在玉米秸秆烧制的生物炭(La-biochar)表面上,SEM分析该生物炭表面上分布着许多纳米颗粒,XPS分析负载后生物炭含有大量镧氧化物纳米颗粒,其主要形态为La2O3和La2(C2O4)3。
(2)制备的La-biochar对As(Ⅴ)吸附随着投加量的增大而增大,在投加量为2.0 g·L-1时达到最大去除率。随着pH值的增大,载镧生物炭对砷酸根的吸附能力呈下降趋势。
(3)La-biochar对As(Ⅴ)吸附在短时间内即达到平衡,吸附过程符合准二级动力学方程。吸附过程更加符合Langmiur吸附等温模型,La-biochar对As(Ⅴ)的最大饱和吸附量为38.02 mg·g-1,高于文献报道的炭基吸附材料对砷酸根的吸附能力,具有较好的应用前景。
(4)La-biochar对As(Ⅴ)的吸附是复杂的离子交换过程。
致谢:中国科学院南京土壤研究所戴敏先生参加了本研究部分试验的具体操作,在此表示感谢。
| [1] | Mathieu N K, 曾希柏, 李莲芳, 等. 几种叶类蔬菜对砷吸收及累积特性的比较研究[J]. 农业环境科学学报, 2013, 32(3):485-490. Mathieu N K, ZENG Xi-bai, LI Lian-fang, et al. A screening study of five leafy vegetable species for torlerance and accumulation of toxic inorganic arsenic(V) under hydroponic conditions[J]. Journal of Agro-Environment Science, 2013, 32(3):485-490. |
| [2] | Liu Y, Zheng B H, Fu Q, et al.Risk assessment and management of arsenic in source water in China[J]. Journal of Hazardous Materials, 2009, 170(2/3):729-734. |
| [3] | 李 彤, 易 雯, 付 青, 等. 极端暴雨条件下北江重金属非点源污染负荷估算[J]. 环境科学研究, 2014, 27(9):990-997.LI Tong, YI Wen, FU Qing, et al. Load estimation of non-point heavy metal pollution in Beijiang River during extreme storm runoff event[J]. Research of Environmental Sciences, 2014, 27(9):990-997. |
| [4] | He J, Charlet L. A review of arsenic presence in China drinking water[J]. Journal of Hydrology, 2013, 492:79-88. |
| [5] | Sorg T J, Chen A S, Wang L L. Arsenic species in drinking water wells in the USA with high arsenic concentrations[J]. Water Research, 2014, 48:156-169. |
| [6] | Dou X M, Mohan D, Pittman C U. Arsenate adsorption on three types of granular schwertmannite[J]. Water Research, 2013, 47(9):2938-2948. |
| [7] | Oncel M, Muhcu A, Demirbas E, et al. A comparative study of chemical precipitation and electrocoagulation for treatment of coal acid drainage wastewater[J]. Journal of Environmental Chemical Engineering, 2013,1(4):989-995. |
| [8] | Neumann A, Kaegi R, Voegelin A, et al. Arsenic removal with composite iron matrix filters in Bangladesh:A field and laboratory study[J]. Environmental Science & Technology, 2013, 47(9):4544-4554. |
| [9] | Do V T, Tang C Y, Reinhard M, et al. Effects of hypochlorous acid exposure on the rejection of salt, polyethylene glycols, boron and arsenic(V) by nanofiltration and reverse osmosis membranes[J]. Water Research, 2012, 46(16):5217-5223. |
| [10] | An B, Liang Q Q, Zhao D Y. Removal of arsenic(V) from spent ion exchange brine using a new class of starch-bridged magnetite nanoparticles[J]. Water Research, 2011,45(5):1961-1972. |
| [11] | Xu P, Capito M, Cath T Y. Selective removal of arsenic and monovalent ions from brackish water reverse osmosis concentrate[J]. Journal of Hazardous Materials, 2013, 260:885-891. |
| [12] | 席北斗, 王晓伟, 霍守亮, 等. 纳滤膜技术在地下水除砷应用中的研究进展[J]. 环境工程学报, 2012, 2(6):353-360.XI Bei-dou, WANG Xiao-wei, HUO Shou-liang, et al. Investigation progress of arsenic removal from groundwater by nanofiltration membrane technology[J]. Chinese Journal of Environmental Engineering, 2012, 2(6):353-360. |
| [13] | Altun M, Sahinkaya E, Durukan I, et al. Arsenic removal in a sulfidogenic fixed-bed column bioreactor[J]. Journal of Hazardous Materials, 2014, 269:31-37. |
| [14] | Li W G, Gong X J, Wang K, et al. Adsorption characteristics of arsenic from micro-polluted water by an innovative coal-based mesoporous activated carbon[J]. Bioresource Technology, 2014, 165:166-173. |
| [15] | Mertens J, Rose J R M, Kagi R, et al. Adsorption of arsenic on polyaluminum granulate[J]. Environmental Science & Technology, 2012, 46(13):7310-7317. |
| [16] | Feng Y F, Yang F, Wang Y Q, et al. Basic dye adsorption onto an agro-based waste material Sesame hull(Sesamum indicum L.)[J]. Bioresource Technology, 2011, 102(22):10280-10285. |
| [17] | Guo Y W, Zhu Z L, Qiu Y L, et al. Adsorption of arsenate on Cu/Mg/Fe/La layered double hydroxide from aqueous solutions[J]. Journal of Hazardous Materials, 2012, 239/240:279-288. |
| [18] | Zhang C G, Shan C, Jin Y J, et al. Enhanced removal of trace arsenate by magnetic nanoparticles modified with arginine and lysine[J]. Chemical Engineering Journal, 2014, 254:340-348. |
| [19] | Jiang M, Park J K, Shin E W. Lanthanum functionalized highly ordered mesoporous media:implications of arsenate removal[J]. Microporous and Mesoporous Materials, 2004, 75(1):159-168. |
| [20] | Bohlandt A, Schierl R, Diemer J, et al. High concentrations of cadmium, cerium and lanthanum in indoor air due to environmental tobacco smoke[J]. Science of the Total Environment, 2012, 414:738-741. |
| [21] | Zhang L, Zhou Q, Liu J Y, et al. Phosphate adsorption on lanthanum hydroxide-doped activated carbon fiber[J]. Chemical Engineering Journal, 2012, 185:160-167. |
| [22] | Setyono D, Valiyaveettil S. Chemically modified sawdust as renewable adsorbent for arsenic removal from water[J]. ACS Sustainable Chemistry & Engineering, 2014, 2(12):2722-2729. |
| [23] | Feng Y F, Dionysiou D D, Wu Y H, et al. Adsorption of dyestuff from aqueous solutions through oxalic acid-modified swede rape straw:Adsorption process and disposal methodology of depleted bioadsorbents[J]. Bioresource Technology, 2013, 138C:191-197. |
| [24] | 李瑞月, 陈 德, 李恋卿, 等. 不同作物秸秆生物炭对溶液中Pb2+、 Cd2+的吸附[J]. 农业环境科学学报, 2015, 34(5):1001-1008.LI Rui-yue, CHEN De, LI Lian-qing, et al. Adsorption of Pb2+ and Cd2+ in aqueous solution by biochars derived from different crop residues[J]. Journal of Agro-Environment Science, 2015, 34(5):1001-1008. |
| [25] | Mohan D, Sarswat A, Ok Y S, et al. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent a critical review[J]. Bioresource Technology, 2014, 160:191-202. |
| [26] | Yao Y, Gao Bin, Zhang M, et al. Effect of biochar amendment on sorption and leaching of nitrate, ammonium, and phosphate in a sandy soil[J]. Chemosphere, 2012, 89(11):1467-1471. |
| [27] | Liu Y X, Yang M, Wu Y M, et al. Reducing CH4 and CO2 emissions from waterlogged paddy soil with biochar[J]. Journal of Soils and Sediments, 2011, 11(6):930-939. |
| [28] | Wang S G, Gao B, Zimmerman A R, et al. Removal of arsenic by magnetic biochar prepared from pinewood and natural hematite[J]. Bioresource Technology, 2015, 175:391-395. |
| [29] | Lehmann J. A handful of carbon[J]. Nature, 2007, 447(7174):143-144. |
| [30] | Jiang J, Xu R K. Application of crop straw derived biochars to Cu(Ⅱ)contaminated Ultisol:Evaluating role of alkali and organic functional groups in Cu(Ⅱ) immobilization[J]. Bioresource Technology, 2013, 133:537-545. |
| [31] | 于志红, 黄一帆, 廉 菲, 等. 生物炭-锰氧化物复合材料吸附砷(Ⅲ)的性能研究[J]. 农业环境科学学报, 2015, 34(1):155-161.YU Zhi-hong, HUANG Yi-fan, LIAN Fei, et al. Adsorption of arsenic(Ⅲ) on biochar-manganese oxide composites[J]. Journal of Agro-Environment Science, 2015, 34(1):155-161. |
| [32] | Feng Y F, Zhou H, Liu G H, et al. Methylene blue adsorption onto swede rape straw(Brassica napus L.) modified by tartaric acid:Equilibrium, kinetic and adsorption mechanisms[J]. Bioresource Technology, 2012, 125:138-144. |
| [33] | Wang S G, Gao B, Li Y C, et al. Manganese oxide-modified biochars:Preparation characterization, and sorption of arsenate and lead[J]. Bioresource Technology, 2015, 181:13-17. |
| [34] | Zhou X Y, Wei J F, Zhang H, et al. Adsorption of phthalic acid esters(PAEs) by amphiphilicpolypropylene nonwoven from aqueous solution:The study of hydrophilic and hydrophobic microdomain[J]. Journal of Hazardous Materials, 2014, 273:67-69. |
| [35] | Wu D B, Sun Y H, Wang Q G. Adsorption of lanthanum(Ⅲ) from aqueous solution using 2-ethylhexyl phosphonic acid mono-2-ethylhexyl ester-grafted magnetic silica nanocomposites[J]. Journal of Hazardous Materials, 2013, 260:409-419. |
| [36] | Jian M P, Liu B, Zhang G S. Adsorptive removal of arsenic from aqueous solution by zeolitic imidazolate framework-8(ZIF-8) nanoparticles[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2015, 465:67-76. |
| [37] | Honkkanen S, Repo E, Lou S, et al. Removal of arsenic(V) by magnetic nanoparticle activated microfibrillated cellulose[J]. Chemical Engineering Journal, 2015, 260:886-894. |
| [38] | Salameh Y, Albadarin A B, Allen S, et al. Arsenic(Ⅲ, Ⅴ) adsorption onto charred dolomite:Charring optimization and batch studies[J]. Chemical Engineering Journal, 2015, 259:663-671. |
| [39] | Agrafioti E, Kalderis D, Diamadopoulos E. Arsenic and chromium removal from water using biochars derived from rice husk, organic solid wastes and sewage sludge[J]. Journal of Environmental Management, 2014, 133:309-314. |
| [40] | Velickovic Z, Vukovic G D, Marinkovic A D, et al. Adsorption of arsenate on iron(Ⅲ) oxide coated ethylenediamine functionalized multiwall carbon nanotubes[J]. Chemical Engineering Journal, 2012, 181:174-181. |
| [41] | Jun H, Zhu Z L, Lu H T, et al. Effect of metal composition in lanthanum-doped ferric-based layered double hydroxides and their calcined products on adsorption of arsenate[J]. RSC Advances, 2014, 4:5156-5164. |
 2015, Vol. 34
2015, Vol. 34