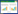文章信息
- 张伟明,管学超,黄玉威,孙大荃,孟军,陈温福
- ZHANG Wei-ming, GUAN Xue-chao, HUANG Yu-wei, SUN Da-quan, MENG Jun, CHEN Wen-fu
- 玉米芯生物炭对大豆的生物学效应
- Biological Effects of Corncob-derived Biochar on Soybean Plants
- 农业环境科学学报, 2015, 34(2): 391-400
- Journal of Agro-Environment Science, 2015, 34(2): 391-400
- http://dx.doi.org/10.11654/jaes.2015.02.025
-
文章历史
- 收稿日期:2014-8-31
我国粮食总产已实现了十连增,伴随而来的是大量农业废弃物的持续攀升,特别是农业废弃物的随意丢弃、焚烧等粗放处理方式使环境污染加剧,成为制约生态环境与农业可持续发展的“瓶颈”[1].目前,对此还没有理想的解决途径.
生物炭(Biochar)通常是指由农林废弃物在缺氧条件下不完全燃烧而产生的一种富碳产物[2],是最近几年迅速发展起来的研究热点之一.由于其具有广泛的原材料来源,独特的结构与理化特性,良好的多功能作用[3, 4],目前已得到学术界、政府及专家们的广泛认可.生物炭技术及其应用,可能是有效解决上述问题的重要可行性措施之一.
生物炭相关理论与应用研究,在国内外已有众多研究进展,但很多研究在制炭设备、工艺、材质和生物炭应用的环境、方式等方面差异较大,使相关试验结果难以进行统一比较,甚至相悖,对农业生产的指导作用和意义有限.研究认为,制炭条件、工艺和材质等是影响生物炭性质及其应用效果的重要因素[5].在设备、工艺方面,大型化、高成本、操控复杂是国外的主要特点,而在国内则普遍存在设备良莠不齐、技术繁杂等特点,与目前我国农业现状相背离,也制约了生物炭的农业应用.特别在制炭材质方面,由于原材料地域来源、元素组成、基本属性等差异,亦使得不同材质生物炭的应用效果迥异.因此,基于我国农业发展现状,开展适时、适地的新型制炭技术及特定材质生物炭的基础与应用技术研究,具有重要意义[6].
国内外众多研究表明,施用生物炭对水稻(Oryza sativa L.)、玉米(Zea mays L.)、小麦(Triticum aestivum L.)、高粱[Sorghum bicolor(L.)Moench]、番茄(Lycopersicon esculentum Mill.)、萝卜(Raphanus sativus L.)等作物生长发育和产量等具有积极作用[7, 8, 9, 10, 11, 12],而对大豆[Glycine max(L.)Merr.]、豌豆(Pisum sativum L.)、绿豆[Vigna radiata(L.)Wilczek]等豆科作物亦有相关研究报道.在火山灰壤土中以500 kg·hm-2标准施用生物炭,发现大豆产量增加了51%[13];在印度德里地区土壤中施用生物炭(500 kg·hm-2),结果发现豌豆的生物量增加了60%,大豆的产量增加了50%,绿豆的产量增加了22%[14].生物炭亦对作物生长和产量表现一定累加或持续效应.在巴西亚马逊河地区土壤中施用生物炭(11 t·hm-2),经过2年4个生长季,水稻和高粱产量累积增加了约75%[15];在哥伦比亚热带草原土壤中施用生物炭(20 t·hm-2),在第1年玉米产量没有明显提高,但在第2、3、4年玉米产量比对照分别提高了28%、30%、140%,持续效应明显[16].
目前,生物炭对作物的促长、增产等效应,已得到了大多数研究结果印证,但也有少数由于用量不当等而产生负效应的报道.当生物炭施用量在0.5 t·hm-2时,作物产量有降低趋势[17];而在火山灰壤土中分别以5 t·hm-2和15 t·hm-2施用生物炭时,大豆产量分别下降了37%和71%[13].生物炭的作物学效应与生态环境,土壤、作物类型,施用量等诸多因素有关,不同材质生物炭的作用效果也不尽一致.目前,有关玉米芯生物炭对东北地区大豆的生物学效应研究很少.
本研究采用适应我国农业国情,具有“低碳、低成本、可移动性强”等突出特点的新型炭化技术设备,以常见农业废弃物--玉米芯为原材料,生产农用玉米芯生物炭材料,并应用于东北大豆生产,旨在明确玉米芯炭结构与理化特性及其对大豆的生物学效应,将生物炭“制备-性质-应用”有效结合,为生物炭的制备技术及农业应用提供基础和依据.
1 材料与方法 1.1 试验材料与地点以大豆(铁丰40,辽宁省铁岭市农业科学院提供)为试验材料,于2010年在沈阳农业大学试验基地进行.土壤为东北典型棕壤土,其基本理化性质为:pH5.46,有机质含量17.8 g·kg-1,全氮含量1.36 g·kg-1,碱解氮含量52.9 mg·kg-1,速效磷含量22.7 mg·kg-1,速效钾含量83.5 mg·kg-1.以玉米芯为原材料,将其自然风干(含水量降至16%以下)后粉碎,粒度为2~5 cm.采用专利炭化技术(ZL201110073104.1),缺氧干馏分解工艺,在亚高温(450 ℃左右)条件下对玉米芯进行炭化.炭化过程中,将玉米芯逐次、分层装入炉内点燃,无需外源加热,调节加料厚度控制氧气供给量,使玉米芯在缺氧状态下受热分解.当温度达到450 ℃左右时,停留约1~2 h,进行充分炭化.出炉后,将玉米芯炭制备为0.05~2 cm的炭颗粒,作为供试生物炭材料.
1.2 试验设计采用大田随机区组试验设计.试验设5个处理,分别为:不施用生物炭,不做任何处理(CK);以750 kg·hm-2标准施用生物炭(C1),以1500 kg·hm-2标准施用生物炭(C2);以3000 kg·hm-2标准施用生物炭(C3);以6000 kg·hm-2标准施用生物炭(C4).
试验小区行长5 m,宽3.6 m,每小区18 m2,3次重复,共计15小区,总面积270 m2.每小区6行,行距0.6 m,株距0.11 m,每穴1株.5月18日播种,大豆播种按当地常规种植方式进行,玉米芯炭于播种前开沟垄施,其后大豆生长期间不再追肥,田间常规管理.
1.3 测定项目与方法 1.3.1 玉米芯生物炭结构与理化性质微观结构表征,采用表面扫描电镜(日本,TM-1000)测定.比表面积、孔容、孔径等采用比表面积分析仪(PS2-0003)测定.主要元素组成采用元素分析仪(德国,Vario Macro Cube)测定,P测定采用钒钼黄比色法,K测定采用火焰光度法[18],微量矿质元素测定采用电感耦合等离子体质谱仪(ICP-MS).pH值参照木质活性炭pH的测定方法(GB/T 12496.7-1999).灰分、挥发分、固定碳,参照木炭和木炭试验方法(GB/T 17664-1999).阳离子交换量(CEC),参照乙酸铵法[18].
1.3.2 大豆生物学性状分别于苗期(6月24日)、开花期(7月26日)、结荚期(8月20日),在田间每小区选取10株代表性植株,调查株高性状.同时,每小区取3株,将地上部叶、茎秆(包括叶柄)等器官分离,在烘箱于105 ℃杀青30 min,然后于80 ℃烘干至恒重,用电子天平称量各器官干物重;光合生理特性,选择在苗期、开花期、结荚期的晴天上午9:00-11:00,每小区选择5株,选取大豆主茎的功能叶片(倒四叶),采用光合仪(美国,LI-6400)测定;营养生理特性,分别于苗期、开花期、结荚期、鼓粒期取主茎倒三叶片,测定叶绿素、可溶性糖、可溶性蛋白含量[19];养分吸收特性,分别于苗期、开花期、结荚期、成熟期每小区取具有代表性大豆3株,茎、叶分离、杀青烘干后用植物粉碎机粉碎待测氮、磷、钾养分.采用H2SO4-H2O2法进行前处理,全N采用元素分析仪(德国,Vario Macro Cube),P采用钒钼黄比色法[18],K采用火焰光度法(英国,M-410)测定.
于成熟期(10月6日),每小区选择去除边行后的中间行,随机抽取具有代表性的10株大豆,风干后进行室内考种.调查株高、茎粗、主茎节数、单株荚数、单株粒数、单株荚重、百粒重等农艺性状和产量构成因素等指标[20].每小区取中间3行,每行取中间3 m,进行小区实际测产.品质指标,脂肪、蛋白质含量于收获后1个月内采用近红外谷物品质分析仪(丹麦,Foss-241)测定.
2 结果与讨论 2.1 玉米芯生物炭结构及主要理化特性 2.1.1 微观结构与孔容、孔径表征炭化前的玉米芯横截面如图 1所示,薄壁组织细胞、维管束等组织结构健全,主维管束较为清晰.经过升温、裂解等炭化过程后,可见原有部分组织(不稳定、易挥发部分)消失或形成微小孔隙,形成炭化木质素等支撑起的多孔炭架结构,原有主体结构得到了保留,其外围轮廓清晰,层次分明,微孔丰富(图 2).本试验所采用的炭化技术属于常规热解,在炭化过程中有一个相对缓慢的升温、热解过程,不会发生快速热解裂变.因此,部分不稳定、易受热挥发组织逐渐热解消失或产生微孔,形成丰富的多孔炭架构型.

|
| 图 1 玉米芯微观表面扫描(炭化前) Figure 1 SEMmicrograph of corncob(Before carbonization) |

|
| 图 2 玉米芯炭微观表面扫描(炭化后) Figure 2 SEMmicrograph of corncob-biochar(After carbonization) |
这种丰富的多微孔结构,使生物炭具备了比表面积大、吸附能力强等特性,在土壤中可吸附更多有机物质、养分离子等,对土壤肥力及微生态环境等产生积极作用[3, 4, 7, 16].
如表 1所示,玉米芯的孔容、孔径表征在炭化前、后发生了明显变化.玉米芯的总孔体积在炭化后比炭化前提高了5.54倍.而在不同孔形中,圆筒孔与平行孔(较大型孔)分别提高了5.1倍和5.31倍,微孔体积则提高了4.67倍.平均孔直径,在炭化后提高了0.51倍,孔径变大.不同孔容体积,特别是微孔体积的大幅提升,对提高其总体比表面积与吸附力有重要作用,其表征大小与原材料结构、组成及炭化条件等因素相关[5].
如表 2所示,玉米芯的理化性质在炭化前、后发生了明显变化.pH在炭化后提高了4.85,增幅近1倍,由酸性变为强碱性,与生物炭所含有的表面-COO-和-O-等有机官能团及碳酸盐总量有关[21].比表面积(BET多点法)、固定碳含量、灰分含量在炭化后比炭化前分别提高了3.74、5.03、0.26倍.但挥发成分含量则降低了近75%,可能与炭化过程中易挥发、分解组织等的大量损失有关.玉米芯炭具有一定阳离子交换量,表明其表面含有较为活跃的官能团.
此外,如表 3所示,玉米芯炭还含有丰富的元素种类,尤其含有作物生长发育所必需的大量营养元素(N、P、K)和一些微量矿质元素(Mg、Fe、Ca)等.在不同元素中,C含量最高,N、P、K次之,S、Ca、Si也相对较高.高含C量、高度羧酸酯化和芳香化结构[22, 23],使玉米芯炭在土壤中不易被分解而可以实现稳定的“碳封存”.
玉米芯炭所含有的N、P、K、S以及微量生长调节元素Mg、Fe、Ca等,则可能在特定条件下有一定释放,从而为作物生长提供一定养分来源[24].玉米芯炭的元素种类及含量,与原材料所含元素种类、组成及炭化条件等密切相关[5].
综上可知,玉米芯生物炭具有丰富的多微孔结构及元素种类,呈碱性、碳含量高、比表面积大,为其在改良土壤、促进作物生长等方面奠定了重要的结构与理化特性基础.
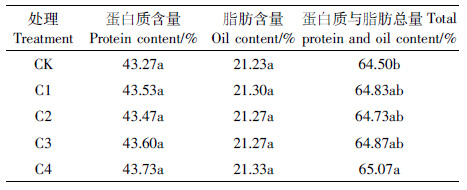
2.2 玉米芯生物炭对大豆生物学性状的影响 2.2.1 对株高与干物质积累的影响如表 4所示,在苗期、开花期与结荚期,玉米芯炭处理的株高均大于对照,表现为随炭量增加而提高且趋势明显.茎、叶干物质积累,玉米芯炭处理在生长前期影响不大,但随着生育期推移,逐渐大于对照.除开花期C1处理的叶干重略小于对照外,其余时期玉米芯炭处理均大于对照,在结荚期高施炭量(C4)处理比对照提高了28.05%.而除苗期与结荚期的C1处理外,其余玉米芯炭处理的茎干重均大于对照.在开花期,随炭量增加而增大,较高施炭量(C3、C4)的茎干重与对照差异显着.
 |
玉米芯炭对大豆株高、地上部干物质积累表现出一定的促进作用,这与其结构及理化特性有关.生物炭质轻而多微孔,施入土壤可降低容重[25],改善土壤水、气状况[25],利于促进根系生长[26],提高作物对水分、养分等的吸收利用[27, 28].土壤物理性状改善,水、肥协调,尤其是对根系的良好作用,有利于促进作物生长发育,从而对株高、茎叶干物质积累表现促进效应.而在数量和调控强度上,显然高施炭量的作用更大,效应也更明显.
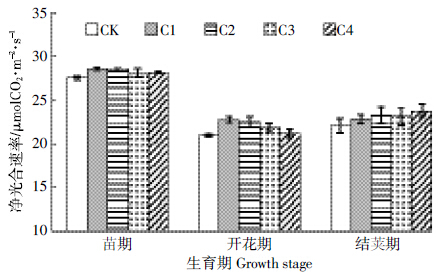
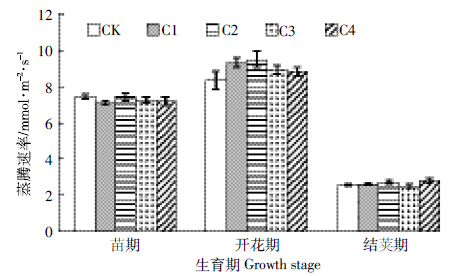
2.2.2 对主要生理特性的影响 2.2.2.1 对光合生理的影响由图 3可见,在苗期和开花期,玉米芯炭处理的净光合速率均高于对照,表现随炭量减少而提高的趋势,其中较低施炭量处理(C1、C2)与对照差异显着,在结荚期玉米芯炭处理的净光合速率仍高于对照,但无显着差异.由图 4可见,在苗期除C2处理外,其余玉米芯炭处理的蒸腾速率均低于对照,在开花期玉米芯炭处理均高于对照,在结荚期除C3处理略低于对照外,其余玉米芯炭处理的蒸腾速率均高于对照.在全生育期,各处理间无显着差异.
|
| 图 3 玉米芯炭对大豆主要生育期净光合速率的影响 Figure 3 Effects of corncob-biochar on net photosynthetic rates of soybean at major growth stages |
|
| 图 4 玉米芯炭对大豆主要生育期蒸腾速率的影响 Figure 4 Effects of corncob-biochar on transpiration rates of soybean at major growth stages |
在苗期,表现高光合与低蒸腾速率协同,利于增加光合产物积累,促进植株生长;而在开花期与结荚期,表现高光合与高蒸腾速率协同,利于提高光合作用效率,促进光合产物形成、积累与分配.玉米芯炭对光合生理进程表现促进效应,对提升光合生产潜力,实现增产有重要意义.
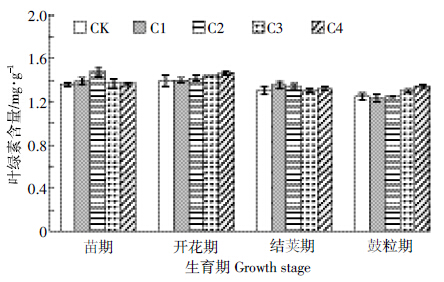
2.2.2.2 对营养生理的影响玉米芯炭对叶绿素含量的影响见图 5.在苗期,玉米芯炭处理均高于对照,其中C2处理与对照差异显着;在开花期与结荚期,玉米芯炭处理均高于对照,但差异不显着;至鼓粒期,表现为C4>C3>CK>C2>C1,随炭量增加而提高,其中C3、C4处理与对照差异显着.可见,较高施炭量对提高生长后期叶片叶绿素含量,延缓衰老,提高光合能力有重要作用.
|
| 图 5 玉米芯炭对大豆不同生育期叶绿素含量的影响 Figure 5 Effects of corncob-biochar on chlorophyll contents of soybean at different growth stages |
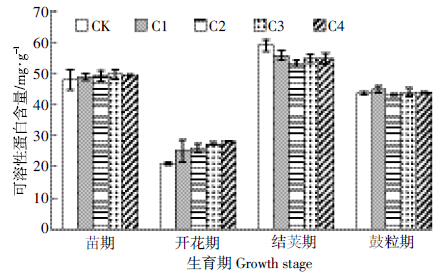
玉米芯炭对叶片可溶性蛋白含量的影响见图 6.在苗期与开花期,玉米芯炭处理均高于对照,且随炭量增加而提高.其中在开花期,C4、C3处理分别比对照提高了33.10%、29.50%,且差异显着.而在结荚期玉米芯炭各处理均小于对照,到鼓粒期除C2处理外,其余玉米芯炭处理均高于对照,但无显着差异.
|
| 图 6 玉米芯炭对大豆不同生育期可溶性蛋白含量的影响 Figure 6 Effects of corncob-biochar on soluble protein contents of soybean at different growth stages |
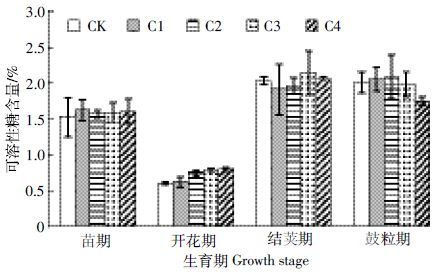
玉米芯炭对叶片可溶性糖含量的影响见图 7.在苗期、开花期,玉米芯炭处理均高于对照.其中,在开花期,随炭量增加而提高,C4、C3、C2处理与对照差异显着.在结荚期较高施炭量(C3、C4)高于对照,而在鼓粒期较低施炭量(C1、C2)高于对照,其余玉米芯炭处理均低于对照,但差异不显着.
|
| 图 7 玉米芯炭对大豆不同生育期可溶性糖含量的影响 Figure 7 Effects of corncob-biochar on soluble sugar contents of soybean at different growth stages |
光合作用是作物生长过程最重要的生理进程之一,直接决定了作物产量和品质等重要性状,其大小与地上部生长量、叶绿素含量、代谢产物供给等密切相关[29].本试验中,玉米芯炭处理的各生育期茎、叶干物质积累增加,为提高植株光合能力奠定了物质基础;而叶绿素含量的提高,则为叶片进行光化学反应提供了重要生理基础;特别是生物炭对土壤水、肥、气、热条件的改善[5, 7, 8, 9, 16, 24],以及对根系生长的积极影响[26],为营养物质的合成、转运、分配等生理进程提供了水分、矿物质元素等基础物质保障.因此,在不同生育期提高了净光合速率,并在营养、生殖生长阶段与蒸腾速率表现出良好协同作用.
可溶性蛋白、可溶性糖是作物生长过程中物质合成、代谢、信号传导、基因功能表达等生理过程顺利进行的重要基础[30].在大豆生长前期,玉米芯炭处理的可溶性蛋白与可溶性糖均呈上升趋势,但在后期有所下降,呈现一定波动性.这与作物的自身调控和适应性有关.在生长前期处于营养生长阶段,需要更多的可溶性蛋白、可溶性糖用于物质合成、积累,以满足不同生理进程的代谢需求,因而会提高其代谢强度和水平;而在生长后期处于生殖生长阶段,由“源”积累转向“库”输出,叶片可溶性蛋白、可溶性糖将优先用于荚、粒等生殖生长需要,从而进行大量转移、输出,因而表现下降趋势.这也表明,玉米芯炭作为外源输入物质,对可溶性蛋白、可溶性糖的调控作用和趋势,符合作物自身生长特性.特别在开花期,玉米芯炭显着提高了可溶性蛋白、可溶性糖含量,而这一时期正值作物对营养物质需求最为旺盛、关键的时期,玉米芯炭的作用显然契合了这一生长阶段的内在需求,故调控能力增强.另一方面,作物生理进程的体现是一系列由“外因”-“内因”反应过程的充分表达,玉米芯炭显然在这一过程中起到了正向、积极作用.研究认为,生物炭的输入会促进微生物,特别是一些有益菌群的生长与繁殖[31].微生物活动增强将促进土壤理化反应进程,诱导产生更多新的有机代谢产物及根系分泌物等,对作物生理进程产生一定影响.此外,研究发现生物炭含有的较高灰分,在水土交融、微生物等作用下会释放一些小分子类物质(相关结果另文发表),也可能在一定程度上调控或干预植物某些蛋白合成、基因表达等基础生化过程,从而影响植物生理进程.
2.2.3 对大豆养分吸收特性的影响 2.2.3.1 对氮的影响如表 5所示,除结荚期C2处理外,其他不同生育期玉米芯炭处理的叶片氮含量均高于对照;在开花期,C2、C3、C4处理与对照差异显着,作用明显;至成熟期,玉米芯炭处理平均比对照提高20.33%,C1、C2、C4处理与对照差异显着.在苗期,玉米芯炭处理的茎秆氮含量显着高于对照,平均提高29.58%,可见,玉米芯炭对促进苗期茎秆氮吸收有重要作用;在开花期,除C2处理外,其余玉米芯炭处理均高于对照,但差异不显着;在结荚期,C2、C4处理高于对照,而C1、C3处理低于对照,但无显着差异;在成熟期,表现为C1>C2>CK>C4>C3,其中C1处理与对照差异显着,低施炭量的作用明显.
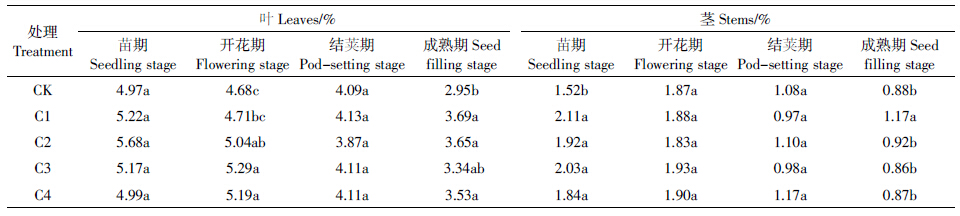 |
玉米芯炭对叶片氮吸收有一定促进作用,但对茎秆氮吸收的影响表现不同,即在前期明显,中、后期影响不大.
2.2.3.2 对磷的影响如表 6所示,在苗期与开花期,除C3处理外,其余玉米芯炭处理均低于对照,但差异不显着;在结荚期,玉米芯炭处理均高于对照,随炭量增加而提高;至成熟期,玉米芯炭处理均低于对照,随炭量增加而减少,其中C2、C3、C4处理与对照差异显着.
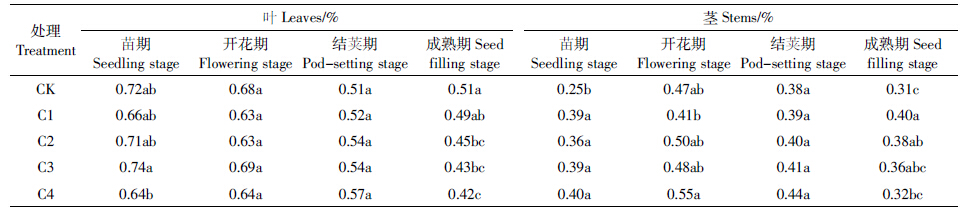 |
在苗期,玉米芯炭处理的茎秆磷含量均高于对照,且差异显着,对促进茎秆磷吸收的作用明显;在开花期,除C1处理略低于对照外,其余玉米芯炭处理均高于对照,其中C4处理比对照提高了15.65%;在结荚期,玉米芯炭处理均高于对照,随炭量增加而提高,但在成熟期随炭量增加而降低,其中C1、C2处理与对照差异显着.
玉米芯炭对叶片磷吸收的影响不大,但对茎秆磷吸收有一定促进作用,在前期高施炭量作用明显,而在后期低施炭量作用更明显.
2.2.3.3 对钾的影响如表 7所示,在苗期,玉米芯炭处理的叶片钾含量均高于对照,其中C4处理与对照差异显着,高施炭量作用明显;在开花期,玉米芯炭处理均低于对照,而在结荚期与成熟期,玉米芯炭处理则均高于对照,但差异不显着.在苗期,玉米芯炭处理的茎秆钾含量均高于对照,其中C1、C4处理与对照差异显着;在开花期,玉米芯炭处理均低于对照,而在结荚期,则表现为C1、C2处理高于对照,而C4、C3处理低于对照,差异不显着;至成熟期,玉米芯炭处理均高于对照,随炭量增加而提高,其中C4处理比对照提高了14.32%.
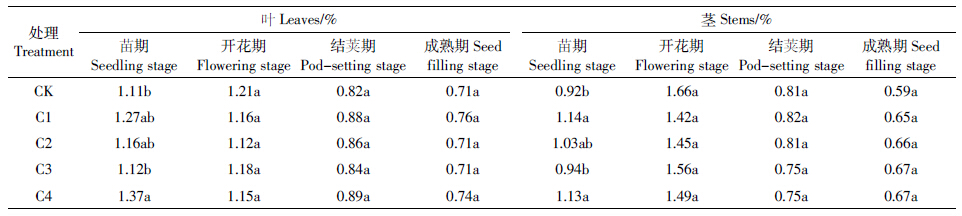 |
玉米芯炭对生长前期叶片、茎秆的钾吸收有一定促进作用,而对其余时期没有明显影响.
在不同生育期,玉米芯炭对大豆生长前期叶、茎的氮、磷、钾吸收影响明显大于后期,呈现前促后控的趋势.这与作物自身生长的营养需求和分配特性有关.在生长前期,是作物对氮、磷、钾养分需求的临界、关键期,大量养分将集中、优先输送至茎、叶生长点,以满足生长发育需要;而在后期,氮、磷、钾等养分将由叶、茎生长“源”转向荚、粒生长“库”,进行养分重新分配、转移,以满足生殖生长期需求.因而在不同时期表现不同,从大豆不同生育期的茎、叶不同部位对氮、磷、钾的吸收来看,玉米芯炭起到了一定促进作用.这与其结构和理化特性有关.很多研究表明,生物炭对氮、磷等养分离子有一定吸附作用[15, 32],可减少养分流失,从而为作物不同生育期提供更多适时养分,促进植株养分吸收.由于生物炭中所含有的氮、磷、钾等养分在特定条件下有一定程度的释放[33, 34],本试验中玉米芯炭的氮、磷、钾含量相对较高,可能释放并为大豆生长补充一定外源养分.另外,生物炭丰富的孔隙结构和所含有的碳、氮元素,为微生物生长提供了良好的生长空间及养分、能量来源,而对微生物数量、群落结构、功能等产生积极影响[35, 36, 37].微生物数量及活动能力增强,有利于增加土壤有机质含量,提高总体肥力,为作物生长提供更多养分.此外,土壤水、肥、气、热等微生态环境条件的改善以及根系的良好生长,也将进一步促进氮、磷、钾养分的吸收、运转和分配,从而增强地上部茎、叶养分吸收.
2.2.4 对大豆产量与品质的影响 2.2.4.1 对产量及其构成因素的影响如表 8所示,大豆单株荚数、单株粒数、单株粒重均表现为C3>C4>C2>C1>CK.C3、C4、C2、C1处理的单株荚数分别比对照提高了20.88%、15.74%、9.37%、7.27%,平均提高13.31%;单株粒数分别比对照提高了23.85%、19.65%、16.15%、12.45%,平均提高18.03%;单株粒重分别比对照提高了24.43%、20.63%、13.90%、10.10%,平均提高17.26%.可见,玉米芯炭对提高大豆单株荚数、单株粒数、单株粒重有促进作用,较高施炭量(C3、C4)的作用更大.但从百粒重来看,玉米芯炭没有明显影响.小区产量表现为C3>C4>C2>C1>CK,C3、C4、C2、C1处理分别比对照提高了11.54%、10.41%、8.25%、2.68%,平均提高了8.22%,其中C3处理与对照差异显着.
玉米芯炭在提高了大豆单株荚数、单株粒数、单株粒重基础上,表现增产效应,其中较高施炭量(C3、C4)的作用明显.
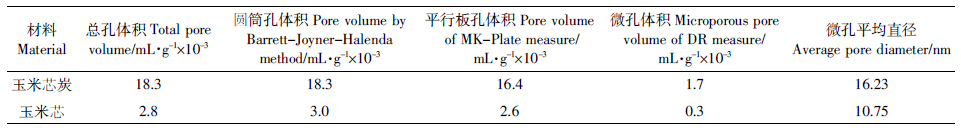
2.2.4.2 对品质的影响如表 9所示,玉米芯炭处理的大豆蛋白质与脂肪含量均高于对照,其中高施炭量(C4)表现相对较高,但无显着差异.蛋白质与脂肪总量表现为C4>C3>C1>C2>CK,其中高施炭量处理(C4)与对照差异显着.可见,高施炭量有利于提高大豆蛋白质与脂肪总量,提升大豆品质.
玉米芯炭对大豆产量与品质的良好作用,来源于生物炭对土壤结构,水、肥、气、热以及微生物等土壤生态环境的调控与改善,为大豆生长发育提供了良好外界生长环境条件,因而促进了茎、叶干物质积累,提高了光合速率,增强了营养物质合成与氮、磷、钾养分吸收,为最终产量和品质形成奠定了良好的物质、养分和生理基础,表现增产提质效应.在不同施炭量处理中,高施炭量在不同时期株高、干物质积累、营养生理、养分吸收等方面均优于其他处理,因而在产量、品质上表现相对较好.从不同生育期来看,较高施炭量处理表现一定持续、累加效应,可能与生物炭的稳定性有关.生物炭具有多微孔碳架,高度羧酸酯化、芳香化结构和高C量,使得其比其他任何形式的有机碳都更具有生物化学、热稳定性[38],因而可在土壤中长期存在并持续发挥作用.
生物炭对作物生长的影响与材质、环境条件等密切相关,也因此体现出不可预测的复杂性与特殊性,其与土壤、作物的互作关系、过程、机制等,还有待进一步深入研究探索.
3 结论(1)采用新型炭化技术,亚高温(450 ℃)缺氧干馏条件下制备的玉米芯生物炭,其微孔结构丰富,呈碱性,比表面积、总孔体积、固定碳含量、灰分含量较炭化前大幅度提高,含较高的C及作物生长所必需的营养元素,具有良好的结构与理化特性,是可应用于农业、环境等领域的一种理想的农用生物炭材料.
(2)玉米芯炭对大豆株高,茎、叶干物质积累,光合生理、营养生理及氮、磷、钾养分吸收等生物学性状有一定积极影响,最终产量明显提高.施用玉米芯炭(1500、3000 kg·hm-2)的增产效果良好.
(3)东北典型棕壤条件下,玉米芯炭可应用于大豆生产,且具有较好的应用前景.
| [1] | 孙振钧, 孙永明. 我国农业废弃物资源化与农村生物质能源利用的现状与发展[J]. 中国农业科技导报, 2006, 8(1):6-13. SUN Zhen-jun, SUN Yong-ming. Review of China agricultura science and technology situation and development of agricultural residues as energy resource utilization in rural areas in China[J]. Journal of Agricultural Science and Technology, 2006, 8(1):6-13. |
| [2] | Antal Jr M J, Gronli M. The art, science and technology of charcoal production[J]. Industrial and Engineering Chemistry, 2003, 42(8):1619-1640. |
| [3] | Lehmann J. A handful of carbon[J]. Nature, 2007, 447:143-144. |
| [4] | Kleiner K. The bright prospect of biochar[J]. Nature Reports-Climate Change, 2009, 3(6):72-74. |
| [5] | Ma?ek O, Brownsort P, Cross A, et al. Influence of production conditions on the yield and environmental stability of biochar[J]. Fuel, 2013, 103:151-155. |
| [6] | 陈温福, 张伟明, 孟 军. 生物炭与农业环境研究回顾与展望[J]. 农业环境科学学报, 2014, 33(5):821-828. CHEN Wen-fu, ZHANG Wei-ming, MENG Jun. Advances and prospects in research of biochar utilization in agriculture[J]. Journal of Agro-Environment Science, 2014, 33(5):821-828. |
| [7] | Macdonald L M, Farrell M, Van Zwieten L, et al. Plant growth responses to biochar addition:An australian soils perspective find out how to access preview-only content[J]. Biology and Fertility of Soils, 2014, 50(7):1035-1045. |
| [8] | Liu X Y, Zhang A F, Ji C Y, et al. Biochar's effect on crop productivity and the dependence on experimental conditions a meta-analysis of literature data[J]. Plant and Soil, 2013, 373(1-2):583-594. |
| [9] | Zhao X, Wang J W, Wang S Q, et al. Successive straw biochar application as a strategy to sequester carbon and improve fertility:A pot experiment with two rice/wheat rotations in paddy soil[J]. Plant and Soil, 2014, 378(1-2):279-294. |
| [10] | Dong D, Yang M, Wang C, et al. Responses of methane emissions and rice yield to applications of biochar and straw in a paddy field[J]. Journal of Soils and Sediments, 2013, 13(8):1450-1460. |
| [11] | Partey S T, Preziosi R F, Robson G D. Short-term interactive effects of biochar, green manure, and inorganic fertilizer on soil properties and agronomic characteristics of maize[J]. Agricultural Research, 2014, 3(2):128-136. |
| [12] | Chan K Y, Van Zwieten L, Meszaros I, et al. Agronomic values of green waste biochar as a soil amendment[J]. Australian Journal of Soil Research, 2007, 45(8):629-634. |
| [13] | Kishimoto S, Sugiura G. Charcoal as a soil conditioner[J]. International Achievements for the Future, 1985, 5:12-23. |
| [14] | Iswaran V, Jauhri K S, Sen A. Effect of charcoal, coal and peat on the yield of moong, soybean and pea[J]. Soil Biology and Biochemistry, 1980, 12(2):191-192. |
| [15] | Steiner C, Teixeira W G, Lehmann J, et al. Long term effects of manure, charcoal and mineral fertilization on crop production and fertility on a highly weathered Central Amazonian upland soil[J]. Plant and Soil, 2007, 291(1-2):275-290. |
| [16] | Major J, Rondon M, Molina D, et al. Maize yield and nutrition during 4 years after biochar application to a Colombian savanna oxisol[J]. Plant and Soil, 2010, 333(1-2):117-128. |
| [17] | Glaser B, Haumaier L, Guggenberger G, et al. The "Terra Preta" phenomenon:A model for sustainable agriculture in the humid tropics[J]. Naturwissenschaften, 2001, 88(1):37-41. |
| [18] | 鲍士旦. 土壤农化分析[M]. 北京:中国农业科技出版社, 2000:241-294. BAO Shi-dan. Agricultural soil analysis[M]. Beijing:China Agriculture Press, 2000:241-294. |
| [19] | 李合生. 植物生理生化实验原理和技术[M]. 北京:高等教育出版社, 2000:130-201. LI He-sheng. Principles and techniques of plant physiological biochemical experiment[M]. Beijing:Higher Education Press, 2000:130-201. |
| [20] | 邱丽娟, 常汝镇. 大豆种质资源描述规范和数据标准[M]. 北京:中国农业出版社, 2006:2-95. QIU Li-juan, CHANG Ru-zhen. Descriptors and data standard for soybean[M]. Beijing:China Agriculture Press, 2006:2-95. |
| [21] | Yuan J H, Xu R K, Zhang H. The forms of alkalis in the biochar produced from crop residues at different temperatures[J]. Bioresource Tech-nology, 2011, 102(3):3488-3497. |
| [22] | Joseph W J, Pignatello J J. Sorption hystersis of benzene in charcoal particles[J]. Environmental Science and Technology, 2003, 37(2):409-417. |
| [23] | Kramer R W, Kujawinski E B, Hatcher P G. Identification of black carbon derived structures in a volcanic ash soil humic acid by Fourier transform ion cyclotron resonance mass spectrometry[J]. Environmental Science Technology, 2004, 38(12):3387-3395. |
| [24] | Laird D A, Fleming P, Davis D D, et al. Impact of biochar amendment on the quality of a typical midwestern agricultural soil[J]. Geoderma, 2010, 158(3-4):443-449. |
| [25] | Oguntunde P G, Abiodun B J, Ajayi A E. Effects of charcoal production on soil physical properties in Ghana[J]. Joumal of Plant Nutrient and soil Science, 2008, 171(4):591-596. |
| [26] | 张伟明, 孟 军, 陈温福, 等. 生物炭对水稻根系形态与生理特性及产量的影响[J]. 作物学报, 2013, 39(8):1445-1451. ZHANG Wei-ming, MENG Jun, CHEN Wen-fu, et al. Effect of biochar on root morphological and physiological characteristics and yield in Rice[J]. Acta Agronomica Sinica, 2013, 39(8):1445-1451. |
| [27] | Akhtar S S, Li G T, Andersend M N, et al. Biochar enhances yield and quality of tomato under reduced irrigation[J]. Agricultural Water Management, 2014, 138:37-44. |
| [28] | Robertso F A, Thorbum P J. Management of sugarcane harvest residues:Consequences for soil carbon and nitrogen[J]. Australian Journal of Soil Research, 2006, 45(1):13-23. |
| [29] | Sharkey T D. Advances in photosynthesis and respiration photosynthesis research[J]. Photosynthesis Research, 2012, 111:327-329. |
| [30] | Koch K E, Ying Z, Wu Y, et al. Multiple paths of sugar-sensing and a sugar/oxygen overlap for genes of sucrose and ethanol metabolism[J]. Journal of Experimental Botany, 2000, 51:417-427. |
| [31] | Simone E K, Kevin J F, Mathew E D. Effect of charcoal quantity on microbial biomass and activity in temperate soils[J]. Soil Science Society of America Journal, 2009, 73(4):1173-1181. |
| [32] | Mizuta K, Matsumoto T, Hatate Y, et al. Removal of nitrate-nitrogen from drinking water using bamboo powder charcoal[J]. Bioresource Te-chnology, 2004, 95(3):255-257. |
| [33] | Glaser B, Lehmann J, Zech W. Ameliorating physical and chemical properties of highly weathered soils in the tropics with charcoal:A review[J]. Biology and Fertility of Soils, 2002, 35(4):219-230. |
| [34] | Amymarie A D, Gschwend P M. Assessing the combined roles of natural organic matter and black carbon as sorbents in sediments[J]. Environmental Science & Technology, 2002, 36(1):21-29. |
| [35] | Kim J S, Sparovek G, Longo R M, et al. Bacterial diversity of terra preta and pristine forest soil from the Western Amazon[J]. Soil Biology and Biochemistry, 2007, 39(2):684-690. |
| [36] | Rondon M, Lehmann, J, Ramírez J, et al. Biological nitrogen fixation by common beans(Phaseolus vulgaris L.) increases with biochar additions[J]. Biology and Fertility of Soils, 2007, 43(6):699-708. |
| [37] | Warnock D D, Lehmann J, Kuyper T W, et al. Mycorrhizal responses to biochar in soil concepts and mechanisms[J]. Plant and Soil, 2007, 300(1-2):9-20. |
| [38] | 陈温福, 张伟明, 孟 军. 农用生物炭研究进展与前景[J]. 中国农业科学, 2013, 46(16):3324-3333. |
 2015, Vol. 34
2015, Vol. 34