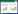文章信息
- 银子毅, 杨新瑶, 陈芳敏, 邓仕槐, 杨悦锁
- YIN Zi-yi, YANG Xin-yao, CHEN Fang-min, DENG Shi-huai, YANG Yue-suo
- EDTA对饱和多孔介质中纳米银迁移机制的影响
- Influence of EDTA on Transport of Silver Nanoparticles in Saturated Porous Media
- 农业环境科学学报, 2015, 34(8): 1569-1574
- Journal of Agro-Environment Science, 2015, 34(8): 1569-1574
- http://dx.doi.org/10.11654/jaes.2015.08.020
-
文章历史
- 收稿日期:2015-02-18
2. 沈阳大学区域污染环境生态修复教育部重点实验室, 沈阳 110044
2. MoE Key Lab for Eco-restoration of Regional Contaminated Environment, Shenyang University, Shenyang 110044
纳米银具有优良的光电学性质及良好的抗菌性能,被广泛应用于各个行业,其产量在全球呈持续上升趋势[1]。大规模的应用使纳米银不可避免地进入环境体系,并最终进入到地下水中[2]。研究结果表明,纳米银对植物、细菌等会产生不同程度的毒副作用[3]。在地下水中,纳米银的迁移能力直接影响其毒性效应的发挥。由于纳米银比表面积巨大,极易吸附土壤地下水中存在的其他环境物质,如持久性有机污染物、微生物、重金属等,并受此类物质的影响改变自身在环境中的迁移能力,从而导致污染距离及污染范围的变化,进一步威胁生态环境的安全[4, 5]。因此,探讨纳米银在含水层中自身迁移规律及其与其他环境物质协同迁移过程和受影响机制,对全面了解纳米银在环境中的运移、归趋特征有着重大意义。
工程中通常使用大分子有机聚合物(如 PVP)或电解质(如柠檬酸盐)修饰纳米银表面,二者分别通过空间位阻效应和双电层效应提高纳米银颗粒在水溶液中的分散性能(稳定性)。这些表面修饰剂对纳米银在饱和多孔介质中的迁移和沉降具有重要的控制作用[6, 7]。Yang等[8]发现含硫氢根的有机分子(如半胱氨酸)能与银形成稳定的化学键,并置换纳米银表面的聚合物,从而削减聚合物涂层对纳米银迁移的控制效果。
虽然EDTA(乙二胺四乙酸)不含硫氢根,但其对包括银在内的多种金属元素都具有极强的络合能力,被广泛用于土壤重金属修复中[9]。Yang等[10]发现 EDTA 能在柱实验时间尺度内络合并溶解砂介质表面的铁氧化物涂层,从而改变胶体颗粒的迁移能力。那么EDTA 能否置换纳米银表面的聚合物并改变其迁移能力?EDTA 与铁氧化物涂层砂介质的相互作用对纳米银的迁移有何影响?这些疑问目前尚未见明确解答报道。
本文选用石英砂及铁氧化物石英砂两种介质作为饱和柱实验的填料,以离子强度为1 mmol·L-1及 300 mmol·L-1的硝酸钠溶液分别模拟地下淡水及咸水,通过纳米银与EDTA的混合批实验研究EDTA对纳米银表面聚合物涂层的置换作用,通过三脉冲柱实验研究不同离子强度下,EDTA对纳米银在不同砂介质中迁移的影响。研究结果对探明纳米银在有机物污染地下水中的迁移转化过程具有重要意义。 1 材料与方法 1.1 实验材料 1.1.1 多孔介质及其制备
使用分样筛(60目及100目,企航仪器,成都)筛选出粒径范围150~250 μm的石英砂(纯度99.9%,密度2.2 g·cm-3,明盛石英砂厂,江苏)以模拟含水层介质。将石英砂用浓度为 12 mol·L-1的盐酸浸泡 24 h 后用高纯水洗净至pH=7,以去除石英砂表面的金属氧化物[11],之后90 ℃烘干备用。
铁氧化物涂层砂采用Yang等[10]的方法制备:将纯净石英砂置入浓度为 1.5 mol·L-1的氯化铁(AR,科龙试剂,成都)溶液中浸泡30 min,过滤后35 ℃空气干燥 2~3 h,随后使用浓度为 3 mol·L-1的氨水(AR,科龙试剂,成都)浸泡 30 min,60 ℃烘烤过夜。将所得铁氧化物涂层砂置入高纯水中超声(KH-800KDE,禾创,昆山)清洗,直至清洗液基本无色以除去砂面松散的铁氧化物涂层,55 ℃烘干后置于清洁干燥处密封保存,备用。 1.1.2 背景溶液
采用离子强度为1 mmol·L-1及300 mmol·L-1的背景溶液代表地下淡水及地下咸水环境,使用硝酸钠(AR,科龙试剂,成都)调节离子强度。所有溶液在实验前使用超声波清洗仪-真空泵[SHZ D(Ⅲ),予华,巩义]联合脱气 30 min以除去微小气泡[8]。 1.1.3 纳米银悬浮液制备与表征
供试纳米银悬浮液制备方法[8]:将 20 g PVP(PVPK30,AR,科龙试剂,成都)及1.5 g硝酸银(AR,科龙试剂,成都)先后溶解于 50 mL 乙二醇(AR,科龙试剂,成都)中,140 ℃恒温油浴(HH-S,金坛新瑞,江苏)加热24 h。将上述试液1∶10 稀释于高纯水中,15 000×g离心(Allegra 64R,Beckman,CA,USA)1 h 后去上清液并将沉淀重新分散于高纯水中,重复离心过程 3 次,以除去游离的 PVP,得到纳米银贮备液。用杜克大学纳米中心(Duke CEINT)制备的纳米银标准储备液制作标准曲线,用紫外可见分光光度法(UV-Vis,U-2910,HITACHI,TYO,JPN)测得纳米银贮备液浓度为 1500 mg·L-1。供试纳米银悬浮液使用相应背景溶液进行稀释。
纳米银颗粒的形态与粒径分别使用透射电镜(TEM,Tecnai G2 Twin,FEI,OR,USA)与动态激光粒度分析仪(DLS,90 Plus,Brookhaven,NY,USA)进行表征。 1.2 EDTA 对纳米银粒径及吸光度变化的影响
使用DLS测定 1 mmol·L-1及 300 mmol·L-1离子强度下浓度为 1.5 mg·L-1的纳米银与浓度为1 mmol·L-1的EDTA(AR,科龙试剂,成都)混合后粒径随时间的变化情况,测定时间为混合后5、30、60、120 min。
使用紫外分光光度计测定 1 mmol·L-1及300 mmol·L-1离子强度下浓度为 15 mg·L-1的纳米银与浓度为 10 mmol·L-1的EDTA混合后在 425 nm 处吸光度值随时间的变化,测定时间为混合后1、20、30、60、90、120 min。 1.3 纳米银三脉冲饱和砂柱实验
实验分为两组:(1)以纯净石英砂作为饱和多孔介质,考察不同离子强度下(1 mmol·L-1和300 mmol·L-1)EDTA对纳米银迁移行为的影响;(2)以1 mmol·L-1为背景离子强度,考察不同类型饱和多孔介质(纯净石英砂和铁氧化物涂层砂)中EDTA 对纳米银迁移及沉积的影响。
所用填充玻璃柱(C10/10,GE Healthcare,Piscataway,NJ)内径 1 cm,柱内多孔介质使用低频超声湿法填充,砂粒分布均匀紧密,填充长度为3 cm,填充质量为3.25 g,计算得出孔隙体积约为 0.89 mL[8]。实验装置如图 1 所示。实验前用蠕动泵(BF-100,雷弗,保定)向砂柱内通入 60个孔隙体积(Pore volume,PV)的背景溶液以稳定实验条件。实验采用底部进样的方式通入所有液体,以消除重力对水流速度的干扰。纳米银注入砂柱前,使用超声波清洗仪超声分散。
|
| 图 1 实验装置示意图 Figure 1 Schematic illustration of experimental setup |
三脉冲实验方式由Yang等[21]开发,步骤如下:第 1 脉冲向砂柱中注入9 PV纳米银悬浮液,第 2 脉冲注入15 PV EDTA溶液,第 3脉冲再次注入9 PV纳米银悬浮液;每个脉冲后均注入9 PV背景溶液,对孔隙水中的纳米银颗粒或EDTA进行充分淋洗。全程溶液流速恒定为 1 mL·min-1,纳米银悬浮液浓度为15 mg·L-1,EDTA 浓度为 1 mmol·L-1。每组实验重复 3 次以评价系统误差范围。球形或近球形纳米银颗粒表面等离子体共振吸收出现在 425 nm 附近[12],在同一体系中,吸收值与纳米银颗粒浓度呈线性关系,故流出液纳米银浓度使用 UV-Vis 在波长为 425 nm 处的吸光度值来表征,过柱前的纳米银浓度标记为 C0,过柱后纳米银浓度记为 C,以 PV 为横坐标,C/C0为纵坐标,生成纳米银的穿透曲线(Breakthrough curve,BTC)。 2 结果与讨论 2.1 纳米银的表征
使用 TEM 观察了制备后 3 d及 90 d的纳米银在高纯水中的粒径分布及分散情况。所获图像显示纳米银粒径约 40 nm,粒径分布范围较窄,分散良好,长时间放置未发生明显团聚现象(图 2)。

|
| 图 2 透射电镜成像:制备后3 d及90 d的纳米银颗粒在高纯水中的粒径分布及分散情况 Figure 2 TEMimage:Particle size distribution and dispersion status of AgNP in deionized water after 3 and 90 days |
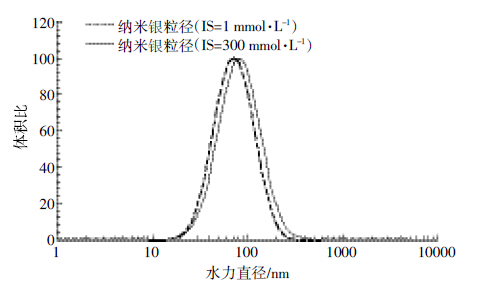
高离子强度会造成纳米银颗粒间的双电层压缩,DLVO 能障降低,从而降低纳米银颗粒之间的静电作用和颗粒体系的分散性。但 DLS 测量结果(图 3)显示,提高背景离子强度(1 mmol·L-1提升至300 mmol·L-1)未诱导纳米银团聚(粒径未成倍增加),表明在实验离子强度范围内,纳米银形态特征及水动力学特征稳定。
|
| 图 3 不同离子强度下纳米银颗粒的粒径分布图 Figure 3 Distribution of AgNP size in different ionic strengths |
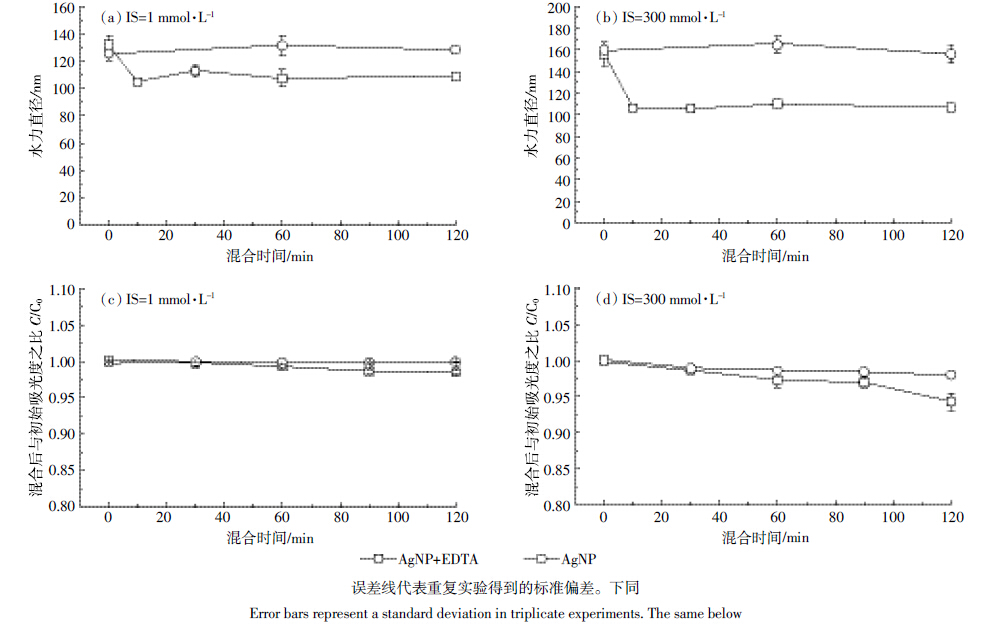
纳米颗粒的沉降速度与粒径密切相关,当纳米颗粒与介质颗粒的粒径比大于 0.008 时,将在饱和多孔介质中发生明显的堵塞现象[13]。此外,根据过滤理论,颗粒团聚会影响弥散(Diffusion)、重力沉降(Gravity sedimentation)以及介质拦截(Interception)等沉降机理[14, 15],因此了解EDTA对纳米银粒径的影响对认识 EDTA 对纳米银迁移影响的机理有重要作用。纳米银 粒径受两个自身因素控制,包括纳米银内核粒径及PVP 涂层厚度。实验结果表明,高低两种离子条件下,EDTA均使得纳米银水力直径在 5 min 内减小并稳定于 100 nm 左右(图 4a、图 4b)。
|
| 图 4 不同离子强度下纳米银(AgNP)与EDTA 混合后水力直径(a,b)及混合后吸光度与初始吸光度的比值(c,d)随时间变化情况 Figure 4 Hydrodynamic diameters(a,b)and relative absorbance(normalized with initial absorbance)(c ,d)for AgNP in the presence (absence)of EDTA in different ionic strengths |
PVP通过分子内酞胺基中的 N-O 偶极键与纳米银内核接近、键合[16],由于 EDTA与银的结合能力较 PVP更强(K(EDTA-Ag)为107数量级,K(PVP-Ag)为106数量级)[17],我们推测 EDTA通过竞争结合破坏PVP与纳米银内核之间的键合导致 PVP涂层脱落,从而产生了纳米银暴露于 EDTA 溶液后水力直径减小的现象。纳米银与 EDTA 混合 5 min后,粒径大小趋于稳定,表明PVP 涂层置换过程结束,且涂层脱落后纳米银尚能维持稳定性。同时纳米银的流出相对浓度(C/C0)在5 min内未发生变化(图 4c、图 4d),说明 EDTA 减小纳米银水力直径的同时并未影响纳米银内核的含量。Yang等[8]发现高离子强度下(300 mmol·L-1)纳米银在PVP 涂层被半胱氨酸置换后会失稳团聚,而本实验结果证明高离子强度下EDTA置换 PVP 涂层后将通过静电排斥作用继续维持纳米银的稳定性。这表明在本实验条件下,EDTA不会诱导纳米银团聚,且在粒径为150~250 μm的多孔介质中的堵塞现象可以忽略不计。EDTA为洗涤剂中常用的添加剂,普遍存在于生活污水中[18, 19],而广泛用于衣物鞋袜等棉纺品中的纳米银将在物品的洗涤过程中被释放[20],该系列活动使纳米银与EDTA在生活污水中相互暴露。本实验结果意味着,在此环境中EDTA对PVP涂层的置换是其控制纳米银稳定性和迁移能力的关键因素。 2.3 不同离子强度下纳米银迁移行为
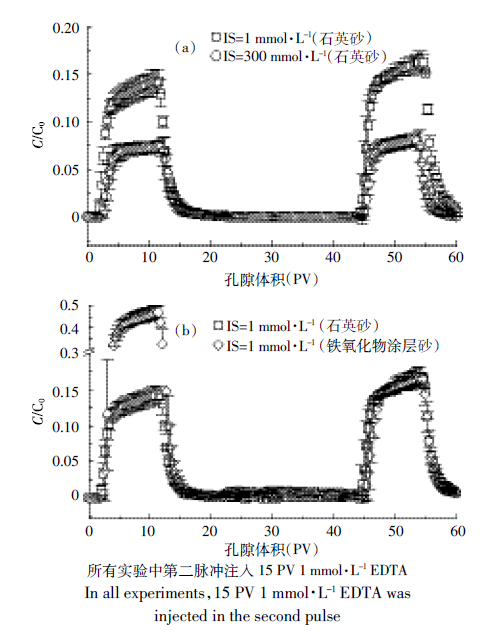
纳米银在石英砂饱和多孔介质中的迁移实验结果显示,离子强度对纳米银的迁移影响趋势明显。随着离子强度的增加,纳米银的流出量降低(图 5a)。当离子强度由 1 mmol·L-1增至 300 mmol·L-1时,柱出口端纳米银的相对流出浓度(C/C0)由 15% 下降至 7.3%,即更多的纳米银被砂柱体系滞留。纳米银内核和石英砂均带负电荷[21, 22],由Derjaguin-Landau-Verwey-Overbeek(DLVO)理论可知,离子强度增加将降低纳米银与石英砂间的静电排斥力,进而提高纳米颗粒在石英砂上的碰撞效率和沉降速度,利于纳米银在饱和体系中的持留,因此C/C0随离子强度的增加呈现降低趋势。这意味着在沿海或盐渍土区的地下水多孔介质中,纳米银的迁移会受到抑制,其污染区域相对较小;而在地下淡水区域,纳米银的迁移性能良好,其污染扩散范围较广,速度较快。
|
| 图 5 不同离子强度(a)及不同多孔介质(b)条件下纳米银的三脉冲穿透曲线图 Figure 5 Triple pulse experimental breakthrough curves of PVP-AgNPs deposition.(a)different ionic strengths. (b)different porous media |
在相同离子条件下(1 mmol·L-1),铁氧化物涂层砂中纳米银第 1 脉冲穿透曲线的C/C0达到 47%,明显高于在石英砂多孔介质中的 15%(图 5b),即纳米银在铁氧化物涂层砂介质中的迁移性能明显高于在石英砂中。石英砂是一种比较稳定的硅酸盐矿物,在水中能吸附配位水,经离解形成大量-OH官能团。虽然纳米银内核与石英砂因同带负电荷而相互排斥,但其PVP涂层却能通过与 Si-OH 形成共价键而稳固吸附在石英砂多孔介质表面[23],在两种作用力的影响下,纳米银在石英砂表面的吸附性能良好,表明 PVP对石英砂的吸附在纳米银沉降过程中起主要作用。铁氧化物涂层砂在本实验溶液条件下带正电[10],这是由于其表面铁氧化物发生了表面水合及氢氧化物离解作用,水合氧化铁吸附 H+而显示出正电荷[24, 25],故与纳米银间存在静电引力。但铁氧化物涂层砂对PVP 等亲水性物质吸附效果不佳[26],同时铁氧化物的覆盖使得介质表面供PVP键合的-OH 减少。综上所述,铁氧化物涂层砂与纳米银间存在静电引力,但提供给纳米银的吸附点位减少,因静电作用力并不是影响纳米银在多孔介质中吸附性能的主要作用力,故铁氧化物涂层砂对纳米银的吸附能力降低。这意味着在矿物质较丰富的天然砂介质含水层中,纳米银由于迁移能力相对强,对水生态的影响会大于在纯砂含水层。 2.5 EDTA对纳米银在多孔介质中迁移行为的影响
由图 5 a可见,第 2 脉冲向石英砂柱注入EDTA的过程中,穿透曲线平台C/C0稳定于 0 附近,未出现纳米银脱附峰,第 3 脉冲穿透曲线平台形状及高度未发生明显变化。这表明EDTA 对石英砂中沉积态纳米银洗脱能力较差,同时其淋洗过程对石英砂柱中纳米银后续迁移行为影响甚微。预实验表明由于EDTA与石英砂面的双电层作用,EDTA在石英砂面沉降量几乎为零。据此可以推测EDTA无法沉降到石英砂表面,从而无法与沉降在石英砂表面的纳米银发生相互作用并影响其后续沉降过程。
值得注意的是,虽然第2脉冲向铁氧化物涂层砂柱注入EDTA过程中得到的穿透曲线与石英砂柱中的一致——平台 C/C0 稳定在 0 附近,但第 3 脉冲穿透曲线的平台却出现明显下降,且与石英砂柱的平台高低基本一致(图 5b)。此现象表明 EDTA 的淋洗可以削弱后续纳米银在铁氧化物涂层砂柱中的迁移性能。EDTA配位性能广泛[27, 28],对铁有极强的络合作用,能溶解铁氧化物涂层[10],故推测 EDTA 注入铁氧化物砂柱后,将迅速与铁氧化物反应生成水溶性络合物FeEDTA,并随着淋洗液排出砂柱,造成石英砂表面铁氧化物涂层脱落,-OH 得以暴露,使纳米银吸附位点增多,迁移行为恢复为石英砂柱中的状态。 3 结论
(1)EDTA能够置换纳米银表面的PVP涂层,从而改变纳米银的稳定性。
(2)纳米银在环境多孔介质中的迁移受离子强度影响,提高离子强度会降低纳米银在多孔介质中的迁移能力。
(3)纳米银迁移能力受多孔介质表面特性影响,金属氧化物的覆盖减少了硅酸盐类介质表面供PVP 类聚合物吸附的点位,导致纳米银沉降量降低。
(4)EDTA通过络合并溶解硅酸盐介质表面的金属氧化物覆盖层,暴露出供纳米银聚合物涂层吸附的点位,一定程度上降低了纳米银在环境多孔介质中的迁移性能,使纳米银易于被多孔介质从水体中滤除,从而降低其与水生生态环境中有益微生物的接触机会,降低其对水生生态平衡的破坏风险。
| [1] | Benn T, Cavanagh B, Hristovski K, et al. The release of nanosilver from consumer products used in the home[J]. Journal of Environmental Quality, 2010, 39(6):1875-1882. |
| [2] | Gottschalk F, Sonderer T, Scholz R W, et al. Modeled environmental concentrations of engineered nanomaterials(TiO2, ZnO, Ag, CNT, Fullerenes) for different regions[J]. Environmental Science and Technology, 2009, 43(24):9216-9222. |
| [3] | 邓芙蓉, 魏红英, 郭新彪. 纳米银毒理学研究进展[J]. 环境工程技术学报, 2011(5):420-424. DENG Fu-rong, WEI Hong-ying, GUO Xin-biao. Research progress in the toxicology of silver nanoparticles[J]. Journal of Environmental Engineering Technology, 2011(5):420-424. |
| [4] | Fang J, Shan X Q, Wen B, et al. Transport of copper as affected by titania nanoparticles in soil columns[J]. Environmental Pollution, 2011, 159(5):1248-1256. |
| [5] | Wang D, Paradelo M, Bradford S A, et al. Facilitated transport of Cu with hydroxyapatite nanoparticles in saturated sand:Effects of solution ionic strength and composition[J]. Water Research, 2011, 45(18):5905-5915. |
| [6] | Neukum C, Braun A, Azzam R. Transport of engineered silver(Ag)nanoparticles through partially fractured sandstones[J]. Journal of Contaminant Hydrology, 2014, 164:181-192. |
| [7] | Wang D, Ge L, He J, et al. Hyperexponential and nonmonotonic retention of polyvinylpyrrolidone-coated silver nanoparticles in an Ultisol[J]. Journal of Contaminant Hydrology, 2014, 164:35-48. |
| [8] | Yang X, Lin S, Wiesner M R. Influence of natural organic matter on transport and retention of polymer coated silver nanoparticles in porous media[J]. Journal of Hazardous Materials, 2014, 264:161-168. |
| [9] | Zhang W, Tsang D C, Lo I M. Removal of Pb by EDTA-washing in the presence of hydrophobic organic contaminants or anionic surfactant[J]. Journal of Hazardous Materials, 2008, 155(3):433-439. |
| [10] | Yang X, Liang D, Deng S. Quantifying the influence of EDTA on polymer nanoparticle deposition and retention in an iron-oxide-coated sand column[J]. Journal of Environmental Monitoring, 2012, 14(9):2392-2398. |
| [11] | Jiang X, Tong M, Lu R, et al. Transport and deposition of ZnO nanoparticles in saturated porous media[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2012, 401:29-37. |
| [12] | Hiramatsu H, Osterloh F E. A simple large-scale synthesis of nearly monodisperse gold and silver nanoparticles with adjustable sizes and with exchangeable surfactants[J]. Chemistry of Materials, 2004, 16(13):2509-2511. |
| [13] | Xu S, Gao B, Saiers J E. Straining of colloidal particles in saturated porous media[J]. Water Resources Research, 2006, 42(12):W12S-W16S. |
| [14] | Tufenkji N, Elimelech M. Correlation equation for predicting single-collector efficiency in physicochemical filtration in saturated porous media[J]. Environmental Science and Technology, 2004, 38(2):529-536. |
| [15] | Chen K L, Elimelech M. Aggregation and deposition kinetics of fullerene(C60) nanoparticles[J]. Langmuir, 2006, 22(26):10994-11001. |
| [16] | Zhang Z, Zhao B, Hu L. PVP Protective mechanism of ultrafine silver powder synthesized by chemical reduction processes[J]. Journal of Solid State Chemistry, 1996, 121(1):105-110. |
| [17] | Mdluli P S, Sosibo N M, Mashazi P N, et al. Selective adsorption of PVP on the surface of silver nanoparticles:A molecular dynamics study[J]. Journal of Molecular Structure, 2011, 1004(1-3):131-137. |
| [18] | Alder A C, Siegrist H, Gujer W, et al. Behaviour of NTA and EDTA in biological wastewater treatment[J]. Water Research, 1990, 24(6):733-742. |
| [19] | 李红路, 甄壮伟, 马建兵, 等. EDTA系列螯合剂的应用及合成工艺进展[J]. 精细与专用化学品, 2013(8):9-11. LI Hong-lu, ZHEN Zhuang-wei, MA Jian-bing, et al. Progress on synthesis and application of a series of EDTA chelators[J]. Fine and Specialty Chemicals, 2013(8):9-11. |
| [20] | Geranio L, Heuberger M, Nowack B. The behavior of silver nanotextiles during washing[J]. Environmental Science and Technology, 2009, 43(21):8113-8118. |
| [21] | Yang X, Flynn R, von der Kammer F, et al. Quantifying the influence of humic acid adsorption on colloidal microsphere deposition onto iron-oxide-coated sand[J]. Environmental Pollution, 2010, 158(12):3498-3506. |
| [22] | Lin S, Cheng Y, Bobcombe Y, et al. Deposition of silver nanoparticles in geochemically heterogeneous porous media:Predicting affinity from surface composition analysis[J]. Environmental Science and Technology, 2011, 45(12):5209-5215. |
| [23] | Cooper C L, Cosgrove T, van Duijneveldt J S, et al. Competition between polymers for adsorption on silica:A solvent relaxation NMR and small-angle neutron scattering study[J]. Langmuir, 2013, 29(41):12670-12678. |
| [24] | Satpathy J K, Chaudhuri M. Treatment of cadmium-plating and chromium-plating wastes by iron oxide-coated sand[J]. Water Environment Research, 1995, 67(5):788-790. |
| [25] | 许光眉. 石英砂负载氧化铁(IOCS)吸附去除锑、磷研究[D]. 长沙:湖南大学, 2006. XU Guang-mei. The study on adsorption removal of antimony and phosphate using iron oxide coated sand[D]. Changsha:Hunan University, 2006. |
| [26] | Korshin G V, Benjamin M M, Sletten R S. Adsorption of natural organic matter(NOM) on iron oxide:Effects on NOM composition and formation of organo-halide compounds during chlorination[J]. Water Research, 1997, 31(7):1643-1650. |
| [27] | Peters R W. Chelant extraction of heavy metals from contaminated soils[J]. Journal of Hazardous Materials, 1999, 66(1-2):151-210. |
 2015, Vol. 34
2015, Vol. 34