文章信息
- 周垂帆, 林静雯, 李莹, 刘爱琴
- ZHOU Chui-fan, LIN Jing-wen, LI Ying, LIU Ai-qin
- 磷与草甘膦在酸性土壤中吸附解吸交互作用机制
- Competitive adsorption and desorption of glyphosate and phosphate on acid soil
- 农业环境科学学报, 2016, 35(12): 2367-2376
- Journal of Agro-Environment Science, 2016, 35(12): 2367-2376
- http://dx.doi.org/10.11654/jaes.2016-0862
文章历史
- 收稿日期: 2016-06-29
2. 海峡两岸红壤区水土保持协同创新中心, 福州 350002
2. Co-innovation center for soil and water conservation in red soil region of the Cross-straits, Fuzhou 350002, China
水土流失是造成农业面源污染的原因之一,这主要是近年来农药、化肥以及农村畜禽养殖、城市生活垃圾等固体废弃物,伴随着水土流失的发生与发展而形成的降雨-径流-侵蚀-水污染负荷输出所导致。除草剂草甘膦和磷肥是我国南方农业最为常用的生产资料,同时草甘膦和过量的磷也是水体中常见的面源污染物。草甘膦是由美国Monsanto公司研发,于1974年投入市场的一种有机磷类除草剂,因其杀草广谱而被广泛应用于农业杂草防除。草甘膦在土壤介质中的半衰期较长,平均半衰期60 d左右,长可达174 d,土壤表层中的草甘膦残余浓度可达0.45~2 mg·kg-1,个别地区甚至高于10 mg·kg-1 [1]。因此,生产中过量使用草甘膦可能会产生土壤残留问题,残留在土壤中的草甘膦或被土壤紧密吸附而导致土壤环境发生改变,对土壤生态系统产生不利影响,或在降雨发生后随着水土流失迁移、沉积污染地表水,或在淋溶作用下下渗,威胁地下水资源安全[1]。虽然大多的研究证实,草甘膦在土壤中不易发生迁移,但仍有较多的研究指出,世界范围内的表层水体中和地下水中,都发现了相当大浓度的草甘膦和其降解产物AMPA的普遍存在,例如:在美国的河流中检测到草甘膦质量浓度达到了2.2 mg·L-1 [2];丹麦政府和格陵兰地质研究所专家共同提供的报告指出,地下水中草甘膦的浓度达到其国家饮用水允许标准的5倍[3];Sanchís J等对西班牙卡塔洛尼亚地区采集的140个地下水样分析发现,有41%的水样草甘膦含量超标,草甘膦平均含量为200 ng· L-1,最高可达到2.5 μg· L-1 [4]。更有数据表明在农产品、鱼类、哺乳动物甚至人体内都检测到草甘膦存在[4]。因此,研究草甘膦在土壤中的化学行为及迁移规律,对减少农药流失,控制农业面源污染,保护生态系统健康有重要的意义。
在我国南方土壤磷有效性较低,人们在农林生产中常通过施用大量磷肥以满足作物对磷素的需求,积累态磷会通过地表径流和土体淋湿进入水环境,造成水体富营养化,近年来越来越引起人们的重视。在南方缺磷严重的地区大量使用草甘膦和磷肥必然出现草甘膦残留与磷积累共存的问题,研究表明,草甘膦与磷酸盐具有非常相似的结构,这意味着草甘膦和磷酸盐在土壤上可能存在吸附位点的竞争[5]。因此,磷的存在可能影响草甘膦在土壤中的移动性,草甘膦也可能影响土壤磷的吸附释放。
吸附作用是一个可以阻滞和延缓污染物进一步迁移和转化,从而在一定程度上抑制污染物流失的重要过程,土壤对污染物质的解吸过程则为土壤吸附的反方向。因此,吸附解吸是土壤-水界面上的重要化学行为,反映了化学物质在土壤环境中的动态与归宿,是影响养分与污染物迁移行为的因素之一,草甘膦与磷在土壤中的吸附特性制约着其迁移、转化等过程。近年来对草甘膦在水-土两相中的吸附行为研究多侧重于重金属复合污染或有机质的吸附影响[6-7],而对草甘膦和磷的交互作用机理鲜有报道。本研究以福建省东部和北部主要地带性土壤为试验土壤,采用振荡平衡法研究草甘膦和磷在酸性土壤中吸附解吸的交互作用过程,探讨不同土壤中草甘膦和磷保持、释放规律及其相互影响机制,对农林业生产过程中农药化肥的合理施用、减少污染物流失、防止水环境污染具有重要理论和实践意义。
1 材料与方法 1.1 试验材料试验用草甘膦为原药粉剂(纯度≥95%),购于天津市天雨一农科技有限公司。
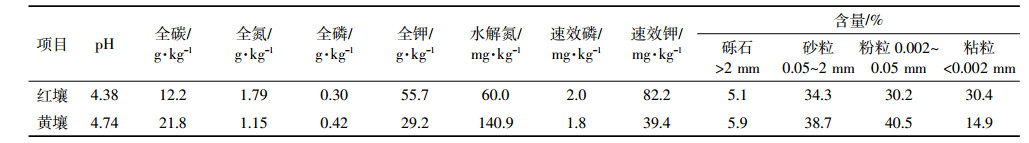
本试验选取2种酸性土壤:于2014年10月采自福建农林大学(26°04’~26°05’N、119°13’~119°14’E)后山粗晶花岗岩发育的富铝湿润富铁土(以下简称红壤);于2014年7月采自武夷山(27°33’~27°54’N、117°27’~117°51’E)桐木辖区内火山凝灰岩-坡积物上发育的铝质常湿淋溶土(以下简称黄壤)。除去土壤表层凋落物及腐殖质,挖取了0~20 cm的土壤样品,带回实验室风干过2 mm筛备用。其基本理化性质如表 1所示。
称取过2 mm筛的风干土0.500±0.001 g于50 mL离心管中,加入15 mL 0.01 mol· L-1 NaNO3溶液,然后加入5 mL含有不同浓度KH2PO4的0.01 mol· L-1 NaNO3溶液,再加入5 mL含有不同浓度草甘膦的0.01 mol· L-1 NaNO3溶液,其中磷浓度分别为0、0.2、0.4、0.6、0.8、1.0 mmol·L -1(0、6.2、12.4、18.6、24.8、31 mg·L -1),草甘膦浓度为0、2.0、4.0 mmol· L -1(0、338、676 mg·L-1),每个处理4个重复。于25 ℃、225 r· min-1振荡平衡2 h,经4500 r·min-1离心8 min,采用钼锑抗比色法测定上清液中磷浓度[5]。在上述吸附实验离心后的土样中加入0.01 mol·L-1 NaNO3溶液25 mL,于25 ℃下225 r·min-1振荡平衡2 h,经4500 r· min-1离心8 min,测定上清液中磷浓度,平衡液中磷的含量即为磷的解吸量。
1.2.2 磷对草甘膦在土壤上吸附解吸称取过2 mm筛的风干土0.500±0.001 g于50 mL离心管中,加入15 mL 0.01 mol·L-1 NaNO3溶液,然后加入5 mL含有不同浓度草甘膦的0.01 mol· L-1 NaNO3溶液,再加入5 mL含有不同浓度KH2PO4的0.01 mol· L-1 NaNO3溶液,其中草甘膦浓度设置参考Wang等[6]的报道分别为0、0.2、0.4、0.6、0.8、1.0 mmol· L-1(0、33.8、67.6、101.4、135.2、169 mg·L-1),磷浓度为0、2.0、4.0 mmol· L-1(0、62、124 mg· L-1),每个处理4个重复。于25 ℃、225 r· min-1振荡平衡2 h,经4500 r· min-1离心8 min,利用岛津HPLC系统(LC-20A Shi原madzu Corporation,Japan),采用高效液相色谱柱前衍生法测定上清液中草甘膦浓度,经对甲基苯磺酰氯衍生化后,注入C18柱中分离,用紫外检测器在235 nm波长检测,其中流动相组成为0.05 mol·L-1磷酸盐缓冲液(pH5.5):甲醇=65:35(V :V),柱温为30 ℃,进样量为20 μL[8]。在上述吸附实验离心后的土样中加入0.01 mol· L-1 NaNO3溶液25 mL,于25 ℃下225 r· min-1振荡平衡2 h,经4500 r·min-1离心8 min,测定上清液中解吸草甘膦浓度,平衡液中草甘膦的含量即为草甘膦的解吸量。
1.3 数据处理土壤磷(或草甘膦)吸附量计算公式:

解吸量计算公式:

式中:C为吸附平衡液磷(或草甘膦)浓度,mg·L-1;C0为初始磷(或草甘膦)浓度,mg·L-1;C1为解吸平衡液磷(草甘膦)浓度,mg·L-1;V为平衡液体积,L;m为土壤质量,kg。
土壤磷(或草甘膦)的吸附等温线中平衡液浓度C与吸附量Q之间的关系常用Freundlich和Lang原muir方程表达,并结合拟合方程特征参数辅助解释。模型方程及其特征参数如下:
Freundlich方程:Q=KFC1/n
Langmuir方程: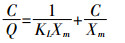
热力学平衡常数:Km=KL×31 000
吸附热:Qm(kJ·moL-1)=nRT
最大缓冲容量:Mb(mg· kg-1)=KL·Xm
标准自由能:ΔG0(kJ· moL-1)=-RTlnKm。
式中:Xm为土壤对磷(或草甘膦)的最大吸附量,mg· kg-1;R为气体常数(8.31 J· moL-1·K-1);T为绝对温度,K[9]。
对吸附试验数据进行拟合后确定适合供试土壤磷素吸附等温曲线和草甘膦吸附等温曲线的拟合方程,并借助Origin 9.2,以平衡液浓度C为横坐标、吸附量Q为纵坐标绘制等温吸附曲线,研究供试土壤对磷和草甘膦的吸附机制。
2 结果与分析 2.1 草甘膦对磷在不同类型土壤上吸附的影响对土壤磷吸附试验数据进行拟合,结果(表 2)显示,除4 mmol· L-1草甘膦处理的黄壤拟合Freundlich方程的决定系数较低外,其他处理拟合方程的决定系数R2均在0.9(P < 0.05)以上,从R2均值来看Lang原muir方程的拟合相关性更好。从磷吸附拟合方程对不同类型土壤的适应性来看,Freundlich和Langmuir方程对黄壤的适应性更好,对红壤的适应性较差,可能是这两种方程更适用于偏碱性土壤对磷吸附行为。此外,草甘膦浓度和土壤类型会影响磷在土壤上的吸附拟合效果,一方面说明了草甘膦和磷在不同类型土壤上的竞争吸附位点存在差异,即土壤吸附能力不同,另一方面说明了不同浓度草甘膦与磷的竞争吸附强度不同。

|
表 3为添加不同浓度草甘膦对两种类型土壤磷素吸附的拟合方程相关特征参数。Xm与土壤理化性质有关,可表征土壤磷库大小。结果显示,不添加草甘膦的对照红壤Xm显著低于对照黄壤。随着草甘膦浓度增加,黄壤Xm先升后降,且当草甘膦浓度为4 mmol·L-1时Xm最低,说明草甘膦在一定程度上能削弱黄壤对磷素的吸附能力,而红壤Xm不减反增。热力学平衡常数Km是与结合能有关的常数,它与最大缓冲容量Mb能反映土壤与磷之间的吸附强度。Km×Mb越大,则强度越大。红壤和黄壤对磷的吸附反应中,Km×Mb均以对照处理最大,4 mmol· L-1草甘膦处理最小,而黄壤在对照处理和2 mmol· L-1草甘膦处理条件下Km×Mb显著大于红壤,可见虽然草甘膦处理降低了黄壤对磷的吸持容量,但提高了黄壤的固持作用使吸附的磷素更难释放。两种土壤吸附热Qm较低,一般在2~3 kJ· moL-1。草甘膦处理下不同土壤与磷吸附反应的ΔG0均为负值,说明这种吸附反应是自发进行的。红壤和黄壤的|ΔG0|均随着草甘膦浓度增加而减小,表明草甘膦浓度越高,土壤吸附磷过程的自发趋势越小,即草甘膦抑制了土壤对磷的吸附。

|
图 1为Langmuir方程拟合得到的等温吸附曲线,描述了不同浓度草甘膦对磷在红壤和黄壤上吸附行为的影响。从图中可看出,由于未添加草甘膦的土壤理化性质稳定、磷吸附位点未饱和且外源磷充足,磷能最大限度地被吸附,对照处理下磷在两种土壤上的吸附量最大,且吸附量均随平衡液磷浓度的增加而升高。但黄壤吸附等温线的斜率明显大于红壤,说明黄壤对磷的吸附能力远大于红壤对磷的吸附能力。这与黄壤含有更高的有机质和CEC有关。随平衡液磷浓度持续增加,红壤吸附等温线逐渐趋于平稳,而黄壤除高浓度草甘膦(4 mmol·L-1)处理对磷的吸附逐渐饱和外,其余处理条件下对磷的吸附仍保持上升趋势,说明黄壤对磷的吸附容量大于红壤。

|
| 图 1 草甘膦对磷在红壤(A)和黄壤(B)上吸附等温线的影响 Figure 1 The influence of glyphosate on phosphate adsorption isotherm in red soil (A) and yellow soil (B) |
草甘膦的存在显著降低磷在两种土壤上的吸附量,土壤吸磷量随草甘膦浓度增加而下降,然而其吸附等温线的变化趋势因土壤类型和草甘膦浓度不同而存在差异。当草甘膦与磷共存时,红壤吸附等温线斜率大幅下降,黄壤吸附等温线斜率虽有所下降但仍较红壤陡,表明草甘膦更容易使红壤吸附固定的磷解吸出来。此外,草甘膦浓度由2 mmol· L-1升至4 mmol· L-1时,红壤吸磷量略有下降但下降程度明显减弱,此时草甘膦对磷在红壤上的吸附行为影响不大。
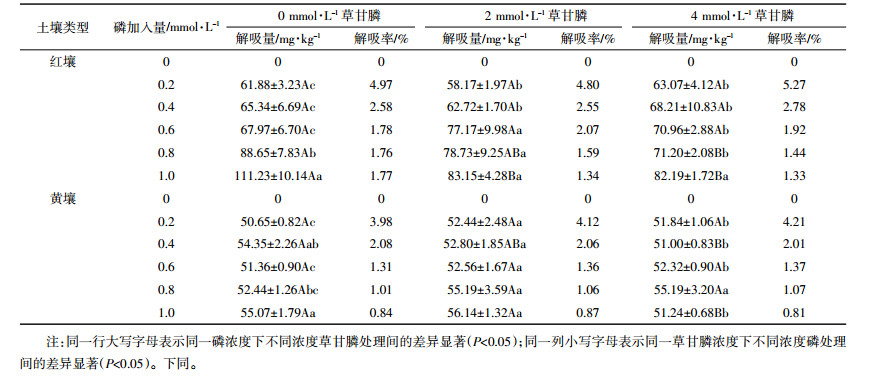
2.2 草甘膦对磷在不同类型土壤上解吸的影响由表 4可知,除对照磷浓度外,红壤中磷的解吸量均随初始磷浓度的增加而逐渐上升,磷在红壤上的吸附位点可能已经达到饱和,磷浓度1.0 mmol·L-1时的解吸量显著高于磷浓度为0.2 mmol·L-1时的磷解吸量(P < 0.05)。在磷浓度较低时,磷解吸率(解吸磷量占吸附磷量的比重)从一个相对较大值(>4%)开始大幅下降,并随着磷浓度升高而逐渐减小。草甘膦对红壤上磷的解吸影响较大,与对照相比,红壤经草甘膦处理后,对高浓度磷(>0.6 mmol· L-1)的解吸具有明显抑制作用,而对低浓度磷( < 0.6 mmol·L-1)的解吸无抑制作用,甚至有促进作用。然而,试验浓度范围内磷浓度变化对黄壤磷的解吸效果影响不大,解吸磷量一般在50~57 mg· kg-1之间,但解吸率随着磷浓度的增加而下降。随着草甘膦浓度增加,黄壤磷的解吸率逐渐上升,说明草甘膦能使被吸附于黄壤上的磷易于解吸。
草甘膦对不同土壤解吸磷的难易程度存在一定差别。总体上看,不同浓度草甘膦处理的黄壤磷解吸率小于红壤,吸附磷的能力则大于红壤,即对磷的吸附能力强的土壤解吸率较低,吸附磷能力弱的土壤解吸率较高,说明土壤对磷的解吸效果与土壤对磷的吸附能力和草甘膦浓度有关。
2.3 磷对草甘膦在不同类型土壤上吸附的影响样品中草甘膦浓度在试验范围内与峰面积呈线性关系。平均回收率及变异系数分别为83%~98%和2.3%~5.3%,说明我们选定的方法回收率与精密度较好,达到农药残留分析对灵敏度的要求。由表 5可看出,采用Freundlich和Langmuir吸附等温式都可以描述土壤对草甘膦的吸附行为,其R2均大于0.9(P < 0.05),但Freundlich方程的拟合效果优于Langmuir。两种吸附拟合方程对黄壤具有更好的适应性,黄壤拟合两种方程得到的平均决定系数分别为0.955和0.950,而红壤拟合得到的平均决定系数为0.947和0.943。存在这种适应性差异的原因可能在于草甘膦在不同类型土壤表面的吸附位点不同。此外,不同外源磷浓度下两种土壤拟合得到的方程也存在较大差异。这是由于磷对草甘膦在土壤表面不同的吸附机制具有不同的影响效果造成的。
|
通过拟合方程计算得到表征草甘膦吸附的相关特征参数见表 6。不添加外源磷时,草甘膦在红壤上的最大吸附量Xm大于黄壤,约为黄壤的1.7倍,可能是草甘膦在红壤上存在更多的吸附位点。随着外源磷浓度增加,红壤Xm先增加后减少,黄壤Xm显著增加。相同外源磷浓度下黄壤Km、Mb和|ΔG0|均显著大于红壤,说明黄壤对草甘膦的吸附强度更大,草甘膦在红壤上更易于被解吸出来。然而随着外源磷浓度增加,红壤的Km、Mb和|ΔG0|均先减少后增加,黄壤则大幅减小,可见外源磷的存在明显抑制了黄壤对草甘膦的吸附强度。另外,ΔG0 < 0说明草甘膦在两种土壤上的吸附反应也是自发进行。总的来看,相同条件下土壤拟合方程特征参数中,Xm分别与表征吸附强度的Km、Mb和|ΔG0|呈反比关系。

|
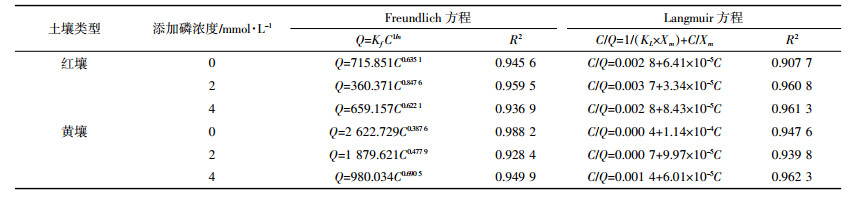
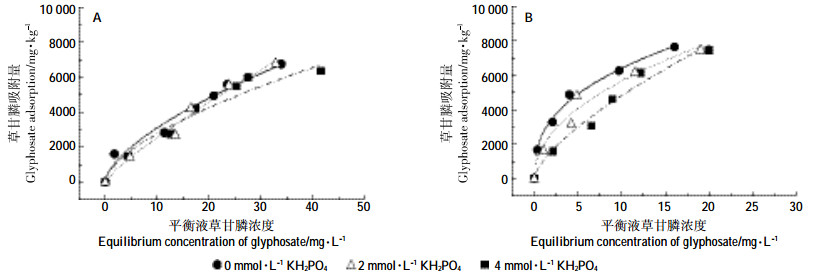
土壤对草甘膦的Freundlich吸附等温线如图 2所示,两种土壤吸附曲线均表现为平衡液草甘膦浓度较低时斜率较大。未添加磷时,随着平衡液草甘膦浓度升高,土壤对草甘膦的吸附能力呈现先稳步上升,随后明显减弱的趋势,证明土壤对草甘膦的吸附作用接近相对饱和的状态,其吸附位点或被磷占据。草甘膦在黄壤上的吸附量大于其在红壤上的吸附量,然而磷的存在明显影响了草甘膦在两种土壤表面的吸附,不同土壤的吸附过程也表现出差异。平衡液草甘膦浓度较低时,竞争吸附起主导作用,即因外源磷竞争草甘膦在红壤上的吸附位点而降低草甘膦的吸附量,但是当草甘膦浓度较高时,低浓度磷(2 mmol·L-1)的存在却增加了草甘膦在红壤表面的吸附,推测其原因可能是高浓度草甘膦显著降低了土壤环境pH,导致草甘膦净电荷增加,草甘膦的吸附量增加。此外,随着磷浓度增加,黄壤对草甘膦的吸附量减少,可见磷的存在抑制了草甘膦在黄壤上的吸附。
|
| 图 2 磷对草甘膦在红壤(A)和黄壤(B)上吸附等温线的影响 Figure 2 The influence of phosphate on glyphosate adsorption isotherm in red soil (A) and yellow soil (B) |
草甘膦在两种土壤上解吸的影响如表 7所示。随着土壤环境中草甘膦浓度的增加,草甘膦在红壤和黄壤上的解吸量无明显规律性变化。这可能与红壤对草甘膦的吸附量小,土壤表面的混乱程度较大有关。当磷浓度为4 mmol·L-1时,两种土壤草甘膦解吸量有所增加,说明在试验浓度范围内草甘膦含量变化对两种土壤的解吸效果影响微弱,而解吸率均呈下降趋势,说明此时草甘膦解吸率的变化主要受土壤吸附量影响。从外源磷对草甘膦解吸的影响方面看,随着外源磷浓度增加,草甘膦在红壤上的解吸量有所下降,解吸率也相应减小,而不同磷处理下黄壤草甘膦解吸量变化一般在1.83~8.42 mmol·kg-1之间,可见外源磷对草甘膦在黄壤上的解吸影响较小。总体来看,相同草甘膦浓度下,黄壤的解吸量小于红壤,而其吸附量大于红壤,表明黄壤对草甘膦的固持作用大于红壤。
在南方地区,使用草甘膦除草和施用磷肥来提高土壤磷素有效性,这种农业措施使得草甘膦和磷成为土壤中共存物质,必然会对彼此在土壤中的迁移转化产生相互影响。在农业生产过程中草甘膦和磷可能以不同顺序进入并累积在土壤中,因此我们分别对两者的吸附解吸特征及相互影响机制进行了研究。
3.1 草甘膦和磷在土壤中的吸附解吸特征已有研究表明,草甘膦和水溶性磷肥进入土壤后,很快会被土壤粘粒、Fe和Al氧化物及腐植酸类化合物吸附[10-11]。吸附等温方程普遍用来描述土壤体系中吸附剂表面和溶液中吸附质数量关系,目前较为普遍使用的分别是Freundlich和Langmuir方程。从吸附本质来看,Freundlich方程是广泛运用于土壤化学的一个经验吸附模型,适用于多分子层吸附,而Lang原muir方程是以均匀表面的单分子层吸附为前提的理论推导模型,这种吸附模型对于吸附位能量相等的假设脱离现实,同时也忽略了吸附质分子间的相互作用,但不失为一种定量化分析方法[10]。在本研究中,Freundlich方程对草甘膦在供试土壤吸附行为的拟合程度要比Langmuir方程好,与Wang[6]和Piccolo等[11]研究结果相似,而Langmuir方程对土壤磷吸附的拟合效果较Freundlich方程更好。因此,吸附数据是否适合拟合方程主要取决于吸附剂和吸附质的性质。
从研究结果来看,供试红壤和黄壤对草甘膦和磷的吸附过程均为以物理吸附为主的自发吸热反应。李岩等[12]的研究结果表明,草甘膦在砖红壤上的吸附反应虽自发进行,但其吸附焓变高达71.39 kJ· moL-1属于化学吸附范畴,这种吸附热差异可能与土壤类型有关。此外我们的研究同样证实草甘膦和磷在土壤中解吸能力较弱,和前人的研究结果是类似的[12-15]。先前研究发现,草甘膦在土壤上的吸附与土壤中的无定型铁铝和有机质含量有关。草甘膦分子中存在羧基、氨基和膦酸基,这些基团均有产生氢键和配位键的能力,草甘膦可以通过磷酸基与针铁矿表面形成的内层配合物而吸附在针铁矿表面,而羧基处于自由状态,可以与土壤中具有很大的表面积的氧化铁和氧化铝水合物结合[11]。对磷而言,在酸性土壤中,磷除了被铁铝氧化物和粘粒矿物表面所吸附外,还与铁铝生成难溶性的磷酸盐,使磷由可溶态向难溶态转变,减少了P向土壤溶液中的释放[9]。除此之外,研究发现吸附平衡时黄壤对草甘膦和磷吸附量均大于红壤,可能是由于支配草甘膦和磷在土壤上吸附的主要因素是有机质。一般来说,黄壤表层有机质含量在50~200 g·kg-1,高出红壤1~2倍,一方面土壤腐植酸等有机质可通过氢键吸附游离草甘膦分子或磷,尤其可溶性有机碳对二者的吸附起到主要作用[10-11],另一方面多价金属离子与腐植酸形成的复合体也是草甘膦和磷的主要吸附剂,因此试验条件下土壤有机质对它们吸附能力的贡献占主导地位,而土壤pH及粘粒矿物含量影响较小[13, 15]。对磷的研究证实,有机质之所以可被看作一种固磷基质,是因为有机质能够与铁、铝氧化物发生溶解、络合、还原作用,从而增强铁、铝氧化物的活性,提高粘粒复合体的吸P量[14-15]。而Yu等对草甘膦的研究发现,当黑土有机质去除后表征土壤对草甘膦吸附容量的Freundlich方程参数Kf下降了75.0%,说明有机质对草甘膦在土壤中的吸附影响十分显著[16]。Mo原rillo等也认为草甘膦吸附行为受铁铝氧化物和有机质的影响,而与阳离子交换量和粘土矿物含量无关[17]。
3.2 草甘膦对磷在土壤上吸附解吸的影响机制本实验结果表明,草甘膦抑制了土壤对磷的吸附,低浓度下促进了土壤对磷的解吸。这主要机制可能与有机酸活化土壤磷素的机制一致,草甘膦的结构决定了它同有机酸一样在土壤溶液中具有有机阴离子络合效应和质子酸效应。一方面草甘膦能降低土壤pH,草甘膦释放的H+吸附到氧化物表面即发生质子化过程,引起矿物晶格表面金属离子(M)与氧离子(O)之间的结合强度降低,从而使得M-O化学键断开,最终导致氧化物表面晶格中金属离子释放到溶液中,特别是使土壤铁铝氧化物对磷的专性吸附受到破坏,减少对磷的吸附,促进磷的释放[18]。另一方面,因为草甘膦分子中包含一个基本酸基--羧基,所以从结构上看它又是一种低分子有机酸。研究证实,有机阴离子能够与铁铝水化氧化物表面吸附态磷的配位基发生交换反应,即竞争磷酸根离子的吸附位点从而降低土壤对磷的吸附固定[19],众多研究表明,有机酸阴离子络合作用能够活化土壤中Fe-P、Al-P、Ca-P等难溶态磷[14-15],由此推测,草甘膦可与难溶性磷所含的Fe3+、Al3+、Ca2+发生离子交换或螯合作用,从而占据磷在土壤上的吸附位点。从本研究反映出的趋势性结果来看,草甘膦的存在确实显著降低了两种土壤对磷的吸附量,说明草甘膦的存在占据了磷在土壤上的吸附位点,且草甘膦浓度越高竞争得到的吸附位点越多。草甘膦与磷的交互作用视土壤类型不同而异,即其竞争程度与吸附剂有关。Gimsing等在另一研究中发现磷在针铁矿和水铝矿上的吸附量大于草甘膦,而在×利石、蒙脱石和高岭石上二者的竞争吸附能力相当[20]。这一结果和有机酸对磷吸附的影响机制类似,有机酸能够在一定程度上通过消除土壤中磷的吸附位点而抑制土壤对磷的吸附,促进磷的解吸[14-15]。
3.3 磷对草甘膦在土壤上吸附解吸影响机制本研究中磷的存在明显抑制了红壤和黄壤对草甘膦的吸附,低浓度下促进了其解吸量。究其原因主要是磷争夺了草甘膦在土壤当中的吸附位点-铁铝氧化物等[15];也可能是由于偏酸性的外源磷改变了土壤环境pH,使草甘膦分子带负电而容易吸附在土壤表面[15]。这一结果也证实了Sasal等的模拟降雨实验,田间使用磷肥使得草甘膦的流失量增加了2.8倍[5];同样,Munira等通过对使用不同年限磷酸铵的加拿大的沙性粘壤土研究表明,草甘膦的Kd(吸附分布常数)值随着Olsen-P含量的增加而降低,即磷同样降低了沙性粘壤土对草甘膦的吸附[21]。类似的是,Dion等利用同位素标记法研究了草甘膦和磷在土壤上的吸附行为,发现草甘膦的吸附取决于磷的浓度,磷作用下土壤为草甘膦提供的吸附位点有限[22]。这是因为,土壤存在对磷的优先吸附现象,且草甘膦难以将土壤表面吸附的磷完全解吸下来,其原因在于磷酸分子(0.25 nm)要比草甘膦分子小(0.43 nm),所以较草甘膦分子所需吸附位点的面积小,相对而言在土壤上的可吸附位点更多[21];再者除膦酸基外,草甘膦分子上的羧基也可吸附于针铁矿上,而磷酸可以将其解吸出来。此外,磷原子在草甘膦分子中与3个氧原子和1个碳原子相连,而在磷分子中则与4个氧原子相连,由于碳原子的电负性较氧原子弱,草甘膦上磷原子极性较弱[13-14]。然而不同的是,卢信等研究发现磷的施用虽抑制了草甘膦在红壤性水稻土上的吸附能力,但却能够促进砂土对草甘膦的吸附能力进而减弱草甘膦的移动性[24]。
4 结论(1)红壤和黄壤对磷的吸附等温线采用Langmuir拟合方程表达更好,而Freundlich方程则对两种土壤吸附草甘膦的拟合相关性更好。红壤最大吸磷量的变化与黄壤对草甘膦的最大吸附量变化趋势均为上升,而黄壤最大吸磷量变化规律则与红壤对草甘膦的最大吸附量变化的规律相同,两种土壤或分别存在对草甘膦和磷的专性吸附区。
(2)草甘膦和磷在两种土壤上均能够自发进行吸热吸附反应。土壤当中草甘膦和磷存在着吸附行为的竞争,草甘膦能够降低土壤对磷的吸附,同时磷也能够抑制土壤对草甘膦的吸附。这说明磷能够增加草甘膦的迁移风险,同样草甘膦也能够引发磷的迁移。
| [1] | Yang X M, Wang F, Bento C P M, et al. Short-term transport of glyphosate with erosion in Chinese loess soil:A flume experiment[J]. Science of the Total Environment, 2015, 512/513 : 406–414. DOI:10.1016/j.scitotenv.2015.01.071 |
| [2] | Contardo-Jara V, Klingelmann E, Wiegand C. Bioaccumulation of glyphosate and its formulation Roundup Ultra in Lumbriculus variegatus and its effects on biotransformation and antioxidant enzymes[J]. Environmental Pollution, 2009, 157(1) : 57–63. DOI:10.1016/j.envpol.2008.07.027 |
| [3] | Kjær J, Olsen P, Ullum M, et al. Leaching of glyphosate and amino-methylphosphonic acid from Danish agricultural field sites[J]. Journal of Environmental Quality, 2005, 34(2) : 608–620. DOI:10.2134/jeq2005.0608 |
| [4] | Sanchís J, Kantiani L, Llorca M, et al. Determination of glyphosate in groundwater samples using an ultrasensitive immunoassay and confirmation by on-line solid-phase extraction followed by liquid chromatography coupled to tandem mass spectrometry[J]. Analytical and Bioanalytical Chemistry, 2012, 402(7) : 2335–2345. DOI:10.1007/s00216-011-5541-y |
| [5] | Sasal M C, Demonte L, Cislaghi A, et al. Glyphosate loss by runoff and its relationship with phosphorus fertilization[J]. Journal of Agricultural and Food Chemistry, 2015, 63(18) : 4444–4448. DOI:10.1021/jf505533r |
| [6] | Wang Y J, Zhou D M, Sun R J, et al. Zinc adsorption on goethite as affected by glyphosate[J]. Journal of Hazardous Materials, 2008, 151(1) : 179–184. DOI:10.1016/j.jhazmat.2007.05.060 |
| [7] | Ololade I A, Oladoja N A, Oloye F F, et al. Sorption of glyphosate on soil components:The roles of metal oxides and organic materials[J]. Soil & Sediment Contamination, 2014, 23(5) : 571–585. |
| [8] | 司友斌, 桑忠营, 程凤侠. 对甲基苯磺酰氯衍生化液相色谱法测定土壤中草甘膦[J]. 安徽农业大学学报, 2009, 36(1) : 136–139. SI You-bin, SANG Zhong-ying, CHENG Feng-xia. Determination of glyphosate in soil by high performance liquid chromate graphy after derivatization with p-toluenesulphonyl chloride[J]. Journal of Anhui Agricultural University, 2009, 36(1) : 136–139. |
| [9] | Yu H, Cao G J, Qing Y, et al. Effects of different phosphorus applications on soil available phosphorus, phosphorus absorption and yield of spring maize[J]. Journal of South China Agricultural University, 2013, 34(4) : 470–474. |
| [10] | Zhou C F, Wang Y J, Yu Y C, et al. Does glyphosate impact on Cu uptake by, and toxicity to, the earthworm Eisenia fetida?[J]. Ecotoxicology, 2012, 21(8) : 2297–2305. DOI:10.1007/s10646-012-0986-0 |
| [11] | Piccolo A, Celano G, Pietramellara G. Adsorption of the herbicide glyphosate on a metal-humic acid complex[J]. Science of the Total Environment, 1992, 123/124(2) : 77–82. |
| [12] | 李岩, 杨敏, 王红斌, 等. 土壤吸附草甘膦的热力学研究[J]. 安徽农业科学, 2008, 36(23) : 10061–10062. LI Yan, YANG Min, WANG Hong-bin, et al. Study on thermodynamics of soil adsorbing glyphosate[J]. Journal of Anhui Agri Sci, 2008, 36(23) : 10061–10062. |
| [13] | Arroyave J M, Waiman C C, Zanini G P, et al. Effect of humic acid on the adsorption/desorption behavior of glyphosate on goethite:Isotherms and kinetics[J]. Chemosphere, 2016, 145 : 34–41. DOI:10.1016/j.chemosphere.2015.11.082 |
| [14] | Wang C, Wang Z, Lin L, et al. Effect of low molecular weight organic acids on phosphorus adsorption by ferric-alum water treatment residuals[J]. Journal of Hazardous Materials, 2012, 203 : 145–150. |
| [15] | Fink J R, Inda A V, Bavaresco J, et al. Adsorption and desorption of phosphorus in subtropical soils as affected by management system and mineralogy[J]. Soil and Tillage Research, 2016, 155 : 62–68. DOI:10.1016/j.still.2015.07.017 |
| [16] | Yu Y, Zhou Q X. Adsorption characteristics of pesticides methamidophos and glyphosate by two soils[J]. Chemosphere, 2005, 58(6) : 811–816. DOI:10.1016/j.chemosphere.2004.08.064 |
| [17] | Morillo E, Undabeytia T, Maqueda C, et al. Glyphosate adsorption on soils of different characteristics:Influence of copper addition[J]. Chemosphere, 2000, 40(1) : 103–107. DOI:10.1016/S0045-6535(99)00255-6 |
| [18] | Wang C, Wang Z, Lin L, et al. Effect of low molecular weight organic acids on phosphorus adsorption by ferric-alum water treatment residuals[J]. Journal of Hazardous Materials, 2012, 203 : 145–150. |
| [19] | Gimsing A L. Effect of KCl and CaCl2 as background electrolytes on the competitive adsorption of glyphosate and phosphate on goethite[J]. Clays & Clay Minerals, 2001, 49(3) : 270–275. |
| [20] | Gimsing A L, Borggaard O K. Competitive adsorption and desorption of glyphosate and phosphate on clay silicates and oxides[J]. Clay Minerals, 2002, 37(3) : 509–515. DOI:10.1180/0009855023730049 |
| [21] | Munira S, Farenhorst A, Flaten D, et al. Phosphate fertilizer impacts on glyphosate sorption by soil[J]. Chemosphere, 2016, 153 : 471–477. DOI:10.1016/j.chemosphere.2016.03.028 |
| [22] | 龚健东, 赵炳梓, 张佳宝, 等. 农药草甘膦在砂质潮土上的迁移行为及其影响因素[J]. 土壤学报, 2007, 44(6) : 1010–1015. GONG Jian-dong, ZHAO Bing-zi, ZHANG Jia-bao, et al. Transport behavior of giyphosate in sandy fluvo-aquic soil and its influencing factors[J]. Acta Pedologica Sinica, 2007, 44(6) : 1010–1015. |
| [23] | 卢信, 赵炳梓, 张佳宝, 等. 磷酸盐对农药草甘膦在不同土壤中迁移的影响[J]. 中国环境科学, 2005, 25(5) : 607–610. LU Xin, ZHAO Bing-zi, ZHANG Jia-bao, et al. Influence of phosphate on the mobility of pesticide glyphosate in different soils[J]. China Environmental Science, 2005, 25(5) : 607–610. |
 2016, Vol. 35
2016, Vol. 35