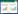文章信息
- 王娇娇, 呼世斌, 魏丽琼, 柴琴琴, 刘晋波, 王佳颖, 杨文晓
- WANG Jiao-jiao, HU Shi-bin, WEI Li-qiong, CHAI Qin-qin, LIU Jin-bo, WANG Jia-ying, YANG Wen-xiao
- 甜菜与牧草间作对多环芳烃污染土壤的修复作用
- Phytoremediation of polycyclic aromatic hydrocarbons(PAHs)-contaminated soil by intercropped beet-grasses
- 农业环境科学学报, 2016, 35(6): 1090-1096
- Journal of Agro-Environment Science, 2016, 35(6): 1090-1096
- http://dx.doi.org/10.11654/jaes.2016.06.010
文章历史
- 收稿日期: 2015-11-25
多环芳烃(PAHs)是一类广泛存在于环境介质中的有机污染物,由两个或两个以上的苯环构成的线状、角状或簇状的中性或非极性化合物,其化学结构稳定,具有“三致”效应,难降解,易在生物体内蓄积[1-2]。PAHs主要是由有机物不完全燃烧或高温裂解产生,可通过空气或水进行长距离输送,参与生物地球化学循环,最终累积在土壤环境中,并在土壤-作物系统中迁移,进而危及生态系统和人体健康[3-4]。因此,PAHs污染土壤的修复问题已成为国内外土壤环境领域的一个研究热点。
植物修复(Phytoremediation)是利用植物来转移、容纳或转化污染物,以减少污染物对环境危害的一种绿色修复技术。与传统的土壤物理、化学修复方法相比,植物修复具有对污染物降解彻底、处理费用较低、保持原土壤理化性质和应用广泛、不易产生二次污染等特点,更适用于大面积土壤污染的修复[5-6],其修复对象往往是受到重金属、有机物或放射性元素污染的土壤及水体[7]。自20世纪80年代问世以来,植物修复技术研究迅速发展,近些年利用植物修复多环芳烃污染土壤屡有报道[3, 8-10]。植物种类不同,其根比表面积、菌根菌、根分泌物、酶等的数量和种类会有所不同,即使同类作物不同品种间也会有差别,导致根际土壤中有机污染物的降解差异很大[11-12]。
植物间作可以充分利用不同植物根系吸收、分泌物、酶和微生物的种类和量不同的特点提高修复率,确保作物品质安全。牧草类植物在PAHs污染土壤的修复方面已取得一定的成效[8-10]。耿贵[13]研究证明了甜菜根系分泌物富含的氨基酸、有机酸、糖分等营养物质,补充或增加了土壤尤其是根际土壤的活性碳、氮量,提高了细菌、真菌、放线菌数量,影响了土壤碳、氮代谢和酶活性。甜菜作为经济作物,根系分泌物含量丰富,与草类间作可产生互惠作用,而甜菜/牧草间作能否进一步提高污染土壤修复效果的研究较少。为此,本研究以菲、荧蒽、芘和苯并[a]芘为PAHs代表,通过盆栽试验,研究了经济作物甜菜与修复牧草黑麦草、香根草、苏丹草分别间作,以及四种植物单作对菲、荧蒽、芘和苯并[a]芘污染土壤的修复效果,并对不同种植模式下土壤中过氧化氢酶和多酚氧化酶活性变化进行了对比分析,为PAHs污染土壤的植物修复技术提供了一定的理论依据。
1 材料与方法 1.1 试验时间与地点本试验在西北农林科技大学智能温室里进行,自2014年11月到2015年4月,为期180 d。
1.2 试验材料 1.2.1 土壤土壤类型为褐土类,塿土亚类,采自杨凌农业示范区穆家寨农田(0~20 cm)。土样采回自然风干后,过2 mm筛备用,其理化性质如下:土壤颗粒组成粘粒23.2%、粉粒50.9%、砂粒25.9%,田间最大体积持水量为19.26%,pH 7.12,有机质7.24 g·kg-1,全氮10.5 g·kg-1,全磷0.16 g·kg-1,全钾1.26 g·kg-1,速效磷17.79 mg·kg-1,阳离子交换量21.54 cmol·kg-1。该土壤中菲、荧蒽、芘和苯并[a]芘四种物质均未检出。
1.2.2 植物供试植物甜菜(Beta vulgaris L.):肉质根,对土壤适应性强,较耐寒,生长期适宜的土壤水分为田间最大持水量的60%。黑麦草(Lolium perenne L.)、苏丹草(Sorghum sudanense(Piper) Stapf.)、香根草(Vetiveria zizanioides L.):三种草适应能力强,分蘖繁殖快,根系发达。种子经隔夜无菌催芽后,播种到盆栽土壤中。
1.2.3 试剂菲(Phenanthrene,>99.9%)、荧蒽(Fluoranthene,>99.9%)、芘(Pyrene,>99.5%)、苯并[a]芘(Benzo(a)pyrene,>99%)(美国Sigma-Alorich公司);甲醇、二氯甲烷(色谱纯,国药集团);丙酮、正己烷、硫酸钠(分析纯,北京百灵威化学科技有限公司);英国尼龙66 0.22 μm针筒式有机滤膜过滤器(北京卓信伟业科技有限公司)。
标准溶液的制备:准确称取PAHs标准品10 mg(精确到0.1 mg),用甲醇配成1.0 mg·mL-1储备溶液,-20 ℃避光保存。
1.2.4 仪器Shimadzu GC-MS-QP2010 Ultra气相色谱-质谱联用仪(日本岛津公司);TDL-60C型低速台式离心机(上海安亭科学仪器厂);KQ-250超声波清洗仪(美国戴安公司)。
1.3 试验方法 1.3.1 试验设计污染土壤中菲、荧蒽、芘污染浓度均设置为100 mg·kg-1,苯并[a]芘的污染浓度为50 mg·kg-1。先将4种污染物溶于丙酮溶液中,与一定量供试土壤混合,待丙酮完全挥发后,再与剩余土壤混合均匀。处理后的土壤在阴凉处稳定一周,装入长1.0 m、宽0.3 m、高0.6 m的试验用盆。经检测,试验用土中菲、荧蒽、芘和苯并[a]芘四种污染物初始浓度分别是(101.23±6.63)、(99.79±4.21)、(105.41±4.59)、(50.12±7.75) mg·kg-1。同时进行无污染物土壤处理试验,该对照试验土壤除不添加4种污染物外,其余同污染土壤。
试验设计15个处理。添加污染物土壤组:T+H(甜菜与黑麦草间作);T+S(甜菜与苏丹草间作);T+X(甜菜与香根草间作);T(甜菜单作);H(黑麦草单作);S(苏丹草单作);X(香根草单作);CK(无植物种植)。无污染物添加土壤组:T0+H0(甜菜与黑麦草间作);T0+S0(甜菜与苏丹草间作);T0+X0(甜菜与香根草间作);T0(甜菜单作);H0(黑麦草单作);S0(苏丹草单作);X0(香根草单作)。各处理均3次重复。
种子经蒸馏水淋洗、隔夜催芽后直接播种于装好供试土壤的盆池中,出苗后定苗。间作处理中每个盆池留甜菜苗7株,黑麦草、苏丹草和香根草均为20株,单作处理中每个盆池留甜菜苗14株,黑麦草、苏丹草和香根草均为40株。试验期间保持土壤田间最大持水量的60%。试验进行两茬植物种植,每3个月种植一批植物,第二次种植试验是在收获植物后的污染土壤中继续进行,整个试验持续6个月。
1.3.2 样品采集每次试验结束后,收获植物样,采集土样约300 g。测定植物样的株高,用蒸馏水冲洗干净分为地上、地下两部分,置于65 ℃下烘干至恒重,测定干物质量。土壤样品室温下风干,研磨过100目筛,放于冰箱中4 ℃保存,用于多环芳烃含量和土壤酶活性的分析测定。
1.3.3 测定分析土壤基本理化性质参照鲍士旦编著的《土壤农化分析》中常规分析方法测定[14]。
土壤菲、荧蒽、芘和苯并[a]芘提取方法参照宋玉芳等[15]的方法并作改进,采用超声提取,GC-MS测定。提取方法:取2.0 g土样于15 mL离心管内,加入2 g无水硫酸钠,混匀;加入10 mL二氯甲烷,40 ℃下超声萃取2 h;4000 r·min-1离心5 min;取3 mL上清液过Fisher Pasteur玻璃管硅胶柱,用1∶1的二氯甲烷和正己烷溶液洗脱,40 ℃下浓缩至干,用甲醇定容到2 mL,过0.22 μm孔径滤膜后用GC-MS分析。GC-MS分析测定条件:
(1) 气相色谱条件:进样口温度290 ℃,分流进样;载气为高纯氦气;进样量1 μL;柱流量1.0 mL·min-1(恒流);柱温80 ℃,2 min→20 ℃·min-1→180 ℃,5 min→10 ℃·min-1→290 ℃,5 min;色谱柱30 m×0.25 mm×0.25 μm。
(2) 质谱条件:扫描选择离子(Sim)模式;离子化能量70 eV;四极杆150 ℃;离子源温度230 ℃;接口温度280 ℃;溶剂延迟时间5 min;调谐方式DFTPP。
菲、荧蒽、芘和苯并[a]芘的回收率达到81.9%~106.3%,相对标准偏差(RSD)为2.8%~8.6%(n=7)。
土壤中过氧化氢酶、多酚氧化酶活性参照周礼恺等[16]土壤酶活性的测定方法。
1.3.4 数据分析土壤中PAHs去除率R(%)=$\frac{{{C}_{0}}-{{C}_{1}}}{{{C}_{0}}}$×100
式中:C0表示土壤中PAHs初始含量,mg·kg-1;Ct表示每次植物收获后土壤所含PAHs的量,mg·kg-1。
将测得的数据用Excel 2010进行整理并作图,利用SPSS.12软件进行统计分析,采用SSR法(P<0.05)进行差异显著性检验。
2 结果与讨论 2.1 不同处理下供试植物的生物量变化植物的生物量和株高是反映植物在污染环境中的抗性和生长能力的重要指标。180 d试验结束后,间作各植物生物量×2(以保证株数与单作相同)与单作生物量的结果如图 1所示。无论添加污染物的土壤还是无污染物的土壤,各种植模式下,甜菜、黑麦草、苏丹草和香根草均可生长。通过对间作植物和单作植物生物量进行比较可以发现,未投加污染物的处理,间作植物对甜菜的生物量影响不大。甜菜与黑麦草、苏丹草、香根草间作其地下部分干重分别为139.77、145.87、143.90 g·盆-1,略高于甜菜单作(135.20 g·盆-1),但提高幅度没有达到显著水平(P>0.05);间作下,黑麦草、苏丹草、香根草的地上部分干重分别为127.53、141.80、125.87 g·盆-1,比单作处理分别高21.67%、18.76%和22.23%,说明间作对四种植物的生长均有不同程度的促进作用。这与李隆报道的间作提高了作物对氮磷钾的吸收,对作物产量有促进作用的研究结论一致[17]。
|
| 图 1 不同处理下供试植物的生物量变化 Figure 1 Biomass of plants in soil under different planting patterns 不同字母表示不同处理组间存在显著差异(P<0.05)。下同 |
进行第一茬植物种植时,土壤中污染物浓度处于一个较高水平,由图 1可以看出,4种植物的生物量和株高明显低于无添加污染物土壤种植的植物。单作甜菜地下部分和地上部分干重分别为74.33、33.47 g·盆-1,比未加污染物处理分别低45.02%、38.16%;单作黑麦草、苏丹草、香根草的地上部分干重分别为86.67、84.60、80.47 g·盆-1,比未加污染物单作处理分别低17.32%、21.33%和21.85%,说明三种牧草较甜菜对多环芳烃有着更好的耐受能力。对比单作与间作中各个植物的生物量和株高发现,间作明显高于单作处理(P<0.05),说明间作一方面发挥了种间互利优势,另一方面提高了植物对污染物的抗性。但无论间作还是单作,第一茬四种植物生物量和株高均低于土壤中无污染物添加的,说明高浓度的多环芳烃污染物对植物的生长有较强的抑制作用。与第一茬植物进行对比发现,第二茬植物生物量和株高均明显提高。除了单作处理的甜菜外,其他处理的植物生物量和株高较无污染物添加土壤中的植物,有略微的增长趋势,说明经第一茬植物种植后,土壤中污染物浓度降低,此浓度对植物的生长有一定的促进作用。以往研究表明[18-19],多数植物在低浓度PAHs处理下,生物量随PAHs浓度的升高而增加,但是如果PAHs浓度较高,植物生物量将明显下降,所以其初始浓度对一些植物修复PAHs的效果有影响。
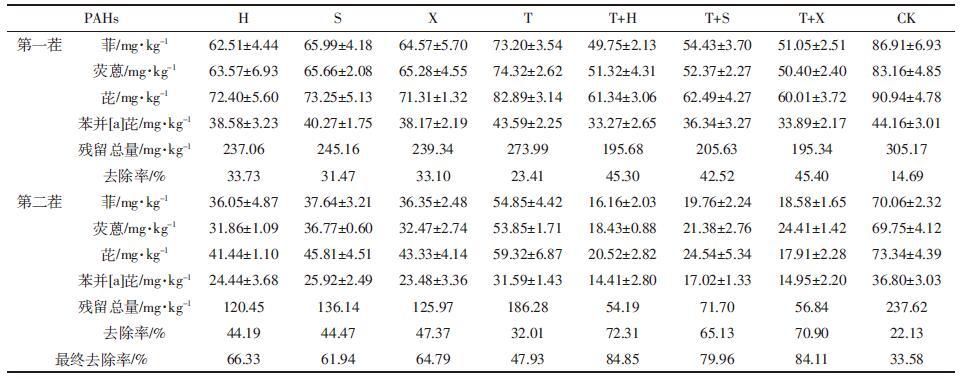
2.2 土壤中PAHs的残留量和去除率经6个月试验,两茬植物种植,不同植物种植模式下,污染土壤中菲、荧蒽、芘和苯并[a]芘残留量及去除率如表 1。经第一茬植物种植后,种植植物的土壤中4种多环芳烃总残留浓度为195.34~273.99 mg·kg-1,去除率为23.41%~45.40%,无植物对照处理土壤4种多环芳烃总残留浓度为305.17 mg·kg-1,去除率为14.69%;经第二茬植物种植后(90 d),种植植物的土壤总残留浓度为54.19~186.28 mg·kg-1,去除率为32.01%~72.31%,而无植物的土壤残留浓度为237.62 mg·kg-1,去除率仅为22.13%。种植植物的土壤中多环芳烃去除率为47.93%~84.85%,未种植植物的土壤中多环芳烃去除率仅为3.58%。这表明,种植植物可以增强土壤中多环芳烃的去除效果(P<0.05),明显促进了土壤中菲、荧蒽、芘和苯并[a]芘的降解。这可能是由于植物的根际效应强化了微生物对污染物的降解作用[20]。
|
在单作种植模式下,黑麦草、苏丹草、香根草和甜菜对4种多环芳烃的去除率为:黑麦草≈香根草>苏丹草>甜菜。黑麦草、苏丹草、香根草单种处理对土壤多环芳烃最终去除率分别为66.33%、61.94%、64.79%,甜菜单种处理的PAHs降解率显著低于前三者,仅有47.93%(P<0.05)。由于植物的根系形态和根际特征存在很大差异性,不同植物对PAHs污染土壤的修复潜力也会有很大的差异[21]。本试验中3种牧草单作处理的土壤中多环芳烃去除率高于甜菜单作,可能与牧草根系发达、植株生长旺盛有关;而苏丹草又低于黑麦草和香根草,可能是黑麦草和香根草较苏丹草须根丰富,一是根比表面积大,对PAHs吸收大,二是两者具有较大的地表覆盖率,根系分泌物数量和种类多,从而刺激了来源于根的酶活性和根际微生物数量,利于PAHs降解。
在间作植物种植模式中,甜菜/黑麦草间作、甜菜/苏丹草间作及甜菜/香根草间作处理的 PAHs最终去除率分别为84.85%、79.96%、84.11%,显著高于单种处理。由此可知,甜菜与三种牧草间作明显促进了土壤中多环芳烃的降解,间作模式的修复效果优于单作。潘声旺等[22]通过研究紫花苜蓿和油菜间作对菲、芘污染土壤的修复,认为间作模式的修复效果明显优于单作模式。张晓斌等[23]通过研究黑麦草和苜蓿间作对菲污染土壤的修复效应,得出了类似的结论。这可能是由于不同植物品种组合形成的间作系统,能改变根际微环境的理化性质和生物学特性,特别是能通过根系分泌物和其他根际过程改变根际微生物的种类和数量、根际土壤酶的活性和植物生长的营养条件等,最终影响PAHs的根际降解和植物吸收[24]。
同等条件下,土壤中污染物降解率顺序为菲>荧蒽>芘>苯并[a]芘,并且苯并[a]芘的降解率显著低于其他3种污染物。这可能与分子量增大、苯环数增加,降解难度变大,在土壤中持留性增强有关。袁馨等[25]研究了苏丹草对土壤中菲、芘的去除效果,种植苏丹草60 d后,土壤菲、芘去除率分别为73.07%~83.92%、63%~77.62%,可见三环菲的去除率高于四环芘。
2.3 不同处理下土壤中多酚氧化酶活性的变化土壤酶活性不仅易受土壤环境中的物理、化学及生物因素的影响,又能反映出土壤微生物的总体活性,对环境因素和人为因素都极其敏感[26-27],常被作为指示土壤污染的重要生物活性之一[28]。
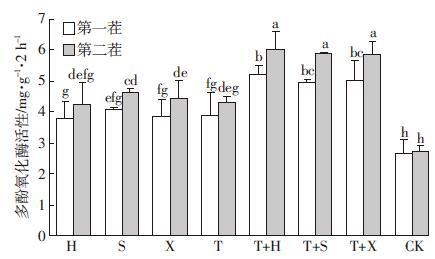
多酚氧化酶是土壤中重要的氧化还原酶,能够参与芳香族类化合物的分解转化过程,含苯环的物质进入土壤能诱导和激活其中的多酚氧化酶,促进此类物质的氧化分解[29],而是否种植植物下土壤中多酚氧化酶活性的差值反映植物根系对土壤中多酚氧化酶活性影响的强度。如图 2所示,无植物种植的土壤两次采样后,多酚氧化酶活性没有明显变化。H、S、X、T单作与CK多酚氧化酶活性差值分别为1.13、1.44、1.18、1.22 mg·g-1·2h-1,T+H、T+S、T+X与CK多酚氧化酶活性差值分别为2.56、2.32、2.38 mg·g-1·2h-1,单作、间作各自之间多酚氧化酶活性没有明显差别,但间作种植多酚氧化酶活性明显高于单作。间作促进多酚氧化酶活性增强,可能是基于甜菜和牧草间作在土壤生化过程中共同作用改善了根际生态环境和土壤质量,提高了根际微生物群落的新陈代谢活动,使植物根系和微生物分泌释放了更多的多酚氧化酶,从而促进PAHs的降解。无论是间作还是单作,第一茬植物种植后土壤中多酚氧化酶活性均低于第二茬,可能是由于第一茬植物种植时土壤中多环芳烃处于一个高浓度水平,而高浓度PAHs的毒性抑制了土壤中多酚氧化酶活性。这是由于高浓度PAHs对植物及土壤微生物产生毒害所致,但对低中浓度来说,效果不明显。丁克强等[8]在黑麦草对菲污染土壤修复研究发现,低剂量菲处理的植物对酶活性的作用最大,而中、高剂量处理的可能由于菲的抑制作用,土壤的多酚氧化酶活性减少;并且黑麦草对土壤多酚氧化酶的产生有促进作用,这种作用与植物生长时间、土壤中菲含量和毒性有关,表现为随时间而变化。本研究结果与之一致。
|
| 图 2 不同处理土壤中多酚氧化酶活性变化 Figure 2 Changes of polyphenol oxidase activities under different planting patterns |
过氧化氢酶是在生物呼吸和有机物的生物化学氧化反应过程中形成的,对土壤有机质分解和转化起着重要作用,同时它能促进H2O2分解,有利于防止H2O2对生物体的毒害作用,因此也常被用作 PAHs 引起的氧化胁迫生物标志物[30]。通过探讨不同种植模式对土壤中过氧化氢酶活性的影响,可以比较全面地了解多环芳烃对土壤酶活性的影响及过氧化氢酶在多环芳烃降解过程中所起的作用。
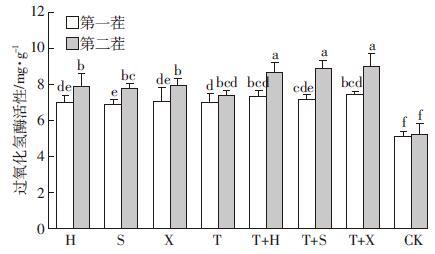
如图 3,对于无植物种植土壤中过氧化氢酶活性变化情况类似于多酚氧化酶,说明植物种植与否对于两种酶的活性是一个关键因素。第一茬植物种植后土壤中过氧化氢酶在H、S、X、T单作,T+H、T+S、T+X间作这7个处理中的活性变化幅度较小,且处理间差异不显著(P>0.05),但活性是无植物种植土壤的1.33~1.45 倍,说明植物的种植增强了土壤中过氧化氢酶的活性,但过氧化氢酶对外加PAHs较多酚氧化酶更为敏感。马恒亮等[31]研究认为在35 d小麦/苜蓿套作期间,过氧化氢酶活性达到极值所需时间短,其对污染物相对敏感,过氧化氢酶可作为关键酶,用于评价土壤PAHs污染状况。第二茬植物种植后土壤中过氧化氢酶活性间作与单作处理间出现明显差别,间作过氧化氢酶活性均值是单作的1.14 倍。这说明两茬植物种植后,植物与微生物等作用改善了土壤环境,并且间作优于单作,在低浓度污染水平下过氧化氢酶活性提高。
|
| 图 3 不同处理土壤中过氧化氢酶活性变化 Figure 3 Changes of catalase activities under different planting patterns |
(1) 在试验浓度(0~350 mg·kg-1)范围内,甜菜、黑麦草、苏丹草、香根草能够在PAHs污染土壤中正常生长,污染水平、栽培模式差异对植物生长有一定影响,在土壤污染条件下,甜菜与牧草间作更有利于其生长。
(2) 甜菜与3种牧草间作时的去除率高于单独种植,强化效应明显。两茬植物种植后,土壤中PAHs总去除率高于无植物种植的土壤,植物促进了PAHs降解。植物根系发达、根系分泌物丰富更有利于PAHs去除。
(3) 同等条件下,土壤中污染物解率顺序为菲>荧蒽>芘>苯并[a]芘,并且苯并[a]芘的降解率显著低于其他3种污染物。
(4) 土壤酶活性对 PAHs 污染的响应受物种影响差异不显著,但间作酶活性明显高于单作处理。植物增强了土壤中多酚氧化酶和过氧化氢酶的活性,间接提高了土壤中生物活性,从而促进了土壤中PAHs的降解。
| [1] | 苑金鹏, 王晓利, 周家斌, 等. 济南市表层土壤中PAHs分布、来源及风险分析[J]. 环境化学, 2015, 34 (1) : 166–171 . YUAN Jin-peng, WANG Xiao-li, ZHOU Jia-bin, et al. Distribution, source and risk analysis of polycyclic aromatic hydrocarbons in top-soil from Jinan City[J]. Environmental Chemistry, 2015, 34 (1) :166–171 . |
| [2] | 曹云者, 柳晓娟, 谢云峰, 等. 我国主要地区表层土壤中多环芳烃组成及含量特征分析[J]. 环境科学学报, 2012, 32 (1) : 197–203 . CAO Yun-zhe, LIU Xiao-juan, XIE Yun-feng, et al. Patterns of PAHs concentrations and components in surface soils of main areas in China[J]. Acta Scientiae Circumstantiae, 2012, 32 (1) :197–203 . |
| [3] | Hamdi H, Benzarti S, Aoyama I, et al. Rehabilitation of degraded soils containing aged PAHs based on phytoremediation with alfalfa(Medicago sativa L.)[J]. International Biodeterioration & Biodegradation, 2012, 67 :40–47 . |
| [4] | Fismes J, Perrin-Ganier C, Empereur-Bissonnet P, et al. Soil-to-root transfer and translocation of polycyclic aromatic hydrocarbons by vegetables grown on industrial contaminated soils[J]. Journal of Environmental Quality, 2002, 31 (5) :1649–1656 . |
| [5] | 周际海, 袁颖红, 朱志保, 等. 土壤有机污染物生物修复技术研究进展[J]. 生态环境学报, 2015, 24 (2) : 343–351 . ZHOU Ji-hai, YUAN Ying-hong, ZHU Zhi-bao, et al. A review on bioremediation technologies of organic pollutants contaminated soils[J]. Ecology and Environmental Sciences, 2015, 24 (2) :343–351 . |
| [6] | 贾婵, 呼世斌, 张春慧, 等. 苏丹草对镉-芘复合污染土壤的修复作用[J]. 农业环境科学学报, 2014, 33 (6) : 1139–1145 . JIA Chan, HU Shi-bin, ZHANG Chun-hui, et al. Phytoremediation of cadmium and pyrene co-polluted soil by Sudan grass(Sorghumvulgare L.)[J]. Journal of Agro-Environment Science, 2014, 33 (6) :1139–1145 . |
| [7] | 范淑秀, 李培军, 何娜, 等. 多环芳烃污染土壤的植物修复研究进展[J]. 农业环境科学学报, 2008, 27 (6) : 2007–2013 . FAN Shu-xiu, LI Pei-jun, HE Na, et al. Research of phytoremediation on contaminated soil with polycyclic aromatic hydrocarbons(PAHs)[J]. Journal of Agro-Environment Science, 2008, 27 (6) :2007–2013 . |
| [8] | 丁克强, 骆永明, 刘世亮, 等. 黑麦草对菲污染土壤修复的初步研究[J]. 土壤, 2002, 34 (4) : 233–236 . DING Ke-qiang, LUO Yong-ming, LIU Shi-liang, et al. Study on phytoremediation of phenanthrene-contaminated soil with ryegrass(Lolium multiflorum Lam)[J]. Soil, 2002, 34 (4) :233–236 . |
| [9] | 范淑秀, 李培军, 巩宗强, 等. 苜蓿对多环芳烃菲污染土壤的修复作用研究[J]. 环境科学, 2007, 28 (9) : 2080–2084 . FAN Shu-xiu, LI Pei-jun, GONG Zong-qiang, et al. Study on phytoremediation of phenanthrene-contaminated soil with alfalfa(Medicago sativa L.)[J]. Environmental Science, 2007, 28 (9) :2080–2084 . |
| [10] | 沈源源, 滕应, 骆永明, 等. 几种豆科、禾本科植物对多环芳烃复合污染土壤的修复[J]. 土壤, 2011, 43 (2) : 253–257 . SHEN Yuan-yuan, TENG Ying, LUO Yong-ming, et al. Remediation efficiency of several legumes and grasses in PAH-contaminated soils[J]. Soils, 2011, 43 (2) :253–257 . |
| [11] | Xiao N, Liu R, Jin C X, et al. Efficiency of five ornamental plant species in the phytoremediation of polycyclic aromatic hydrocarbon(PAH)-contaminated soil[J]. Ecological Engineering, 2015, 75 (2) :384–391 . |
| [12] | D'Orazio V, Ghanem A, Senesi N. Phytoremediation of pyrene contaminated soils by different plant species[J]. CLEAN-Soil, Air, Water, 2013, 41 (4) :377–382 . |
| [13] | 耿贵. 作物根系分泌物对土壤碳、氮含量、微生物数量和酶活性的影响[D]. 沈阳:沈阳农业大学, 2011. GENG Gui. Effect of crop root exudates on carbon and nitrogen contents, microorganisms quatity and enzyme activities in soil[D]. Shenyang:Shenyang Agricultural University, 2011. |
| [14] | 鲍士旦. 土壤农化分析[M].三版. 北京: 中国农业出版社, 2008 BAO Shi-dan. Soil agro-chemistrical analysis[M].3rd edition. Beijing: China Agriculture Press, 2008 . |
| [15] | 宋玉芳, 区自清, 孙铁珩, 等. 土壤、植物样品中多环芳烃(PAHs)分析方法研究[J]. 应用生态学报, 1995, 6 (1) : 92–96 . SONG Yu-fang, OU Zi-qing, SUN Tie-heng, et al. Analytical method of polycyclic aromatic hydrocarbons(PAHs) in soil and plant samples[J]. Chinese Journal of Applied Ecology, 1995, 6 (1) :92–96 . |
| [16] | 周礼恺, 张志明. 土壤酶活性的测定方法[J]. 土壤通报, 1980, 5 (1) : 37–38 . ZHOU Li-kai, ZHANG Zhi-ming. The determination methods of soil enzyme activity[J]. Chinese Journal of Soil Science, 1980, 5 (1) :37–38 . |
| [17] | 李隆, 杨思存, 孙建好, 等. 小麦/大豆间作中作物种间的竞争作用和促进作用[J]. 应用生态学报, 1999, 10 (2) : 197–200 . LI Long, YANG Si-cun, SUN Jian-hao, et al. Interspecific competition and facilitation in wheat/soybean intercropping system[J]. Chinese Journal of Applied Ecology, 1999, 10 (2) :197–200 . |
| [18] | Cheema S A, Khan M I, Tang X, et al. Enhancement of phenanthrene and pyrene degradation in rhizosphere of tall fescue(Festuca arundinacea)[J]. Journal of Hazardous Materials, 2009, 166 (2) :1226–1231 . |
| [19] | 高彦征, 凌婉婷, 朱利中, 等. 黑麦草对多环芳烃污染土壤的修复作用及机制[J]. 农业环境科学学报, 2005, 24 (3) : 498–502 . GAO Yan-zheng, LING Wan-ting, ZHU Li-zhong, et al. Ryegrass-accelerating degradation of polycyclic aromatic hydrocarbons(PAHs) in soils[J]. Journal of Agro-Environment Science, 2005, 24 (3) :498–502 . |
| [20] | Sun T R, Cang L, Wang Q Y, et al. Roles of abiotic losses, microbes, plant roots, and root exudates on phytoremediation of PAHs in a barren soil[J]. Journal of Hazardous Materials, 2010, 176 (1-3) :919–925 . |
| [21] | Khan S, Hesham A E L, Qing G, et al. Biodegradation of pyrene and catabolic genes in contaminated soils cultivated with Lolium multiflorum L.[J]. Journal of Soils and Sediments, 2009, 9 (5) :482–491 . |
| [22] | 潘声旺, 魏世强, 袁馨, 等. 油菜-紫花苜蓿混种对土壤中菲、芘的修复作用[J]. 中国农业科学, 2009, 42 (2) : 561–568 . PAN Sheng-wang, WEI Shi-qiang, YUAN Xin, et al. Mechanisms of the removal and remediation of phenanthrene and pyrene in soil with mixed cropping of alfalfa and rape[J]. Scientia Agricultura Sinica, 2009, 42 (2) :561–568 . |
| [23] | 张晓斌, 占新华, 周立祥, 等. 小麦/苜蓿套作条件下菲污染土壤理化性质的动态变化[J]. 环境科学, 2011, 32 (5) : 1462–1470 . ZHANG Xiao-bin, ZHAN Xin-hua, ZHOU Li-xiang, et al. Dynamic changes of physicochemical properties in phenanthrene-contaminated soil under wheat and clover intercropping[J]. Environmental Science, 2011, 32 (5) :1462–1470 . |
| [24] | 李隆, 李晓林, 张福锁. 小麦-大豆间作中小麦对大豆磷吸收的促进作用[J]. 生态学报, 2000, 20 (4) : 629–633 . LI Long, LI Xiao-lin, ZHANG Fu-suo. Facilitation of wheat to phosphorus uptake by soybean in the wheat-soybean intercropping[J]. Acta Ecologica Sinica, 2000, 20 (4) :629–633 . |
| [25] | 袁馨, 魏世强, 潘声旺. 苏丹草对土壤中菲芘的修复作用[J]. 农业环境科学学报, 2009, 28 (7) : 1410–1415 . YUAN Xin, WEI Shi-qiang, PAN Sheng-wang. The remediation of phenanthrene and pyrene in soil by Sudan grass(Sorghum vulgare L.)[J]. Journal of Agro-Environment Science, 2009, 28 (7) :1410–1415 . |
| [26] | Allison S D, Jastrow J D. Activities of extracellular enzymes in physically isolated fractions of restored grassland soils[J]. Soil Biology and Biochemistry, 2006, 38 (11) :3245–3256 . |
| [27] | De Mora A P, Ortega-Calvo J J, Cabrera F, et al. Changes in enzyme activities and microbial biomass after “in situ” remediation of a heavy metal-contaminated soil[J]. Applied Soil Ecology, 2005, 28 (2) :125–137 . |
| [28] | Wang Y P, Shi J Y, Wang H, et al. The influence of soil heavy metals pollution on soil microbial biomass, enzyme activity, and community composition near a copper smelter[J]. Ecotoxicology and Environmental Safety, 2007, 67 (1) :75–81 . |
| [29] | Gianfreda L, Rao M A, Piotrowska A, et al. Soil enzyme activities as affected by anthropogenic alterations:Intensive agricultural practices and organic pollution[J]. Science of the Total Environment, 2005, 341 (1) :265–279 . |
| [30] | Lionetto M G, Caricato R, Giordano M E, et al. Integrated use of biomarkers(acetylcholinesterase and antioxidant enzymes activities) in Mytilus galloprovincialis and Mullus barbatus in an Italian coastal marine area[J]. Marine Pollution Bulletin, 2003, 46 (3) :324–330 . |
| [31] | 马恒亮, 占新华, 张晓斌, 等. 小麦/苜蓿套作对菲污染土壤酶活性的影响[J]. 环境科学, 2009, 30 (12) : 3684–3690 . MA Heng-liang, ZHAN Xin-hua, ZHANG Xiao-bin, et al. Enzymatic activities of phenanthrene contaminated soil in wheat and clover intercropping system[J]. Environmental Science, 2009, 30 (12) :3684–3690 . |
 2016, Vol. 35
2016, Vol. 35