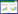文章信息
- 常红, 李利芬, 黄丽
- CHANG Hong, LI Li-fen, HUANG Li
- 皂角苷对红壤和黄褐土中Pb2+、Zn2+的解吸特征
- Desorption characteristics of Pb2+ and Zn2+ from red soil and yellow-cinnamon soil by saponin
- 农业环境科学学报, 2017, 36(1): 93-100
- Journal of Agro-Environment Science, 2017, 36(1): 93-100
- http://dx.doi.org/10.11654/jaes.2016-0948
文章历史
- 收稿日期: 2016-07-22
近年来,重金属污染事故不断发生,引起人们的普遍关注,2016 年国务院颁布了《土壤污染防治行动计划》,强调对重金属污染进行综合整治。土壤中重金属具有隐蔽性、难降解、移动性差与易富集等特点,能通过食物链、人体接触等多种途径对人类及生态环境造成危害,铅、锌是土壤中常见的重金属[1]。据统计,目前我国受As、Cu、Hg、Pb、Zn 等重金属污染的耕地面积已达2000 万hm2,超出耕地总面积的10%,受污染粮食多达1200万t,且多集中于经济较发达地区[2]。因此,如何有效降低或减少重金属的污染危害成为土壤环境领域的重点课题[3-5]。
化学淋洗技术是一种有效的土壤修复方法,被广泛应用[6]。常用的淋洗剂包括无机或有机酸、无机盐化合物、螯合剂和表面活性剂等[7-9]。由于生物表面活性剂(Bio-surfactant)来源广泛,化学结构多样,易降解,环境相容性好,在重金属污染耕地土壤的修复研究中日益受到关注[10]。皂角苷作为一种生物表面活性剂,其结构中的羧基和酯基等能够有效地络合土壤中的重金属离子[11]。研究表明,皂角苷浓度与重金属的去除效率有很大关系,用皂角苷去除三种土壤(粘土、砂土和含有大量有机质的土壤)中的重金属,其对Cu2+、Pb2+和Zn2+的去除率分别达到了90%~100%、40%~50%和85%~98%[12];当皂角苷浓度为50 g·L-1、pH 值为5.2 时,土壤中Cu2+、Cd2+、Pb2+和Zn2+的解吸率分别可达24.4%、45.6%、17.6%和19.0%,并且提高皂角苷浓度和降低溶液pH 值,这4 种重金属的解吸率均得到提高[12]。用茶皂素洗脱土壤中的重金属,其酸溶态和可还原态的含量显著降低,皂素与柠檬酸的配合作用下Zn2+、Pb2+的去除率显著提高[13]。
土壤中矿物组成和结构不同使土壤表面电荷性质存在差异,是影响土壤吸附-解吸重金属最根本的因素之一。我国南方分布着大面积的酸性红黄壤、红壤等,这些土壤风化程度较高,主要粘土矿物是高岭石和氧化物等,可变电荷表面多,永久负电荷表面很少[14]。从南向北,恒电荷土壤逐渐增多。黄褐土作为典型的恒电荷土壤分布在我国长江中下游沿岸,主要成分为伊利石等。研究表明,可变电荷土壤的阳离子交换量较恒电荷土壤的少,具有较小的重金属离子吸附量[15]。恒电荷土壤对Cu2+、Cd2+、Zn2+、Ni2+、Co2+的吸附量比可变电荷土壤的高[16]。红壤对Co2+、Cu2+、Pb2+、Zn2+吸附主要受控于它的氧化物和高岭石的可变电荷表面,而恒电荷表面为主的2:1型粘土矿物的作用不大[15]。
目前,对土壤中重金属吸附解吸行为的研究较多,但对不同电荷类型土壤中皂角苷解吸重金属影响的报道较少。为此,本文以亚热带地区的红壤和黄褐土作为研究对象,分析皂角苷浓度、溶液pH、解吸次数等对污染土壤中Pb2+和Zn2+解吸效果的影响,比较解吸前后土壤中重金属的形态变化,并分析皂角苷与金属的作用机理等,旨在揭示土壤的不同电荷性质对Pb2+和Zn2+解吸的影响,为皂角苷修复重金属污染土壤的研究提供理论依据。
1 材料与方法 1.1 供试土壤供试土壤分别为红壤和黄褐土。红壤采自湖南桃源的荒地,属第四纪Q2 沉积物母质发育的铁铝纲(美国土壤系统分类,1985);黄褐土采自湖北省襄阳市襄州区石桥镇竹园村的小麦田,属第四纪Q3 沉积物母质发育的淋溶土纲。采集表层0~27 cm 的土壤样品,经自然风干后,研碎,过100 目筛,保存备用。
土壤胶体制备方法:称取土壤样品20 g于1 L高脚烧杯中,加入约200 mL蒸馏水,人工搅拌状态下逐渐加入30% H2O2 50 mL,去除有机质,微热条件下不断搅拌直至无气泡产生,再加热使多余H2O2分解≥出。将分散均匀的混合物转入2 L 烧杯中,根据虹吸法提取粒径小于2 μm 的粘粒,提取后的胶体溶液静置24 h 自然沉淀,导出上层清液,下层悬液在12 000r·min-1条件下离心,并用95%酒精清洗3 次,然后将提取出的土壤胶体冷冻干燥,在玛瑙研钵中研磨过100目筛,于干燥器中保存备用[17]。
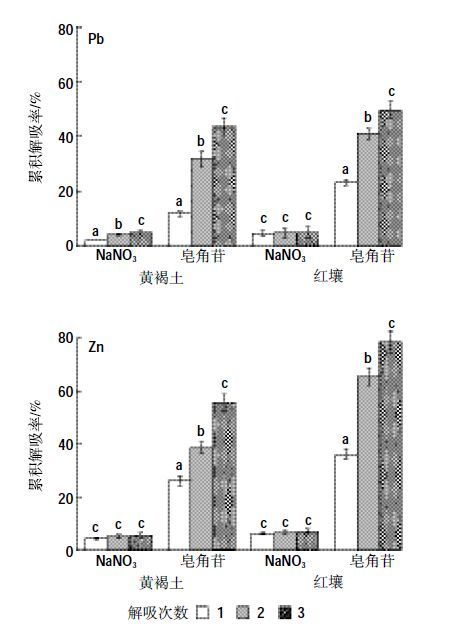
供试土壤的pH 用电位法测定(土液比为1:2.5);阳离子交换量用乙酸铵交换法测定;质地用吸管法测定;粘土矿物组成用X-射线衍射法测定,并采用峰面积半定量计算主要粘粒矿物含量;有机质的分析用重铬酸钾氧化法(外加热法)测定;比表面积(SSA)用全自动比表面和孔径分布分析仪(Quantachrome Au原tosorb-1)测定;游离Fe2O3 用连二亚硫酸钠-柠檬酸钠-重碳酸钠(DCB)比色法测定;MnO2 用醋酸铵-原子吸收光谱法测定[18];全铅、全锌用王水-高氯酸消煮,原子吸收光谱法测定[19]。供试土壤的物质组成和基本理化性质结果分别见表 1 和表 2。
供试红壤的pH 值较黄褐土的低,其有机质与铁氧化物远高于黄褐土的;红壤中伊利石和高岭石所占百分比较黄褐土的多,而黄褐土中主要粘土矿物为伊利石与蛭石;红壤较黄褐土具有较小的阳离子交换量,二者化学性质有较大的差别。
称取两种土壤样品各500 g,分别单独添加浓度为1000 mg·L-1的Pb(NO3)2 和1000 mg·L-1 的Zn(NO3)2溶液500 mL,室温下培养,间歇搅拌并保持24%含水量,自然陈化6个月,制备重金属污染土壤样品。红壤和黄褐土的Pb2+含量分别为1 865.31、1 564.03 mg·kg-1,Zn2+含量分别为1 033.51、830.64 mg·kg-1。
1.2 供试试剂皂角苷(Quillajasaponin)购买于Sigma-Aldich 公司,其临界胶团浓度为0.51 g·L-1,相对分子量为1200~2800,熔点223~224℃,水溶液呈茶褐色,pH 值为5~7,表面张力为47~51 mN·m-1[20]。其他试剂均为市售分析纯试剂,实验用水为去离子水。
2 实验方法 2.1 不同浓度的皂角苷对重金属的解吸分别称取人工污染土壤样品0.1 g于各离心管中,分别加入pH 为5.0(0.1 mol·L-1 HNO3 调节)浓度为0~10 g·L-1 的皂角苷溶液10 mL,25℃下250 r·min-1振荡24 h,离心并收集上清液,采用原子吸收分光光度法测定上层清液中Pb2+或Zn2+的含量。每个实验均设3 个重复[19]。
2.2 不同pH 的皂角苷对重金属的解吸分别称取人工污染土壤样品0.1 g于各离心管中,分别加入pH为3.6、4.8、5.2、6.0、7.0,浓度为5 g·L-1的皂角苷溶液10 mL,25益下250 r·min-1振荡24 h,离心收集上清液,采用原子吸收分光光度法测定上层清液中Pb2+或Zn2+的含量。每个实验均设3 个重复[19]。
2.3 多次解吸分别称取人工污染土壤样品0.1 g于各离心管中,分别加入pH 3.0(根据2.2 的解吸结果与文献[12]报道确定)浓度为5 g·L-1 的皂角苷溶液10 mL,25℃下250 r·min-1振荡24 h,收集上清液,计为解吸1 次。按此步骤连续解吸3 次,每次收集上清液,采用火焰原子吸收分光光度法测定上层清液中Pb2+或Zn2+的含量[21]。同时,对照组为0.1 mol·L-1的NaNO3,称取土壤样品0.1 g于各离心管中并加入NaNO3溶液,其后试验过程同吸附试验。待该次解吸完成后,重复上述过程。测定扣除解吸残留液中的剩余重金属离子。
2.4 解吸前后土壤中重金属形态的测定从2.3 获得的土壤残渣量不足以完成形态分析试验,因此重新称取人工污染土壤样品10.0 g,用pH3.0、浓度5 g·L-1的皂角苷溶液进行解吸试验。25℃下250 r·min-1 振荡24 h,离心后去除上层清液,样品冷冻干燥。分别称取经皂角苷处理前、后的土壤样品0.5g各3份,采用BCR 分级方法[22-24]对样品中各金属的形态进行分析,分别测得金属Pb2+、Zn2+酸溶态、还原态、氧化态和残渣态四种形态的含量。
2.5 土壤Zeta电位测定称取0.04 g 土壤胶体样品于250 mL 三角瓶中,分别加入200 mL 0.1 g·L-1和1 g·L-1皂角苷溶液以及0.01 mol·L-1 NaNO3(作对照),超声1 h 后,分装在100mL 三角瓶中(各30 mL),用NaOH/HNO3 调节pH 分别为2、2.5、3、4、5、6,放置3 d,在此期间控制pH 在预设范围内(2~6),而后测定pH 值(pH 计)及Zeta 电位(纳米粒度及Zeta电位分析仪ZEM3600)[25]。
3 结果与讨论 3.1 皂角苷浓度对Pb2+和Zn2+解吸的影响随着皂角苷浓度的升高(0~10 g·L-1),黄褐土和红壤中Pb2+和Zn2+的解吸率(图 1)均增大,与颜建婷等[11]的研究结果类似。黄褐土中Pb2+的最大解吸率小于10%,红壤Pb2+的解吸率高于黄褐土,最大解吸率达到16%(皂角苷浓度为10 g·L-1,pH 3时)。相较于Pb2+,相同条件下两种土壤中Zn2+的解吸率明显高很多,黄褐土中Zn2+的最大解吸率约为30%,红壤中Zn2+的解吸率甚至达到了47%。总体来看,对于Pb2+和Zn2+,红壤的解吸率均大于黄褐土,可见皂角苷对红壤中重金属的解吸较黄褐土的容易;另外,两种土壤中Zn2+的解吸率明显高于Pb2+。一方面可能是由于红壤与黄褐土的氧化物含量和电化学性质不同,另一方面铅和锌两种金属的性质也不同。

|
| 图 1 不同皂角苷浓度下两土壤中重金属的解吸率 Figure 1 Desorption rates of heavy metal from two kinds of soils under different saponin concentrations |
在皂角苷浓度相同(5 g·L-1)时,随着pH 的升高,红壤和黄褐土中Pb2+、Zn2+的解吸率下降(图 2),与蒋煜峰[27]等的研究结果类似。pH从3.6上升到4.1,Pb2+解吸率下降不明显;pH 从4.1 上升到5.9,单位pH 的升高导致红壤的Pb2+解吸率下降约4.0%,大于黄褐土(2.1%);而在pH 5.9~6.5 范围内,红壤对pH 变化表现出一定的缓冲能力,解吸率没有明显下降;pH 大于6.5,红壤中Pb2+的解吸率迅速降低,其降幅大于黄褐土。对于Zn2+的解吸,在pH 3.6~5.9 范围内,单位pH 的升高导致黄褐土的Zn2+解吸率下降约20.3%,而红壤的Zn2+解吸率下降仅12.2%;当pH 从5.9 升高到6.5,红壤中Zn2+的解吸率大于黄褐土;pH 高于6.5后,pH的变化对Zn2+的解吸率影响不大。
|
| 图 2 不同pH下重金属的解吸率 Figure 2 Desorption rates of heavy metal from two kinds of soils under different pH values |
Hong 等[28]研究认为,随pH 值的增加,皂角苷与重金属的结合能力减弱,即皂角苷与重金属配合物稳定常数下降,导致在碱性条件下皂角苷淋洗重金属的效率降低。pH对重金属去除效果除了与重金属的形态以及皂角苷本身的性质有关外,还与这两种土壤的不同类型电荷表面有关。相比黄褐土,供试红壤中有机质和铁氧化物多(表 1),2:1 型矿物少等因素,使其可变电荷表面较多,造成了皂角苷对红壤与黄褐土中重金属解吸的差异。土壤本身组成对外加酸碱液所具有的较强缓冲能力,也减弱了pH变化带来的影响[29]。
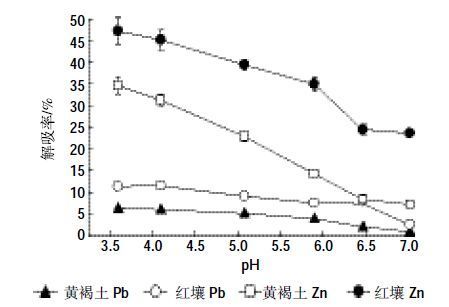
3.3 解吸次数对Pb2+和Zn2+解吸的影响皂角苷解吸土壤中的重金属,无论是对Pb2+还是Zn2+,都表现出了较好的效果(图 3)。1 至3 次解吸结果表明,红壤中Pb2+的累积解吸率分别为23.16%、41.00%、49.60%,黄褐土的分别为11.82%、31.89%、43.52%。可以看到第二次解吸后,红壤中Pb2+的累积解吸率约增加0.8倍,黄褐土的增加约1.8 倍,第三次解吸率的增幅较第二次的低。对于Zn2+而言,经过1至3 次解吸后,红壤的累积解吸率分别为35.99%、65.37% 、78.57%,黄褐土的为26.10%、38.54%、55.66%。第二、三次Zn2+的解吸率增幅低于Pb2+,表明虽然Zn2+的解吸率较Pb2+的高,但多次解吸对Pb2+的增效更明显。相比较而言,电解质溶液(0.01 mol·L-1NaNO3溶液)的解吸率要低得多,连续3 次解吸后总解吸率均低于10%,且多次解吸的增效并不明显。一些研究结果也证实[21, 29-30],连续多次淋洗时重金属的不同形态间发生再分配,可显著增加重金属的淋洗量。
|
| 图 3 多次解吸下重金属的解吸率 Figure 3 Desorption rates of heavy metal from two kinds of soils by multiple washings 皂角苷浓度为5 g·L-1,pH 3;不同小写字母表示处理间差异显著(P<0.05) |
解吸前红壤中的Pb2+含量大于黄褐土(表 1),以可还原态的含量最高(约占34%),酸溶态的占27%,其次是残渣态的,可氧化态的含量最少(仅占20%);黄褐土中可还原态Pb2+的含量约占50%,残渣态的含量约占22%,可氧化态和酸溶态Pb2+的含量相差不大,所占比例也较小。红壤和黄褐土中全量Zn2+的含量相当,但赋存形态有差异。红壤中以酸溶态Zn2+的含量最多,约占34%,其次是残渣态和可还原态的,可氧化态的含量最少;黄褐土中可还原态Zn2+的含量最多,约占29%,酸溶态和残渣态的含量相差不大,最少的是可氧化态的Zn2+。Zn2+在土壤中的存在形态可能与有机质含量有关(表 1)。与黄褐土相比,红壤中的有机质含量要高得多(红壤为17.87 g·kg-1,黄褐土为7.94 g·kg-1),而红壤中可氧化态Zn2+的含量比黄褐土约高36%(表 3)。
 |
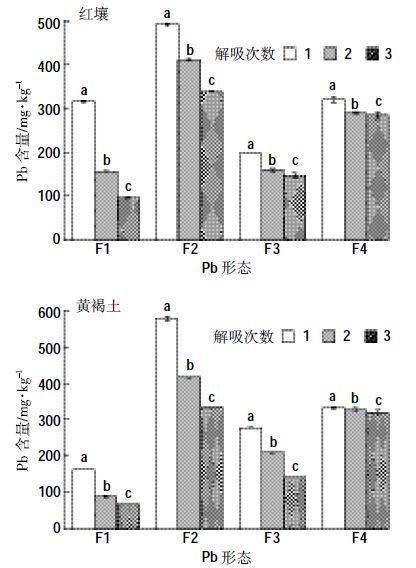
与解吸前相比,红壤第一次解吸后,酸溶态Pb2+含量降低最为明显(图 4),降低约38%;可还原态Pb2+含量减少略低,为22%;其次是残渣态的Pb2+,降低15%;可氧化态Pb2+的变化不大。从图 4 还可以看出,增加解吸次数,不同形态的Pb2+含量显著降低,特别是第一次解吸和第二次解吸差异显著,第三次解吸后,可氧化态和残渣态Pb2+的含量变化不大。
|
| 图 4 皂角苷对不同形态Pb 的解吸 Figure 4 Pb Desorption of different fractions from soils using saponin 皂角苷浓度为5g·L-1、pH3;不同小写字母表示处理间差异显著(P<0.05);F1、F2、F3、F4分别为酸溶态、可还原态、可氧化态、残渣态 |
单次解吸,黄褐土中可还原态Pb2+含量的变化最大,降低约26%,酸溶态Pb2+含量下降15%,残渣态Pb 含量降低4%,可氧化态Pb含量不降反升。这可能是在解吸反应过程中Pb2+的形态转化所致。3次解吸后,其酸溶态、可还原态、可氧化态和残渣态含量累计减少分别为64%、57%、32%、7%。
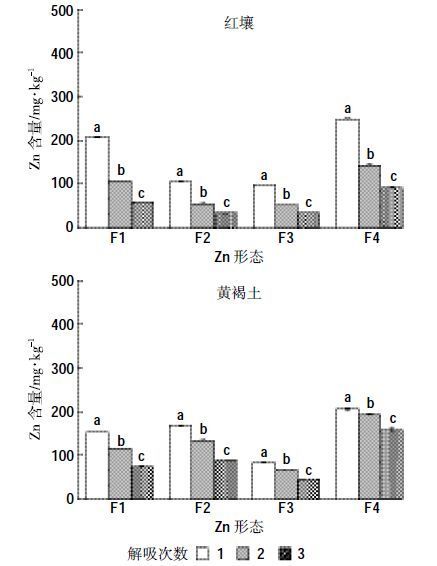
3.4.2 Zn对红壤来说,第一次解吸后,下降最大的是酸溶态的Zn2+,约40%(图 5);可还原态Zn2+含量的下降略低,约51%;可氧化态和残渣态Zn2+含量减少较低,分别为35%和10%。增加解吸次数,不同形态Zn2+含量均显著降低,累计可达66%~84%。
|
| 图 5 皂角苷对不同形态Zn 的解吸 Figure 5 Zn Desorption of different fractions from soils using saponin 皂角苷浓度为5g·L-1、pH3;不同小写字母表示处理间差异显著(P<0.05),F1、F2、F3、F4分别为酸溶态、可还原态、可氧化态、残渣态 |
对黄褐土来说,各形态Zn2+的解吸量均显著低于红壤。单次解吸,酸溶态和可还原态Zn2+下降约30%,而可氧化态和残渣态Zn2+仅下降23%和6%。多次解吸后不同形态Zn2+含量明显减少,三次解吸后酸溶态、可还原态、可氧化态和残渣态的累计下降分别为66%、62%、58%、28%。
两种土壤经单次解吸后,皂角苷能较大程度地降低土壤中酸溶态和可还原态Zn2+,对残渣态Zn2+的效果则不明显,但是经三次解吸后,残渣态Zn2+的解吸率达到了66%(红壤)和28%(黄褐土)。这表明多次解吸能够提高Zn2+的解吸率。一般酸溶态在环境中最不稳定,容易受外界pH、水分等条件的影响而重新释放进入土壤环境中,其生物可利用性较高[31]。
3.5 皂角苷对土壤Zeta 电位的影响红壤和黄褐土胶体的Zeta 电位(图 6)均随pH 升高而减小;在不加皂角苷的空白对照中,相同pH 下红壤胶体的Zeta 大于黄褐土。红壤胶体在pH 3.8 左右的Zeta 电位为零,而黄褐土胶体在pH 2时Zeta 电位为负。

|
| 图 6 吸附皂角苷后土壤表面Zeta 电位的变化 Figure 6 Changes of Zeta potential after saponin adsorption on soils |
添加皂角苷后,两种土壤胶体的Zeta 电位变化情况也不同。红壤胶体在pH<3.80时表面带正电荷,pH>3.8 时表面带负电荷;加入皂角苷处理使其Zeta电位向负值位移,且添加低浓度皂角苷时其位移较添加高浓度时的大。红壤胶体吸附皂角苷后Zeta 电位降低,可能是皂角苷离解提供的负离子促使其表面负电荷增加(皂角苷结构基团中的羧基离解出H+而带负电荷),而皂角苷溶液浓度较高的情况下会形成胶束,减少向红壤胶体表面转移负电荷,使得高浓度下位移减小。黄褐土胶体吸附皂角苷后Zeta 电位向正值位移,可能是皂角苷与黄褐土表面基团发生了缩合反应,消除了一部分负电荷量。总的来说,皂角苷能使黄褐土胶体的表面电荷向零趋近,即可使原本带负电荷的表面向正值位移,而红壤胶体的变化与其pH 有关,pH<4 时,带负电荷的表面向正值位移,pH>4 则相反。皂角苷浓度越大,向Zeta电位为零的线趋近越明显,并且随着pH的增加Zeta 电位变化趋缓。
添加皂角苷后,两种土壤的Zeta 电位均发生的不同变化,可能会在一定程度上影响两种土壤对Pb2+和Zn2+的吸附量。皂角苷对红壤中重金属的解吸率均较黄褐土高,原因可能是两种土壤的氧化物含量与表面化学性质差异较大。有待进一步深入研究。
4 结论皂角苷对两种供试土壤中Zn2+的解吸率明显高于Pb2+,且红壤中Zn2+和Pb2+的解吸率均大于黄褐土。红壤和黄褐土的表面电荷性质的不同,不仅决定着其对重金属的吸附特性,而且影响土壤对重金属的解吸。红壤中Pb2+的最大解吸率为16%,在黄褐土中则低于10%;红壤和黄褐土中Zn2+的最大解吸率分别为47%和30%(皂角苷浓度为10 g·L-1,pH 3时)。单次解吸,红壤中酸溶态Pb2+的含量降低最大,黄褐土中可还原态Pb2+的含量减少最多;红壤中Zn2+含量降低最大的是酸溶态,可氧化态和残渣态Zn2+的含量变化不大,黄褐土中酸溶态和可还原态的Zn2+含量下降约30%,而可氧化态和残渣态的Zn2+降低较少。增加解吸次数,不同形态的Pb2+和Zn2+解吸量均上升。
| [1] | 刘勇, 岳玲玲, 李晋昌. 太原市土壤重金属污染及其潜在生态风险评价[J]. 环境科学学报, 2011, 31(6) : 1285–1293. LIU Yong, YUE Ling-ling, LI Jin-chang. Evaluation of heavy metal contamination and its potential ecological risk to the soil in Taiyuan, China[J]. Acta Scientiae Circumstantiae, 2011, 31(6) : 1285–1293. |
| [2] | Wu G, Kang H B, Zhang X Y, et al. A critical review on the bio-removal of hazardous heavy metals from contaminated soils:Issues, progress, eco-environmental concerns and opportunities[J]. Journal of Hazardous Materials, 2010, 174 : 1–8. DOI:10.1016/j.jhazmat.2009.09.113 |
| [3] | 刘凤, 李梅, 张荣飞, 等. 拉萨河流域重金属污染及健康风险评价[J]. 环境化学, 2012, 31(5) : 580–585. LIU Feng, LI Mei, ZHANG Rong-fei, et al. Pollution analysis and health risk assessment of heavy metals in Lhasa River[J]. Environmental Chemistry, 2012, 31(5) : 580–585. |
| [4] | 俞斌, 夏会龙. 添加茶籽粕和EDTA对土壤中镍和锌形态变化及植物有效性的影响[J]. 应用生态学报, 2013, 24(6) : 1615–1620. YU Bin, XIA Hui-long. Effects of applying tea seed meal and EDTA on the speciation transformation and phyto-availability of nickel and zinc in soil[J]. Chinese Journal of Applied Ecology, 2013, 24(6) : 1615–1620. |
| [5] | 钮志远, 李长霞, 徐志兵. 安庆市部分市售蔬菜中铜含量及清洗方式的影响[J]. 环境化学, 2013, 32(2) : 331–332. NIU Zhi-yuan, LI Chang-xia, XU Zhi-bing. Effect of copper content and cleaning methods on the sale of vegetables in Anqing City[J]. Environmental Chemistry, 2013, 32(2) : 331–332. |
| [6] | 董汉英, 仇荣亮, 赵芝灏, 等. 工业废弃地多金属污染土壤组合淋洗修复技术研究[J]. 土壤学报, 2010, 47(6) : 1126–1133. DONG Han-ying, QIU Rong-liang, ZHAO Zhi-hao, et al. Sequential elution technique for remediation of multimetal contaminated brown field soil[J]. Acta Pedologica Sinica, 2010, 47(6) : 1126–1133. |
| [7] | 易龙生, 王文燕, 刘阳, 等. 柠檬酸、EDTA和茶皂素对重金属污染土壤的淋洗效果[J]. 安全与环境学报, 2014, 14(1) : 225–228. YI Long-sheng, WANG Wen-yan, LIU Yang, et al. Removal effects of the citric acid, EDTA and saponin on heavy metal contaminated soil[J]. Journal of Safety and Environment, 2014, 14(1) : 225–228. |
| [8] | 梁金利, 蔡焕兴, 段雪梅, 等. 有机酸土柱淋洗法修复重金属污染土壤[J]. 环境工程学报, 2012, 6(9) : 3339–3343. LIANG Jin-li, CAI Huan-xing, DUAN Xue-mei, et al. Remediation of heavy metal-polluted soils using organic acid washing[J]. Chinese Journal of Environmental Engineering, 2012, 6(9) : 3339–3343. |
| [9] | 曲蛟, 罗春秋, 丛俏, 等. 表面活性剂对土壤中重金属清洗及有效态的影响[J]. 环境化学, 2012, 31(5) : 620–624. QU Jiao, LUO Chun-qiu, CONG Qiao, et al. Extraction and availabilities of heavy metals in the soil by surfactants[J]. Environmental Chemistry, 2012, 31(5) : 620–624. |
| [10] | 雷国建, 陈志良, 刘千钧, 等. 生物表面活性剂及其在重金属污染土壤淋洗中的应用[J]. 土壤通报, 2013, 44(6) : 1508–1511. LEI Guo-jian, CHEN Zhi-liang, LIU Qian-jun, et al. Biosurfactants and their applications in soil flushing of heavy metal pollution[J]. Chinese Journal of Soil Science, 2013, 44(6) : 1508–1511. |
| [11] | 颜建婷, 莫创荣, 王东波, 等. 皂角苷对土壤中重金属铬的去除[J]. 广西大学学报(自然科学版), 2015, 40(3) : 558–564. YAN Jian-ting, MO Chuang-rong, WANG Dong-bo, et al. Removal of chromium from soil by saponin[J]. Journal of Guangxi University(Nat Sci Ed), 2015, 40(3) : 558–564. |
| [12] | 朱清清, 邵超英, 张琢, 等. 生物表面活性剂皂角苷增效去除土壤中重金属的研究[J]. 环境科学学报, 2010, 30(12) : 2491–2498. ZHU Qing-qing, SHAO Chao-ying, ZHANG Zhuo, et al. Saponin biosurfactant-enhanced flushing for the removal of heavy metals from soils[J]. Acta Scientiae Circumstantiae, 2010, 30(12) : 2491–2498. |
| [13] | 许丹丹, 许中坚, 邱喜阳, 等. 重金属污染土壤的柠檬酸-皂素联合修复研究[J]. 水土保持学报, 2013, 27(6) : 57–61. XU Dan-dan, XU Zhong-jian, QIU Xi-yang, et al. Study on combined remediation of citric acid and saponin in heavy metal contaminated soil[J]. Journal of Soil and Water Conservation, 2013, 27(6) : 57–61. |
| [14] | 刘冬碧, 贺纪正, 刘凡, 等. 中南地区几种土壤的表面电荷特性Ⅳ. 氧化铁铝对土壤表面电荷性质的影响[J]. 土壤学报, 2001, 38(1) : 46–50. LIU Dong-bi, HE Ji-zheng, LIU Fan, et al. Surface charge characteristics of soils in central and southern China Ⅳ. The effect of Fe and Al oxides on surface change characteristics of soils[J]. Acta Pedologica Sinica, 2001, 38(1) : 46–50. |
| [15] | 凌婉婷, 李学垣, 贺纪正, 等. 土壤表面电荷特征与重金属吸附-解吸的相互关系[J]. 土壤通报, 2002, 33(6) : 456–460. LING Wan-ting, LI Xue-yuan, HE Ji-zheng, et al. Interaction between heavy metals adsorption-desorption and charge character of soils[J]. Chinese Journal of Soil Science, 2002, 33(6) : 456–460. |
| [16] | 马毅杰, 陈家坊. 我国红壤中氧化铁形态及其特性和功能[J]. 土壤, 1998, 30(1) : 1–6. MA Yi-jie, CHEN Jia-fang. Morphology, characteristics and function of iron oxide in red soil of China[J]. Soil, 1998, 30(1) : 1–6. |
| [17] | 袁朝良. 几种土壤胶体电荷零点(ZPC)的初步研究[J]. 土壤学报, 1981, 18(4) : 345–352. YUAN Chao-liang. A preliminary study on the Zero Point of Charge(ZPC) of some soil colloids[J]. Acta Pedologica Sinica, 1981, 18(4) : 345–352. |
| [18] | 鲍士旦. 土壤农化分析[M]. 北京: 中国农业出版社, 1981: 136-139. BAO Shi-dan. Soil agricultural chemistry analysis[M]. Beijing: China Agriculture Press, 1981: 136-139. |
| [19] | Chen W J, Hsiao L C, Chen K K Y. Metal desorption from copper(Ⅱ)/nickel(Ⅱ)-spiked kaolin as a soil component using plant-derived saponin biosurfactant[J]. Process Biochem, 2008, 43 : 488–498. DOI:10.1016/j.procbio.2007.11.017 |
| [20] | 江和源, 张建勇, 高晴晴, 等. 茶皂素的性质、制备与应用[J]. 中国茶叶, 2007, 29(3) : 14–15. JIANG He-yuan, ZHANG Jian-yong, GAO Qing-qing, et al. Preparation and application properties of tea saponin[J]. China Tea, 2007, 29(3) : 14–15. |
| [21] | Gusiatin Z M, Klimiuk E. Metal(Cu, Cd and Zn) removal and stabilization during multiple soil washing by saponin[J]. Chemosphere, 2012, 86 : 383–391. DOI:10.1016/j.chemosphere.2011.10.027 |
| [22] | Maity J P, Huang Y M, Fan C W, et al. Evaluation of remediation process with soapberry derived saponin for removal of heavy metals from contaminated soils in Hai-Pu, Taiwan[J]. Journal of Environmental Sciences, 2013, 25(6) : 1180–1185. DOI:10.1016/S1001-0742(12)60162-4 |
| [23] | 蓝梓铭, 莫创荣, 段秋实, 等. 鼠李糖脂对剩余污泥中铜和镍的去除[J]. 环境工程学报, 2014, 8(3) : 1174–1178. LAN Zi-ming, MO Chuang-rong, DUAN Qiu-shi, et al. Removal of cooper and nickel from excess sludge by rhamnolipid[J]. Chinese Journal of Environmental Engineering, 2014, 8(3) : 1174–1178. |
| [24] | Wu Q, Cui Y, Li Q, et al. Effective removal of heavy metals from industrial sludge with the aid of a biodegradable chelating ligand GLDA[J]. Journal of Hazardous Materials, 2015, 283 : 748–754. DOI:10.1016/j.jhazmat.2014.10.027 |
| [25] | Leroy P, Tournassat C, Bernard O, et al. The electrophoretic mobility of montmorillonite:Zeta potential and surface conductivity effects[J]. J Colloid Interf Sci, 2015, 451 : 21–39. DOI:10.1016/j.jcis.2015.03.047 |
| [26] | 蒋煜峰, 展惠英, 张德懿, 等. 皂角苷络合洗脱污灌土壤中重金属的研究[J]. 环境科学学报, 2006, 26(8) : 1315–1319. JIANG Yu-feng, ZHAN Hui-ying, ZHANG De-yi, et al. Study on desorption of heavy metal in sewage-irrigated soil by complexing with saponin[J]. Acta Scientiae Circumstantiae, 2006, 26(8) : 1315–1319. |
| [27] | Hong K J, Tokunaga S, Ishigami T, et al. Extraction of heavy metals from MSW incinerator fly ash using saponins[J]. Chemosphere, 2000, 41(3) : 345–352. DOI:10.1016/S0045-6535(99)00489-0 |
| [28] | Li X, Shen Z, Wai O W H, et al. Chemical forms of Pb, Zn and Cu in the sediment profiles of the Pearl River Estuary[J]. Marine Pollution Bulletin, 2001, 42(3) : 215–223. DOI:10.1016/S0025-326X(00)00145-4 |
| [29] | 刘霞, 王建涛, 张萌, 等. 螯合剂和生物表面活性剂对Cu、Pb污染塿土的淋洗修复[J]. 环境科学, 2013, 34(4) : 1590–1597. LIU Xia, WANG Jian-tao, ZHANG Meng, et al. Remediation of Cu-Pb-Contaminated loess soil by leaching with chelating agent and biosurfactant[J]. Environmental Science, 2013, 34(4) : 1590–1597. |
| [30] | 邓红侠, 刘霞, 王建涛, 等. 不同淋洗剂对污染塿土Cu、Pb的淋洗修复研究[J]. 西北农林科技大学学报(自然科学版), 2014, 42(8) : 191–198. DENG Hong-xia, LIU Xia, WANG Jian-tao, et al. Leaching remediation of copper and lead in contaminated Lou soil using different eluents[J]. Journal of Northwest A&F University(Nat, Sci, Ed,), 2014, 42(8) : 191–198. |
| [31] | 雷鸣, 廖柏寒, 秦普丰. 土壤重金属化学形态的生物可利用性评价[J]. 生态环境, 2007, 16(5) : 1551–1556. LEI Ming, LIAO Bo-han, QIN Pu-feng. Assessment of bioavailability of heavy metal in contaminated soils with chemical fractionation[J]. Ecology and Environment, 2007, 16(5) : 1551–1556. |
 2017, Vol. 36
2017, Vol. 36