文章信息
- 苗育, 郭学涛, 宋晓梅, 高良敏, 胡友彪
- MIAO Yu, GUO Xue-tao, SONG Xiao-mei, GAO Liang-min, HU You-biao
- 氧化石墨烯对泰乐菌素的吸附特性
- The sorption properties of tylosin on graphene oxide
- 农业环境科学学报, 2017, 36(1): 183-188
- Journal of Agro-Environment Science, 2017, 36(1): 183-188
- http://dx.doi.org/10.11654/jaes.2016-0861
文章历史
- 收稿日期: 2016-06-29
近年来,石墨烯引起了人们的广泛关注,因为这不仅是一种新型的二维碳纳米材料,还是碳纳米管、石墨和布基球的基本构成物质。而用改良Hummers方法将石墨强氧化过后得到的氧化石墨烯(GO),更是一种新兴的纳米材料,在很多方面都得以应用,包括环境修复[1]。GO 由多种官能团组成,比如羟基、羧基和环氧基树脂官能团等,这不但可以加强其本身的可分配性,而且可以用作吸附剂[2]。
吸附是环境中污染物去除的重要途径,通过研究污染物和吸附剂间的吸附特性,可以明确污染物与吸附剂间的吸附机理[3]。GO 所具有的网状结构更有利于去除水中的污染物[4]。Gao 等[1]报道了GO吸附水中的四环素主要是通过π-π键和阳离子-π结合键。Tang等[5]报道了GO 对环丙沙星和诺氟沙星的吸附主要以π-π电子力和疏水作用为主导。
泰乐菌素作为目前被普遍使用的兽用抗生素,已经在环境中普遍被检测到[6]。泰乐菌素作为大环内酯类抗生素的一种,含有一个内酯结构的16 元大环,呈弱碱性,pKa在7.1~8.0 之间,易溶于水;而四环素、环丙沙星和诺氟沙星均是小分子抗生素,物理化学特性和泰乐菌素明显不同,其在氧化石墨烯上的吸附机制不适用于泰乐菌素。
通过吸附动力学、吸附等温线实验及pH 值和离子强度对吸附的影响实验,可进一步明确GO 对泰乐菌素的吸附特性和机制,此研究可以为微污染水体中抗生素的去除提供一定的理论依据。
1 材料与方法 1.1 实验材料泰乐菌素(TYL,纯度>95%)购于美国Sigma 公司;乙腈和甲酸均为色谱纯,购于美国Sigma 公司;其他试剂均为分析纯,购于国药试剂有限公司;实验用水为超纯水,由Milli-Q 超纯水制备(Merck MilliporeAdvantage A10)。
1.2 氧化石墨烯的制备GO 是由改良的Hummers 方法[7]制备的。取石墨薄片1.5 g,加入200 mL 浓H2SO4/H3PO4混合液(9:1),在冰浴条件中搅拌并冷却,再向上述混合液中缓缓加入KMnO4 9 g,反应中放出少量热量并且使溶液升温至35~45℃,然后将反应溶液加热至50℃,搅拌24 h后冷却至室温,再将反应溶液倒入200 mL 含30%H2O2(4 mL)的冰水中。将溶液在1000 r·min-1条件下离心5 min 后,取用上清液离心分离(5000 r·min-1)10min 后,弃去其上清液,留混合物。依次用100 mL 去离子水、40 mL 30%HCl 洗涤,所得悬浮溶液在3000r·min-1下离心10 min,再进行冷冻干燥,制得蓬松的石墨烯粉末。最后将上述石墨烯粉末在50℃下真空干燥24 h。
1.3 氧化石墨烯的表征本研究通过扫描电子显微镜(SEM)、透射电子显微镜(TEM)、X 射线衍射法(XRD)、傅里叶变换红外光谱法(YTIR)和Raman 光谱法对GO 进行表征。SEM 和TEM 的型号分别为美国FEI 公司的NOVANANOSEM430 和日本JEOL 的JEM-2010HR。做SEM 时,将样品粘在导电胶上,用10 kV 的加速电压对GO 的形貌和微观结构进行观察;而TEM,是先将样品分散于乙醇中,再滴在炭支撑膜上,干燥后进行表征,加速电压为200 kV。XRD、FTIR和Raman光谱的测量方法如下:使用岛津XD-3A 型X 射线衍射仪对GO 在5°~60°内进行X 射线衍射,X 射线发射源为CuKα(波长0.154 nm),管压40 kV,管流100 mA;在波数500~4000 cm-1的范围内,将样品与研磨的KBr粉末混合后压片,用Thermo Nicolet 6700 型傅里叶变换红外光谱仪对GO 进行测量,以确定GO 所含官能团类别;最后设激光波长为532 nm 以判断GO 结晶是否有序,采用法国HJY 公司的LabRAM Aramis 型显微激光Raman光谱仪。
样品的表面电势用Zetasizer Nano ZS90(英国Malvern 公司)进行电位分析,表面电势的测试在pH=4~11 的溶液中进行。样品的孔隙结构参数通过ASAP2020 和TriStar3000(美国Micromeritics 公司)进行分析。样品首先在200℃下真空脱气4 h,然后在液氮温度(77.4 K)下测试其对氮气的吸-脱附等温线。采用BET 法计算比表面积(SBET),密度泛函数理论(DFT)或BJH法计算孔径分布。
1.4 试验方法 1.4.1 吸附动力学试验称取0.01 g GO 样品于离心管中,加入用0.01mol·L-1 KNO3溶液配制的泰乐菌素的吸附液,并加入微量的叠氮化钠NaN3,使其浓度为0.001 mol·L-1,以抑制水体中微生物,恒温(25±2)℃振荡,分别在相应的时间点取样。于3000 r·min-1离心10 min,取上清液分析检测。
1.4.2 吸附等温线试验配置一系列初始浓度范围为0.5~50 mg·L-1 泰乐菌素的溶液。分别加入一定量的GO 样品,用30 mL的玻璃离心管作为反应容器,放入恒温(25±2)℃、150 r·min-1的摇床中振荡达到平衡。每个样品重复2个平行样,每个浓度设置空白样品对照。平衡后静置24 h取上清液,使GO 颗粒完全沉淀。用移液枪吸取1.0mL的上清液于棕色色谱瓶中待测试。
1.4.3 pH 值和离子强度影响实验pH 值的影响实验:泰乐菌素的初始浓度为10mg·L-1,用HNO3或KOH把体系pH值调为3.0~11.0,离子强度为0.01 mol·L-1 的KNO3。离子强度影响实验:设置泰乐菌素的初始浓度为10 mg·L-1,用KNO3将体系离子强度调节至0~0.1 mol·L-1,pH 值为5.0。
1.4.4 泰乐菌素的分析检测吸附泰乐菌素后的分析检测采用高效液相色谱法(High Performance Liquid Chromatography,HPLC),所选用的仪器是Hitachi Lachrom L-2000 高效液相色谱仪。色谱柱型号为菲罗门C18(2)型(250 mm×4.6mm,5 μm);流动相为乙腈和pH=2、浓度为0.01 mol·L-1 的磷酸二氢钾,比例为35:65,进样量为50 μL,流速为1 mL·min-1;检测波长为290 nm。
1.5 吸附模型吸附动力学采用拉格朗日一级动力学方程和拉格朗日二级动力学方程分别进行拟合,其表达式分别如公式(1)和(2)所示:
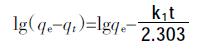 (1)
(1)  (2)
(2) 式中:qe为吸附达到饱和时的饱和吸附量,mg·g-1;qt为吸附时间为t 时的吸附量,mg·g-1;k1为拉格朗日一级动力学吸附反应速率常数,h-1;k2 为拉格朗日二级动力学吸附速率反应常数,g·mg-1·h-1。
吸附等温线分别用线性吸附模型、Freundlich 吸附模型、Langmuir 吸附模型进行拟合:
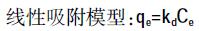 (3)
(3) 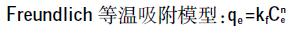 (4)
(4)  (5)
(5) 式中:qe为泰乐菌素在固相中的平衡浓度,mg·kg-1;Ce为泰乐菌素在液相中的平衡浓度,mg·L-1;kd 为泰乐菌素在固相和液相中的线性分配系数,L·kg-1;kf 是Freundlich 分配系数,(mg·kg-1)·(mg·L-1)-n,用于表征吸附作用强弱;n 无量纲指数,可以表征吸附等温线的非线性程度;qm为Langmuir 饱和吸附量,mg·kg-1;b是Langmuir 吸附常数,L·mg-1。
2 结果与讨论 2.1 氧化石墨烯的表征图 1 为GO 的SEM和TEM图。从SEM 图上可以清晰地看到GO 表面呈现片状褶皱且纹路杂乱无序的层状结构,可能是因为氧化作用后的含氧官能团减弱了层与层间的作用力。从TEM 图中能够清晰地看出其表面呈半透明不规则模状,阴影部分表明了GO的层状结构,印证了SEM图。

|
| 图 1 氧化石墨烯的SEM图(a)和TEM图(b) Figure 1 SEM(a)and TEM(b)images of GO |
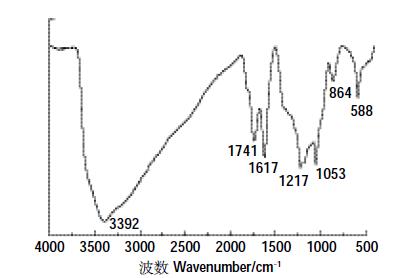
从GO 样品FTIR 光谱上可以看到一系列吸收峰(图 2),表明GO 表面有大量含氧官能团:在3392cm-1处出现明显的-OH 的伸缩振动峰[8];在1741 cm-1和1617 cm-1处分别出现了羧基基团的C=O 和C=C的伸缩振动峰,可能是由GO 晶体本身的sp2网状结构形成的;在1217 cm-1、1053 cm-1 和864 cm-1 处均有不同的特征峰出现,依次是酚的C-OH 的伸缩振动峰、烷氧基C-O 的伸缩振动峰和C-O-C 的伸缩振动峰[4, 7, 9]。
|
| 图 2 氧化石墨烯的红外光谱图 Figure 2 FTIR spectra of GO |
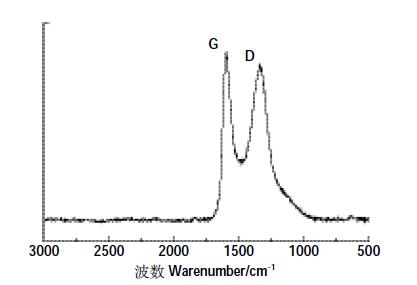
Raman 光谱是进一步探测GO 特征结构的直接有效的方法,特别是可以确认GO 的不足和结构是否有序。图 3为氧化石墨烯的Raman光谱。第一个特征峰G峰出现在1598 cm-1处,它主要来自于平面内sp2键的振动;第二个特征峰D 峰出现在1342 cm-1处,D峰的存在说明了GO结构存在缺陷。在本次实验中,这是由于石墨氧化成GO 导致的,这样的结构包括含共价键的含氧官能团(如羟基、环氧、羰基),这些官能团破坏了共轭双键的网状结构。它主要是因为GO的缺陷激活了六元环的呼吸模式[10]。G 和D 的相对强度峰值比(IG/ID)能够衡量物质障碍程度,尽管含氧官能团能破坏结构使D峰升高,但D峰仍然相对较低。
|
| 图 3 氧化石墨烯拉曼光谱图 Figure 3 Raman spectra of GO |
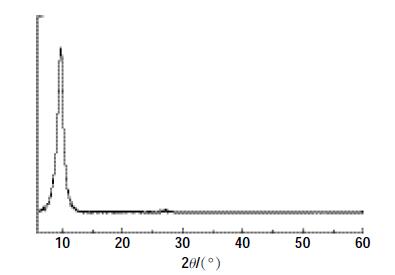
图 4 为GO 的XRD 图,在2θ=10°处明显出现了尖锐狭窄的特征峰。这表明石墨的成功氧化和石墨烯的形成[11]。GO 表层在水中完整地剥落,然后在干燥的过程中重新聚集形成。GO 中存在的包括羟基、环氧和羧基组在内的含氧官能团可能是导致层间距增加的主要原因[12]。
|
| 图 4 氧化石墨烯的X 射线衍射图 Figure 4 XRD patterns of GO |
通过氮气的吸附-脱附等温线可知,GO 的平均孔径和比表面积分别为3.693 nm 和8.638 m2·g-1。等电点为9.2,因此当pH<9.2 时,GO 表面带正电荷,吸附表面带负电荷的物质的能力比较强;而当pH>9.2时,表面带负电荷的GO 吸附表面带正电荷的物质的能力就比较强。
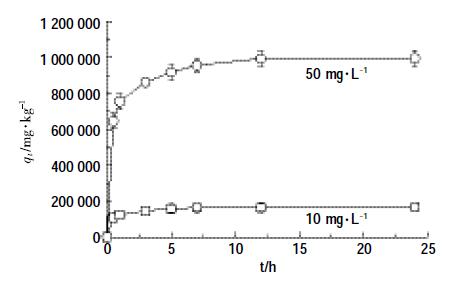
2.2 氧化石墨烯对泰乐菌素的吸附动力学特性GO对不同浓度的泰乐菌素的吸附动力学以及用一级和二级动力学模型对动力学数据拟合参数分别见图 5 和表 1(吸附的pH=7.0)。从图中可见,10、50mg·L-1泰乐菌素在GO 上表现出的动力学行为相似:在24 h时吸附基本达到完全动态平衡,在0~5 h内是快速吸附的过程,这期间泰乐菌素的吸附量超过总吸附量的92%;随后吸附速率平稳放缓,到12 h时吸附量达到总吸附量的99%,此后吸附量随着时间的延续略微增加直至达到吸附平衡。Guo 等[13]的研究表明泰乐菌素在针铁矿与腐植酸复合物上于7 h达到吸附平衡。这种差异可能是因为GO 表面的吸附点位有限,随着吸附反应的进行,吸附点位逐渐减少,吸附逐步达到动态平衡。
|
| 图 5 氧化石墨烯对不同浓度泰乐菌素的吸附动力学 Figure 5 Effect of initial concentration on the sorption kinetics of tylosin on graphene oxide |
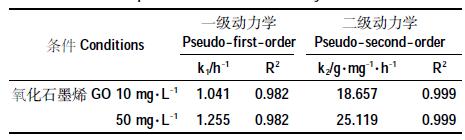 |
用拉格朗日一级和二级动力学模型对不同浓度泰乐菌素在氧化石墨烯上吸附的动力学数据进行拟合可知,相比拉格朗日一级动力学方程(决定系数R2=0.982),拉格朗日二级动力学模型拟合效果较好,其R2均为0.999。因此泰乐菌素在GO 上的吸附可能存在多种吸附作用,其中化学吸附可能是主导其吸附的主要机制[13]。与此同时,我们发现泰乐菌素浓度与吸附速率k2成反比。这可能是因为分子之间的碰撞几率随着泰乐菌素初始浓度的升高而增大,进而延长了吸附剂活性位点结合泰乐菌素的时间[14]。
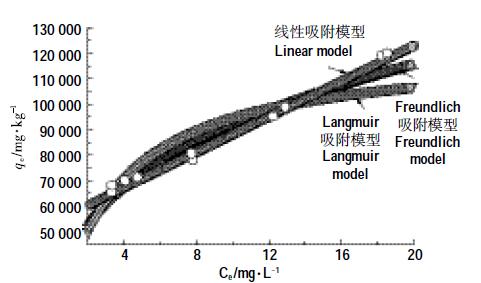
2.3 氧化石墨烯对泰乐菌素的吸附等温线泰乐菌素在GO 上的吸附等温线如图 6 所示,吸附的pH=7.0。分别用线性吸附模型、Freundlich 吸附模型以及Langmuir 吸附模型进行拟合,拟合参数见表 2。从拟合结果可以看出,线性吸附模型和Fre原undlich 吸附模型能够较好地拟合泰乐菌素在GO 上的吸附(R2>0.94)。因此泰乐菌素在GO 上的吸附存在明显的疏水性分配作用,且吸附还受化学作用的影响。Guo 等[13]报道的泰乐菌素在针铁矿和不同浓度腐植酸的复合物上的kd值均在300 左右,而本研究的kd值将近其10倍,说明合成的氧化石墨烯对泰乐菌素有更好的吸附性能。Gao等[1]报道了氧四环素在GO上的吸附,吸附等温线可以用Freundlich 吸附模型较好地拟合,拟合的kf值为46.498,n 值为0.995。
|
| 图 6 氧化石墨烯对泰乐菌素的吸附等温线 Figure 6 Sorption isotherms of tylosin on graphene oxide |
在Freundlich吸附模型中,n值用来表征吸附的非线性程度。从表 2可知,GO对泰乐菌素吸附的n值为0.329,吸附具有明显的线性,因此GO吸附泰乐菌素是一个非均质的多分子层吸附过程。在吸附过程中泰乐菌素首先占据GO上的高能吸附位点,当这些高能吸附位点被完全占据后,再由低能吸附位点进行吸附[15]。
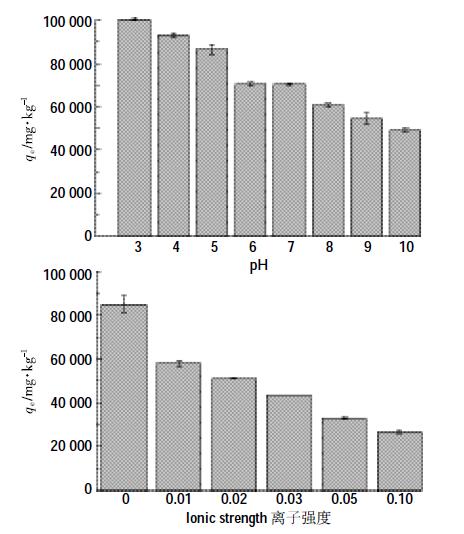
2.4 pH 值和离子强度对氧化石墨烯吸附泰乐菌素的影响泰乐菌素在不同pH 值下,会以不同的形态存在,因此溶液的pH值和离子强度会影响其在GO 上的吸附。不同的pH值和离子强度对GO 吸附泰乐菌素的影响如图 7 所示。从图上可以看出,GO 对泰乐菌素的吸附随着pH 值和离子强度的增加而呈整体减弱趋势。这一实验结果与GO 表面官能团以及泰乐菌素分子结构有关。因为泰乐菌素在溶液pH值小于7.1时带正电荷,而GO 表面有含氧基团,所以带很多负电荷,两者间可能发生静电引力;在pH 值大于7.1时,泰乐菌素呈分子态与GO 带负电荷的表面既无引力也无斥力[1]。由于这些基团的电子接受能力随pH的升高而降低,从而抑制了GO和泰乐菌素间的静电引力。另外,我们推测π-π键也是主要的吸附机理,事实上,π-π键通常都被认为是芳香族有机物和碳基物质之间的主要吸附机理[16]。所以泰乐菌素随着pH 值的增加而下降,静电引力和π-π键力是主要的吸附机理。
|
| 图 7 pH 和离子强度对GO 吸附泰乐菌素的影响 Figure 7 Effects of ionic strength and pH on the sorption of tylosin on graphene oxide |
通过离子强度对GO 吸附泰乐菌素的影响可以看出,GO 对泰乐菌素的吸附随离子强度的增强而逐渐减小,可能是因为离子强度的增加会导致其与泰乐菌素竞争GO 表面有限的活性吸附点,使泰乐菌素的吸附减弱,且GO 对泰乐菌素的吸附存在着π-π共价键的作用[7, 17],而离子强度的增加,会使π-π共价键作用减弱,从而使吸附降低。
3 结论(1) GO 是具有缺陷的层状结构的物质,且表面含有大量的含氧官能团。GO 的平均孔径和比表面积分别为3.693 nm和8.638 m2·g-1,等电点为9.2。
(2) 泰乐菌素在GO 上的吸附是一个先快速后缓慢的过程,在24 h内可以达到吸附动态平衡,动力学曲线符合伪二级动力学方程。吸附等温线可以用线性吸附模型和Freundlich 吸附模型较好地拟合,且吸附受溶液pH值和离子强度的影响较大。
| [1] | Gao Y, Li Y, Zhang L, et al. Adsorption and removal of tetracycline antibiotics from aqueous solution by graphene oxide[J]. Journal of Colloid and Interface Science, 2012, 368(1) : 540–546. DOI:10.1016/j.jcis.2011.11.015 |
| [2] | Ramesha G K, Kumara A V, Muralidhara H B, et al. Graphene and graphene oxide as effective adsorbents toward anionic and cationic dyes[J]. Journal of Colloid and Interface Science, 2011, 361(1) : 270–277. DOI:10.1016/j.jcis.2011.05.050 |
| [3] | Pavlovic M D, Curkovic L, Blazek D, et al. The sorption of sulfamethazine on soil samples:Isotherms and error analysis[J]. Science of the Total Environment, 2014, 497-498 : 543–552. DOI:10.1016/j.scitotenv.2014.08.018 |
| [4] | Chen H, Gao B, Li H. Removal of sulfamethoxazole and ciprofloxacin from aqueous solutions by graphene oxide[J]. Journal of Hazardous Materials, 2015, 282(3) : 201–207. |
| [5] | Tang Y L, Guo H G, Xiao L, et al. Synthesis of reduced graphene oxide/magnetite composites and investigation of their adsorption performance of fluoroquinolone antibiotics[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2013, 424(5) : 74–80. |
| [6] | Guo X T, Ge J H, Yang C, et al. Sorption behavior of tylosin and sulfamethazine on humic acid:Kinetic and thermodynamic studies[J]. RSC Advances, 2015, 5(5) : 58865–58872. |
| [7] | Yu F, Ma J, Bi D S. Enhanced adsorptive removal of selected pharmaceutical antibiotics from aqueous solution by activated graphene[J]. Environmental Science and Pollution Research, 2015, 22(6) : 4715–4724. DOI:10.1007/s11356-014-3723-9 |
| [8] | 杨勇辉, 孙红绢, 彭同江. 石墨烯的氧化还原法制备及结构表征[J]. 无机化学学报, 2010, 26(11) : 2083–2090. YANG Yong-hui, SUN Hong-juan, PENG Tong-jiang. Synthesis and structural characterization of graphene by oxidation reduction[J]. Chinese Journal of Inorganic Chemistry, 2010, 26(11) : 2083–2090. |
| [9] | 张秀蓉, 龚继来, 曾光明, 等. 磁性氧化石墨烯制备及去除水中刚果红的研究[J]. 中国环境科学, 2013, 33(8) : 1379–1385. ZHANG Xiu-rong, GONG Ji-lai, ZENG Guang-ming, et al. Synthesis of magnetic graphene oxide adsorbent for congo red removal from aqueous solution[J]. China Environmental Science, 2013, 33(8) : 1379–1385. |
| [10] | Adnan N N, Bidin N, Taib N A M, et al. Passively Q-switched flashlamp pumped Nd:YAG laser using liquid graphene oxide as saturable absorber[J]. Optics & Laser Technology, 2016, 80 : 28–32. |
| [11] | Tang J H, Shen J F, Li N, et al. Facile synthesis of layered MnWO4/reduced graphene oxide for supercapacitor application[J]. Journal of Alloys and Compounds, 2016, 666 : 15–22. DOI:10.1016/j.jallcom.2015.12.219 |
| [12] | Liu L, Cui Z J, Ma Q C, et al. One-step synthesis of magnetic iron-aluminum oxide/graphene oxide nanoparticles as a selective adsorbent for fluoride removal from aqueous solution[J]. RSC Advances, 2016, 6(13) : 10783–10791. DOI:10.1039/C5RA23676B |
| [13] | Guo X T, Zhang J, Ge J H, et al. Sorption and photodegradation of tylosin and sulfamethazine by humic acid-coatedgoethite[J]. Royal Society of Chemistry, 2015, 5 : 100464–100471. |
| [14] | Chakraborty R, Karmakar S, Mukherjee S, et al. Kinetic evaluation of chromium(Ⅵ) sorption by water lettuce(Pistia)[J]. Water Science and Technology, 2014, 69(1) : 195–201. DOI:10.2166/wst.2013.667 |
| [15] | Carabineiro S A C, Thavorn-Amornsri T, Pereira M F R, et al. Adsorption of ciprofloxacin on surface-modified carbon materials[J]. Water Research, 2011, 45(15) : 4583–4591. DOI:10.1016/j.watres.2011.06.008 |
| [16] | Ouyang K, Zhu C H, Zhao Y, et al. Adsorption mechanism of magnetically separable Fe3O4/graphene oxide hybrids[J]. Applied Surface Science, 2015, 355(15) : 562–569. |
| [17] | Doretto K M, Peruchi L M, Rath S. Sorption and desorption of sulfadimethoxine, sulfaquinoxaline and sulfamethazine antimicrobials in Brazilian soils[J]. Science of the Total Environment, 2014, 476/477 : 406–414. DOI:10.1016/j.scitotenv.2014.01.024 |
 2017, Vol. 36
2017, Vol. 36