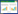文章信息
- 林凡达, 宋新山, 赵志淼, 赵雨枫, 王宇晖, 董国强, 王勃迪
- LIN Fan-da, SONG Xin-shan, ZHAO Zhi-miao, ZHAO Yu-feng, WANG Yu-hui, DONG Guo-qiang, WANG Bo-di
- 负载型纳米零价铁(nZVI)强化垂直流人工湿地反硝化作用研究
- Analysis of the enhancement of denitrification efficiency in vertical flow constructed wetlands by supported nanoscale zero valent iron(nZVI)
- 农业环境科学学报, 2017, 36(11): 2307-2313
- Journal of Agro-Environment Science, 2017, 36(11): 2307-2313
- http://dx.doi.org/10.11654/jaes.2017-0546
文章历史
- 收稿日期: 2017-04-12
- 接受日期: 2017-06-21
南方地区低C/N生活污水排放比较普遍、传统污水处理厂脱氮效率不足以及农业耕作中大量氮肥的无效利用导致目前水环境“三氮”污染形势严峻[1]。人工湿地作为一种生态化、低成本水处理技术,目前在国内外已广泛用于污水的脱氮处理[2]。人工湿地氮的传统去除机制包括植物吸收、氨氮挥发、基质吸附和生物硝化-反硝化等[2],其中生物硝化-反硝化是人工湿地脱氮的主要途经[3]。生物反硝化过程微生物需要有机碳源作为电子供体,将NO3-和NO2-还原为N2。因此,是否存在足够的电子供体,影响着生物反硝化过程能否顺利完成。
外加碳源成为提高人工湿地反硝化效率的常见手段。在现有的研究中,用于人工湿地的碳源主要包括COD或BOD高的污水[4]、低分子碳水化合物[5]、植物生物质[6]等。但传统外加碳源存在投加量难控制、可能造成二次污染[7]、需要设置额外的投加装置[8]等,增加了投资和运行费用。
纳米零价铁(nZVI)比普通零价铁具有更大的比表面积、更高的反应活性,广泛应用于环境污染的修复[9-11]。nZVI在厌氧腐蚀过程中产生的H2可供反硝化细菌进行生物反硝化,一定程度弥补了生物反硝化过程中电子供体的缺失。同时nZVI氧化可提供电子供体参与化学反硝化,一定程度上可减少碳源的需求,对于低碳氮比废水中硝酸盐氮的去除具有一定的积极意义。亦有研究表明[12],nZVI与微生物的耦合体系可在3 d内将硝酸盐氮完全降解。硝酸根离子在nZVI的作用下发生化学反硝化,在无pH值控制的厌氧环境中,nZVI还原硝酸盐的最终产物几乎全部为N2[13]。nZVI与硝酸盐氮反应产生的Fe2+,可进一步氧化提供电子供体参与化学反硝化[14]。nZVI在地下水硝酸盐污染修复中研究广泛[15],然而在人工湿地系统中的应用鲜有报道。因此研究人工湿地中nZVI-氮过程对提高其脱氮效率具有积极意义。
本研究的主要目的:考察负载型nZVI投加对人工湿地硝态氮去除效果的影响;探讨负载型nZVI的生物反硝化与化学反硝化机制以及nZVI与有机碳源的协同脱氮机制;为nZVI强化脱氮的人工湿地设计和运行提供支撑。
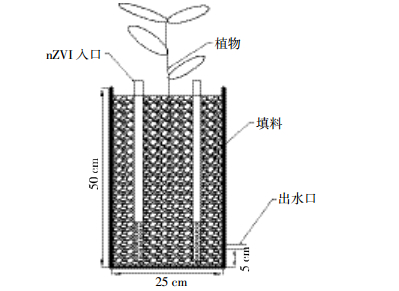
1 材料与方法 1.1 实验装置本实验采用垂直流小试人工湿地(图 1)。装置为7个高50 cm、直径25 cm的PVC材质实验柱,底部5 cm处设置出水口,以粒径2~3 mm的石英砂作为填充介质。插入直径为2 cm、底部多孔的PVC管,管底部中加负载型nZVI(先置于网袋中,再投加到PVC管中)。
|
| 图 1 试验装置示意图 Figure 1 Experimental set-up |
nZVI在空气中稳定性差,易被氧化,在水中易团聚。同时nZVI在使用过程中还存在难以从水中分离、材料的重复利用效率低的问题。因此,本文使用蒙脱石(Mt)改性nZVI(Mt-nZVI),提高其稳定性和耐氧化性,同时使用可生物降解的海藻酸钠(SA)包埋Mt-nZVI以降低分离操作难度,提高出水水质和重复利用率。
本实验采用液相还原法[16]制备蒙脱石负载纳米零价铁(Mt-nZVI),蒙脱石与Fe2+的质量比为4:1。选取一定浓度的海藻酸钠SA溶液,并加入一定量的Mt-nZVI, 将上述混合液逐滴滴入5% CaCl2溶液中,交联成球。SA与Mt-nZVI的质量比为1:3,1 g的SA包埋Mt-nZVI小球(负载型nZVI)的含铁量约为0.187 5 g。
1.3 湿地进水用葡萄糖、硝酸钠、磷酸二氢钾、氯化钙、氯化钾、碳酸氢钠以及微量元素等配制模拟污水。C/N以C6H12O6·H2O和NaNO3调节,以NaHCO3调节进水pH。进水水质:NO3--N 45~55 mg·L-1,COD 0~350 mg·L-1,pH 6.8~7.3,DO 9.8~11.1 mg·L-1。
1.4 运行条件2016年8月底实验装置构建完成,10月初湿地中加入一定量的活性污泥进行驯化。驯化期进水水质为NO3--N 40~50 mg·L-1,COD 80~100 mg·L-1,并加入一定量的微量元素,每1 d换一次水。20 d后,在2~7号湿地中加入一定量的负载型nZVI,1号湿地作为对照,每1 d换水一次,测定出水,20 d后出水水质稳定,11月底进入测试期。
整个实验为:设置4组C/N,分别为0、2、4和6,每组进行4个周期;1~7号湿地中分别加入0、0.5、1、1.5、2、3、4 g负载型nZVI;水力停留时间(HRT)为1 d,每天取样测定,连续测试3 d;负载型nZVI每3 d更换一次,其使用时间为1、2、3 d;一个周期结束后湿地休憩(3~5 d),待湿地稳定后,进入下一个周期;整个实验运行的温度为7~15 ℃。
1.5 测试方法与数据分析主要测试指标及方法:DO和pH值采用Hach HQ40d测定,NO3--N采用紫外分光光度法、TN采用碱性过硫酸钾消解紫外分光光度计法、NO2--N采用GMA3202气相分子吸收光谱仪、NH4+-N采用纳氏试剂分光光度法、COD采用重铬酸钾分光光度法、Fe2+和总铁采用邻菲罗啉分光光度法。
数据分析及绘图工具:采用Microsoft Excel 2013对数据进行初步处理和绘图,采用SPSS 22进行数据的统计分析,主要分析数据的标准误差以及组间差异性。
2 结果与分析 2.1 材料的表征 2.1.1 扫描电镜分析(SEM)和比表面积(BET)图 2为SA小球和负载型nZVI的扫描电镜。可见,SA小球表面均匀规整,在包埋Mt-nZVI后小球表面凹凸不平,且可清楚看到Mt-nZVI颗粒均匀分布在小球表面。说明通过把Mt-nZVI与SA联合做成小球,较好地解决了Mt-nZVI易团聚的问题。

|
| 图 2 SA小球和负载型nZVI的SEM图 Figure 2 The SEM images for SA beads and supported nZVI bead |
对SA小球和负载型nZVI的比表面积测定分析(表 1)表明,负载型nZVI比SA小球的比表面积略小,但孔容和孔径都比SA小球大。这表明Mt-nZVI的加入可以增大SA小球的孔径,更加有利于NO3--N进入小球内部与零价铁发生化学反硝化反应。
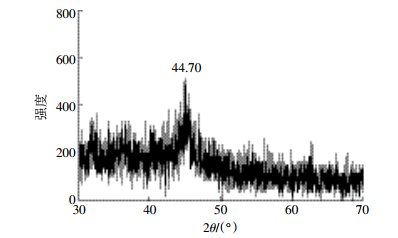
图 3为负载型nZVI的XRD谱图。可见,负载型nZVI小球在2θ=44.70°处有一衍射峰,对照零价铁的标准PDF卡片发现,其刚好对应体心立方结构α-Fe(100)晶面衍射(44.673°),表明负载型nZVI中含有零价铁。
|
| 图 3 负载型nZVI的XRD谱图 Figure 3 XPS pattern of supported nZVI beads |
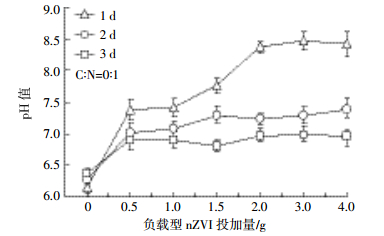
图 4为不同负载型nZVI投加量的出水pH值。从整体上看,随负载型nZVI投加量增加,出水pH值增加。一方面,是因为nZVI与H2O反应产生OH-;另一方面,是因为nZVI与NO3--N反应消耗H+;同时随着改性nZVI使用时间的增加,nZVI活性降低,对出水pH值影响减小。未投加负载型nZVI时,出水pH值在6.3左右,当投加0.5 g的负载型nZVI,且使用时间为1、2、3 d时,所对应的pH值分别提高到7.4、7.0、6.9左右。随使用时间的增加,投加量对出水pH值的影响减小。pH值是影响人工湿地反硝化效果的主要因素,反硝化作用的最佳pH值为7~8[17]。由上述结果可见,nZVI在水中发生氧化还原反应会使溶液的pH值升高,这与文献[18]的研究结果一致。可见在使用nZVI提高反硝化效果时,需要注意其投加量和使用时间,确保其对pH值的改变不会导致生物反硝化的抑制。
|
| 图 4 负载型nZVI不同投加量的出水pH值 Figure 4 The out-put pH in different dosage of supported nZVI |
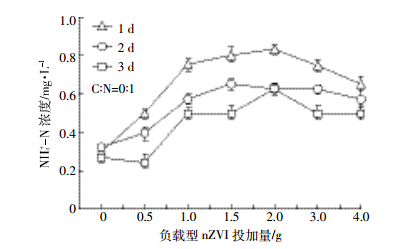
图 5为不同使用时间下,负载型nZVI投加量对人工湿地出水NH4+-N浓度的影响。可见,随负载型nZVI投加量的增加,出水NH4+-N浓度增加。未投加负载型nZVI时,人工湿地NH4+-N的出水浓度在0.28 mg·L-1左右;在负载型nZVI不同使用时间下,投加量达到1.5 g后,NH4+-N的出水浓度变化随投加量变化不明显,分别达到0.80、0.65、0.50 mg·L-1左右。在相同的负载型nZVI投加量下,NH4+-N的出水浓度随使用时间的增加而降低。
|
| 图 5 负载型nZVI不同投加量的出水NH4+-N浓度 Figure 5 The out-put concentration of ammonia nitrogen in different dosage of supported nZVI |
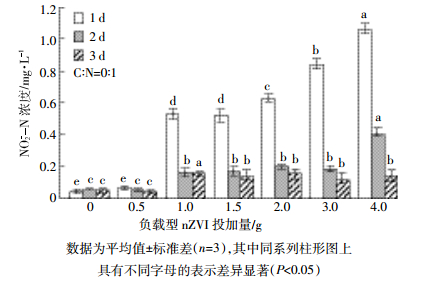
由图 6可见,随负载型nZVI投加量的增加,人工湿地出水NO2--N浓度显著增加(P<0.05)。一方面,可能是因为负载型nZVI在还原NO3--N的过程中产生NO2--N;另一方面,可能是因为生物反硝化过程中缺少碳源作为电子供体,造成NO2--N积累。未投加负载型nZVI时,人工湿地NO2--N的出水浓度在0.05 mg·L-1左右;投加4 g的负载型nZVI时,不同使用时间下,NO2--N的出水浓度分别约为1.06、0.40、0.14 mg·L-1。在不同的负载型nZVI使用时间下,NO2--N出水浓度与投加量的关系呈现一致性,NO2--N出水浓度与负载型nZVI加入量正相关,其中在使用时间为1 d时,投加量对NO2--N出水浓度的影响最显著(P<0.05)。
|
| 数据为平均值依标准差(n=3),其中同系列柱形图上具有不同字母的表示差异显著(P<0.05) 图 6 负载型nZVI不同投加量的出水NO2--N浓度 Figure 6 The out-put concentration of nitrite in different dosage of supported nZVI |
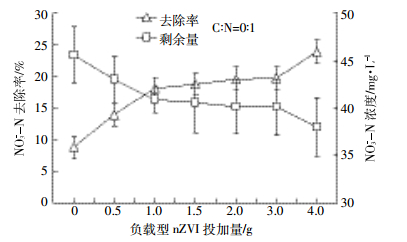
由图 7可见,C/N为0:1、使用时间为1 d、不投加负载型nZVI时,NO3--N去除率仅为8.81%左右,NO3--N去除量为4.39 mg·L-1左右。投加负载型nZVI时湿地NO3--N去除率和去除量显著增加,且随负载型nZVI投加量的增大而逐渐增大。这表明投加负载型nZVI可促进人工湿地反硝化,原因可能是负载型nZVI参与了人工湿地反硝化过程,与NO3--N发生反应从而将其去除。当投加量为1 g时,NO3--N去除率提高到18.14%左右,去除量达到9.06 mg·L-1左右,但当投加量继续增大时,NO3--N去除率和去除量增加不再明显。
|
| 图 7 负载型nZVI不同投加量的NO3--N去除率和剩余量 Figure 7 Surplus and the removal rate of nitrate in different dosage of supported nZVI |
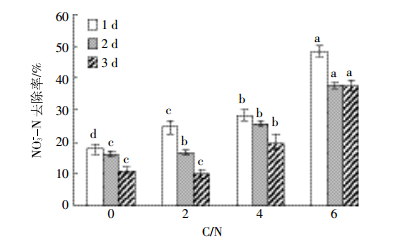
如图 8所示,投加量为1 g、不加碳源时,在不同负载型nZVI使用时间下NO3--N去除率较低,依次为18.14%、16.24%、11.03%。当C/N为6时,在不同负载型nZVI使用时间下NO3--N去除率显著提高到48.42%、37.80%、37.41%。在不同的负载型nZVI使用时间下,NO3--N去除率与C/N间的关系呈现一致性,NO3--N的去除率随C/N的增大显著增大(P<0.05)。一方面,因为C/N的提高有利于促进人工湿地生物反硝化;另一方面,碳源的存在可能会促进nZVI参与化学反硝化。
|
| 图 8 不同C/N下的NO3--N去除率 Figure 8 The removal rate of nitrate in different level of C/N ratio |
表 2为负载型nZVI投加量和C/N两因素方差分析。由表可知,负载型nZVI投加量、C/N和两者协同作用都对NO3--N去除率有显著影响(P<0.05)。三者对NO3--N的去除率贡献大小为C/N>负载型nZVI投加量>负载型nZVI投加量×C/N。

|
相比直接投加nZVI,使用负载型nZVI的优点在于易于分离,且出水水质澄清,不会存在nZVI颗粒的残留。负载型nZVI抗氧化性强、使用时间长,且分离后的nZVI可通过还原再生循环利用。
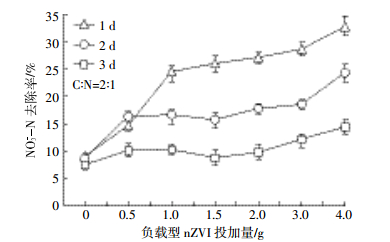
图 9为不同负载型nZVI使用时间下NO3--N去除率变化情况,对于NO3--N去除率,使用时间1 d>2 d>3 d。以投加量1 g为例,负载型nZVI对NO3--N去除率从1 d的24.27%下降到2 d的16.57%、3 d的10.30%。从图中可看出,负载型nZVI虽然随使用时间的增加,对NO3--N去除率降低,但与空白湿地对比去除率仍有所上升。
|
| 图 9 负载型nZVI不同使用时间下NO3--N去除率 Figure 9 The removal rate of nitrate in different adding retention time |
在投加不同质量的负载型nZVI时,湿地出水均未检出Fe2+、总铁(最低检出限为0.03 mg·L-1)。出现这种情况的原因可能为:由图 4所示,负载型nZVI投加到湿地后,提高了湿地的pH值,湿地环境变为弱碱性,而Fe2+、Fe3+在中性或弱碱性环境以氢氧化物存在,从而被吸附到湿地填料或负载型nZVI表面。
3 讨论 3.1 nZVI参与人工湿地反硝化作用投加负载型nZVI后可显著提高人工湿地NO3--N去除率(P<0.05),且去除率随初始负载型nZVI投加量增加而逐渐增加。表明负载型nZVI可促进反硝化过程的进行,负载型nZVI可能参与反硝化作用从而去除NO3--N。陈西亮等[19]研究nZVI炭微电解体系去除水中硝酸盐,结果发现添加nZVI后NO3--N去除率显著提高,与本研究结论一致。nZVI参与人工湿地反硝化作用的机制主要有以下几种:
(1)nZVI与NO3--N发生化学反硝化反应[20]。
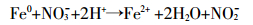 ①
① 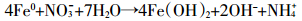 ②
② 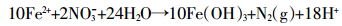 ③
③ 从式①和②可看出,nZVI与NO3--N反应产物主要为NO2-和NH4+,这就导致出水NO2--N和NH4+-N浓度随nZVI添加量增加而升高。同时随着改性nZVI使用时间的增加,其被氧化为Fe2+或Fe3+,使NO3--N去除率和去除量、NO2--N和NH4+-N出水浓度也相应减小,这与本研究图 4、图 5和图 9所示结果相一致。从式③可以看出,Fe2+与硝酸盐也可发生化学反应,但一般液相条件下,该反应不容易发生或反应很缓慢[21]。
(2)nZVI参与人工湿地反硝化生物反硝化。
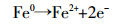 ④
④ 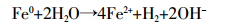 ⑤
⑤ 其产物Fe2+与NO3--N发生生物反硝化,Weber等[22]研究表明,铁存在下NO3--N依赖某些微生物进行还原代谢,这种微生物可以在氧化Fe2+的同时还原NO3--N,产物H2,被认为是反硝化细菌的理想电子供体。
(3)nZVI调节人工湿地的酸碱度和溶解氧。生物反硝化的最佳pH值是7~8,而投加适宜的负载型nZVI可以调节水溶液pH值,为反硝化细菌创造适宜的酸碱环境。nZVI通过与水中O2发生反应,去除水中O2,为厌氧反硝化细菌创造缺氧环境,促进生物反硝化。
(4)吸附作用。负载型nZVI具有较大的比表面积,可将一部分NO3--N吸附到表面;同时nZVI反应产物Fe2+、Fe3+都是很好的吸附剂。
使用SA包埋Mt改性nZVI得到的负载型nZVI,更换方便,解决了nZVI团聚的问题,且重复使用3 d后对人工湿地内硝氮去除仍有促进作用。湿地出水的Fe2+、总铁测试结果表明使用负载型nZVI解决了nZVI易流失、出水铁浓度超标的问题。
3.2 有机物与零价铁反硝化的相互影响作用本研究显示,有机物的存在对负载型nZVI参与反硝化具有较大的影响,通过对负载型nZVI投加量与C/N的两因素方差分析,发现有机物与负载型nZVI对人工湿地的反硝化具有协同作用。可能的原因是:首先,有机物可以促进铁的循环[23],从而促进反硝化的进行。其次,有机碳源的投加促进了异养/自养微生物的繁殖,生物量的增加有利于加快生物反硝化。Brian等[24]研究表明,nZVI与水反应产生的H2可以为自氧反硝化细菌提供能量,所需的无机碳源则可由异养反硝化细菌分解有机物提供。
这种nZVI与有机物的协同作用,对于人工湿地反硝化具有重要意义。对于人工湿地处理有机物含量较少的污水,可以通过投加nZVI,缓解由于电子供体不足而导致NO3--N去除率较低的问题。
4 结论(1)人工湿地进水中投加负载型nZVI可以显著提高NO3--N的去除率,NO3--N的去除率随负载型nZVI投加量增加而增加,但NO2--N、NH4+-N浓度、pH值同时也随着投加量增加而增加。表明nZVI可以作为人工湿地反硝化的电子供体参与反硝化反应。
(2)C/N与负载型nZVI投加量对人工湿地反硝化作用都具有显著影响,且两者具有协同作用,有机碳源的存在可以促进负载型nZVI参与反硝化。
(3)负载型nZVI重复使用结果表明,C/N为2:1、负载型nZVI投加量为4 g时,经过3 d重复使用后对NO3--N去除率仍能提高7.23%。
| [1] |
王允妹, 陈明. SBR法处理低C/N污水的工程应用-以某基地污水处理站改造工程为例[J]. 环境保护与循环经济, 2014, 34(3): 47-49. WANG Yun-mei, CHEN Ming. SBR Engineering application of low C/N wastewater treatment:Example of certain base sewage treatment plant renovation project[J]. Environmental Protection and Circular Economy, 2014, 34(3): 47-49. |
| [2] |
Zhang S, Liu F, Xiao R. Nitrogen removal in Myriophyllum aquaticum wetland microcosms for swine wastewater treatment:15N-labelled nitrogen mass balance analysis[J]. Journal of the Science of Food & Agriculture, 2017, 97(2): 505-511. |
| [3] |
Wang J F, Song X S, Wang Y H, et al. Nitrate removal and bioenergy production in constructed wetland coupled with microbial fuel cell:Establishment of electrochemically active bacteria community on anode[J]. Bioresour Technol, 2016, 221: 358-365. DOI:10.1016/j.biortech.2016.09.054 |
| [4] |
谭洪新, 刘艳红, 周琪, 等. 添加碳源对潜流+表面流组合湿地脱氮除磷的影响[J]. 环境科学, 2007, 28(6): 1209-1215. TAN Hong-xin, LIU Yan-hong, ZHOU Qi, et al. Effects of external carbon source on nitrogen and phosphorus removal in subsurface flow and free water surface integrated constructed wetland[J]. Environmental Science, 2007, 28(6): 1209-1215. |
| [5] |
Wu H, Fan J, Zhang J. Strategies and techniques to enhance constructed wetland performance for sustainable wastewater treatment[J]. Environmental Science and Pollution Research, 2015, 22(19): 14637-50. DOI:10.1007/s11356-015-5151-x |
| [6] |
Zhang M L, Zhao L F, Mei C H, et al. Effects of plant material as carbon sources on TN removal efficiency and N2O flux in vertical-flow-constructed wetlands[J]. Water, Air, & Soil Pollution, 2014, 225(11): 2181. |
| [7] |
Nguyen L M. Organic matter composition, microbial biomass and microbial activity in gravel-bed constructed wetlands treating farm dairy wastewaters[J]. Ecological Engineering, 2000, 16(2): 199-221. DOI:10.1016/S0925-8574(00)00044-6 |
| [8] |
王旭明, 从二丁, 罗文龙, 等. 固体碳源用于异养反硝化去除地下水中的硝酸盐[J]. 中国科学, 2008(9): 824-828. WANG Xu-ming, CONG Er-ding, LOU Wen-long, et al. Removal of nitrate from groundwater by solid carbon source for heterotrophic denitrification[J]. Science China, 2008(9): 824-828. |
| [9] |
Danish M, Gu X G, Lu S G. Degradation of chlorinated organic solvents in aqueous percarbonate system using zeolite supported nano zero valent iron(Z-nZVI) composite[J]. Environmental Science and Pollution Research, 2016, 23(13): 13298-13307. DOI:10.1007/s11356-016-6488-5 |
| [10] |
Reardon E J, Fagan R, Vogan J L. Anaerobic corrosion reaction kinetics of nanosized iron[J]. Environmental Science & Technology, 2016, 42(7): 2420-2425. |
| [11] |
Lowry G V, Johnson K M. Congener-specific dechlorination of dissolved PCBs by microscale and nanoscale zerovalent iron in a water/methanol solution[J]. Environmental Science & Technology, 2004, 38(19): 5208-5216. |
| [12] |
An Y, Li T, Jin Z. Decreasing ammonium generation using hydrogenotrophic bacteria in the process of nitrate reduction by nanoscale zero-valent iron[J]. Science of the Total Environment, 2009, 407(21): 5465-5470. DOI:10.1016/j.scitotenv.2009.06.046 |
| [13] |
Chew C F, Zhang T C. In-situ remediation of nitrate-contaminated ground water by electrokinetics/iron wall processes[J]. Water Science & Technology, 1998, 38(38): 135-142. |
| [14] |
王苏艳, 宋新山, 赵志淼, 等. 亚铁对水平潜流人工湿地反硝化作用的影响[J]. 环境科学学报, 2016, 36(2): 557-563. WANG Su-yan, SONG Xin-shan, ZHAO Zhi-miao, et al. The influence of Fe2+ on denitrification in horizontal subsurface flow constructed wetlands[J]. Acta Scientiae Circumstantiae, 2016, 36(2): 557-563. |
| [15] |
安毅, 李铁龙, 金朝晖. 零价铁-反硝化菌在地下水硝酸盐污染修复中的应用[J]. 安全与环境学报, 2009, 9(6): 40-43. AN Yi, LI Tie-long, JIN Zhao-hui. Application of zero valent iron and denitrifying bacteria in remediation of nitrate pollution in groundwater[J]. Journal of Safety and Environment, 2009, 9(6): 40-43. |
| [16] |
Huang L H, Zhou S J, Jin F, et al. Characterization and mechanism analysis of activated carbon fiber felt-stabilized nanoscale zero-valent iron for the removal of Cr(Ⅵ) from aqueous solution[J]. Colloids & Surfaces A Physicochemical & Engineering Aspects, 2014, 447(5): 59-66. |
| [17] |
Al-Omari A, Fayyad M. Treatment of domestic wastewater by subsurface flow constructed wetlands in Jordan[J]. Desalination, 2003, 155(1): 27-39. DOI:10.1016/S0011-9164(03)00236-4 |
| [18] |
Wang W, Jin Z H, Li T L, et al. Preparation of spherical iron nanoclusters in ethanol-water solution for nitrate removal[J]. Chemosphere, 2006, 65(8): 1396-1404. DOI:10.1016/j.chemosphere.2006.03.075 |
| [19] |
陈西亮, 刘国, 高阳阳, 等. 零价纳米铁炭微电解体系去除水中硝酸盐[J]. 环境化学, 2016, 35(8): 1670-1675. CHEN Xi-liang, LIU Guo, GAO Yang-yang, et al. removal of nitrate from water by nano-zero-valent iron-carbon microelectrolysis system[J]. Environmental Chemistry, 2016, 35(8): 1670-1675. DOI:10.7524/j.issn.0254-6108.2016.08.2015123003 |
| [20] |
Ryu A, Jeong S W, Jang A, et al. Reduction of highly concentrated nitrate using nanoscale zero-valent iron:Effects of aggregation and catalyst on reactivity[J]. Applied Catalysis B Environmental, 2011, 105(1/2): 128-135. |
| [21] |
Picardal F. Abiotic and Microbial Interactions during Anaerobic Transformations of Fe(Ⅱ) and[J]. Frontiers in Microbiology, 2012, 3(3): 112. DOI:10.3389/fmicb.2012.00112 |
| [22] |
Weber K A, Urrutia M M, Churchill P F. Anaerobic redox cycling of iron by freshwater sediment microorganisms[J]. Environmental Microbiology, 2006, 8(1): 100-113. DOI:10.1111/EMI.2006.8.issue-1 |
| [23] |
冯欢, 梁禹翔, 杜耀, 等. 填埋场中铁的生物化学循环对反硝化的影响[J]. 环境科学学报, 2014, 34(2): 409-416. FENG Huan, LIANG Yu-xiang, DU Yao, et al. Effect of microbial redox cycling of iron on denitrification in landfill[J]. Acta Scientiae Circumstantiae, 2014, 34(2): 409-416. |
| [24] |
Till B A, Weathers L J, Alvarez P J J. Fe(0)-Supported Autotrophic Denitrification[J]. Environmental Science & Technology, 1998, 32(5): 634-639. |
 2017, Vol. 36
2017, Vol. 36