文章信息
- 平巍, 李波, 董建丰, 杨槟榕, 闫晨宇, 吴彦
- PING Wei, LI Bo, DONG Jian-feng, YANG Bin-rong, YAN Chen-yu, WU Yan
- 生物质改性吸附材料的制备工艺优化及对氨氮的吸附特性
- Optimization of preparation technology for biomass-modified adsorption material and its adsorption properties for ammonia nitrogen
- 农业环境科学学报, 2017, 36(12): 2521-2526
- Journal of Agro-Environment Science, 2017, 36(12): 2521-2526
- http://dx.doi.org/10.11654/jaes.2017-0731
文章历史
- 收稿日期: 2017-05-19
- 录用日期: 2017-09-01
2. 重庆市渝东水务有限公司, 重庆 404100;
3. 重庆大学城市建设与环境工程学院, 重庆 400045
2. Chongqing Yudong Water Co., Ltd., Chongqing 404100, China;
3. College of Urban Construction and Environmental Engineering, Chongqing University, Chongqing 400045, China
氨氮是一种营养盐污染物,进入水体后会引起水体富营养化,从而造成水环境的破坏[1]。氨氮通过亚硝化细菌和硝化细菌在好氧条件下形成对饮用水产生很大危害的亚硝酸盐和硝酸盐,对人体健康产生很大的威胁。目前,氨氮的去除方法主要有空气吹脱法[2]、选择项离子交换法、折点加氯法[3]、生物脱氮法、电渗析法和吸附法等[4-6]。其中,吸附法是应用较为广泛的技术之一[7]。近年来,以低成本吸附材料去除水中氨氮的研究成果较多,其中主要有粘土、沸石和石灰石等,但这些材料对氨氮的吸附能力不高,且易受温度和pH值变化的影响,适用范围有限[8]。因此,新型吸附材料的开发和应用将成为吸附法处理氨氮废水的研究热点。
目前,国内外研究学者针对农林废弃物制备吸附材料领域做了广泛的研究,其中,利用化学改性制备天然吸附剂,因其制备方法简单、成本低,已经成为了新的研究热点[9-13]。香蕉是热带和亚热带的水果,在我国华南地区有较大的产量。香蕉皮中营养成分丰富,含有大量的果胶、低聚糖、纤维素、半纤维素、木质素等膳食纤维[14],其内部结构疏松多孔,是制备吸附剂的理想材料[15-16]。相关研究结果表明,香蕉皮可以有效去除废水中Cu2+和Zn2+等重金属离子[17-18],但未见香蕉皮对水中氨氮吸附去除及吸附参数的相关研究。本项目组的前期研究结果表明[19],利用香蕉皮制备改性吸附剂去除水中氨氮,具有较高的可行性。
本文以香蕉皮为原料,通过化学药剂改性制备吸附材料,用以去除水中的氨氮。以氨氮去除能力和制备的产率为评价指标,探讨了制备过程的改性剂浓度、改性时间、原材料粒径及固液比对制备过程的影响,优选出最佳的工艺参数,并利用扫描电镜(SEM)和傅里叶变换红外光谱(FT-IR)对制得的材料进行表征,最终,通过吸附等温模型,初步探讨了制成的吸附剂对水中氨氮的吸附能力,旨在研究和开发一种高效、廉价的绿色吸附材料。
1 材料与方法 1.1 实验材料、仪器、化学试剂原料:市售香蕉去皮,外皮用去离子水冲洗,于103~105 ℃烘至恒重,研碎过筛分级,存入干燥器备用。
含氮废水的配制,称取3.819 0 g氯化铵(NH4Cl,分析纯,在103~105 ℃干燥2 h)溶于蒸馏水中,移入1000 mL容量瓶中,稀释至标线,得到氨氮标准储备液。实验中所需氨氮水样浓度均由标准储备液稀释而成。
仪器:85-1型集热式恒温磁力搅拌器,重庆东跃仪器有限公司;HG-9070A电热恒温鼓风干燥箱,上海齐欣科学仪器有限公司;荣华SHA-C水浴恒温振荡器,江苏常州荣华仪器制造有限公司;T6新世纪紫外可见分光光度计,北京普析通用仪器有限责任公司;JSM-7800F扫描电镜,日本电子株式会社;Nicolet 6700傅立叶红外光谱仪,美国热电科学仪器公司;V-Sorb 2800P比表面积及孔径分析仪,北京金埃谱科技有限公司。
1.2 香蕉皮改性方法称取某一粒径范围的香蕉皮粉末(质量W1),按一定投加比例加入改性剂溶液,置于恒温磁力器于25 ℃搅拌一段时间,再用去离子水反复清洗、抽滤,直至滤出液pH值为7左右。放入恒温箱于105 ℃烘至恒重,用分析天平称得其质量(W2)。
为优化改性工艺参数,以水中氨氮去除率和制备产率为指标,对比了不同改性剂的改性效果,筛选出最佳改性剂。在此基础上先后考察了改性剂浓度、改性时间、固液比(香蕉皮粉末投加量与改性剂体积之比)、香蕉皮粉末粒径对制备过程的影响。其中改性剂浓度因素水平设定为0.01、0.02、0.06、0.08、0.1、0.2、0.4、0.6、0.8、1 mol·L-1;改性时间因素水平设定为1、2、5、10、15、20、30、40、50、60 min;固液比因素水平设定为1、2、5、10、15、20、50、100 g·L-1;粒径因素水平设定为0~20、20~40、40~60、60~80、80~100、100~120、120~140、140~160、160~180目。
1.3 吸附实验取0.2 g改性材料于100 mL锥形瓶中,加入100 mg·L-1的氨氮模拟废水50 mL,放入恒温水浴摇床,在25 ℃下振荡1 h,然后立即采用0.25 μm的滤膜进行过滤,用纳氏试剂比色法测定滤液中氨氮的剩余浓度。
1.4 效果评价方法氨氮去除率的计算参照公式(1),改性吸附剂的产率计算参照公式(2)。对比试验采用相同条件下不加吸附剂的氨氮水溶液进行,空白试验为去离子水。
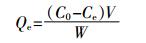 (1)
(1) 式中:Qe为吸附量,mg·g-1;C0为吸附前氨氮浓度,mg·L-1;Ce为吸附后氨氮浓度,mg·L-1;V为水样体积,L;W为吸附剂用量,g。
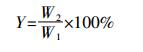 (2)
(2) 式中:Y为产率,%;W1为改性前原料质量,g;W2为改性后所得材料质量,g。
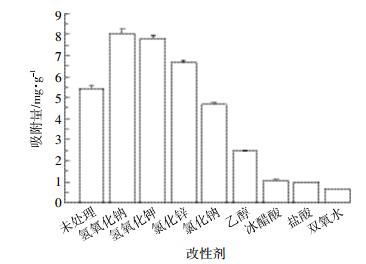
2 结果与讨论 2.1 化学改性剂筛选对NaOH等8种化学改性剂处理效果进行了对比,改性剂浓度均为0.2 mol·L-1,原料与改性剂投加比例(固液比)为10 g·L-1,其结果如图 1所示。结果表明,化学改性剂处理效果差异较大,总体上看,利用强碱对原料进行改性能显著提高材料对水中氨氮的吸附能力。其中,又以NaOH改性效果为最好,改性得到的材料对氨氮的吸附量达到8.065 mg·g-1。其原因是一方面NaOH对香蕉皮内的纤维素等成分具有一定的溶解浸出作用[20],改性过程中材料部分组织被改性剂浸出,留下疏松骨架结构,有利于氨氮粒子扩散进入材料内部而被吸附;另一方面,在改性过程中,部分Na+、K+等碱性金属离子通过离子交换等作用附着在材料表面,金属离子对NH4+具备较强的交换势,从而在吸附过程中,发生离子交换吸附。又因为离子交换势K+>Na+,故采用NaOH溶液改性效果最佳[21]。
|
| 图 1 化学改性剂对氨氮吸附能力的影响 Figure 1 Effect of chemical modification agent on the ammonia nitrogen removal rate |
图 2a所示的结果表明,在0~0.2 mol·L-1浓度范围内,随着改性剂浓度增大,制得的材料对氨氮的吸附量迅速提高,产率则相应降低。改性剂浓度越高,浸出作用越强烈,制得的材料的孔道结构越发达,同时材料表面的Na+负载越充分,制得的材料对氨氮的吸附效果越好。另一方面,浸出物增多导致产率下降。当改性剂浓度达到0.2 mol·L-1,进一步提高改性剂浓度,吸附量和产率变化幅度减弱,逐渐趋于稳定。综合考虑吸附量、产率和制备成本,0.2 mol·L-1是较为适宜的改性剂浓度。

|
| 图 2 改性参数对氨氮的吸附量及产率的影响 Figure 2 Effects of modification parameter on the ammonia nitrogen removal rate and yield |
图 2b所示的结果表明,在0~20 min内,随着改性时间的延长,制得的材料对氨氮的吸附量显著提高,而产率下降。这种趋势在改性时间超过20 min后明显减弱,逐渐趋向稳定。由此表明,改性剂对原材料的作用在前20 min比较强烈。结合改性时间对吸附剂的性能和产率的影响,确定20 min是较为适宜的改性时间。
图 2c所示的结果表明,在10~100 g·L-1(原料质量/改性剂体积)固液比范围内,随着改性剂的相对用量的增加(即降低固液比),制得的材料对氨氮的吸附量逐步提高,产率则逐渐降低。当固液比低于10 g·L-1,进一步提高改性剂的相对用量,对吸附量和产率的变化幅度都不明显。选择10 g·L-1作为改性的固液比较为合适。
图 2d所示的结果表明,在20~120目范围内,减小原料粒径,能显著提高制得材料对氨氮的吸附能力,同时产率逐渐下降;当粒径小于120目,则制得的吸附材料对氨氮的吸附性能随着粒径的减小而下降,产率则进一步降低。可能是过小的原料粒径引起剧烈的浸出反应,破坏了原料本身的骨架结构,从而导致其对氨氮的吸附性能下降。综合考虑制得材料的性能和制备的产率,原料在改性阶段的粒径控制在120目的范围较为合适。
2.3 改性前后材料表面结构变化图 3是香蕉皮粉末改性前后的扫描电镜图片。对比图 3a和图 3b可看出,改性前的香蕉皮表面孔隙结构发达,孔径大多在10 μm以下,且其表面被较多的有机物覆盖。改性后,材料表面大部分覆盖物被去除,孔道外露,表面孔径也有所增大,更有利于离子通过扩散快速进入材料内部而被吸附。

|
| 图 3 改性前后材料的扫描电镜图片 Figure 3 SEM images of before and after modified materials |
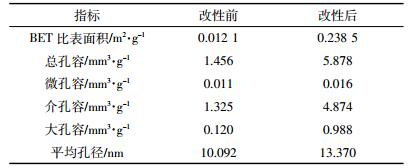
香蕉皮粉末改性前后的比表面积和孔径分布如表 1所示。由表 1可以看出,改性后材料的BET比表面积、孔容积显著增加,微孔、介孔、大孔容积增加幅度分别为45.5%、267.8%、723.3%,平均孔径也有所增加。这是由于材料内部孔道部分的物质被NaOH溶解浸出[20],导致孔径增大,同时,结构更为疏松,这些变化有利于向材料内部扩散,这与扫描电镜观察到的结果一致。但由表 1可知,改性后的香蕉皮粉末比表面积仍远小于活性炭(最高可达2000 m2·g-1以上)[22],因此,改性香蕉皮粉末对氨氮吸附的主要作用并非物理吸附。
图 4曲线1和曲线2分别是香蕉皮粉末改性前后的红外光谱图。在3420 cm-1处的吸收峰是由材料所含的O-H伸缩振动引起的。在2931、1620(曲线1)、1633(曲线2)、1248、1048 cm-1处有吸收峰说明材料含有饱和C-H、C=C、C-O。1395、662 cm-1两处的吸收峰分别是C-H和O-H的弯曲振动引起的。对比香蕉皮粉末改性前后的红外光谱图,吸收峰位置无实质区别,但曲线2在3420 cm-1处吸收峰的强度及峰面积明显弱于曲线1,说明改性后O-H伸缩振动减弱,这可能是因为材料表面部分缔合OH的H+被Na+取代导致的。交换势的强弱排序H+>NH4+>Na+,因此,Na+取代H+对NH4+吸附有利[23]。结合比表面积的结果,可初步推断,这种离子交换作用是改性蕉皮粉末吸附氨氮的重要因素。
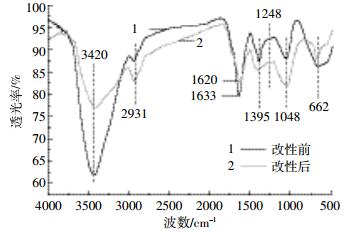
|
| 图 4 改性前后材料的红外光谱图 Figure 4 FT-IR spectra of raw and modified materials |
用实验确定的最佳改性条件制备的吸附材料对不同浓度的氨氮水溶液进行吸附实验,吸附材料投加量为0.4%,吸附时间1 h,结果见图 5。由实验结果可知,在氨氮浓度为0~100 mg·L-1范围内,材料对氨氮的吸附量随氨氮浓度的提高迅速增加,当氨氮浓度为100 mg·L-1,材料对氨氮的吸附量达到8.048 mg·g-1。继续提高氨氮浓度,吸附量随氨氮浓度提高不明显,趋向饱和。
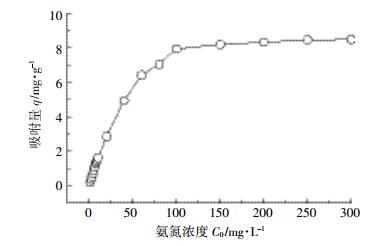
|
| 图 5 不同氨氮浓度下的吸附结果 Figure 5 Adsorption results under different ammonia nitrogen concentrations |
对不同浓度氨氮吸附实验结果采用Freundlich方程和Langmuir方程拟合,拟合结果见图 6、表 2。
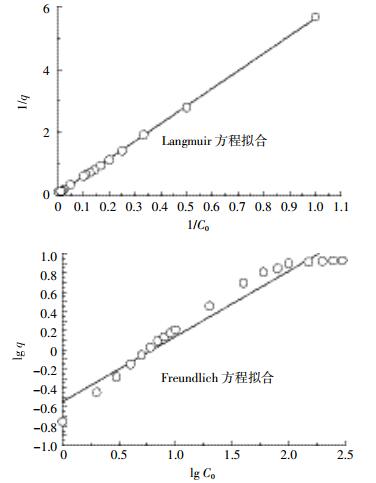
|
| 图 6 改性香蕉皮吸附剂吸附水中氨氮等温吸附曲线 Figure 6 Ammonium absorption isotherm of modified banana peel |

|
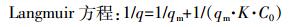 (3)
(3) 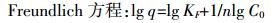 (4)
(4) 由图 6和表 2可知参数可信,香蕉皮吸附水中氨氮的等温式与Langmuir等温式的相关性较好,说明香蕉皮改性吸附剂对水中氨氮的吸附更倾向于单层吸附,结合材料的表面结构特性和官能团性质,可初步推断改性香蕉皮吸附材料对氨氮吸附可能以化学吸附为主。通过Langmuir等温式进行估算,香蕉皮改性吸附材料对水中氨氮饱和吸附量为16.051 mg·g-1,优于沸石(1.27 mg·g-1)和活性炭(0.53 mg·g-1)[24]。通过Freundlich等温式来分析,1/n < 1,且KF值较大,表明改性材料吸附水中氨氮属于较易发生的吸附。
3 结论(1)用强碱溶液对香蕉皮进行改性可明显增强其对氨氮的吸附能力。
(2)香蕉皮改性吸附材料制备最佳改性条件是用0.2 mol·L-1 NaOH作为改性剂,原料粒径为100~120目,固液比为10 g·L-1,改性时间为20 min。
(3)对改性香蕉皮吸附材料的氨氮吸附进行等温拟合,结果与Langmuir等温模型具有较好的相关性。由Langmuir等温式推算其对氨氮的饱和吸附量为16.051 mg·g-1,优于沸石和活性炭。
| [1] |
郑焕春, 周青. 微生物在富营养化水体生物修复中的作用[J]. 中国生态农业学报, 2009, 17(1): 197-202. ZHENG Huan-chun, ZHOU Qing. Function of microorganism in bioremediation of eutrophic water[J]. Chinese Journal of Eco-Agriculture, 2009, 17(1): 197-202. |
| [2] |
孙华, 申哲民. 吹脱法去除氨氮的模型研究[J]. 环境科学与技术, 2009, 32(8): 84-87. SUN hua, SHEN Zhe-min. Model of air stripping of ammonia nitrogen[J]. Environmental Science & Technology, 2009, 32(8): 84-87. |
| [3] |
刘莉峰, 宿辉, 李凤娟, 等. 氨氮废水处理技术研究进展[J]. 工业水处理, 2014, 34(11): 13-17. LIU Li-feng, SU Hui, LI Feng-juan, et al. Research progress in the treatment technology of ammonia nitrogen wastewater[J]. Industrial Water Treatment, 2014, 34(11): 13-17. DOI:10.11894/1005-829x.2014.34(11).013 |
| [4] |
余光亚, 杨战社, 呼世斌. 氨氮废水的电渗析处理[J]. 西北农业学报, 2008, 17(3): 332-335. YU Guang-ya, YANG Zhan-she, HU Shi-bin. Electrodialysis treatment of ammonia nitrogen wastewater[J]. Acta Agriculturae Boreali-occidentalts Sinica, 2008, 17(3): 332-335. |
| [5] |
Baker H M, Fraij H. Principles of interaction of ammonium ion with natural Jordanian deposits:Analysis of uptake studies[J]. Desalination, 2010, 251(1): 41-46. |
| [6] |
崔树军, 谷立坤, 张建云, 等. 高氨氮废水的处理技术及研究应用现状[J]. 中国给水排水, 2010, 26(14): 26-29. CUI Shu-jun, GU Li-kun, ZHANG Jian-yun, et al. Treatment technologies of high concentration ammonia nitrogen wastewater and their research and application status[J]. China Water & Wastewater, 2010, 26(14): 26-29. |
| [7] |
Gupta V, Imran A M. Adsorbents for water treatment:Development of low-cost alternatives to carbon[J]. Encyclopedia of Surface and Colloid Science, 2006, 2: 149-184. |
| [8] |
Karapinar N. Application of natural zeolite for phosphorus and ammonium removal from aqueous solutions[J]. Journal of Hazardous Materials, 2009, 170(2/3): 1186-1191. |
| [9] |
Wang D, He S H, Lin Z B, et al. Agricultural waste material as adsorbent for sequestering heavy metal ions from aqueous solutions[J]. Water Sciences & Engineering Technology, 2013, 6: 22-24. |
| [10] |
Wang B W, Wang Y, Li R J, et al. Development of preparation and application of modified biomass adsorbent[J]. Guangzhou Chemical Industry, 2015, 43(16): 34-36, 98. |
| [11] |
Sud D, Mahajan G, Kaur M P. Agricultural waste material as potential adsorbent for sequestering heavy metal ions from aqueous solutions:A review[J]. Bioresource Technology, 2008, 99(14): 6017-6027. DOI:10.1016/j.biortech.2007.11.064 |
| [12] |
Banerjee K, Ramesh S T, Gandhimathi R, et al. A novel agricultural waste adsorbent, watermelon shell for the removal of copper from aqueous solutions[J]. Iranica Journal of Energy & Environment, 2012, 3(2): 143-156. |
| [13] |
揭诗琪, 乔丽媛, 李明明, 等. 改性生物质材料对Cr(Ⅵ)的吸附性能[J]. 中国有色金属学报, 2015(5): 1362-1369. JIE Shi-qi, QIAO Li-yuan, LI Ming-ming, et al. Adsorption properties of Cr(Ⅵ) by modified biomass materials[J]. The Chinese Journal of Nonferrous Metals, 2015(5): 1362-1369. |
| [14] |
贾宝珠, 鲍金勇, 杨公明. 香蕉皮中功能性成分的研究进展[J]. 食品研究与开发, 2014(14): 128-134. JIA Bao-zhu, BAO Jin-yong, YANG Gong-ming. Advances on functional component of banana peel[J]. Food Research and Development, 2014(14): 128-134. DOI:10.3969/j.issn.1005-6521.2014.14.035 |
| [15] |
Memon J R, Memon S Q, Bhanger M I, et al. Characterization of banana peel by scanning electron microscopy and FT-IR spectroscopy and its use for cadmium removal[J]. Colloids & Surfaces B:Biointerfaces, 2008, 66(2): 260-265. |
| [16] |
Kaewsarn P, Saikaew W, Wongcharee S. Dried biosorbent derived from banana peel:A potential biosorbent for removal of cadmium ions from aqueous solution[C]. Thai Institute of Chemical Engineering and Applied Chemistry, 2008.
|
| [17] |
Lai Y L, Thirumavalavan M, Lee J F. Effective adsorption of heavy metal ions(Cu, Pb, Zn) from aqueous solution by immobilization of adsorbents on Ca-alginate beads[J]. Toxicological & Environmental Chemistry, 2010, 92(4): 697-705. |
| [18] |
Castro R S D, Caetano L, Ferreira G, et al. Banana peel applied to the solid phase extraction of copper and lead from river water:Preconcentration of metal ions with a fruit waste[J]. Ind Eng Chem Res, 2011, 50(6): 3446-3451. DOI:10.1021/ie101499e |
| [19] |
董建丰, 平巍, 付川, 等. 香蕉皮改性吸附剂对氨氮吸附特性[J]. 环境工程学报, 2016, 10(4): 1807-1812. DONG Jian-feng, PING Wei, FU Chuan, et al. Adsorption characteristics of banana peel modified adsorbent[J]. Chinese Journal of Environmental Engineering, 2016, 10(4): 1807-1812. DOI:10.12030/j.cjee.20160435 |
| [20] |
朱中原. 香蕉皮中水不溶性膳食纤维提取工艺研究[J]. 食品工程, 2012(3): 29-31. ZHU Zhong-yuan. Study on extraction of soluble dietary fiber in banana peel[J]. Food Engineering, 2012(3): 29-31. |
| [21] |
袁俊生, 杨永春. 钠型斜发沸石在K+-Na+-NH4+和K+-Na+-Ca2+水溶液体系中的离子交换平衡[J]. 离子交换与吸附, 2008, 24(6): 496-503. YUAN Jun-sheng, YANG Yong-chun. Ion exchange equilibria between clinoptilolite and aqueous solutions of K+-Na+-NH4+ and K+-Na+-Ca2+[J]. Ion Exchange and Adsorption, 2008, 24(6): 496-503. |
| [22] |
Hasegawa G. Monolithic electrode for electric double-layer capacitors based on macro/meso/microporous S-containing activated carbon with high surface area[M]//Hasegawa G. Studies on porous monolithic materials prepared via Sol-Gel Processes. Japan:Springer 2012:79-89.
|
| [23] |
Booker N A, Cooney E L, Priestley A J. Ammonia removal from sewage using natural Australian zeolite[J]. Water Science & Technology, 1996, 34(9): 17-24. |
| [24] |
田琳, 孔强, 任宗明, 等. 活性炭和沸石对氨氮的吸附特性及生物再生[J]. 环境工程学报, 2010, 6(10): 3424-3428. TIAN Lin, KONG Qiang, REN Zong-ming, et al. Adsorption characteristics of activated carbon and zeolite and their biological regeneration[J]. Chinese Journal of Environmental Engineering, 2010, 6(10): 3424-3428. |
 2017, Vol. 36
2017, Vol. 36