文章信息
- 陈安强, 雷宝坤, 刘宏斌, 翟丽梅, 王洪媛, 毛妍婷, 张丹
- CHEN An-qiang, LEI Bao-kun, LIU Hong-bin, ZHAI Li-mei, WANG Hong-yuan, MAO Yan-ting, ZHANG Dan
- 洱海近岸菜地不同土壤发生层的NH4+-N吸附解吸特征
- Adsorption and desorption of NH4+-N in the different soil genesis layers in the nearshore vegetable field of Erhai Lake
- 农业环境科学学报, 2017, 36(2): 345-352
- Journal of Agro-Environment Science, 2017, 36(2): 345-352
- http://dx.doi.org/10.11654/jaes.2016-1023
文章历史
- 收稿日期: 2016-08-09
2. 中国农业科学院农业资源与农业区划研究所, 农业部面源污染控制重点实验室, 北京 100081;
3. 云南农业大学资源与环境学院, 昆明 650201
2. Institute of Agricultural Resources and Regional Planning, Chinese Academy of Agricultural Sciences, Key Laboratory of Nonpoint Source Pollution Control, Ministry of Agriculture, Beijing 100081, China;
3. College of Resources and Environment, Yunnan Agricultural University, Kunming 650201, China
农田土壤氮素在地表径流、地下淋溶和浅层地下水等水文过程作用下的入湖通量增加是导致湖泊水体富营养化的重要因素之一[1],对水域生态系统的生物地球化学循环构成严重威胁。目前,洱海湖滨带农田缓冲带较少,即使存在农田缓冲带,其宽度也较窄,多数农田紧靠环海路与洱海相隔,所以,近岸农田成为土壤环境对流入洱海水体氮素等污染物截留转化的唯一屏障。洱海近岸菜地土壤也是水-陆域生态系统进行物质交换过程中最重要的中间场所,近岸土壤主要通过土壤吸附-解吸、微生物固定利用以及生物化学过程(如硝化、反硝化作用等)途径对地表径流、淋溶或浅层地下水渗流中的氮污染物进行截留转化[2-3],是流入洱海的氮污染物“源-汇”功能转换的重要载体,其中土壤对氮素的吸附-解吸是氮素“源-汇”功能转换的重要影响因素之一。因此,研究土壤对氮的吸附-解吸特征对于控制农田面源氮素流失、保护受纳水体的环境安全具有重要意义。
目前,关于氮吸附-解吸特征的研究主要侧重于铵态氮的吸附-解吸热力学、动力学及其影响因素等方面,并采用Langmuir模型、Freundlich模型或Temkin模型和一级反应动力学模型、二级反应动力学模型或Elovich模型对吸附-解吸的热力学和动力学过程进行预测[4-7],对氮吸附-解吸的影响因素,如土壤机械组成、团聚体组成、有机质、pH、阳粒子含量和温度的关系也进行了一些研究[8-10]。氮吸附-解吸载体的研究主要集中在高效吸附材料[11]和湖泊底泥[4, 8, 12]上,前者主要关注其对氮污染物的处理,后者主要是研究底泥中内源氮在上覆水作用下释放对水质的影响。可见,以往的研究主要是针对氮污染物高效吸附材料筛选及湖泊底泥内源氮磷与上覆水互作用下的吸附-解吸特征。洱海近岸菜地耕作强度高、水肥投入量大,造成氮素在土壤中过量累积,加之近岸菜地浅层地下水位埋深浅(最浅埋深0.2 m),季节和年际间水位波动大(0.2~1.1 m),而且洱海水位与近岸农田浅层地下水水位变化息息相关[13],使得菜地土壤中累积的氮在洱海水与湖滨带农田浅层地下水互作用下时刻发生着吸附-解吸行为,极易造成氮素流失。目前,对洱海近岸不同土壤发生层对NH4+-N吸附-解吸的机理研究还未见报道。本文通过研究洱海近岸菜地不同土壤发生层对NH4+-N吸附-解吸的热力学特征,明确不同土壤发生层理化性质对NH4+-N吸附-解吸的影响,以期为洱海近岸菜地不同土壤发生层氮素通过浅层地下水向洱海水体扩散通量的确定提供重要参数。
1 材料与方法 1.1 采样点及样品采集采样点位于云南省大理州下关市大庄村蔬菜地,东经100°12′35″,北纬25°40′14.6″,海拔1966 m。气候类型为亚热带高原性季风气候区,年均气温13~20 ℃,年均降水量1100 mm。土壤类型为水稻土,属湖积冲积土。自20世纪80年代中后期稻田改种蔬菜,现为下关市的露地蔬菜基地。在距离洱海30 m同一等高线的菜地上,挖2个土壤剖面(图 1),根据土壤发生层的层次分布,分别取耕作层A(0~30 cm)、犁底层P(30~40 cm)、潴育层W(40~60 cm)和潜育层G(>60 cm)4个土壤发生层样品,每个发生层取3个重复样,一部分样品测定土壤的pH、有机质OM、全氮TN、硝态氮NO3--N、铵态氮NH4+-N、总铁TFe、总锰TMn、土壤的机械组成和微团聚体组成,另一部分风干后过2 mm筛备用。同时每个土壤发生层取3个环刀样,测定土壤的容重、孔隙度。

|
| 图 1 不同土壤发生层分布 Figure 1 Distribution of the different soil genesis layers |
采用先吸附、后解吸的方法研究不同土壤发生层NH4+-N的吸附-解吸特征。称取制备样品4 g,置于50 mL聚乙烯塑料离心管中,并加入40 mL由蒸馏水配置的不同浓度的NH4+-N标准液,初始NH4+-N标准液用(NH4)2SO4配置,浓度分别为:0、5、10、20、30、40、60、80 mg·L-1。向聚乙烯塑料离心管中加入0.1%的氯仿,抑制微生物的影响。旋紧盖后置于振荡机上于(25±1)℃振荡36 h,平衡后以4800 r·min-1离心5 min,上清液过0.45 μm的微孔滤膜,用AA3型连续流动分析仪测定吸附后平衡溶液中的NH4+-N浓度。样品对NH4+-N吸附饱和后,弃去离心管中的上清液,加入40 mL的去离子水振荡解吸36 h,平衡后以4800 r·min-1离心5 min,上清液过0.45 μm的微孔滤膜,用AA3型连续流动分析仪测定解吸平衡溶液的NH4+-N浓度。每个浓度重复3次,试验时间为2016年3月。
1.3 计算方法[5] 1.3.1 吸附量计算用初始NH4+-N浓度C0(mg·L-1)与吸附平衡溶液NH4+-N浓度Ce(mg·L-1)的差值计算得出土壤对NH4+-N的吸附量Cs(mg·kg-1):
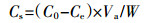
式中:Va为吸附平衡溶液体积,mL;W为土样质量,g。
1.3.2 解吸量计算由解吸平衡溶液NH4+-N浓度Ce(mg·L-1)计算得到土壤吸附NH4+-N的解吸量Ds(mg·kg-1):
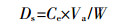
式中:Va为解吸平衡溶液体积,mL;W为土样质量,g。
1.3.3 等温吸附参数的计算采用Langmuir和Freundlich模型对不同土壤发生层NH4+-N的吸附过程分别进行拟合[5]。

式中:Cs为吸附量,mg·kg-1;Ce为平衡浓度,mg·L-1;Q0为饱和吸附量,mg·kg-1;K1为等温吸附平衡系数;Q0K1为最大缓冲容量MBC,mg·kg-1。

式中:K2为吸附分配系数,表征吸附质在固相液相的分配比,K2越大则吸附能力越强;n为吸附速率常数,表示随着吸附质溶液浓度的增加,吸附量增加的速度[6]。
1.3.4 等温解吸参数的计算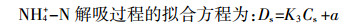
式中:Ds为解吸量,mg·kg-1;Cs为吸附量,mg·kg-1;K3为解吸速率,表示单位吸附量中的解吸量;a为解吸常数。
1.4 测试方法NO3--N、NH4+-N采用AA3型连续流动分析仪测定,OM采用重铬酸钾外加热法测定,TN用凯氏定氮法测定,土壤机械组成采用比重计法测定,土壤微团聚体(土壤中直径<0.25 mm的土壤微结构体)的组成采用吸管法测定,pH用酸度计测定,TFe用邻菲罗啉分光光度法测定,TMn用高碘酸钾分光光度法测定,土壤容重和孔隙度采用环刀法测定[14]。
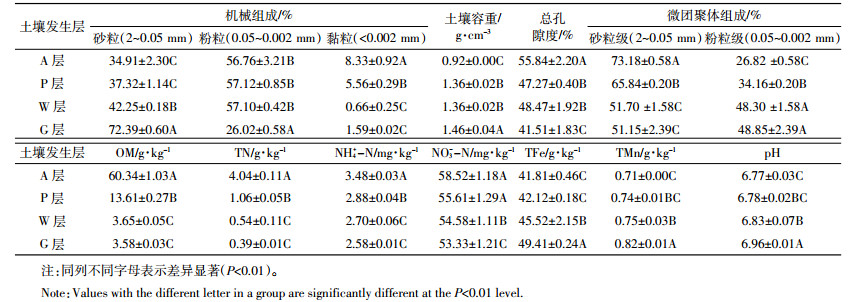
2 结果与讨论 2.1 菜地不同土壤发生层理化性质不同土壤发生层物理性状差别较大(表 1),潜育层G和潴育层W的砂粒含量较高,其次是犁底层P和耕作层A,各层土壤砂粒(2~0.05 mm)含量为72.39%~34.91%,各层土壤黏粒( < 0.002 mm)含量为0.66%~8.33%,其大小顺序与砂粒相反。除了A层和P层的砂粒含量及G层和W层的黏粒含量差异不显著外(P>0.01),其他土壤发生层砂粒和黏粒含量都呈显著性差异(P<0.01)。A、P和W层的粉粒(0.05~0.002 mm)含量(56.76%~57.12%)与G层(26.02%)相差较大,呈显著性差异(P<0.01)。不同土壤发生层只存在砂粒级(2~0.05 mm)和粉粒级(0.05~0.002 mm)微团聚体,不同土壤发生层砂粒级微团聚体含量为51.15%~73.18%,其大小顺序为A层>P层>W层>G层,而粉粒级的微团聚体含量为26.82%~48.85%,两者大小顺序相反。除了G层和W层的砂粒和粉粒级微团聚体差异不显著外(P>0.01),其他土壤发生层砂粒级和粉粒级微团聚体都分别呈显著性差异(P<0.01)。不同土壤发生层的土壤容重(0.92~1.46 g·cm-3)和总孔隙度(41.51%~48.47%)差异也较大。
不同土壤发生层化学性质差别较大(表 1),OM、TN、NH4+-N、NO3--N、TFe、TMn的含量分别为3.58~60.34、0.39~4.04、2.58~3.48、53.33~58.52、41.81~49.41、0.71~0.82 g·kg-1,pH为6.77~6.96,说明土壤呈中性。各发生层土壤的OM、TN、NH4+-N、NO3--N大小顺序一致,为A层>P层>W层>G层,而各发生层土壤TFe、TMn和pH大小顺序正相反。除了G层和W层的OM、TN、NH4+-N以及A层和P层的NO3--N、TFe差异不显著外(P>0.01),其他土壤发生层之间都分别呈显著性差异(P<0.01)。G层的TMn、pH也与其他土壤发生层之间都分别呈显著性差异(P<0.01)。
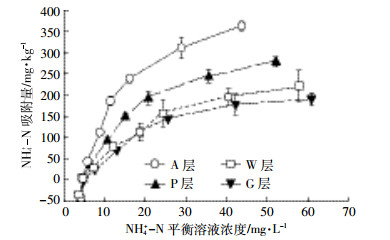
2.2 菜地不同土壤发生层NH4+-N的吸附特征等温吸附-解吸是氮素在固液界面中扩散、迁移、转化的一个重要途径。图 2表明在NH4+-N平衡溶液浓度为0~30 mg·L-1时,不同土壤发生层吸附的NH4+-N与液相浓度呈线性递增吸附,随着吸附平衡溶液浓度的增加,土壤对NH4+-N吸附速率减缓,吸附量缓慢趋于一个常数。根据吸附平衡溶液浓度与土壤对NH4+-N吸附量的变化曲线,采用Langmuir和Freundlich模型对不同土壤发生层NH4+-N的吸附过程进行拟合[5],结果(表 2)表明Freundlich模型的决定系数R2(0.852~0.885)要低于Langmuir模型的决定系数R2(0.871~0.911),不同土壤发生层的NH4+-N的吸附量和平衡浓度都呈显著相关(P<0.01)。
|
| 图 2 不同土壤发生层NH4+-N的吸附曲线 Figure 2 Adsorption curve of NH4+-N on the different soil genesis layers |
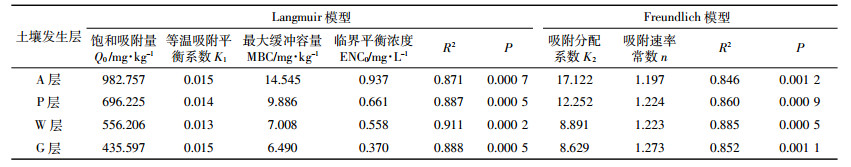 |
利用Langmuir等温吸附模型确定的饱和吸附量Q0、最大缓冲容量MBC参数可反映土壤对NH4+-N的吸附能力及环境风险。其中Q0可反应土壤吸附NH4+-N容量的大小,也可用于评价土壤中NH4+-N释放的风险,Q0越大环境风险越小。由表 2可见,洱海近岸菜地不同土壤发生层NH4+-N的Q0依次为A层(982.757 mg·kg-1)>P层(696.225 mg·kg-1)>W层(556.206 mg·kg-1)>G层(435.597 mg·kg-1),显示不同土壤发生层NH4+-N的Q0相差较大,而且越往深层,土壤中NH4+-N释放风险越大,因为在浅层地下水作用下,土壤中NH4+-N极易流失。西辽河流域沙土NH4+-N的Q0为573.81~3 666.18 mg·kg-1 [5],滦河三角洲典型包气带介质NH4+-N的Q0为138~534 mg·kg-1 [15],长江中下游浅水湖泊沉积物NH4+-N的Q0为294.11~1 466.67 mg·kg-1 [8]。土壤对NH4+-N的MBC是土壤中增加或减少NH4+-N时,土壤抵御NH4+-N浓度变化的最大能力。表 2表明洱海近岸菜地不同土壤发生层NH4+-N的MBC为A层(14.545 mg·kg-1)>P层(9.886 mg·kg-1)>W层(7.008 mg·kg-1)>G层(6.490 mg·kg-1)。鄱阳湖南矶山自然保护区沼泽湿地土壤对NH4+-N的MBC为117.65 mg·kg-1 [7]。不同区域土壤NH4+-N的Q0和MBC的差异较大,除了与土壤理化性质密切相关外,也与测定方法中是否加入微生物抑制剂有一定关系,因为氯仿能杀死系统中的微生物或者抑制系统中微生物的繁殖。卢少勇等[16]认为氯仿在沉积物-水系统中对硝化和反硝化细菌的活性有一定的抑制作用,导致沉积物的硝化速率和反硝化速率降低,但是硝化活性和反硝化活性并未被彻底抑制。在本试验中,加入了0.1%的氯仿来抑制微生物活性,而王而力等[5]、弓晓峰等[7]和王娟等[8]在研究氮的吸附-解吸过程中未加入氯仿。
ENC0是不同土壤发生层发生吸附-解吸过程中的临界平衡NH4+-N浓度,是土壤发生吸附或解吸的转折点。当水体NH4+-N浓度小于ENC0时,土壤出现解吸行为,表现为NH4+-N的“源”;反之,土壤出现吸附行为,表现为NH4+-N的“汇”[8]。表 2表明不同土壤发生层的ENC0为A层(0.937 mg·L-1)>P层(0.661 mg·L-1)>W层(0.558 mg·L-1)>G层(0.370 mg·L-1),说明越往土壤下层,ENC0越低,土壤吸附的NH4+-N越容易成为浅层地下水或洱海水的“源”。
由Freundlich模型确定的吸附分配系数K2[17](表 2)可知:A层土壤的K2最大,为17.122,说明该层土壤对NH4+-N的固持能力最强,减少了固持在土壤中NH4+-N向地下水中的扩散;而W层和G层的K2较小,分别为8.891和8.629,说明该层土壤中的NH4+-N最容易向地下水中释放,而且该层土壤与地下水互作用时间也最长,环境风险较大。
洱海近岸菜地土壤氮素过量累积,加之菜地浅层地下水与洱海水交汇贯通[13],使得土壤氮素在浅层地下水和洱海水互作用下不断进行着迁移(弥散过程、扩散过程)和转化(硝化、反硝化、有机氮矿化),极易造成氮素流失,其中NH4+-N的吸附-解吸行为是氮素迁移转化过程中的重要环节。因此,上述关于Q0、MBC、ENC0和K2的分析,对明确洱海近岸菜地土壤对NH4+-N的吸附参数,提高菜地土壤的氮库容量,减少耕层土壤氮的径流、淋溶或浅层地下水渗流流失,具有重要意义。研究表明,越往深层土壤对NH4+-N的吸附能力越差,NH4+-N释放风险越大,在浅层地下水作用下,土壤固持的NH4+-N极易释放到环境中。加之洱海近岸浅层地下水NH4+-N平均浓度为0.163 mg·L-1,洱海上覆水NH4+-N浓度为0.127~0.222 mg·L-1 [18],即无论是地下水还是洱海水NH4+-N浓度都低于不同土壤发生层的ENC0,因而在浅层地下水或洱海水作用下,不同发生层土壤吸附的NH4+-N极易解吸,起到“源”的作用。另外,明确不同土壤发生层NH4+-N的吸附参数,也可为氮素随浅层地下水迁移模型的建立提供必要参数。
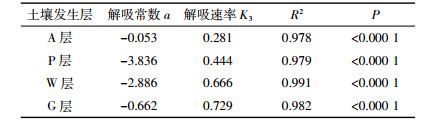
2.3 菜地不同土壤发生层NH4+-N的解吸特征解吸是吸附的逆过程[5],解吸不仅关系到吸附氮的再利用,还影响到土壤中内源氮释放对水环境的威胁。图 3表明随着NH4+-N吸附量的增加,NH4+-N的解吸量也呈增加趋势,两者呈显著性相关(P<0.000 1)。就解吸速率K3而言(表 3),G层土壤的解吸速率最大,为0.729,说明G层土壤吸附的NH4+-N有72.9%再次被释放到环境中,其对外源NH4+-N的缓冲能力最差;其次是W层(0.666)和P层(0.444);A层土壤解吸速率最小(0.281),说明A层吸附的NH4+-N不易被释放,仅占吸附量的28.1%。通过图 1和图 2看出,不同土壤发生层对NH4+-N吸附-解吸过程具有不可逆性,解吸存在滞后性[6],这种滞后性在黏粒和粉粒中的表现更为突出[5]。

|
| 图 3 不同土壤发生层NH4+-N的解吸曲线 Figure 3 Desorption curve of NH4+-N on the different soil genesis layers |
 |
对吸附-解吸参数Q0、MBC、ENC0和K3与不同土壤发生层的理化性质进行相关分析表明(表 4、表 5),机械组成中的粉粒和黏粒含量和砂粒级微团聚体与吸附参数Q0、MBC、ENC0呈正相关关系,与K3呈负相关关系,而机械组成中的砂粒含量和粉粒级微团聚体与吸附-解吸参数却相反,黏粒含量与吸附-解吸参数相关程度明显大于粉粒和砂粒。这说明机械组成中的粉粒、黏粒含量和砂粒级微团聚体含量越多,越有利于土壤的吸附,其含量越少则越有利于解吸发生,主要是因为机械组成中的粒径越小,所具有的比表面积和质量越大,土壤颗粒表面活性点位越多,吸附能力越强。而且,较多的研究者也认为,不同粒径土壤的吸附能力为黏粒>粉粒>砂粒[8, 12, 15, 19]。微团聚体通过有机胶体或矿物颗粒相互共生富集,而由于微团聚体中存在大量微孔隙[20],砂粒级微团粒径较大,微孔隙度较多,使得微团聚体对NH4+-N的吸附不仅包括胶体、颗粒表面和粒子交换吸附,还包括微孔隙填充吸附[5]。
 |
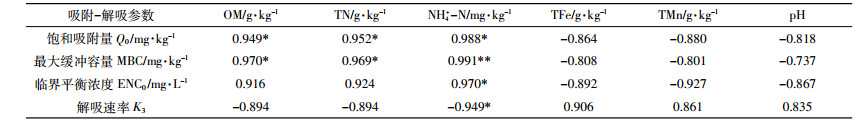 |
表 5表明,吸附相关的参数Q0、MBC、ENC0与不同土壤发生层OM、TN和NH4+-N呈正相关关系,与TFe、TMn和pH呈负相关关系,与吸附相关参数相比,K3与不同土壤发生层化学性质却有相反的变化。从吸附-解吸参数与土壤化学性质的相关程度看,NH4+-N>TN>OM>TFe或TMn>pH,说明吸附介质中的氮(TN或NH4+-N)浓度显著影响着不同土壤发生层对NH4+-N的吸附解吸。有机质含量是影响不同土壤发生层NH4+-N吸附-解吸的重要因素。这是因为腐殖质等形成的胶体在粘土矿物及各种氧化物上形成不同粒径的团聚体[21],有利于NH4+-N的吸附。而有些研究者[22-23]也认为,NH4+-N与有机质在吸附过程中存在竞争关系,这些差异主要是前者中的有机质在吸附介质中,而后者中的有机质在吸附溶液中。TFe、TMn和pH与吸附参数呈负相关,而与解吸参数呈正相关关系。一些研究[24]之所以认为深层土壤的铁锰与NH4+-N含量呈显著正相关,主要是因为土壤中的铁锰氧化物在兼氧或厌氧条件下,作为氧化剂促进了NH4+-N的硝化,使得平衡溶液中的NH4+-N浓度降低,铁促进了NH4+-N的吸附[25]。另外,张晨东等[4]研究认为随着吸附溶液pH的增加,NH4+-N的吸附量增加,因为pH<8时H+和NH4+-N间的吸附竞争大,吸附量较低,当pH>8时随着H+和NH+4间的吸附竞争减弱,吸附量会增加。但本研究中不同土壤发生层pH为6.765~6.955,而且张晨东等[4]研究的是吸附溶液中的pH与NH4+-N浓度的关系,并非吸附剂的pH。以上关于TFe、TMn和pH对NH4+-N吸附的研究与本研究结果不尽一致,主要由于以往的研究[23-24]是对TFe、TMn和pH与NH4+-N浓度进行的相关分析,本研究中是对这些因子与NH4+-N吸附-解吸参数的相关分析,而NH4+-N吸附-解吸参数的确定又是土壤理化性质多重复合因子综合作用的结果。
3 结论洱海近岸菜地不同土壤发生层NH4+-N的等温吸附-解吸特征分别符合Langmuir模型和一元线性方程,土壤对NH4+-N的吸附能力为A层>P层>W层>G层,解吸速率与此相反,越往深层土壤对NH4+-N的吸附能力越小,对外源NH4+-N的缓冲能力越差,土壤中NH4+-N释放风险越大。
土壤机械组成中粉粒、黏粒含量和砂粒级微团聚体与吸附参数Q0、MBC、ENC0呈正相关关系,与解吸参数K3呈负相关关系,粉粒、黏粒含量和砂粒级微团聚体含量越多,越有利于土壤吸附。吸附参数Q0、MBC、ENC0与土壤OM、TN和NH4+-N呈正相关关系,与TFe、TMn和pH呈负相关关系,而解吸参数K3正相反,吸附介质中氮浓度和有机质是影响NH4+-N吸附-解吸的重要因素。
| [1] | 程波, 张泽, 陈凌, 等. 太湖水体富营养化与流域农业面源污染的控制[J]. 农业环境科学学报, 2005, 24(Suppl1) : 118–124. CHENG Bo, ZHANG Ze, CHEN Ling, et al. Eutrophication of Taihu Lake and pollution from agricultural non-point sources in Lake Taihu Basin[J]. Journal of Agro-Environment Science, 2005, 24(Suppl1) : 118–124. |
| [2] | Rassam D W, Pagendam D E, Hunter H M. Conceptualisation and application of models for groundwater-surface water interactions and nitrate attenuation potential in riparian zones[J]. Environmental Modelling & Software, 2008, 23(7) : 859–875. |
| [3] | 王庆成, 于红丽, 姚琴, 等. 河岸带对陆地水体氮素输入的截流转化作用[J]. 应用生态学报, 2007, 18(11) : 2611–2617. WANG Qing-cheng, YU Hong-li, YAO Qin, et al. Retaining and transformation of incoming soil N from high land to adjacent terrestrial water body in riparian buffer zone[J]. Chinese Journal of Applied Ecology, 2007, 18(11) : 2611–2617. |
| [4] | 张晨东, 马秀兰, 安娜, 等. 典型湖库底泥对氮吸附特性的影响[J]. 水土保持学报, 2014, 28(1) : 161–166. ZHANG Chen-dong, MA Xiu-lan, AN Na, et al. Characteristics of nitrogen adsorption by sediments in typical lakes and reservoirs[J]. Journal of Soil and Water Conservation, 2014, 28(1) : 161–166. |
| [5] | 王而力, 王雅迪, 王嗣淇. 西辽河不同粒级沉积物的氨氮吸附-解吸特征[J]. 环境科学研究, 2012, 25(9) : 1016–1023. WANG Er-li, WANG Ya-di, WANG Si-qi. Sorption and desorption of ammonium nitrogen on sediments of different grain sizes in Western Liao River[J]. Research of Environmental Sciences, 2012, 25(9) : 1016–1023. |
| [6] | 赵东洋, 王雅迪, 王而力. 沉积物不同天然有机组分对氨氮解吸特征的影响[J]. 地球环境学报, 2015, 6(2) : 113–119. ZHAO Dong-yang, WANG Ya-di, WANG Er-li. Effect of natural organic matter fraction on desorption characteristic of ammonium nitrogen on sediment in Western Liao River[J]. Journal of Earth Environment, 2015, 6(2) : 113–119. |
| [7] | 弓晓峰, 张静, 张振辉, 等. 鄱阳湖南矶山自然保护区沼泽湿地土壤对NH4+-N吸附能力的研究[J]. 农业环境科学学报, 2006, 25(1) : 179–181. GONG Xiao-feng, ZHANG Jing, ZHANG Zhen-hui, et al. Study on the ammonium adsorption of the wetland soils in the Nanjishan Nature Reserve[J]. Journal of Agro-Environment Science, 2006, 25(1) : 179–181. |
| [8] | 王娟, 王圣瑞, 金相灿, 等. 长江中下游浅水湖泊表层沉积物对氨氮的吸附特征[J]. 农业环境科学学报, 2007, 26(4) : 1224–1229. WANG Juan, WANG Sheng-rui, JIN Xiang-can, et al. Ammonium adsorption characteristics onto the sediments from shallow lakes in the middle and lower reaches of the Yangtze River[J]. Journal of Agro-Environment Science, 2007, 26(4) : 1224–1229. |
| [9] | Sander M, Lu Y, Pignatello J J. A thermodynamically based method to quantify true sorption hysteresis[J]. Journal of Environmental Quality, 2005, 34(3) : 1063–1072. DOI:10.2134/jeq2004.0301 |
| [10] | Lumbanraja J, Evangelou V P. Adsorption-desorption of potassium and ammonium at low cation concentrations in three Kentucky subsoils[J]. Soil Science, 1994, 157(5) : 269–278. DOI:10.1097/00010694-199405000-00001 |
| [11] | 张文艺, 郑泽鑫, 韩有法, 等. 改性沸石对猪场沼液氮磷吸附特性与机理分析[J]. 农业环境科学学报, 2014, 33(9) : 1837–1842. ZHANG Wen-yi, ZHEN Ze-xin, HAN You-fa, et al. Mechanisms of nitrogen and phosphorus adsorption from biogas slurry of piggery by modified zeolite[J]. Journal of Agro-Environment Science, 2014, 33(9) : 1837–1842. |
| [12] | 王圣瑞, 焦立新, 金相灿, 等. 长江中下游浅水湖泊沉积物总氮、可交换态氮与固定态铵的赋存特征[J]. 环境科学学报, 2008, 28(1) : 37–43. WANG Sheng-rui, JIAO Li-xin, JIN Xiang-can, et al. Distribution of total, exchangeable and fixed nitrogen in the sediments from shallow lakes in the middle and lower reaches of the Yangtze River[J]. Acta Scientiae Circumstantiae, 2008, 28(1) : 37–43. |
| [13] | 汤承彬. 洱海水位与湖区地下水位相关研究[J]. 云南环保, 1988(1) : 40–47. TANG Cheng-bin. Study on the relationship between water level of Erhai Lake and groundwater level in the lake region[J]. Yunnan Environmental Protection, 1988(1) : 40–47. |
| [14] | 鲁如坤. 土壤和农业化学分析法[M]. 北京: 中国农业科技出版社, 2000. LU Ru-kun. Analytical method of soil agrochemistry[M]. Beijing: China Agricultural Science and Technology Press, 2000. |
| [15] | 田华. 氨氮在滦河三角洲典型包气带介质上的吸附性能研究[J]. 环境工程学报, 2011, 5(3) : 507–510. TIAN Hua. Ammonia-nitrogen adsorption characteristics onto vadose zone soils in Luanhe Delta[J]. Chinese Journal of Environmental Engineering, 2011, 5(3) : 507–510. |
| [16] | 卢少勇, 金相灿, 郭建宁, 等. 氯仿作为抑制剂对沉积物-水系统中氮转化的影响[J]. 生态环境, 2006, 15(6) : 1133–1137. LU Shao-yong, JIN Xiang-can, GUO Jian-ning, et al. Effect of CH3Cl as inhibiter in sediment-water system on nitrogen transformation[J]. Ecology and Environment, 2006, 15(6) : 1133–1137. |
| [17] | 王而力, 王嗣淇, 王亮. 西辽河流域沙土对氨氮的吸附行为研究[J]. 环境科学与技术, 2011, 34(Suppl) : 102–106. WANG Er-li, WANG Si-qi, WANG Liang. Sorption behavior of ammonium nitrogen on sandy soil in Western Liao River Basin[J]. Environmental Science & Technology, 2011, 34(Suppl) : 102–106. |
| [18] | 赵海超, 王圣瑞, 焦立新, 等. 洱海上覆水不同形态氮时空分布特征[J]. 中国环境科学, 2013, 33(5) : 874–880. ZHAO Hai-chao, WANG Sheng-rui, JIAO Li-xin, et al. Space-time evolution trends of water nitrogen in Lake Erhai[J]. China Environmental Science, 2013, 33(5) : 874–880. |
| [19] | Zhang C, Wang L, Li G, et al. Grain size effect on multi-element concentrations in sediments from the intertidal flats of Bohai Bay, China[J]. Applied Geochemistry, 2002, 17(1) : 59–68. DOI:10.1016/S0883-2927(01)00079-8 |
| [20] | Smucker A J M, Park E J, Dorner J, et al. Soil micropore development and contributions to soluble carbon transport within Macroaggregates[J]. Vadose Zone Journal, 2007, 6(2) : 282–290. DOI:10.2136/vzj2007.0031 |
| [21] | 蒋小欣, 阮晓红, 邢雅囡, 等. 城市重污染河道上覆水氮营养盐浓度及DO水平对底质氮释放的影响[J]. 环境科学, 2007, 28(1) : 87–91. JIANG Xiao-xin, RUAN Xiao-hong, XING Ya-nan, et al. Effects of nutrient concentration and DO status of heavily polluted urban stream water on nitrogen release from sediment[J]. Environmental Science, 2007, 28(1) : 87–91. |
| [22] | Boatman C D, Murray J W. Modeling exchangeable NH4+ adsorption in marine sediments:Process and controls of adsorption[J]. Limnology & Oceanography, 1982, 27(1) : 99–110. |
| [23] | Hedges J I, Keil R G. Sedimentary organic matter preservation:An assessment and speculative synthesis[J]. Marine Chemistry, 1995, 49(2/3) : 81–115. |
| [24] | 陈建平, 李想, 王明玉, 等. 水稻田铁锰对氮素转化影响的实验研究[J]. 水资源与水工程学报, 2012, 23(1) : 106–108. CHEN Jian-ping, LI Xiang, WANG Ming-yu, et al. Experiment on effect of iron and manganese on nitrogen transformation in agri-ecosystem paddy field[J]. Journal of Water Resources & Water Engineering, 2012, 23(1) : 106–108. |
| [25] | 杨维, 王泳, 郭毓, 等. 地下水中铁锰对氮转化影响的实验研究[J]. 沈阳建筑大学学报(自然科学版), 2008, 24(2) : 286–290. YANG Wei, WANG Yong, GUO Yu, et al. Test about effect of iron and manganese on nitrogen transformation in underground water[J]. Journal of Shenyang Jianzhu University Natural Science, 2008, 24(2) : 286–290. |
 2017, Vol. 36
2017, Vol. 36