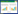文章信息
- 刘鸣达, 李彩, 赵玉婷, 应博, 杨丹, 何娜, 王耀晶
- LIU Ming-da, LI Cai, ZHAO Yu-ting, YING Bo, YANG Dan, HE Na, WANG Yao-jing
- 硅对不同pH水田土壤吸附-解吸镉的影响
- Effect of added silicon on adsorption-desorption characteristics of cadmium on paddy soil with different pH
- 农业环境科学学报, 2017, 36(4): 672-677
- Journal of Agro-Environment Science, 2017, 36(4): 672-677
- http://dx.doi.org/10.11654/jaes.2016-1548
文章历史
- 收稿日期: 2016-12-03
2. 沈阳农业大学理学院, 沈阳 110866;
3. 辽宁省环境监测实验中心, 沈阳 110161
2. College of Science, Shenyang Agricultural University, Shenyang 110866, China;
3. Liaoning Environmental Monitoring and Experiment Center, Shenyang 110161, China
镉是毒性最强的重金属之一, 它能在植物体中积累, 并通过食物链富集到动物体中。长期食用镉污染食物就会使镉蓄积, 由于人类寿命较长, 其对人的毒性远高于动植物[1-2]。近几十年来, 由于采矿、污灌、三废排放和肥料不合理施用, 我国农田土壤镉污染日趋严重。2011年《新世纪》周刊报道多地市场约10%大米镉超标, 引起了社会热议。2014年发布的全国土壤污染状况调查公报显示, 镉居耕地重金属污染的元素之首。因此研究镉在土壤-植物系统内的迁移、富集规律, 对于防治污染, 保障食品安全与人体健康具有重要意义。
有关硅抑制植物吸收镉或缓解镉胁迫的研究已有很多报道。从生物学角度来看, 施硅抑制了镉向植物地上部分转运, 降低了植株中镉的含量[3-5]; 有研究表明, 硅的沉积在一定程度上限制了镉的质外体运输[6-9]。此外, 硅能够激活植物的抗氧化系统, 也可以缓解镉的胁迫[10-14]。在土壤化学方面的相关机制研究相对较少, 普遍认为施硅提高了土壤的pH值, 使硅酸根与镉发生反应形成不易被吸收的硅酸盐沉淀, 从而抑制镉等的活性[15-17]; 也有学者认为施硅肥抑制小白菜吸收镉是其促进土壤吸附镉所致[18]; 陈怀满[19]则认为活性硅本身可能是抑制镉吸收的一个重要因素。因此, 含硅物质抑制作物吸收镉包括了提高土壤pH和硅的双重作用[20-22]。以往试验中加入的硅酸钠、硅酸钾、钢渣、硅肥等含硅物料均为碱性物质, 同时还引入了相应的伴随离子, 而钙、镁、钾、钠等元素均能抑制植物对镉的吸收转运[23]或影响镉的土壤化学行为。显然, 硅对土壤中镉活性的影响机制尚不清楚。为此, 本文在消除pH及伴随离子影响的基础上, 研究硅对土壤镉吸附-解吸特性的影响, 以期为揭示硅对土壤中镉的界面化学行为的影响机制提供理论依据。
1 材料与方法 1.1 供试土壤供试土壤均为种稻多年的水田土壤, 其中A采自辽宁省沈阳市康平县 (123°24´48.8″E, 42°56´00.1″N), B采自辽宁省抚顺市新宾县 (125°20´44.4″E, 41°34´9.1″N)。采样深度为0~20 cm, 样品经风干后去除水稻根茬残体和砾石, 过1 mm筛后备用。土壤的基本理化性质如表 1所示。
称取土壤1.25 g (烘干重) 若干份置于已知质量的50 mL塑料离心管中, 分别加入0、10、20、40、60、80、100 mg·L-1(以Cd2+计) 的CdCl2溶液和0、90、120 mg·L-1(以SiO2计) 的Na2SiO3溶液共25 mL, 用HNO3中和Na2SiO3的碱性, 以NaNO3补齐各处理间的离子差异, 保证支持电解质的浓度为0.01 mol·L-1 NaNO3。以上共21个不同硅镉组合, 每个处理3次重复。上述处理在25℃条件下振荡2 h (200 r·min-1), 接着培养24 h后离心5 min (4000 r·min-1), 取其中上清液测定镉的浓度, 残液和土样用于解吸试验。镉的吸附量计算公式如下:
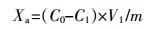 (1)
(1) 式中:Xa为土壤对镉的吸附量, mg·kg-1; C0为镉的初始浓度, mg·L-1; C1为镉的吸附平衡浓度, mg·L-1; V1为吸附反应溶液的体积, mL; m为土样质量, g。
1.2.2 解吸试验完成上述等温吸附试验后, 称含有残液和土样的离心管质量, 计算残液质量 (体积) 及其中镉含量。向离心管中加入0.01 mol·L-1 NaNO3溶液 (补足到先前的质量), 重复1.2.1的操作, 测定上清液中镉的浓度。镉的解吸量计算公式如下:
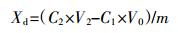 (2)
(2) 式中:Xd为土壤对镉的解吸量, mg·kg-1; C1为镉的吸附平衡浓度, mg·L-1; C2为镉的解吸平衡浓度; V2为解吸反应溶液的体积, mL; V0为残留液的体积, mL; m为土样质量, g。
离心管中残留液体积通过称重法求得, 假定溶液的密度为1 g·mL-1。
1.3 测定方法土壤pH值采用酸度计法进行测定[24]; 土壤有机质采用重铬酸钾-外加热法测定[24]; 碱性土壤阳离子交换量采用乙酸钠-火焰光度法测定, 酸性土壤阳离子交换量采用乙酸铵交换法测定[24]; 土壤有效硅采用1 mol·L-1醋酸-醋酸钠 (pH 4) 缓冲液提取, 硅钼蓝比色法测定[24]; 土壤全镉采用氢氟酸-硝酸消化[25], 消化液和吸附解吸平衡液中的镉用原子吸收分光光度计法测定; 土壤机械组成采用比重计法测定[24]。
1.4 数据分析试验数据采用Excel 2007进行统计分析。
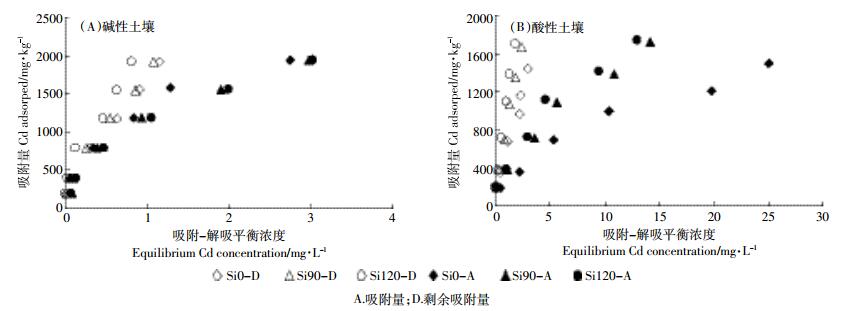
2 结果与分析 2.1 加硅后土壤镉的吸附-解吸特征不同硅浓度条件下2种土壤对镉的吸附-解吸等温线如图 1所示。总体来看, 无论酸性还是碱性土壤, 不同处理镉的吸附量均随其平衡浓度的增大而增加; 相同的平衡浓度下, 碱性土壤吸附镉的量高于酸性土壤。加硅改变了土壤吸附镉的特征; 与无硅处理相比, 碱性土壤对镉的吸附有所降低, 酸性土壤对镉的吸附有所增加, 其效应均随加硅量的增加而更趋明显。随着解吸平衡浓度的增加, 2种土壤的吸附量均逐渐增加; 同一平衡浓度下, 加硅量越高, 吸附量也越大, 说明无论是酸性还是碱性土壤, 加硅均导致土壤镉的解吸受到抑制。从图中还可以看出, 同一处理的解吸过程明显存在滞后现象。
|
| 图 1 不同硅水平下土壤对镉的吸附等温线 Figure 1 Adsorption-desorption isotherms of Cd by soils at different Si levels |
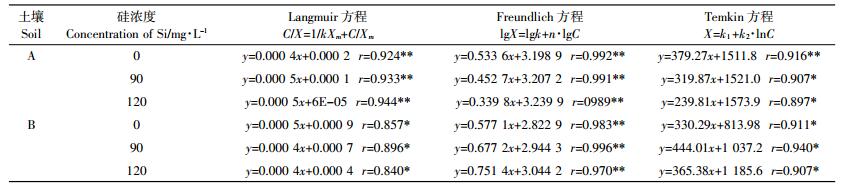
用不同的直线型吸附等温模型对吸附和解吸试验数据进行拟合, 得到的方程分别列于表 2和表 3。可以看出, 各处理3种方程的相关系数均达到统计学上的显著水平, 说明Langmuir、Freundlich、Temkin直线模型均可以较好地描述土壤吸附-解吸镉的特征。

|
|
考虑到硅酸具有复杂的聚合特性, 综合吸附、解吸直线模型相关系数的显著水平, 选用Freundlich直线模型讨论硅对土壤吸附-解吸镉特征的影响。将方程参数列于表 4, 其中:na和ka为吸附方程常数; nd和kd为解吸方程常数; k是与最大吸附量有关的常数, 其值越大则吸附容量越大; n是表征吸附强度的常数, 其值越大则土壤对离子的吸附能力越强。

|
由表 4可知, 与不加硅处理相比, 加硅使碱性土壤方程ka值变小、na值变大, 说明加硅可降低镉的吸附容量、增大吸附强度; 加硅使酸性土壤方程ka值变大、na值变小, 说明加硅可增大镉的吸附容量、降低吸附强度。上述效应随加硅量增加而趋于明显。k值和n值决定了吸附或解吸曲线的形状, 因此Δk=kd-ka和Δn=nd-na可反映吸附等温线与解吸等温线在横轴和纵轴方向的变化程度, 说明吸附-解吸反应的可逆性大小。通常将Δk+Δn称为滞后系数 (Hc, Hysteretic coefficient)[26], 滞后系数越大, 则吸附-解吸的可逆性愈小。计算求得两种土壤镉吸附-解吸的滞后系数列于表 4。可以看出, 加硅后2种土壤的滞后系数均增大, 说明加硅抑制了镉的解吸。这也能从解吸率的变化得到印证, 从表 5来看, 无论加硅与否, 随着镉浓度的增加解吸率逐渐升高; 但加硅降低了镉的解吸率, 且随着硅浓度的增加解吸率有所降低。
pH为影响土壤中镉活性的重要因素, 土壤pH越高, 镉活性越低。前人研究中使用的硅肥多是碱性物质, 施加后会使土壤pH升高, 因此其促进镉吸附的结果可能是由土壤pH升高所致。本试验是在调节吸附溶液pH的基础上进行的, 消除了硅酸钠的碱性对吸附的影响。结果表明, 加硅降低了碱性土壤对镉的吸附, 促进了酸性土壤对镉的吸附。这与前人的研究结果[27]相反。出现这种情况的原因可能是采用原子吸收光谱法测定平衡溶液中的镉浓度, 获得的是镉的总量, 而无法区分镉的存在形态。研究表明, 在中性或碱性条件下, 硅酸可与铜离子发生配位反应[28]。而镉与铜均为过渡金属中的ds区元素, 向碱性土壤中加入硅时可能同镉离子也发生了类似反应, 降低了土壤对镉的吸附。但这未必意味着镉毒害植物的风险会增大, 因为通常植物主要是以单硅酸的形式吸收硅[29], 可能并不吸收以配合物形态存在的镉。加硅促进酸性土壤吸附镉的机制可能是:在酸性条件下, 硅酸会聚合成硅凝胶, 且硅凝胶在一定pH范围内产生负电荷[30], 这相当于增加了土壤的负电荷表面, 从而促进镉的吸附。此外, 有研究表明, 加入的硅酸可与培养液中铝离子形成高分子硅酸铝复合物并产生沉淀[31]; 若硅酸与镉存在着类似反应, 也会导致可溶态镉浓度的降低。
Freundlich方程是一个经验公式, 形式简单、计算方便, 尽管方程参数的物理意义不甚明确, 不能说明吸附机理, 但在很多土壤吸附解吸现象的模拟中都获得了很好的应用效果。这可能是由于土壤颗粒组成和性状都具有非均一性, 导致其对物质的吸附不是理想的单层吸附。因硅酸具有复杂的聚合特性, 可能会形成直链、环链和双环等聚硅酸或缩聚物[32], 使得土壤加入硅酸后性状更为复杂, 多层吸附模型可能接近于土壤吸附-解吸镉的实际。因此, 以Freundlich方程描述不同硅浓度下2种土壤镉的吸附-解吸特征效果最佳。
通常认为, Freundlich方程中k是与吸附容量有关的常数, 其值越大则吸附容量越大; n是表征吸附强度的常数, 其值越大则土壤对离子的吸附能力越强。加硅使碱性土壤方程的k值变小、n值变大, 可能是硅酸与镉离子生成了可溶性配合物, 导致土壤表面物理吸附甚至离子交换吸附的镉比例降低, 相应的化学吸附的镉比例相对提高, 故而镉的吸附容量降低, 而吸附强度提高; 加硅使酸性土壤方程的k值变大、n值变小, 可能是由于硅酸会聚合成带有负电荷的硅凝胶, 增加了土壤的负电荷表面, 促进了镉的吸附。镉在硅凝胶表面的吸附可能多为表面物理吸附或离子交换吸附, 致使相应的化学吸附态镉的比例相对降低, 所以镉的吸附容量增大, 而吸附强度降低。
吸附解吸过程通常存在着滞后现象。滞后现象产生的原因可能是重金属元素在土壤中形成了内圈配合物[33], 或形成更难解吸的双核内圈配合物[34], 从而使其较难解吸; 还有可能是由于解吸试验过程中持续振荡, 造成土粒结构被破坏, 产生了新的吸附位点, 吸附已解吸的镉。滞后系数可用来描述解吸滞后现象, 滞后系数愈大, 吸附-解吸的可逆性愈差。加硅后滞后系数降低, 表明施硅后土壤镉吸附-解吸的可逆性降低, 镉的解吸量有所减少。这可能是当土壤溶液中硅浓度较高时, 过量的硅酸会发生聚合反应沉淀在土壤或铁、铝氧化物表面, 其结合能力强, 解吸困难[35]; 聚合反应生成的硅凝胶表面有大量的羟基[36], 可能会与镉离子进行配位交换, 形成氧与镉结合的双配体螯合物而难以解吸。此外, 当硅酸聚合成环状和双笼状聚合物时, 可将阳离子包络在环内或笼内, 形成能量较低、稳定性较高的配位化合物[32]。这也可能是硅抑制土壤镉解吸的机制之一。上述推论尚有待于深入研究加以证明。
4 结论(1) 以Freundlich方程描述不同硅浓度下2种土壤镉的吸附-解吸特征效果最佳, 说明多层吸附模型更接近于土壤吸附-解吸镉的实际。
(2) 加硅使碱性土壤方程的k值变小、n值变大, 降低了镉的吸附容量却增大了吸附强度; 酸性土壤方程的k值变大、n值变小, 增加了镉的吸附容量却降低了吸附强度。
(3)2种土壤镉的解吸量均随加硅量的增加而降低, 加硅后滞后系数 (Δk+Δn) 增大, 加剧了吸附-解吸过程中的滞后效应。
| [1] | Tudoreanu L, Phillips C J C. Modeling cadmium uptake and accumulation in plants[J]. Advances in Agronomy, 2004, 84: 121–157. DOI:10.1016/S0065-2113(04)84003-3 |
| [2] | Cheng W W L, Gobas F A P C. Assessment of human health risk of consumption of cadmium contaminated oysters[J]. Human and Ecological Risk Assessment, 2007, 13(2): 370–382. DOI:10.1080/10807030701226301 |
| [3] | 秦淑琴, 黄庆辉. 硅对水稻吸收镉的影响[J]. 新疆环境保护, 1997, 19(3): 51–52. QIN Shu-qin, HUANG Qing-hui. Effect of silicon on cadmium uptakes by rice[J]. Environmental Protection of Xinjiang, 1997, 19(3): 51–52. |
| [4] | 陈秀芳, 赵秀兰, 夏章菊, 等. 硅缓解小麦镉毒害的效应研究[J]. 西南农业大学学报 (自然科学版), 2005, 27(4): 447–450. CHEN Xiu-fang, ZHAO Xiu-lan, XIA Zhang-ju, et al. Alleviation of cadmium toxicity of wheat plants by silicon[J]. Journal of Southwest Agricultural University (Natural Science), 2005, 27(4): 447–450. |
| [5] | 杨超光, 豆虎, 梁永超, 等. 硅对土壤外源镉活性和玉米吸收镉的影响[J]. 中国农业科学, 2005, 38(1): 116–121. YANG Chao-guang, DOU Hu, LIANG Yong-chao, et al. Influence of silicon on cadmium availability and cadmium uptake by maize in cadmium-contaminated soil[J]. Scientia Agricultura Sinia, 2005, 38(1): 116–121. |
| [6] | Shi X H, Zhang C C, Wang H, et al. Effect of Si on the distribution of Cd in rice seedlings[J]. Plant and Soil, 2005, 272(1/2): 53–60. |
| [7] | Zhang C C, Wang L J, Nie Q, et al. Long-term effects of exogenous silicon on cadmium translocation and toxicity in rice (Oryza sativa L.)[J]. Environmental and Experimental Botany, 2008, 62(3): 300–307. DOI:10.1016/j.envexpbot.2007.10.024 |
| [8] | Ye J, Yan C L, Liu J C, et al. Effects of silicon on the distribution of cadmium compartmentation in root tips of Kandelia obovata (S., L.) Yong[J]. Environmental Pollution, 2011, 162: 369–373. |
| [9] | da Cunha K P V, do Nascimento C W A, da Silva A J. Silicon alleviates the toxicity of cadmium and zinc for maize (Zea mays L.) grown on contaminated soil[J]. Journal of Plant Nutrition and Soil Science, 2008, 171(6): 849–853. DOI:10.1002/jpln.v171:6 |
| [10] | Chika C N, Alfredo J H. Effects of silicon nutrition on cadmium uptake, growth and photosynthesis of rice plants exposed to low-level cadmium[J]. Plant and Soil, 2008a, 311(1/2): 73–86. |
| [11] | Chika C N, Alfredo J H. Silicon-induced cadmium resistance in rice (Oryza sativa L.)[J]. Journal of Plant Nutrition and Soil Science, 2008, 171(6): 841–848. DOI:10.1002/jpln.v171:6 |
| [12] | Feng J P, Shi Q H, Wang X F, et al. Silicon supplementation ameliorated the inhibition of photosynthesis and nitrate metabolism by cadmium (Cd) toxicity in Cucumis sativus L.[J]. Scientia Horticulture, 2009, 123(4): 521–530. |
| [13] | 刘鸣达, 王丽丽, 李艳利. 镉胁迫下硅对水稻生物量及生理特性的影响[J]. 中国农学通报, 2010, 26(13): 187–190. LIU Ming-da, WANG Li-li, LI Yan-li. Effect of Si on biomass and physiological characteristics of rice under Cd stress[J]. Chinese Agricultural Science Bulletin, 2010, 26(13): 187–190. |
| [14] | 王耀晶, 付田霞, 苏瑛, 等. 镉胁迫下硅对草莓生长及生理特性的影响[J]. 农业环境科学学报, 2012, 31(12): 2335–2339. WANG Yao-jing, FU Tian-xia, SU Ying, et al. Effect of silicon on growth and physiological characteristics of strawberry (Fragaria ananassa Duch.) under cadmium stress[J]. Journal of Agro-Enviroment Science, 2012, 31(12): 2335–2339. |
| [15] | 蔡德龙, 陈常友, 小林均. 硅肥对水稻镉吸收影响初探[J]. 地域研究与开发, 2000, 19(4): 69–71. CAI De-long, CHEN Chang-you, XIAO Lin-jun. The influence of the silicon fertilizer on the Cd adsorption by paddy[J]. Areal Research and Development, 2000, 19(4): 69–71. |
| [16] | Neumann D, Zur Nieden U. Silicon and heavy metal tolerance of higher plants[J]. Phytochemistry, 2001, 56(7): 685–692. DOI:10.1016/S0031-9422(00)00472-6 |
| [17] | Li P, Wang X X, Zhang T L, et al. Distribution and accumulation of copper and cadmium in soil-rice system as affected by soil amendments[J]. Water, Air & Soil Pollution, 2009, 196(1/2/3/4): 29–40. |
| [18] | 陈晓婷, 王果, 梁志超, 等. 钙镁磷肥和硅肥对Cd、Pb、Zn污染土壤上小白菜生长和元素吸收的影响[J]. 福建农林大学学报 (自然科学版), 2002, 31(1): 109–112. CHEN Xiao-ting, WANG Guo, LIANG Zhi-chao, et al. Effect of calcium magnesium phosphate and silicon fertilizer on the growth and element uptake of pakchoi in cadmium, lead and zinc contaminated soil[J]. Journal of Fujian Agriculture and Forestry University (Natural Science), 2002, 31(1): 109–112. |
| [19] | 陈怀满. 土壤植物系统的重金属污染[M]. 北京: 科学出版社, 1996: 115-125. CHEN Huai-man. Heavy metal pollution in soil-plant system[M]. Beijing: Science Press, 1996: 115-125. |
| [20] | Liang Y C, Wong J W C, Wei L. Silicon-mediated enhancement of cadmium tolerance in maize (Zea mays L.) grown in cadmium contaminated soil[J]. Chemosphere, 2005, 58(4): 475–483. DOI:10.1016/j.chemosphere.2004.09.034 |
| [21] | Zhao X L, Saigusa M. Amelioration of cadmium polluted paddy soils by porous hydrated calcium silicate[J]. Water, Air & Soil Pollution, 2007, 183(1/2/3/4): 309–315. |
| [22] | Rizwan M, Meunier J D, Miche H, et al. Effect of silicon on reducing cadmium toxicity in durum wheat (Triticum turgidum L.cv.Claudio W.) grown in a soil with aged contamination[J]. Journal of Hazardous Materials, 2012(209/210): 326–334. |
| [23] | 周卫, 汪洪, 李春花, 等. 添加碳酸钙对土壤中镉形态转化与玉米叶片镉组分的影响[J]. 土壤学报, 2001, 38(2): 219–225. ZHOU Wei, WANG Hong, LI Chun-hua, et al. Effect of calcium carbonate addition on transformation of cadmium species in soil and cadmium in leaves of maize[J]. Acta Pedologica Sinica, 2001, 38(2): 219–225. DOI:10.11766/trxb199909140210 |
| [24] | 劳家柽. 土壤农化分析手册[M]. 北京: 农业出版社, 1988. LAO Jia-cheng. Soil agricultural chemistry analysis[M]. Beijing: Agriculture Press, 1988. |
| [25] | 刘雷, 杨帆, 刘足根, 等. 微波消解ICP-AES法测定土壤及植物中的重金属[J]. 环境化学, 2008, 27(4): 511–514. LIU Lei, YANG Fan, LIU Zu-gen, et al. Determination of heavy metal in soils and plants with microwave digestion and ICP-AES[J]. Environment Chemistry, 2008, 27(4): 511–514. |
| [26] | 朱端卫, 皮美美, 刘武定. 硼在土壤中的吸附-解吸及其对植物吸收硼的影响[J]. 土壤学报, 1998, 35(1): 70–75. ZHU Duan-wei, PI Mei-mei, LIU Wu-ding. Adsorption-desorption of boron in soils its effect on boron uptake of plant[J]. Acta Pedologica Sinica, 1998, 35(1): 70–75. DOI:10.11766/trxb199603080110 |
| [27] | 赵昕欣, 李军, 刘洋, 等. 钢渣对辽宁地区水稻土壤镉素吸收的影响[J]. 中国农学通报, 2006, 22(7): 507–511. ZHAO Xin-xin, LI Jun, LIU Yang, et al. The effect of slag mucks on paddy soil absorbed in Liaoning area[J]. Chinese Agricultural Science Bulletin, 2006, 22(7): 507–511. |
| [28] | 李瑞延, 王金晞, 郭腊梅, 等. Cu2+与硅酸、硅胶表面硅羟基的反应及其平衡常数[J]. 无机化学学报, 1996, 12(1): 50–54. LI Rui-yan, WANG Jin-xi, GUO La-mei, et al. Reaction of Cu2+ with silicic acid and surface silanol groups and their equilibrium constants[J]. Journal of Inorganic Chemistry, 1996, 12(1): 50–54. |
| [29] | Takahashi E, Hino K. Silica uptake by rice plant with special reference to the forms of dissolved silica[J]. Journal of the Science of Soil and Manure Japan, 1978, 49: 357–360. |
| [30] | 袁可能. 土壤化学[M]. 北京: 农业出版社, 1990. YUAN Ke-neng. Soil chemistry[M]. Beijing: Agriculture Press, 1990. |
| [31] | 顾明华, 黎晓峰. 硅对减轻水稻的铝胁迫效应及其机理研究[J]. 植物营养与肥料学报, 2002, 8(3): 360–366. GU Ming-hua, LI Xiao-feng. Effect of silicon on alleviation of aluminum toxicity and corresponded mechanisms in rice[J]. Plant Nutrition and Fertilizer Science, 2002, 8(3): 360–366. DOI:10.11674/zwyf.2002.0319 |
| [32] | 卢晨, 季敦生, 朱纯熙, 等. 水玻璃的基本组成及定量测定[J]. 上海交通大学学报, 1997, 31(9): 86–89. LU Chen, JI Dun-sheng, ZHU Chun-xi, et al. Determination and research on constituents of water glass[J]. Journal of Shanghai Jiaotong University, 1997, 31(9): 86–89. |
| [33] | Roe A L, Hayes K F, Chisholm-Brause C. In-situ X-ray absorption study of lead ion surface complexes at the goethite water interface[J]. Langmuir, 1991, 7(2): 367–373. DOI:10.1021/la00050a029 |
| [34] | Rouff A A, Elzinga E J, Reeder R J, et al. X-ray absorption spectroscopic evidence for the formation of Pb (Ⅱ) inner-sphere adsorption complexes and precipitates at the calcite-water interface[J]. Environmental Science & Technology, 2004, 38(6): 1700–1707. |
| [35] | 高明, 魏朝富, 陈世正, 等. 紫色水稻土对硅酸盐的吸附与解吸特性研究[J]. 土壤通报, 1998, 29(4): 179–181. GAO Ming, WEI Chao-fu, CHEN Shi-zheng, et al. Characteristics of silicate adsorption and desorption in purple paddy soil[J]. Chinese Journal of Soil Science, 1998, 29(4): 179–181. |
| [36] | 戴安邦, 江龙. 硅酸及其盐的研究Ⅰ.硅酸聚合的速度和机制[J]. 化学学报, 1957, 2: 90–98. DAI An-bang, JIANG Long. Studies on silicic acid and its salts:Ⅰ.Rate of gelation and mechanism of polymerization of silicic acid[J]. Acta Chimica Sinica, 1957, 2: 90–98. |
 2017, Vol. 36
2017, Vol. 36