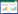文章信息
- 王立果, 钟金魁, 赵保卫, 张建宇, 李柳, 杨巧珍, 陈伟仡
- WANG Li-guo, ZHONG Jin-kui, ZHAO Bao-wei, ZHANG Jian-yu, LI Liu, YANG Qiao-zhen, CHEN Wei-yi
- 水中镉和芘在核桃壳生物炭上的吸附行为及其交互作用
- Adsorption and interaction of Cd(Ⅱ) and pyrene in water on walnut shell biochar
- 农业环境科学学报, 2017, 36(9): 1868-1876
- Journal of Agro-Environment Science, 2017, 36(9): 1868-1876
- http://dx.doi.org/10.11654/jaes.2017-0217
文章历史
- 收稿日期: 2017-02-24
重金属和多环芳烃是水体中存在的两类主要污染物质,它们通过矿山开采、化石燃料燃烧、工业废水排放等方式进入水体,对水体造成严重的污染[1-2],其“三致”效应和毒性威胁人类的健康和生态系统的安全。在众多去除方法中,吸附法以其去除污染物种类多、操作简单且无二次污染等优点被广泛关注[3]。生物炭作为一种很好的吸附材料,因其来源广泛、成本低、去除效率高、环境稳定性好[4],能够吸附固定水中的重金属[5]和多环芳烃[6],而受到广大学者的关注。
目前利用生物炭对水体中重金属或多环芳烃吸附的研究大多集中在单一污染方面,如Chen等[1]和Kim等[7]分别研究了城市污水厂污泥生物炭和芒草生物炭对镉的吸附特性,谢超然等[8]研究了核桃青皮生物炭对重金属铅、铜的吸附特性,吴晴雯等[9]研究了芦苇秸秆生物炭对水中菲的吸附特性,史兵方等[10]研究了麻疯树籽壳生物质炭对水体中PAHs的吸附性能,而对重金属和多环芳烃复合污染的吸附研究鲜见报道。作为水体中两种典型的污染物,重金属和多环芳烃往往不是以单一污染的状态存在,而是以复合污染的形式被同时发现[11]。事实上,水体中并不存在绝对的单一污染,复合污染更能反映水体污染的真实情况[12]。另外,生物炭吸附水体中重金属和多环芳烃时可能存在交互作用,其机理无法用吸附单一污染的机理解释[13],这种交互作用可能影响重金属和多环芳烃的迁移转化,对生物炭修复重金属和多环芳烃复合污染水体有着重要的作用。因此,研究生物炭吸附重金属和多环芳烃复合污染的交互作用,对重金属和多环芳烃复合污染水体的修复有重要的意义。我国是核桃种植大国,每年有大量的核桃壳作为农业废弃物或者燃料烧掉,造成很大的浪费。用核桃壳制备生物炭,不仅可以减少资源浪费,还可以防止环境污染。
实验以核桃壳为原料制备生物炭,利用扫描电子显微镜(SEM)和傅立叶变换红外光谱仪(FTIR)对样品进行表征分析,研究了核桃壳生物炭对水中重金属和多环芳烃的典型代表——Cd(Ⅱ)和芘的吸附特性,考察了吸附时间、初始浓度、pH值、生物炭粒径对吸附的影响,以及Cd(Ⅱ)和芘在核桃壳生物炭上的交互作用,为重金属和多环芳烃复合污染水体的生物炭修复提供了理论参考。
1 材料与方法 1.1 材料与仪器选用新疆和田核桃壳为原料,用蒸馏水清洗干净,置于烘箱中在85 ℃条件下烘干,粉碎过40目筛后装入瓷坩埚,置于马弗炉中于600 ℃下厌氧炭化5 h,待冷却后取出,用1 mol·L-1的盐酸洗5次,去除灰分,再用去离子水洗至中性,在烘箱中85 ℃烘干后分别过40、60、80目筛制得核桃壳生物炭,分别标记为WSBC40、WSBC60、WSBC80。
芘(98%,北京百灵威科技有限公司);硝酸镉(分析纯,天津市大茂化学试剂厂);气浴恒温振荡器(THZ-82型,金坛市丹阳门石英玻璃厂);马弗炉(SX2系列,上海跃进医疗器械厂);电热恒温干燥箱(202-2型,北京科伟永兴仪器有限公司);火焰原子分光光度仪(SpectrumAA110/220型,美国瓦里安);紫外分光光度计(UV-180型,上海美普达仪器有限公司);SEM(Hitachi S-4800,日本日立公司);FTIR光谱仪(Bruker VERTEX 70v,德国布鲁克)。
1.2 生物炭结构表征利用场发射扫描电子显微镜(SEM)观察WS-BC60颗粒外观形貌结构;利用FTIR光谱仪KBr压片法扫描生物炭,分析WSBC60表面官能团,扫描波长范围400~4000 cm-1。
1.3 批吸附实验准确称取0.1 g WSBC,加入到50 mL碘量瓶中,在25 ℃、150 r·min-1条件下,将装有溶液[芘或Cd(Ⅱ)]和WSBC的碘量瓶置于气浴恒温振荡器中振荡,反应结束后,将悬浮液过0.45 μm滤膜,分别采用火焰原子分光光度仪(波长228.8 nm,光谱带宽0.2 nm,灯电流4.0 mA,燃烧器高度7.5 mm,燃气流量1.4 L·min-1,空气流量6.0 L·min-1)和紫外分光光度计(波长254 nm)测定溶液中Cd(Ⅱ)和芘的浓度。
1.3.1 吸附动力学实验在50 mL碘量瓶中加入浓度为200 mg·L-1的Cd(Ⅱ)溶液或5 mg·L-1的芘溶液20 mL,吸附时间设为10、20、30、40、60、120、240、360、480、720、960、1200、1440 min。
1.3.2 等温吸附实验在50 mL碘量瓶中加入浓度为100、150、200、250、300、400、500 mg·L-1的Cd(Ⅱ)溶液或浓度为0.1、0.5、1、2、3、5、7 mg·L-1的芘溶液20 mL,吸附20 h和16 h后分别测定溶液中Cd(Ⅱ)或芘的浓度。
1.3.3 pH影响实验在50 mL碘量瓶中加入浓度为200 mg·L-1的Cd(Ⅱ)溶液(1 mol·L-1的NaOH和HNO3调节pH值)或5 mg·L-1的芘溶液(1 mol·L-1的NaOH和HCl调节pH值)20 mL,pH分别设为1、3、5、7、9或3、5、7、9、11,吸附20 h和16 h后分别测定溶液中Cd(Ⅱ)或芘浓度。
1.3.4 粒径影响实验在50 mL碘量瓶中加入100、150、200、250、300 mg·L-1的Cd(Ⅱ)溶液或浓度为0.1、0.5、1、3、5 mg·L-1的芘溶液20 mL,分别投加0.1 g的WSBC40、WSBC60、WSBC80,吸附20 h和16 h后测定溶液中Cd(Ⅱ)或芘的浓度。
1.3.5 Cd(Ⅱ)和芘交互作用实验Cd(Ⅱ)对芘吸附影响实验,在50 mL碘量瓶中加入浓度为0.1、0.5、1、2、3、5、7 mg·L-1的芘溶液10 mL,再加入400 mg·L-1的Cd(Ⅱ)溶液10 mL,吸附20 h后测定溶液中芘浓度;芘对Cd(Ⅱ)吸附影响实验,先在50 mL碘量瓶中加入100、150、200、250、300、400、500 mg·L-1的Cd(Ⅱ)溶液10 mL,再加入2 mg·L-1的芘溶液10 mL,吸附20 h后测定溶液中Cd(Ⅱ)浓度。
1.4 数据分析方法实验均设置3个平行样,取平均值作为测定结果,用OriginPro 2016和Microsoft Excel 2013软件进行数据处理。
核桃壳生物炭对Cd(Ⅱ)和芘的吸附量Qe按下式计算:
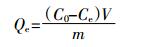
式中:Qe为单位质量生物炭对Cd(Ⅱ)或芘的吸附量,mg·g-1;V为溶液体积,mL;C0和Ce分别为溶液中Cd(Ⅱ)或芘的初始浓度和平衡浓度,mg·L-1;m为投加生物炭的质量,g。
2 结果与讨论 2.1 生物炭的表征 2.1.1 扫描电镜分析扫描电镜能够直观地反映物质的微观形貌、形态,通常用于样品结构分析。WSBC60的电镜扫描结果如图 1所示。在2000倍下可以清晰地看到WSBC60结构较紧密,表面粗糙且褶皱较多,分布着大小不等的孔隙;随着放大倍数增大(2.00、2.50、5.00、10.0 k倍数),可以明显看到WSBC60表面凹凸不平,孔隙结构明显。由此可知WSBC60炭化受热时,大量能量从孔道内部瞬间释放出来,冲开WSBC60内部孔道,增大了生物炭的粗糙程度,有利于WSBC60的吸附。

|
| 图 1 WSBC60样品扫描电镜图 Figure 1 SEM images of WSBC60 samples |
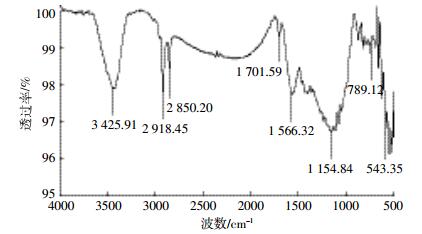
傅里叶红外光谱分析法主要用于判定WSBC60官能团的存在及物质结构变化,WSBC60红外光谱图如图 2所示。位于3 425.91 cm-1处的吸收峰为羟基-OH振动产生,2 918.45 cm-1附近为脂肪族CH2的吸收峰[14],1 701.59 cm-1处为芳香酸类-COO振动峰[8],1 566.32 cm-1处的峰为环状结构中的C=C和羰基中的C=O伸缩振动引起,1 154.84 cm-1附近的峰则由C-O伸缩振动引起,789.12 cm-1处的峰由苯环上C-H的面外弯曲振动引起[9],543.35 cm-1处的峰由吡啶、呋喃等杂环振动产生[14]。上述分析表明,WSBC60表面含有羟基、羧基、羰基等含氧官能团,并且具有高度芳香和杂环化的结构。这些含氧官能团具有重金属离子活性,在结合Cd(Ⅱ)的过程中起着重要作用,而高度芳香和杂环化的结构,在吸附芘时和芘中的苯环形成π-π作用,对芘的吸附作用很大。
|
| 图 2 WSBC60样品红外谱图 Figure 2 FTIR spectrum of WSBC60 samples |
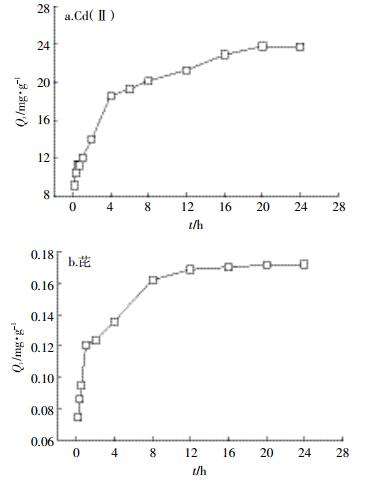
WSBC60对Cd(Ⅱ)和芘的吸附量随时间变化见图 3。整个吸附过程分为快速和慢速两个阶段[15],吸附开始时速率较快,4 h时Cd(Ⅱ)和芘的吸附量分别为18.58、0.14 mg·g-1,达到最大吸附量的78.09%和78.93%;4 h后吸附速率变慢,20 h时Cd(Ⅱ)达到最大吸附量,且基本达到吸附平衡,而芘在16 h后吸附量变化不再明显,认为达到吸附平衡。其原因是开始时WSBC60的孔隙通道及表面官能团吸附位点数量充足,Cd(Ⅱ)和芘容易被吸附,随着反应的进行,WSBC60的表面吸附位点减少,吸附量增加缓慢[8],最后趋于吸附平衡[10, 16]。
|
| 图 3 吸附时间对Cd(Ⅱ)和芘吸附的影响 Figure 3 Effect of contact time on the absorption of Cd (Ⅱ)and pyrene by WSBC60 |
为进一步探究WSBC60对Cd(Ⅱ)和芘的吸附机理,用准一级动力学、准二级动力学、颗粒内扩散方程拟合实验数据,相关拟合参数见表 1。

|
准一级动力学方程: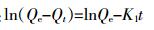
准二级动力学方程: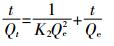
颗粒内扩散方程: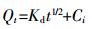
式中:t为吸附时间,h;Qt为t时生物炭对Cd(Ⅱ)或芘的吸附量,mg·g-1;Qe为吸附平衡时生物炭对Cd(Ⅱ)或芘的吸附量,mg·g-1;K1为准一级动力学反应速率常数,h-1;K2为二级动力学反应速率常数,g·mg-1·h-1;Kd为颗粒内扩散动力学速率常数,mg·g-1·h-1/2;Ci为截距常数,反映边界层效应,mg·g-1。
由表 1中的动力学参数可知,准二级动力学方程拟合所得的Cd(Ⅱ)和芘的R2均大于准一级动力学方程,同时其拟合所得的Cd(Ⅱ)和芘的平衡吸附量分别为24.35、0.18 mg·g-1,与实验所测得的平衡吸附量Cd(Ⅱ)23.79 mg·g-1和芘0.17 mg·g-1非常接近,说明准二级动力学方程能更好地描述WSBC60对Cd(Ⅱ)和芘的吸附行为,表明该吸附过程速率的控制步骤为化学反应[10, 14]。这个控速步骤主要是Cd(Ⅱ)和芘从水溶液中扩散到WSBC60表面(膜扩散),以及扩散到WSBC60的孔隙内(颗粒内扩散)和通过吸附作用吸附到WSBC60孔隙内表面(吸附作用),或者这三者之间的任意组合[17]。
Cd(Ⅱ)和芘颗粒内扩散方程拟合所得相关参数见表 1。WSBC60对Cd(Ⅱ)和芘吸附的颗粒内扩散过程分为两个阶段[18],第一阶段为膜扩散过程,Cd(Ⅱ)和芘扩散到WSBC60表面,第二阶段为内扩散过程,Cd(Ⅱ)和芘扩散到WSBC60孔隙内。根据表 1的数据可知,Cd(Ⅱ)和芘的扩散速率常数Kd1>Kd2,边界层C1 < C2,说明第一阶段Cd(Ⅱ)和芘扩散到WSBC60表面的速率较快,第二阶段扩散到WSBC60孔隙内的速率较慢[19]。这是由于随着吸附的进行,Cd(Ⅱ)和芘的浓度降低,WSBC60吸附趋于饱和,Cd(Ⅱ)和芘的扩散阻力增加,导致扩散速率降低,所以第二阶段的速率比第一阶段的小[20]。由颗粒内扩散理论可知,拟合直线通过原点,则颗粒内扩散是速率控制步骤;若直线不通过原点,速率控制步骤由颗粒内扩散和其他过程共同控制。由表 1可知,C1、C2都不为0,说明拟合所得的直线不经过原点,WSBC60对Cd(Ⅱ)和芘的吸附速率由表面吸附和颗粒内扩散共同控制,且颗粒内扩散是主要的控速步骤[21]。
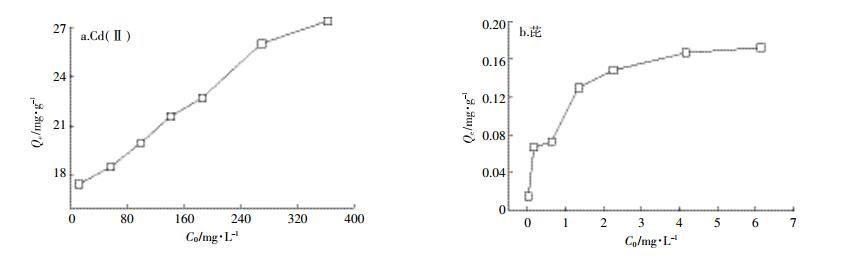
2.3 等温吸附模型分析WSBC60对Cd(Ⅱ)和芘的等温吸附曲线见图 4。随着Cd(Ⅱ)和芘的初始浓度增加,WSBC60对Cd(Ⅱ)和芘的吸附量增大,说明增大初始浓度有利于WSBC60对Cd(Ⅱ)和芘的吸附,初始浓度增加量是吸附发生的驱动力,能够克服水溶液与WSBC60之间的转移阻力,另外较大的初始浓度增大了WSBC60与Cd(Ⅱ)和芘接触概率,从而使WSBC60对Cd(Ⅱ)和芘吸附量增加[22];但并不是初始浓度越高越好,Cd(Ⅱ)在初始浓度大于300 mg·L-1和芘在初始浓度大于3 mg·L-1后,WSBC60对二者的吸附量增加趋于平缓,且芘逐渐达到吸附平衡。
|
| 图 4 Cd(Ⅱ)和芘初始浓度对吸附的影响 Figure 4 Isotherms parameters of Cd (Ⅱ)and pyrene absorption on biochar |
为进一步探究等温吸附机理,用Langmuir和Freundlich等温吸附模型[23]拟合WSBC60对Cd(Ⅱ)和芘的等温吸附实验数据,相关参数见表 2。
Langmuir等温吸附方程: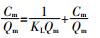
Freundlich等温吸附方程: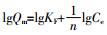
式中:Ce为平衡时溶液中Cd(Ⅱ)或芘的浓度,mg·L-1;Qe为平衡时生物炭对Cd(Ⅱ)或芘的吸附量,mg·g-1;Qm为生物炭对Cd(Ⅱ)或芘的最大吸附量,mg·g-1;KL为Langmuir等温方程常数,L·mg-1;KF、1/n为Freundlich等温方程常数,L·mg-1。
由表 2可知,Langmuir等温吸附方程中Cd(Ⅱ)和芘的R2均大于Freundlich等温吸附方程,同时其拟合所得的最大吸附量Cd(Ⅱ)=28.41 mg·g-1和芘=0.18 mg·g-1与实验所得的最大吸附量Cd(Ⅱ)=28.86 mg·g-1和芘=0.18 mg·g-1非常接近或相同,说明Langmuir等温吸附模型能更好地描述WSB60对Cd(Ⅱ)和芘的等温吸附特性[3, 9]。
通过Langmuir等温吸附方程平衡参数RL[24](也称分离因子),可以判断吸附剂对吸附质的亲和程度,其值受吸附质初始浓度影响,公式如下:
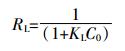
当0 < RL < 1有利于吸附;RL>1不利于吸附;RL=1为线性关系;RL趋于0为不可逆吸附。从表 2可知,WSBC60对Cd(Ⅱ)和芘的平衡参数RL介于0~1之间,说明WSBC60有利于Cd(Ⅱ)和芘的吸附[24]。
2.4 pH对吸附的影响从图 5a可以看出,随着溶液初始pH的增加,WSBC60对Cd(Ⅱ)的吸附量呈现增大的趋势,pH为1~3时吸附量增加相对缓慢;pH在3~5时吸附量增加最快,从5.44 mg·g-1增至20.54 mg·g-1;pH为5~7时趋于稳定,吸附量变化不大。其原因可能是水溶液pH较低时存在着大量H+,直径较小的H+与Cd(Ⅱ)在生物炭表面产生竞争吸附,占据了大量吸附点位[16],同时阻碍WSBC60表面活性官能团的离解,降低Cd(Ⅱ)与WSBC60表面活性官能团的络合反应[25],此时溶液pH < pHpzc 4.72,WSBC60表面带正电,与溶液中的Cd(Ⅱ)相互排斥,Cd(Ⅱ)不易被吸附,所以吸附量也较低[14];随着pH升高,溶液中OH-浓度增大,溶液中pH>pHpzc 4.72,OH-与WSBC60表面H+结合,溶液中H+浓度降低,竞争吸附减弱,WSBC60表面带负电的吸附位点增多,WSBC60对Cd(Ⅱ)吸附量增加[26]。pH大于7时,Cd(Ⅱ)会与大量的OH-发生沉淀反应生成CdOH+和Cd(OH)2,此时所得的吸附量不全是WSBC60吸附作用下的结果,沉淀反应是Cd(Ⅱ)去除的主要因素[27]。综上所述,pH=5时WSBC60对Cd(Ⅱ)的吸附效果最好。

|
| 图 5 pH对WSB60吸附Cd(Ⅱ)和芘的影响 Figure 5 Effect of pH on the absorption of Cd (Ⅱ) and pyrene by WSBC60 |
从图 5b可以看出,随着溶液初始pH的增加,WSBC60对芘的吸附呈现减小的趋势,在pH为7~9时下降速率最快,从0.11 mg·g-1下降到0.085 mg·g-1,说明溶液的初始pH值越低越有利于WSBC60对芘的吸附。其原因可能是开始时WSBC60对芘主要是表面吸附,通过范德华引力和芘与WSBC60之间的化学作用吸附,范德华引力是分子之间普遍存在的相互作用力,而化学作用主要是芘中的苯环和WSBC60上类似的芳香化表面形成π-π作用,芘作为π电子供体,WSBC60上的官能团作为电子受体[28]。pH较低时WSBC60表面的部分功能基团作为π电子受体质子化,增加了WSBC60表面接收π电子的吸附位点,所以pH值较低时WSBC60对芘的吸附量较大[13]。
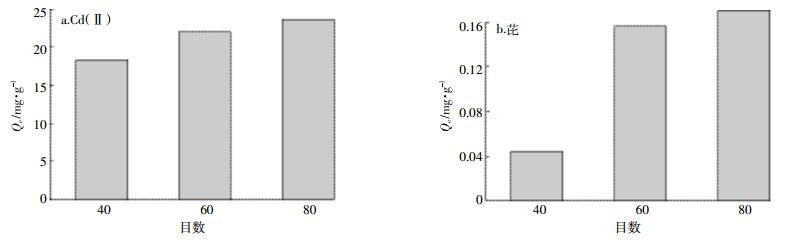
2.5 粒径对吸附的影响WSBC对Cd(Ⅱ)和芘吸附量随粒径变化见图 6。随着粒径的减小,WSBC对Cd(Ⅱ)和芘的吸附量增加。图 6a在Cd(Ⅱ)的初始浓度为300 mg·L-1时,WSBC粒径从40目减小到80目,WSBC对Cd(Ⅱ)的吸附量从18.40 mg·g-1增加到23.65 mg·g-1;图 6b在芘的初始浓度为5 mg·L-1时,WSBC粒径从40目减小到80目,WSBC对芘的吸附量从0.04 mg·g-1增加到0.17 mg·g-1。究其原因,基质对Cd(Ⅱ)和芘的吸附和比表面积大小有关,粒径小的WSBC比表面积更大,对Cd(Ⅱ)和芘的吸附能力也更强,所以粒径越小的生物炭吸附效果越好[29]。
|
| 图 6 粒径对WSBC吸附Cd(Ⅱ)和芘的影响 Figure 6 Effect of particle size on the absorption of Cd (Ⅱ) and pyrene by WSBC |
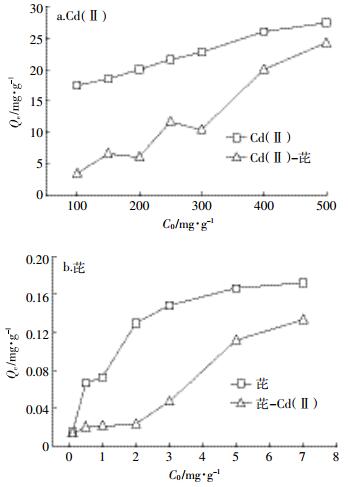
单一和混合体系WSBC60对Cd(Ⅱ)和芘吸附量随初始浓度变化情况如图 7。在单一和混合体系下,WSBC60对Cd(Ⅱ)和芘的吸附量随初始浓度增大而增大,混合体系下的吸附量明显低于单一体系,并随着初始浓度增加,差距逐渐减小。图 7a为WSBC60对单一和混合体下Cd(Ⅱ)的吸附,混合体系下加入芘之后,WSBC60对Cd(Ⅱ)的吸附量在Cd(Ⅱ)初始浓度较低时影响较大,在Cd(Ⅱ)初始浓度较高时影响较小。如Cd(Ⅱ)在低浓度100 mg·L-1时,单一吸附量为17.46 mg·g-1,混合吸附量为3.46 mg·g-1,两者相差80.18%;Cd(Ⅱ)在高浓度500 mg·L-1时,单一吸附量为27.38 mg·g-1,混合吸附量为24.22 mg·g-1,两者相差11.54%。图 7b为WSBC60对单一和混合体系下芘的吸附,混合体系下加入Cd(Ⅱ)之后,WSBC60对芘的吸附量在芘初始浓度较低时影响较小,随着芘初始浓度增加,影响逐渐增大,在芘高浓度时影响又变小。如芘初始浓度在0.1 mg·L-1时,单一吸附量为0.015 mg·g-1,复合吸附量为0.014 mg·g-1,两者相差6.67%;芘初始浓度在2 mg·L-1时,单一吸附量为0.13 mg·g-1,混合吸附量为0.024 mg·g-1,两者相差81.54%;芘初始浓度在7 mg·L-1时,单一吸附量是0.17 mg·g-1,复合吸附量是0.13 mg·g-1,两者相差23.53%。
|
| 图 7 Cd(Ⅱ)和芘单一和混合体系下的等温吸附 Figure 7 Isotherm adsorption of Cd (Ⅱ) and pyrene under the single and mixed system |
为进一步探究Cd(Ⅱ)和芘的交互作用,取Cd(Ⅱ)和芘在单一和复合体系下的平衡吸附量之和为100,分别计算Cd(Ⅱ)和芘在单一和混合状态下平衡吸附量所占的百分数,以此作为指标衡量混合条件下对Cd(Ⅱ)和芘吸附的影响[30],具体参数见表 3。单一体系中Cd(Ⅱ)和芘的吸附率明显大于50%,而在混合体系中,该指标大部分远小于50%;Cd(Ⅱ)和芘在单一体系中均值接近70%,在混合体系中均值在30%左右。从而说明,Cd(Ⅱ)和芘之间存在明显的交互作用,混合体系中会抑制对方在WSBC60上的吸附。这与Kong等[31]的研究结果相同。

|
根据实验结果,Cd(Ⅱ)和芘在混合体系中都会抑制对方的吸附,原因可能与WSBC60及Cd(Ⅱ)和芘自身的性质有关,高温下制得的WSBC60通常有更大的微孔数量和比表面积[32],很高的芳香程度,吸附时表面吸附大于分配作用[29];而芘是一种非极性的有机物,WSBC60对芘的吸附由疏水作用支配,在芘浓度较低时表面吸附的贡献大于分配作用,吸附作用主要是表面吸附,在高浓度时分配作用的贡献更高一些,此时以分配作用为主[33];表面吸附主要是通过疏水作用为主的范德华力和芘与WSBC60之间的化学作用吸附到WSBC60表面,范德华力是分子间普遍作用力,而化学作用主要是芘中的苯环和WSBC60上类似的芳香化表面形成π-π作用[11]。生物炭对重金属离子的吸附主要机理是离子交换、阳离子-π作用、表面吸附,以及络合反应[27]。通过对FTIR红外光谱结果分析,WSBC60对Cd(Ⅱ)的吸附机理可能是生物炭表面含氧官能团与Cd(Ⅱ)之间的离子交换或络合反应[14, 16]。另外吸附到WSBC60上的Cd(Ⅱ)和芘,都可能改变WSBC60的表面化学和微孔结构,还可能堵塞WSBC60表面的微孔,导致WSBC60表面有效的吸附位点减少[31]。
图 7a混合体系下芘对WSBC60吸附Cd(Ⅱ)的影响显示,Cd(Ⅱ)在低浓度时,芘与Cd(Ⅱ)会产生强烈的竞争,WSBC60对芘的吸附主要是表面吸附[33],芘占据了WSBC60表面的吸附位点,导致吸附位点减少[34],从而WSBC60对Cd(Ⅱ)的吸附量较低,因此单一体系和混合体系下WSBC60对Cd(Ⅱ)的吸附量差距较大;Cd(Ⅱ)初始浓度升高时,由图 4a等温吸附模型可知,高浓度形成的驱动力大幅增加[22],Cd(Ⅱ)在高浓度时更容易被WSBC60吸附,此时芘的浓度没有发生变化,芘的影响减小,混合体系下WSBC60对Cd(Ⅱ)的吸附量增大,因此单一和混合体系下WSBC60对Cd(Ⅱ)的吸附量差距减小。图 7b混合体系下Cd(Ⅱ)对WSBC60吸附芘的影响显示,芘的浓度很低时,不足以克服水溶液与WSBC60之间的转移阻力[22],虽然Cd(Ⅱ)会抑制WSBC60对芘的吸附[31],但是单一和混合体系下WSBC60对芘的吸附量本身很小,因此二者差距不大;芘的浓度较低时,Cd(Ⅱ)通过离子交换或络合作用吸附到WSBC60表面,与芘竞争WSBC60表面的吸附位点,而此时芘的吸附主要是表面吸附,位点的减少会影响WSBC60对芘的吸附[35],因此单一和混合体系下,WSBC60对芘的吸附量差距较大;芘浓度升高时,WSBC60对芘的吸附以分配作用为主,芘能够通过分配作用吸附到WSBC60表面,Cd(Ⅱ)的影响降低,WSBC60对芘吸附量增加[33],因此单一和混合体系下WSBC60对芘的吸附量差距减小。
3 结论(1)SEM和FTIR结果表明,WSBC60表面粗糙,孔隙结构明显,富含羟基、羧基、羰基等含氧官能团,具有高度芳香和杂环结构。
(2)在25 ℃时,Cd(Ⅱ)和芘吸附平衡时间分别为20 h和16 h,饱和吸附量分别为23.79 mg·g-1和0.17 mg·g-1,Cd(Ⅱ)在pH为5时吸附量最大,芘随着pH值增加吸附量减少,WSBC粒径越小对Cd(Ⅱ)和芘的吸附量越大。
(3)Cd(Ⅱ)和芘的吸附均符合准二级动力学和Langmuir模型,吸附过程是一种近似单分子的化学吸附。
(4)Cd(Ⅱ)和芘共存时会产生竞争吸附,互相抑制对方在WSBC60上的吸附。
| [1] |
Chen T, Han R, Wang H T, et al. Adsorption of heavy metals by biochar derived from municipal sewage sludge[J]. Journal of Tsinghua University, 2014, 54(8): 1062-1067. |
| [2] |
Crisafuiiy R, Milhome M A L, Cavalcante R M, et al. Removal of some polycyclic aromatic hydrocarbons from petrochemical wastewater using low-cost adsorbents of natural origin[J]. Bioresource Technology, 2008, 99(10): 4515-4519. DOI:10.1016/j.biortech.2007.08.041 |
| [3] |
Beesley L, Moreno-Jiménez E, Gomez-Eyles J, et al. A review of biochars' potential role in the remediation, revegetation and restoration of contaminated soil[J]. Environmental Pollution, 2011, 159(12): 3269-3282. DOI:10.1016/j.envpol.2011.07.023 |
| [4] |
Kumar S, Masto R E, Ram L C, et al. Biochar preparation from parthenium hysterophorus and its potential use in soil application[J]. Ecological Engineering, 2013, 55: 67-72. DOI:10.1016/j.ecoleng.2013.02.011 |
| [5] |
Inyang M I, Gao B, Yao Y, et al. A review of biochar as a low-cost adsorbent for aqueous heavy metal removal[J]. Critical Reviews in Environmental Science and Technology, 2016, 46(4): 406-433. DOI:10.1080/10643389.2015.1096880 |
| [6] |
王宁, 侯艳伟, 彭静静, 等. 生物炭吸附有机污染物的研究进展[J]. 环境化学, 2012, 31(3): 287-295. WANG Ning, HOU Yan-wei, PENG Jing-jing, et al. Research progess on sorption of orgnic contaminants to biochar[J]. Environmental Chemistry, 2012, 31(3): 287-295. |
| [7] |
Kim W K, Shim T, Kim Y S, et al. Characterization of cadmium removal from aqueous solution by biochar produced from a giant Miscanthus at different pyrolytic temperatures[J]. Bioresource Technology, 2013, 138(2): 266-270. |
| [8] |
谢超然, 王兆炜, 朱俊民, 等. 核桃青皮生物炭对重金属铅、铜的吸附特性研究[J]. 环境科学学报, 2016, 36(4): 1190-1198. XIE Chao-ran, WANG Zhao-wei, ZHU Jun-min, et al. Adsorption of lead and copper from aqueous solutions on biochar produced from walnut green husk[J]. Acta Scientiae Circumstantiae, 2016, 36(4): 1190-1198. |
| [9] |
吴晴雯, 孟梁, 张志豪, 等. 芦苇秸秆生物炭对水中菲和1, 1-二氯乙烯的吸附特性[J]. 环境科学, 2016, 37(2): 680-699. WU Qing-wen, MENG Liang, ZHANG Zhi-hao, et al. Sorption characteristics of phenanthrene and 1, 1-dichloroethene onto reed straw biochar in aquatic solutions[J]. Environmental Science, 2016, 37(2): 680-699. |
| [10] |
史兵方, 仝海娟, 左卫元, 等. 麻疯树籽壳生物质炭的制备及其吸附水中PAHs性能研究[J]. 中国环境科学, 2016, 36(4): 1059-1066. SHI Bing-fang, TONG Hai-juan, ZUO Wei-yuan, et al. Biochar prepared by the husk ash of Jatropha curcas seeds and its sorption ability for polycyclic aromatic hydrocarbons in water[J]. China Environmental Science, 2016, 36(4): 1059-1066. |
| [11] |
Reddy M S, Basha S, Joshi H V, et al. Seasonal distribution and contamination levels of total PHCs, PAHs and heavy metals in coastal waters of the Alang-Sosiya ship scrapping yard, Gulf of Cambay, India[J]. Chemosphere, 2006, 61(11): 1587-1593. |
| [12] |
Amaraneni S R. Distribution of pesticides, PAHs and heavy metals in prawn ponds near Kolleru Lake wetland, India[J]. Environment International, 2006, 32(3): 294-302. DOI:10.1016/j.envint.2005.06.001 |
| [13] |
钟金魁, 赵保卫, 朱琨, 等. 菲和Cu2+在黑垆土上的吸附及其交互影响[J]. 农业环境科学学报, 2011, 30(10): 1985-1990. ZHONG Jin-kui, ZHAO Bao-wei, ZHU Kun, et al. The interaction between phenanthrene and Cu2+ sorption on dark loessial soil[J]. Journal of Agro-Environment Science, 2011, 30(10): 1985-1990. |
| [14] |
徐楠楠, 林大松, 徐应明, 等. 玉米秸秆生物炭对Cd2+的吸附特性及影响因素[J]. 农业环境科学学报, 2014, 33(5): 958-964. XU Nan-nan, LIN Da-song, XU Ying-ming, et al. Adsorption of aquatic Cd2+ by biochar obtained from corn stover[J]. Journal of Agro-Environment Science, 2014, 33(5): 958-964. DOI:10.11654/jaes.2014.05.019 |
| [15] |
Pan B, Wang P, Wu M, et al. Sorption kinetics of ofloxacin in soils and mineral particles[J]. Environmental Pollution, 2012, 171(4): 185-190. |
| [16] |
程启明, 黄青, 刘英杰, 等. 花生壳与花生壳生物炭对镉离子吸附性能研究[J]. 农业环境科学学报, 2014, 33(10): 2022-2029. CHENG Qi-ming, HUANG Qing, LIU Ying-jie, et al. Adsorption of cadmium(Ⅱ) on peanut shell and its biochar[J]. Journal of Agro-Environment Science, 2014, 33(10): 2022-2029. DOI:10.11654/jaes.2014.10.020 |
| [17] |
Salima A, Benaouda B, Noureddine B, et al. Application of ulva lactuca and systoceira stricta algae-based activated carbons to hazardous cationic dyes removal from industrial effluents[J]. Water Research, 2013, 47(10): 3375-3388. DOI:10.1016/j.watres.2013.03.038 |
| [18] |
Saha P, Kumar I, Chowdhury S, et al. Insight into adsorption equilibrium, kinetics and thermodynamics of malachite green onto clayey soil of Indian origin[J]. Chemical Engineering Journal, 2010, 165(3): 874-882. DOI:10.1016/j.cej.2010.10.048 |
| [19] |
Arami M, Limaee N Y, Mahmoodi N M. Evaluation of the adsorption kinetics and equilibrium for the potential removal of acid dyes using a biosorbent[J]. Chemical Engineering Journal, 2008, 139(1): 2-10. DOI:10.1016/j.cej.2007.07.060 |
| [20] |
Cáceres-Jensena L, Rodríguez-Becerraa J, Parra-Riveroa J, et al. Sorption kinetics of diuron on volcanic ash derived soils[J]. Journal of Hazardous Materials, 2013, 261: 602-613. DOI:10.1016/j.jhazmat.2013.07.073 |
| [21] |
Wu Z B, Zhong H, Yuan X Z, et al. Adsorptive removal of methylene blue by rhamnolipid-functionalized graphene oxide from wastewater[J]. Water Research, 2014, 67: 330-344. DOI:10.1016/j.watres.2014.09.026 |
| [22] |
Liu Z G, Zhang F S. Removal of lead from water using biochars prepared from hydrothermal liquefaction of biomass[J]. Journal of Hazardous Materials, 2009, 167. |
| [23] |
Gerente C, Lee V K C, Cloirec P L, et al. Application of chitosan for the removal of metals from wastewaters by adsorption:Mechanisms and models review[J]. Critical Reviews in Environmental Science and Technology, 2007, 37(1): 41-127. DOI:10.1080/10643380600729089 |
| [24] |
Zhang Z L, Kuang Q, Jia X S. Study on the kinetics and thermodynamics of Pb2+, Cu2+, Cr3+, Cd2+, Ni2+ adsorption onto peanut hull[J]. Ecology and Environment, 2010, 19(12): 2973-2977. |
| [25] |
梁莎. 橘子皮生物吸附剂化学改性合成及其对重金属离子吸附研究[D]. 长沙: 中南大学, 2010. LIANG Sha. Chemical modification of orange peel bio-adsorbent and its adsorption to heavy metal ions[D]. Changsha:Central South University, 2010. http://cdmd.cnki.com.cn/Article/CDMD-10533-2010188162.htm |
| [26] |
Chen X C, Chen G C, Chen L G, et al. Adsorption of copper and zinc by biochars produced from pyrolysis of hardwood and corn straw in aqueous solution[J]. Bioresource Technology, 2011, 102(19): 8877-8884. DOI:10.1016/j.biortech.2011.06.078 |
| [27] |
谭光群, 袁红雁, 刘勇, 等. 小麦秸秆对水中Pb2+和Cd2+的吸附特性[J]. 环境科学, 2011, 32(8): 2298-2304. TAN Guang-qun, YUAN Hong-yan, LIU Yong, et al. Characteristics of Pb2+ and Cd2+ sorption in aqueous solution by wheat straw[J]. Environmental Science, 2011, 32(8): 2298-2304. |
| [28] |
Surchi K M S. Agricultural wastes as low cost adsorbents for Pb removal:Kinetics, equilibrium and thermodynamics[J]. International Journal of Chemistry, 2011, 3(3): 102-113. |
| [29] |
Lattao C, Cao X Y, Mao J D, et al. Influence of molecular structure and adsorbent properties on sorption of organic compounds to a temperature series of wood chars[J]. Environmental Science & Technolog, 2014, 48(9): 4790-4798. |
| [30] |
赵保卫, 石夏颖, 马锋锋. Cr(Ⅵ)和Cu(Ⅱ)在胡麻和油菜生物质炭上吸附的交互作用[J]. 环境化学, 2016, 35(2): 323-329. ZHAO Bao-wei, SHI Xia-ying, MA Feng-feng. Interacion between Cr(Ⅵ) and Cu(Ⅱ) adsorption onto biochars derived from flax and rape biomasses[J]. Environmental Chemistry, 2016, 35(2): 323-329. DOI:10.7524/j.issn.0254-6108.2016.02.2015082003 |
| [31] |
Kong H L, He J, Gao Y Z, et al. Cosorption of phenanthrene and mercury(Ⅱ) from aqueous solution by Soybean Stalk-Based Biochar[J]. Journal of Agricultural & Food Chemistry, 2011, 59(22): 12116-12123. |
| [32] |
钱林波. 生物炭对酸性土壤中有害金属植物毒性缓解及阻控机理[D]. 杭州: 浙江大学, 2014. QIAN Lin-bo. Toxicity relieving and mechanism of harmful metal plant in acidic soil[D]. Hangzhou:Zhejiang University, 2014. https://www.cnki.com.cn/lunwen-1014361580.nh.html |
| [33] |
Chen B L, Chen Z M. Sorption of naphthalene and 1-naphthol by biochars of orange peels with different pyrolytic temperatures[J]. Chemosphere, 2009, 76(1): 127-138. DOI:10.1016/j.chemosphere.2009.02.004 |
| [34] |
Lian F, Huang F, Chen W, et al. Sorption of apolar and polar organic contaminants by waste tire rubber and its chars in single-and bi-solute systems[J]. Environmental Pollution, 2011, 159(4): 850-857. DOI:10.1016/j.envpol.2011.01.002 |
| [35] |
Chen J Y, Zhu D Q, Sun C. Effect of heavy metals on the sorption of hydrophobic organic compounds to wood charcoal[J]. Environmental Science & Technology, 2007, 41(7): 2536-2541. |
 2017, Vol. 36
2017, Vol. 36