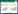文章信息
- 畅凯旋, 叶丽丽, 陈永山, 蒋金平
- CHANG Kai-xuan, YE Li-li, CHEN Yong-shan, JIANG Jin-ping
- 广西喀斯特地区土壤多金属胁迫对水稻重金属积累及生理特性的影响
- Impact of high concentrations of heavy metals in agricultural soil on heavy metals accumulation and physiological characteristics of rice(Oryza sativa L.) in karst areas in Guangxi, China
- 农业环境科学学报, 2018, 37(1): 27-35
- Journal of Agro-Environment Science, 2018, 37(1): 27-35
- http://dx.doi.org/10.11654/jaes.2017-0919
文章历史
- 收稿日期: 2017-06-30
- 录用日期: 2017-09-19
2. 桂林理工大学 广西岩溶地区水污染控制与用水安全保障协同创新中心, 广西 桂林 541004;
3. 泉州师范学院资源与环境科学学院, 福建 泉州 362000
2. Guangxi Collaborative Innovation Center for Water Pollution Control and Water Safety in Karst Area, Guilin 541004, China;
3. School of Resources and Environmental Science, Quanzhou Normal University, Quanzhou 362000, China
重金属污染是全球持续引发关注的环境污染的主要问题之一,其具有难降解、易积累等特点,对环境的可持续性、食品安全、动物及人类健康构成潜在威胁[1-2]。其中,金属矿产的开采及冶炼是引发重金属污染的重要原因之一[3]。据全国土壤环境质量公报(2014年),我国有将近19.4%的可利用土地已受到Cd、Pb、Cu、Ni、As等潜在有毒元素污染[2],其可通过植物积累间接影响到动物及人体健康。
水稻是世界主要粮食作物之一。重金属能够在水稻中积累,进而影响人体健康,同时重金属的累积过程也会对植物生长过程产生一定的抑制作用。有研究表明,重金属能够促使植物体内产生过量的活性氧(ROS),破坏植物膜结构、酶系统及蛋白质等生物大分子,抑制叶绿素合成及植株生长[4-5]。水培条件下,单一外源As(Ⅴ)浓度为500 μmol·L-1,水稻幼苗中丙二醛(MDA)含量增加、超氧化物歧化酶(SOD)活性增强[6],单一外源Pb、Zn、Hg浓度为100 μmol·L-1时,水稻幼苗ROS含量增加,叶绿素(Chl)含量减少,SOD活性降低[7-8]。一定浓度的重金属对植物的株高及生物量也表现出抑制作用。Hg能够阻止植物对矿物质的吸收,抑制植物生长及生物量积累[9]。As胁迫下能够破坏植物代谢过程,高浓度条件下,抑制植物生长,甚至导致植物死亡[10]。Cd浓度达100 mg·kg-1时,Cd敏感性水稻株高显著降低[11]。一般而言,在自然环境中,植物是在多金属胁迫环境下生长发育的。一些学者研究了多种重金属复合胁迫对植株生长的影响。Pb(300.91 mg·kg-1)、Zn(320.47 mg·kg-1)、Cd(43.58 mg·kg-1)、Cu(65.88 mg·kg-1)复合胁迫下水稻幼苗Chl含量显著减少,根系生长受到明显抑制作用[12]。Cd、Pb、Cu、Zn、As复合胁迫下水稻Chl含量显著减少,MDA含量显著增加,SOD活性先升高后降低[13]。而这些研究大部分是通过外源添加一定比例的重金属,研究多金属胁迫对植物生长的影响,具有一定的局限性。
事实上,自然环境中多金属污染土壤中,各重金属之间并不完全存在同增同减规律。土壤多种金属的复合污染不等同于各单一重金属污染的叠加,由于多重金属之间存在协同、拮抗、屏蔽等作用,使得重金属对水稻生长效应尤为复杂。本文采集广西喀斯特地区铅锌尾矿污染的农田土壤[14],以广西地区主要粮食作物水稻作为研究对象,通过盆栽试验,研究了重金属Pb、Zn、Cd、As、Hg不同污染程度的复合污染土壤对水稻重金属积累及生理指标的影响,以期为喀斯特地区多金属污染土壤的合理利用及管理提供数据。
1 材料与方法 1.1 试验材料供试土壤采集于广西壮族自治区阳朔县思的村(24°59′N,110°33′E),该地区以石山、丘陵为主,山地为辅,农田较少,属于典型的“喀斯特”岩溶地区。阳朔县地处亚热带季风性气候,年平均气温20 ℃,年降雨量达1900~2000 mm。思的村以水稻种植为主,靠近铅锌矿尾矿的部分农田由于管理不善而导致污染。试验随机布点,每个点采集1 m×1 m的0~20 cm的表层土壤,借助手持式重金属快速测定仪(Genius 9000 XRF),将Pb、Zn测定结果相近的几个点混合为一个处理土样,分别采集6个不同Pb、Zn污染程度的农田土壤及无污染对照农田土壤样品,带回实验室风干,去除石块和杂物后磨碎过10目筛备用。实验室条件下,重新测定各处理土壤理化性质及重金属浓度,通过负荷污染指数计算结果进行污染分级,将各处理编号为CK(对照)及处理Ⅰ~Ⅵ。具体理化性质见表 1,重金属含量见表 2。供试水稻品种为博优768,为当地种植的主要品种之一。
每个处理组设计种植水稻和不种植水稻两种模式,各设4个重复。试验采用硬质塑料桶(桶底直径20 cm ×高40 cm ×桶口直径30 cm),每桶盛装风干土约5 kg,并施入0.5 g史丹利复合肥(15%N-15%P2O5-15%K2O)作为基肥。在种植前将土壤润湿并稳定1周。种植时选择饱满的水稻种子,浸泡24 h露白后播种,每桶播20颗种子,以旱作方式栽培,保持土壤湿润。出苗20 d后进行间苗,每桶保留5株长势均匀的水稻,出苗67 d后(分蘖期),植株生长迟缓,毒害作用明显。测定株高(精确至0.01 cm),分别采集水稻地上部分和地下部分,清洗、杀青(105 ℃杀青30 min)、烘干至恒重(80 ℃)、称重,粉碎保存。
1.3 测定方法 1.3.1 土壤化学性质的测定土壤pH值采用pH计(土水比1:2.5),全氮采用开氏消煮法,土壤阳离子交换量(CEC)采用氯化铵-乙酸铵法,有机质采用水合热重铬酸钾氧化比色法,具体步骤参照文献[15]。
1.3.2 水稻生理指标测定水稻出苗20 d后,采集水稻新鲜叶片,用去离子水清洗干净,并于低温(-70 ℃)保存,用于测定生理指标。生理指标测定主要参照Cui等[16]的实验方法。取0.1 g新鲜叶片,用95%乙醇提取上清液,用于Chl的测定;取0.2 g新鲜叶片,用10%的三氯乙酸和0.6%的硫代巴比妥酸提取上清液,用于MDA含量测定。水稻叶片SOD、POD活性测定按照SOD、POD试剂盒方法(南京建成生物工程研究所)。
1.3.3 土壤重金属的测定土壤和水稻植株中As、Hg全量均采用王水水浴消解,原子荧光分光光度计(AS-20)测定;Pb、Zn、Cd全量采用硝酸-过氧化氢体系消解,电感耦合等离子体发射光谱仪(ICP-OES)测定[17];土壤重金属形态测定采用改进BCR法[18],其中弱酸提取态F1、可还原态F2和可氧化态F3总和为重金属提取态[19]。
1.3.4 土壤多金属污染评价方法土壤重金属污染评价采用污染负荷指数法,计算如下[17]:
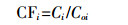 (1)
(1)  (2)
(2) 式中:CFi为重金属i的最高污染系数;Ci为重金属i的实测值;Coi为重金属i的评价标准(本文标准值采用土壤环境质量标准(GB 15618-1995)中Ⅱ类标准中土壤pH < 6.5的标准值)。PLI为某点的综合污染负荷指数,污染评价标准为:若0 < PLI≤1,则无污染,若1 < PLI≤2,则中度污染,若2 < PLI≤3,则为强污染,若PLI>3,则为极强污染。
1.3.5 重金属在水稻植株的积累重金属在水稻植株的生物累积系数(BCF,Bioaccumulation coefficient)的计算方法[3]:

式中:Cm,roots代表水稻根部重金属含量,mg·kg-1; Cm,soil表示土壤重金属含量,mg·kg-1。
1.4 样品控制与数据分析土壤样品数据均以土壤烘干质量计,测定中设置平行实验,并设置空白样和标准物质样,采用标准物质样品GSS-4(GBW07405)、GSB-6(GBW10015)进行质量控制,控制试验回收率在90%~110%。试验数据采用Excel 2010、Origin 9.0、SPSS 19.0软件进行统计分析。
2 结果与分析 2.1 土壤污染评价及多金属形态分析根据表 2结果显示,在各处理中,仅As未超过国家土壤环境质量二级标准(GB 15618-1995)。处理Ⅰ重金属浓度较低,处理Ⅲ~Ⅵ重金属浓度高,特别是Cd浓度超标16倍以上,处理Ⅵ Cd、Zn、Pb分别超过土壤环境质量二级标准24、11、6倍。根据综合污染负荷指数PLI值可知,处理CK无污染;处理Ⅰ和Ⅱ为中等污染;处理Ⅲ~Ⅵ为极强污染。
重金属弱酸提取态F1最易被释放和被植物利用,可还原态F2和可氧化态F3随外部环境改变会被释放,有一定的生物有效性,重金属残渣态F4较稳定,不易被释放,活性小,很少被植物吸收。各处理中重金属形态分析见图 1,测定的5种重金属中,Zn和Cd弱酸提取态比例较高,其次为Pb、Hg,As的弱酸提取态比例最低。各处理中,Pb、Cd可还原态占比较大,Pb可还原态比例大于残渣态,Zn残渣态比例达40%以上,As、Hg残渣态占比达50%以上。

|
| 图 1 土壤重金属形态 Figure 1 Fractions of heavy metals in soils |
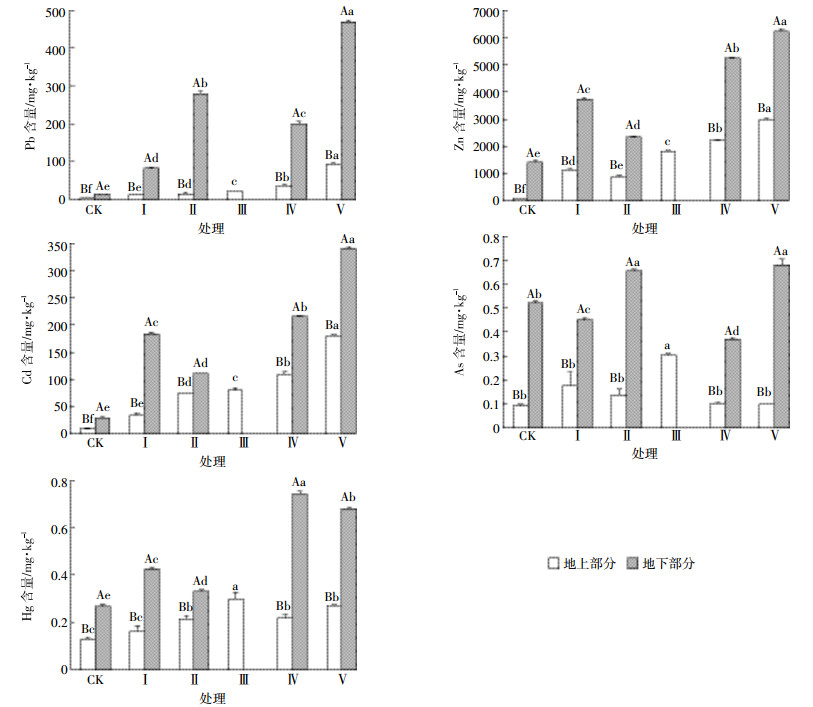
由图 2可知,同一处理水稻地下部分重金属含量高于地上部分,重金属积累量Zn>Cd>Pb>Hg>As,处理Ⅰ~Ⅴ水稻植株中重金属生物积累系数(BCF)整体趋势为Cd(0.19~0.68)>Hg(0.32~0.71)>Zn(0.30~0.48)>As(0.14~0.46)>Pb(0.04~0.28)。与对照相比,处理Ⅰ~Ⅴ水稻重金属积累量明显增加(P < 0.05),其中地下部分Pb、Zn、Cd、Hg和As累积量分别增加了13.12~30.72、1.63~4.37、3.81~11.78、1.22~2.73倍和0.82~1.66倍;地上部分Pb、Zn、Cd、Hg、As累积量分别增加了3.40~25.22、9.36~31.06、3.84~20.84、1.25~2.31倍和1.04~3.29倍。处理Ⅲ可能受低氮含量影响,生长过程中,重金属胁迫对植物毒害作用较强,根部生长被抑制,植株收获无根(处理Ⅲ无数据,下同)。处理Ⅵ为极强污染,苗期结束后,水稻植株逐渐枯黄、死亡,无重金属累积数据(图 2)。
|
| 不同大写字母表示同一处理组地下与地上部分存在显著差异(P < 0.05);不同小写字母表示同一部位不同处理组差异显著(P < 0.05)。下同 The different capital letters indicate significant difference between aboveground and underground at P < 0.05; The lowercase letters indicate significant difference among treatments in the same part at P < 0.05 level, respectively. The same as below. 图 2 水稻植株内重金属含量 Figure 2 Contents of heavy metals in the rice plant |
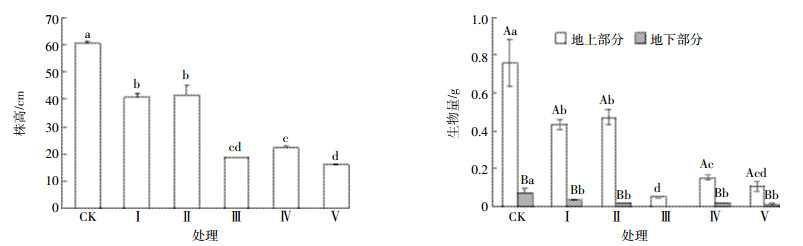
重金属胁迫对水稻株高及生物量有一定的影响,处理Ⅵ重金属污染严重,PLI达5.96,三叶期结束后,水稻植株逐渐枯黄、死亡,植株无收获,处理Ⅵ无株高及生物量数据。由图 3看出,随PLI增加,根部生长受阻,水稻株高及生物量呈下降趋势。与对照CK相比,处理Ⅰ、Ⅱ水稻株高分别降低了32.79%和30.99%,处理Ⅲ~Ⅴ水稻株高分别降低69.14%、63.40%和73.55%。与对照CK相比,处理Ⅰ、Ⅱ地上生物量分别减少了42.89%和37.77%,处理Ⅲ ~Ⅴ水稻地上生物量分别减少了93.44%、79.98%和85.88%。处理Ⅰ~Ⅴ水稻长势较为缓慢,株高、生物量与对照CK存在显著差异(P < 0.05)。
|
| 图 3 水稻生长67 d后株高及生物量(干质量) Figure 3 Rice plant height and biomass after 67 days of growth |
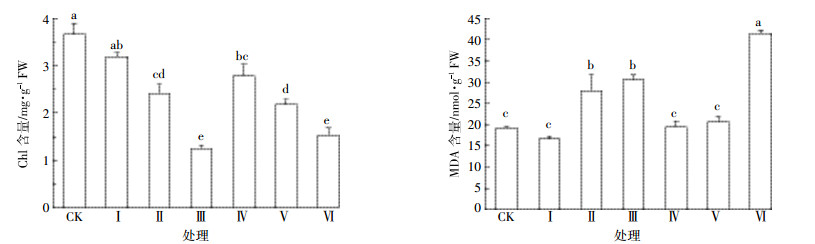
从水稻叶片Chl含量(图 4)可知,随着PLI增加,叶片Chl含量呈下降趋势;与CK相比,处理Ⅰ叶片Chl含量降低了13.09%,差异不显著;与CK相比,处理Ⅱ~Ⅵ叶片Chl含量降低了34.44%、66.20%、24.12%、40.66%和58.42%,差异显著(P < 0.05)。其中处理Ⅲ可能受较低氮含量影响,植株枯黄,Chl含量较低。
|
| 图 4 水稻苗期(20 d)叶片Chl和MDA的含量 Figure 4 Contents of Chl and MDA of rice leaves at seedling stage(20 days) |
从水稻叶片MDA含量(图 4)可知,处理Ⅰ中叶片MDA含量,较对照组下降;其他处理组中叶片MDA含量较对照组上升,且呈现出先上升后下降再上升的趋势。处理Ⅰ叶片MDA含量较对照组下降了13.92%,差异不显著;处理Ⅱ、Ⅲ叶片MDA含量较CK分别提高了45.32%和59.04%,且达到了显著水平(P < 0.05),处理Ⅳ、Ⅴ水稻MDA含量较对照组分别提高了7.52%和1.36%,差异未达到显著水平。处理Ⅵ叶片MDA含量高达41.48 nmol·g-1,较对照组提高了115.99%,显著高于其他处理(P < 0.05)。
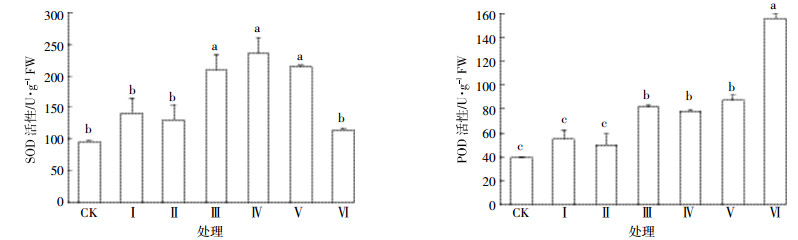
2.4.2 多金属复合污染对水稻叶片SOD、POD活性的影响重金属胁迫下,水稻叶片SOD活性先升高后降低,POD活性呈升高趋势(图 5)。与对照CK相比,处理Ⅰ、Ⅱ SOD活性分别升高了47.85%和36.88%,POD活性分别升高了39.12%和26.71%,但差异未达到显著水平;与对照CK相比,处理Ⅲ~Ⅵ水稻SOD活性分别升高了118.19%、145.06%、122.87%和19.81%,POD活性分别升高了107.48%、99.36%、122.94%和296.26%。处理Ⅳ水稻叶片SOD活性最大,达235.02 U·g-1 FW,而处理Ⅵ水稻叶片POD活性最大,达155.54 U·g-1 FW。
|
| 图 5 水稻苗期(20 d)叶片SOD和POD活性 Figure 5 Activities of SOD and POD of rice leaves at seedling stage(20 days) |
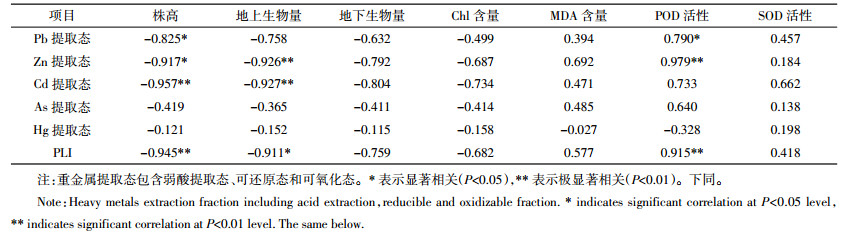
通过Pearson相关性分析(表 3),PLI与水稻株高呈极显著负相关(P < 0.01),与地上生物量呈显著负相关(P < 0.05),与地下生物量呈负相关。PLI与Chl含量呈负相关,与SOD活性、MDA含量呈正相关,但相关性不显著。POD活性与PLI及Zn提取态呈极显著正相关(P < 0.01),与重金属Pb提取态呈显著正相关(P < 0.05)。Pb、Zn提取态与水稻株高呈显著负相关性(P < 0.05),Zn、Cd提取态与地上生物量呈极显著负相关性(P < 0.01)。
|
多元回归分析结果如表 4所示,Zn可提取态对水稻叶片Chl合成表现出抑制作用;Cd可提取态对水稻MDA含量、POD活性表现出抑制作用。Zn、Hg、As可提取态对水稻叶片MDA含量、POD活性表现出协同促进作用,而对水稻叶片SOD活性表现出协同抑制作用(P < 0.05)。

|
重金属主要通过根部进入植物体,由于根部与重金属直接接触,大量重金属附着在根部组织细胞壁中,形成难溶重金属,使得重金属在根部累积量大于地上部累积量[9]。本研究结果显示,随着PLI的增加,水稻对重金属吸收增加,尤其对Zn、Cd和Pb有一定的累积效果。水稻内Cd吸收和转运是主动运输过程,水培试验Zn、Pb浓度为100 μmol·L-1时,水稻幼苗Zn、Pb积累量分别达4635 mg·kg-1 DW和5501 mg·kg-1 DW,且Zn的转移系数高于Pb[7]。本文土壤中Zn浓度远高于Pb,水稻对Zn累积量及BCF高于Pb,且各处理水稻植株重金属含量随土壤重金属提取态浓度增大而增加,地上部重金属含量低于地下部重金属含量,与前人的研究结果[7, 20-21]一致。对As、Hg而言,本研究土壤中As、Hg浓度较低,植物积累量较少。
3.2 多金属复合污染对水稻生长的影响重金属进入植物细胞内,与酶活性中心或蛋白中的巯基结合,取代金属蛋白中的必需元素,导致分子结构改变、酶失去活性,干扰细胞代谢过程,进而产生抑制植物生长、减少植物生物量等毒害作用[1, 12]。很多学者研究了重金属对植物的影响,随着重金属浓度升高,其对植物生长及生物量会产生抑制作用。郑春荣等[20]研究结果表明广西土壤Pb在0~2000 mg·kg-1时,对水稻生长无明显影响,Pb毒性存在隐蔽性,但Zn含量达201 mg·kg-1时,对水稻生长产生明显的抑制作用。随重金属含量增加,毒性增强,Pb、Zn、As、Cd重金属表现为协同作用[13]。本研究结果显示,在多金属复合污染土壤中,随PLI增加,水稻株高和生物量减少,与前人研究结果[13]较一致。当PLI>3.0,多金属复合污染对水稻毒性作用逐渐增强,植物生长受到严重的抑制作用,不利于水稻植株的生长发育。在处理Ⅲ中水稻在苗期死亡可能是由于土壤养分偏低而降低了水稻对重金属毒性的抗性。当PLI达5.96时,重金属综合污染毒性作用最强,随着重金属在水稻植株内的积累,水稻酶系统被破坏,细胞死亡,最后导致植株在苗期结束后死亡。
3.3 多金属复合污染对水稻生理指标的影响叶绿素是植物进行光合作用的主要色素,其含量的高低可以反映出植物光合作用的强弱,可以作为重金属胁迫下生物水平的敏感指标[1]。重金属在水稻植株中持续积累,可能会抑制原叶绿素酸酯还原和影响氨基酮戊酸的合成,进而使得叶绿素含量下降[13],或产生过量的ROS加速叶片衰老[22]。本研究随PLI增大,水稻叶片叶绿素含量下降,二者表现出负相关关系,与前人研究结果[13]较一致。
植物在逆境下会产生大量的O2-·、H2O2等ROS,植物抗氧化酶系统中的SOD能够促使植物体内O2-·生成H2O2,而POD能够消除植物体内的H2O2,有效防止其对植物膜及生物体的损害,SOD、POD活性大小可以作为抗氧化能力强弱的指标,过量的ROS能够与植物细胞原生质膜中的不饱和脂肪酸发生过氧化作用产生MDA,其可以反映植物细胞膜脂过氧化程度,是评价膜受损程度的重要指标[5, 23]。土壤Pb浓度为500~1800 mg·kg-1时,植物SOD酶活性上升[24]。土壤Cd浓度为6.01 mg·kg-1时对水稻的SOD活性有促进作用[4],Zn是植物所必需的微量元素,Zn能缓解Cd对植物的毒害作用,但Zn超过一定浓度时,对植物会表现出毒性作用[25-26]。本研究中,随PLI增大,水稻叶片SOD活性先增大后减少,其中在PLI为4.36时,水稻苗叶片SOD活性最大,较适合水稻幼苗的生长,但随着水稻生长发育对重金属的积累,分蘖期水稻株高、生物量明显受到抑制作用,不利于水稻生长,PLI < 1.95时,株高及生物量抑制作用较弱,较适合水稻的生长。极强污染处理组中,水稻分蘖期已严重受到毒害作用,对重金属的持续积累使得水稻生长严重受阻,故本文只研究了不同污染程度下,复合重金属对水稻幼苗期及分蘖期的影响。而对于PLI<1.95下,重金属对水稻籽粒及产量有何影响,是否有推广价值未做研究。处理Ⅵ中,土壤Zn提取态浓度达1 511.64 mg·kg-1,胁迫作用下产生大量的O2-·,使得SOD活性显著降低,但仍高于对照组,这与孙健等[13]的结果较一致。处理Ⅵ中SOD活性的降低,使得H2O2含量增加趋势减弱,POD活性仍呈增大趋势,这与Wang等[22]的研究结果较一致。较低浓度的重金属胁迫对水稻膜脂过氧化反应影响较小,随PLI增大,水稻MDA含量上升,处理Ⅳ、Ⅴ中含量较低,可能是较高活性的SOD消除了大量的ROS[6],处理Ⅵ水稻MDA含量明显增加,一方面可能是由于重金属胁迫作用增强,大量的O2-·促使发生膜脂过氧化反应,进而产生大量的MDA,另一方面可能是水稻较高的POD活性,导致H2O2分解产生更多的·OH-,加剧膜脂过氧化程度,使MDA含量增加[27]。说明水稻对重金属胁迫的自我调节能力有一定限度。PLI≥4.43时,各处理组中重金属提取态浓度占比高达50%以上,可被植物吸收利用的比例较高,可通过Pb、Zn、Cd富集植物对土壤进行修复。
4 结论(1) 土壤污染负荷指数(PLI)与水稻株高呈极显著负相关性(P < 0.01),与水稻地上生物量呈显著负相关性(P < 0.05)。PLI与MDA和SOD呈正相关关系,与POD呈显著正相关关系。随土壤PLI增加,水稻吸收重金属含量增加,水稻对重金属的吸收表现出累积效应,重金属的积累主要集中在根部,各种重金属的转运系数BCF < 1,不易转移到地上部(茎、叶),但水稻仍对Zn、Cd、Pb有一定的积累。
(2) 随PLI增加,水稻地下部分生长受抑制作用,PLI < 4.36时,水稻苗叶片SOD、POD活性较大,水稻幼苗可以正常生长,但随着水稻生长以及对重金属的不断积累,分蘖期水稻生长逐渐受到抑制,而当土壤污染负荷指数PLI≥4.43时,水稻叶片SOD活性降低,Chl含量下降,水稻幼苗出现生长障碍。
| [1] |
Bhaduri A M, Fulekar M H. Antioxidant enzyme responses of plants to heavy metal stress[J]. Rev Environ Sci Biotechnology, 2012, 11(1): 55-69. DOI:10.1007/s11157-011-9251-x |
| [2] |
Liu H Y, Hussain S, Peng S B, et al. Potentially toxic elements concentration in milled rice differ among various planting patterns[J]. Field Crops Research, 2014, 168: 19-26. DOI:10.1016/j.fcr.2014.08.007 |
| [3] |
Zhao L, Li T X, Zhang X Z, et al. Pb uptake and phytostabilization potential of the mining ecotype of Athyrium wardii(Hook.) grown in Pb-contaminated soil[J]. CLEAN-Soil, Air, Water, 2016, 44(9): 1184-1190. DOI:10.1002/clen.v44.9 |
| [4] |
章秀福, 王丹英, 储开富, 等. 镉胁迫下水稻SOD活性和MDA含量的变化及其基因型差异[J]. 中国水稻科学, 2006, 20(2): 194-198. ZHANG Xiu-fu, WANG Dan-ying, CHU kai-fu, et al. Changes of SOD activity and MDA content in rice exposed to Cd stress as affected by genotype[J]. Chinese J Rice Sci, 2006, 20(2): 194-198. |
| [5] |
Islam E, Liu D, Li T Q, et al. Effect of Pb toxicity on leaf growth, physiology and ultrastructure in the two ecotypes of Elsholtzia argyi[J]. J Hazard Mater, 2008, 154(1/2/3): 914-926. |
| [6] |
Shri M, Kumar S, Chakrabarty D, et al. Effect of arsenic on growth, oxidative stress, and antioxidant system in rice seedlings[J]. Ecotoxicol Environ Saf, 2009, 72(4): 1102-1110. DOI:10.1016/j.ecoenv.2008.09.022 |
| [7] |
Chen Q, Zhang X Y, Liu Y Y, et al. Hemin-mediated alleviation of zinc, lead and chromium toxicity is associated with elevated photosynthesis, antioxidative capacity; suppressed metal uptake and oxidative stress in rice seedlings[J]. Plant Growth Regulation, 2016, 81(2): 253-264. |
| [8] |
Chen Z, Chen M S, Jiang M. Hydrogen sulfide alleviates mercury toxicity by sequestering it in roots or regulating reactive oxygen species productions in rice seedlings[J]. Plant Physiol Biochem, 2017, 111: 179-192. DOI:10.1016/j.plaphy.2016.11.027 |
| [9] |
Marrugo-Negrete J, Durango-Hernandez J, Pinedo-Hernandez J, et al. Mercury uptake and effects on growth in Jatropha curcas[J]. J Environ Sci, 2016, 48: 120-125. DOI:10.1016/j.jes.2015.10.036 |
| [10] |
Dwivedi S, Tripathi R D, Tripathi P, et al. Arsenate exposure affects amino acids, mineral nutrient status and antioxidants in rice(Oryza sativa L.) genotypes[J]. Environ Sci Technol, 2010, 44(24): 9542-9549. DOI:10.1021/es101716h |
| [11] |
Liu J, Cai G, Qian M, et al. Effect of Cd on the growth, dry matter accumulation and grain yield of different rice cultivars[J]. Journal of the Science of Food and Agriculture, 2007, 87(6): 1088-1095. DOI:10.1002/(ISSN)1097-0010 |
| [12] |
刘惠娜, 蔡碧佳, 杨期和, 等. 铅锌尾矿对水稻幼苗生长的影响初探[J]. 生态环境学报, 2013, 22(2): 330-335. LIU Hui-na, CAI Bi-jia, YANG Qi-he, et al. Investigation on effect of Pb-Zn mining tail on the growth of rice seedling[J]. Ecology and Environmental Sciences, 2013, 22(2): 330-335. |
| [13] |
孙健, 铁柏清, 钱湛, 等. Cd、Pb、Cu、Zn、As复合污染对杂交水稻苗的联合生理毒性效应及临界值[J]. 土壤通报, 2006, 37(5): 981-985. SUN Jian, TIE Bai-qing, QIAN Zhan, et al. The combined eco-toxicological effect of Cd, Pb, Cu, Zn and As pollution on a hybrid rice seedling and the critical value[J]. Chinese Journal of Soil Science, 2006, 37(5): 981-985. |
| [14] |
Zhang C L, Li Z Y, Yang W W, et al. Assessment of metals pollution on agricultural soil surrounding a lead-zinc mining area in the karst region of Guangxi, China[J]. Bull Environ Contam Toxicol, 2013, 90(6): 736-741. DOI:10.1007/s00128-013-0987-6 |
| [15] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. LU Ru-kun. Soil agrochemical analysis method[M]. Beijing: Chinese Agricultural Science, 2000. |
| [16] |
Cui Y, Wang Q. Physiological responses of maize to elemental sulphur and cadmium stress[J]. Plant Soil Environ, 2006, 52(11): 523-529. |
| [17] |
张悠然, 李顺安, 熊林, 等. 广西石漠化地区多重金属复合胁迫对玉米生长及生理特性影响[J]. 西南农业学报, 2016, 29(9): 2079-2085. ZHANG You-ran, LI Shun-an, XIONG Lin, et al. Effects of multiple heavy metal stress on growth and physiological characteristics of maize in rocky desertification region in Guangxi[J]. Southwest China Journal of Agricultural Sciences, 2016, 29(9): 2079-2085. |
| [18] |
Li J H, Lu Y, Shim H, et al. Use of the BCR sequential extraction procedure for the study of metal availability to plants[J]. J Environ Monit, 2010, 12(2): 466-471. DOI:10.1039/B916389A |
| [19] |
Kartal S, Aydin Z, Tokalioglu S. Fractionation of metals in street sediment samples by using the BCR sequential extraction procedure and multivariate statistical elucidation of the data[J]. J Hazard Mater, 2006, 132(1): 80-89. DOI:10.1016/j.jhazmat.2005.11.091 |
| [20] |
郑春荣, 孙兆海, 周东美, 等. 土壤Pb、Cd污染的植物效应(Ⅰ):Pb污染对水稻生长和Pb含量的影响[J]. 农业环境科学学, 2004, 23(3): 417-421. ZHENG Chun-rong, SUN Zhao-hai, ZHOU Dong-mei, et al. Plant response to soil lead and cadmium pollution(Ⅰ):Effects of soil lead pollution on wetland rice growth and its uptake of lead[J]. Journal of Agro-Environment Science, 2004, 23(3): 417-421. |
| [21] |
林华, 张学洪, 梁延鹏, 等. 复合污染下Cu、Cr、Ni和Cd在水稻植株中的富集特征[J]. 生态环境学报, 2014, 23(12): 1991-1995. LIN Hua, ZHANG Xue-hong, LIANG Yan-peng, et al. Enrichment of heavy metals in rice under combined pollution of Cu, Cr, Ni, and Cd[J]. Ecology and Environmental Sciences, 2014, 23(12): 1991-1995. DOI:10.3969/j.issn.1674-5906.2014.12.016 |
| [22] |
Wang F B, Liu J C, Zhou L J, et al. Senescence-specific change in ROS scavenging enzyme activities and regulation of various SOD isozymes to ROS levels in psf mutant rice leaves[J]. Plant Physiol Biochem, 2016, 109: 248-261. DOI:10.1016/j.plaphy.2016.10.005 |
| [23] |
Kaur G, Singh H P, Batish D R, et al. A time course assessment of changes in reactive oxygen species generation and antioxidant defense in hydroponically grown wheat in response to lead ions(Pb2+)[J]. Protoplasma, 2012, 249(4): 1091-1100. DOI:10.1007/s00709-011-0353-7 |
| [24] |
Sidhu G P S, Singh H P, Batish D R, et al. Effect of lead on oxidative status, antioxidative response and metal accumulation in Coronopus didymus[J]. Plant Physiol Biochem, 2016, 105: 290-296. DOI:10.1016/j.plaphy.2016.05.019 |
| [25] |
Saifullah, Sarwar N, Bibi S, et al. Effectiveness of zinc application to minimize cadmium toxicity and accumulation in wheat(Triticum aestivum L.)[J]. Environmental Earth Sciences, 2013, 71(4): 1663-1672. |
| [26] |
Sarwar N, Ishaq W, Farid G, et al. Zinc-cadmium interactions:Impact on wheat physiology and mineral acquisition[J]. Ecotoxicol Environ Sa f, 2015, 122: 528-536. DOI:10.1016/j.ecoenv.2015.09.011 |
| [27] |
王晓维, 黄国勤, 徐健程, 等. 铜胁迫和间作对玉米抗氧化酶活性及丙二醛含量的影响[J]. 农业环境科学学报, 2014, 33(10): 1890-1896. WANG Xiao-wei, HUANG Guo-qin, XU Jian-cheng, et al. Effects of copper stresses and intercropping on antioxidant enzyme activities and malondialdehyde contents in maize[J]. Journal of Agro-Environment Science, 2014, 33(10): 1890-1896. DOI:10.11654/jaes.2014.10.003 |
 2018, Vol. 37
2018, Vol. 37