文章信息
- 郑孟杰, 靳红梅, 张松贺, 李继洲
- ZHENG Meng-jie, JIN Hong-mei, ZHANG Song-he, LI Ji-zhou
- 猪粪沼渣水热炭中重金属浸出特征研究
- The leaching characteristics of heavy metals from hydrochars of digested swine manure
- 农业环境科学学报, 2018, 37(1): 157-164
- Journal of Agro-Environment Science, 2018, 37(1): 157-164
- http://dx.doi.org/10.11654/jaes.2017-0868
文章历史
- 收稿日期: 2017-06-19
- 录用日期: 2017-09-06
2. 河海大学环境学院, 南京 210098;
3. 江苏省农业废弃物资源化工程技术研究中心/农业部农村可再生能源开发利用华东科学观测实验站, 南京 210014
2. College of Environment, Hohai University, Nanjing 210098, China;
3. Jiangsu Agricultural Waste Treatment and Recycle Engineering Research Center/East China Scientific Observing and Experimental Station of Development and Utilization of Rural Renewable Energy, Ministry of Agriculture, Nanjing 210014, China
随着我国养殖业的快速发展,畜禽粪便年产生量超过38亿t[1]。我国是生猪养殖大国,截至2015年生猪年存栏量超过4.66亿头[2]。生猪养殖规模化程度的持续提高,使猪场产生的粪便和废水相对集中,其粪污无害化处理已成为畜禽污染处理和防治的重点[3]。
厌氧发酵产沼气技术是规模猪场粪污治理的有效途径,也是发展种养结合循环农业的重要纽带,“十三五”期间,大型沼气工程逐渐成为沼气转型升级发展的核心工程[4]。然而,厌氧发酵后残留的沼液和沼渣数量大(年产生量超过1.3亿t)[5],其无害化处理和资源化利用已成为制约沼气工程发展的瓶颈[6]。畜禽养殖过程中大量添加(如Cu、Zn等)、微量添加(如As)或饲料中带有的重金属(如Pb、Cd等),大部分未被利用而随着猪粪尿直接进入环境[7]。例如,江苏省规模猪场粪便中Cu、Zn含量分别为35.7~1 726.3 mg·kg-1和113.6~1 505.6 mg·kg-1,As为4~78 μg·kg-1,Pb和Cd分别为4.22~82.91 mg·kg-1和23.21~64.67 mg·kg-1[8]。畜禽粪便经厌氧发酵后,大部分重金属仍然保留在沼液和沼渣中,而由于“浓缩”作用,沼渣中的重金属往往是原料和沼液中的数十至数百倍[9-10]。例如,猪粪沼渣中的Cu和Zn分别高达204 mg·kg-1和477 mg·kg-1,As和Pb分别为2.19 mg·kg-1和67.83 mg·kg-1,其浓度是原料中的8~15倍,是沼液中的25~130倍[10]。同时,沼渣中重金属溶解态比例增加,预示着其生物有效性可能大幅提高,直接还田存在环境安全风险[6, 11]。因此,畜禽粪便沼渣还田前必须对其中的重金属进行去除或钝化。
水热炭化(HTC)是在密闭的高压反应釜中,以水(常处于亚临界状态)为反应介质,在一定温度和压强下将其中的生物质转化为水热炭的一种热化学转化过程[12-13]。HTC不受原料含水率的制约,特别适合沼渣这类含水率高(通常在80%以上)的废弃物,其操作简单,耗能低(自身是一个放热过程),可大大降低运行成本[14-15]。利用HTC处理沼渣,可获得纯度高、分散性好、粒度易控制的生物炭材料。Dicke等[16]研究发现,小麦秸秆沼渣水热炭施用于土壤后可提高碳、氮稳定性,并减少N2O和CO2的排放量。然而,热化学转化后原料中的重金属会进一步“浓缩”在生物炭中。Jin等[17]发现,热解污泥生物炭中的重金属含量比原料中提高了2.5~3.5倍,同时发现,生物炭中重金属的可溶性不高,甚至降低,说明热解对原料中的重金属有一定的钝化作用。但HTC工艺与热解工艺相比,反应条件较温和,其所得的畜禽粪便沼渣水热炭中重金属浓缩量到底有多大?对重金属是否有钝化作用?这些尚不明确的问题,直接影响了水热炭农田利用或作为吸附材料使用的安全性。
基于此,本研究以猪粪沼渣为原料,在190 ℃和250 ℃条件下制备水热炭,探讨猪粪沼渣水热炭中主要重金属(Cu、Zn、As、Pb和Cd)的含量变化及其在不同pH条件下的浸出特征,以期为猪粪沼渣水热炭后续利用的安全性评价提供理论支持。
1 材料与方法 1.1 材料获取猪粪沼渣取自江苏省金坛市某规模生猪养殖场的沼气工程,是新鲜猪粪在完全混合式厌氧反应器(CSTR)经中温(35 ℃)厌氧消化所得。猪粪沼渣一次性取样,其含水率为86.20%,于烘箱(电热恒温鼓风干燥箱,DHG-9076A)中80 ℃条件下烘干,即得到猪粪沼渣样品(M-R),并置于干燥器中保存、备用。
1.2 水热炭制备水热炭的制备采用微型聚四氟乙烯水热合成反应釜(HR-200,上海霍铜仪器有限公司,中国),称取预处理后的猪粪沼渣6.0 g浸入60 mL超纯水中混合均匀,装于反应釜,旋紧不锈钢外套,置于烘箱中升温,至目标温度(即190 ℃和250 ℃)后持续一定时间。根据Gao等[18]的研究结果,水热反应时间超过4 h后对样品的化学特性影响甚低,因此,本研究选取的反应时间为4 h。反应结束后,将反应釜移出烘箱,待其自然降至室温,取出样品于烘箱中55 ℃烘干,此时得到的产物即为猪粪沼渣水热炭,记为M-190和M-250。
1.3 重金属浸出试验 1.3.1 溶解态重金属浸提称取制备好的沼渣及其水热炭样品0.3 g置于250 mL三角瓶中,分别加入超纯水(pH约为7.00)100 mL,用封口膜封口后,将三角瓶置于恒温振荡摇床(HZG-X160,太仓华美仪器有限公司,中国)上振荡(25 ℃、250 r·min-1)3 h。振荡结束后,取上清液过0.45 μm滤膜(JTSF,天津津腾实验设备有限公司,中国),滤液用于测定其中的重金属含量。
1.3.2 不同pH条件下重金属的浸出称取制备好的沼渣及其水热炭样品0.3 g置于250 mL三角瓶中,分别加入pH为2.0、4.0、5.5、6.0、7.5、8.0和10.0的溶液各100 mL。溶液pH用HCl或NaOH溶液调节。其中,pH 5.50为一般雨水pH值,pH 7.50为一般灌溉用水pH值。浸提方法同1.3.1。
1.4 测定方法 1.4.1 基本理化指标测定原料和水热炭的pH值采用精密pH计(PHS-2F,上海精科-上海雷磁仪器厂,中国)测定,固液比为1:10;溶解性有机碳(DOC)采用TOC分析仪(LiquiTocII,Elementar,德国)测定[19];近似分析中的固定碳和挥发性物质含量采用差重法测定,主要步骤:将3.0 g样品放入管式炉(TL 1200,南京博蕴通有限公司,中国),通入N2,在无氧条件下分别于600 ℃焙烧1 h,950 ℃焙烧10 min,通过称取残留重量,计算固定碳及挥发性物质含量;元素含量(C、H、O、N、S)采用元素分析仪(FLASH 2000,Thermo Fisher Scientific,美国)测定。
1.4.2 重金属含量测定本研究中测定的重金属为Cu、Zn、As、Pb和Cd,它们在畜禽粪便中普遍存在,也是目前世界卫生组织(WHO)认定的水体和土壤中主要的污染物[20]。溶解态及不同pH浸出液中重金属含量采用电感耦合等离子体原子发射光谱(ICP-AES,Thermo Fisher Scientific,美国)测定。原料和水热炭中重金属总量测定主要步骤:在分析天平上准确称取0.2 g样品,小心转移至50 mL三角瓶中,加入6 mL硝酸用封口膜封口后摇匀浸泡3 h,然后将三角瓶放于加热板(EH35A plus,北京莱博联泰有限公司,中国)上,110 ℃条件下加热,以溶液出现浓烟但不沸腾为准,待样品蒸至1 mL左右时取下,冷却至室温,逐次加入5 mL硝酸(浓度为65.00%~68.00%)和2 mL高氯酸(浓度为70.00%~72.00%),摇匀后重新放回加热板上,循环数次,直至液体澄清透明。将澄清消煮液转移至25 mL容量瓶定容,过0.45 μm滤膜,滤液用于测定重金属含量。试验中的化学试剂均为优级纯。
1.5 数据分析重金属浸出率采用如下公式计算:
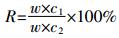
式中:R为重金属浸出率,%;c1为沼渣或水热炭中重金属浸出浓度,μg·g-1;c2为沼渣或水热炭中重金属总浓度,μg·g-1;w为沼渣或水热炭质量,g。
各指标在M-R、M-190和M-250间的差异均采用单因素方差分析(ANOVA),均值比较采用最小显著差法(LSD),显著水平P=0.05;不同温度所得水热炭中重金属(Cu、Zn、Pb、As、Cd)含量间的差异采用独立样本t检验。数据分析采用SPSS软件(v.19.0,SPSS公司,美国)。
2 结果与讨论 2.1 水热炭化后物料基本理化性状变化猪粪沼渣及其水热炭的基本理化特性如表 1所示。经190 ℃水热炭化处理后,猪粪沼渣水热炭的产率保持在50%以上,均高于Smith等[21]利用海草于200 ℃和250 ℃制备的水热炭(其产率在18.40%~39.00%之间)。随着反应温度的升高,原料中纤维素或半纤维素、脂肪组分等发生分解和转化[22],水热炭的产率降低。水热炭化处理后,水热炭中VC(挥发性碳)比例极显著(P < 0.001)降低,而FC(固定碳)和灰分比例显著提高,且反应温度越高,变化越明显。这是由于HTC过程中,VC易被分解,而FC较难分解,故水热炭中二者含量呈反比。同时,反应温度升高会加剧有机物的分解,物料脱水和脱酸程度增强,残留大量无机盐,故灰分的比例增加,这也与Reza等[23]和Ghanim等[24]的研究结论相一致。沼渣水热炭呈弱酸性,与沼渣原料相比,其pH极显著(P < 0.001)降低,这与其他水热炭pH结果基本相同[25],但与热解炭(pH>8)明显不同[26]。造成这一现象的原因主要有两个:一是在HTC过程中,沼渣表面的酸性官能团(如羧基、羰基、羟基等)增多[18];二是HTC较热解炭化的温度低,没有达到K、Ca、Na等一些无机矿物质成分分解温度,而这些可溶性无机组分往往是生物炭碱性的主要来源[27]。水热炭中DOC含量较原料极显著(P < 0.001)降低,且随着炭化温度升高,DOC含量减少极显著(P < 0.001)。这主要是由于HTC过程中,物料中的有机物被转化为CO2而得到释放,且温度越高,DOC的降解越多,故导致水热炭中DOC含量减少。

|
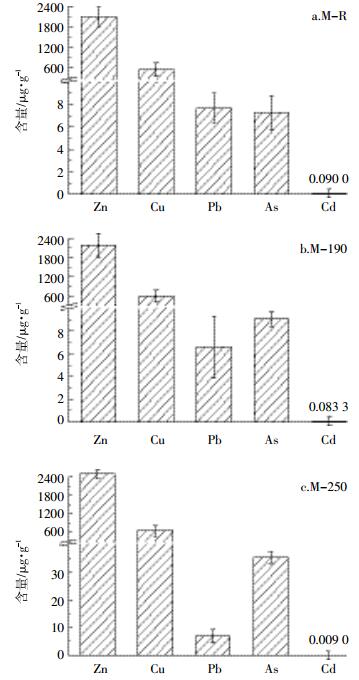
猪粪沼渣水热炭中重金属的总量如图 1所示。水热炭化后,原料中的重金属(图 1a)大部分仍保留在水热炭中(图 1b和图 1c),但不同重金属的变化程度有所差异。水热处理对猪粪沼渣中的Cu、Zn和As有“浓缩”作用,即M-190和M-250中Zn含量分别较M-R增加4.12%和18.99%,Cu分别增加7.00%和14.00%,As分别增加26.57%和289.70%。相反,M-190和M-250中Pb和Cd的含量反而降低,可能是由于HTC后猪粪沼渣中DOC含量降低造成的。DOC中含有大量功能基团,可与Pb和Cd通过络合形成配合物;DOC降解后,与Pb和Cd形成配合物的功能基团随之消失,造成二者的溶解性增加,大量分配在热解液中,进而降低了Pb和Cd在水热炭中的总量[28]。
|
| 数值为平均值±标准差(n=3) 图 1 猪粪沼渣及其水热炭中重金属总量 Figure 1 Changes of total heavy metal contents in digested swine manure and its hydrochars derived from 190 ℃ and 250 ℃, respectively |
炭化温度高可明显促进重金属在水热炭中的“浓缩”(表 2),其中M-250中的Pb和As含量显著(P=0.045和0.019)高于M-190。主要原因是在高温下,挥发性有机物损失多,水热炭的总质量明显降低,进而导致重金属在水热炭中的“浓缩”作用。

|
溶解态重金属可直接与土壤或水体中微生物结合,其浓度高低直接反应重金属的迁移转化能力及其危害程度[29]。因此,研究猪粪沼渣水热炭中溶解态重金属含量变化特征,更有助于反映其后续资源化利用的安全性。
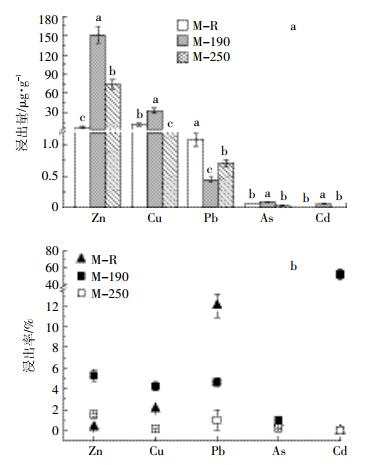
猪粪沼渣及其水热炭中溶解态重金属的含量及其浸出率如图 2所示。190 ℃处理后,M-190中Zn、Cu、Pb和Cd的溶解态含量极显著(P < 0.001)高于M-R,增幅分别为21.74倍、1.89倍、0.60倍和56.00倍(图 2a);其溶出率分别为5.27%、4.20%、0.99%和52.12%,较M-R增加4.96%、2.16%、0.33%和52.12%(图 2b)。而M-190中溶解态As含量及其溶出率却有所降低,可能是由于猪粪沼渣中含有大量的Fe,能将原猪粪沼渣中As(Ⅲ)氧化生成As(Ⅴ);同时,酸性条件下,砷与铁及有机物很快形成褐色絮状物[30-31],从而降低As的移动性。250 ℃处理后,M-250中只有溶解性Zn含量显著(P < 0.001)高于M-R,增幅为10.18倍,其他重金属的溶解态含量均小于M-R。M-250中溶解态Zn、Cu、Pb和As占其总量的比例分别为1.49%、0.14%、1.01%和0.21%,较M-R降低3.79%、4.06%、3.61%和0.78%。这表明,适当提高HTC温度可降低猪粪沼渣水热炭中溶解态重金属的含量,有利于降低其中重金属的生物有效性。
|
| 数值为平均值±标准差(n=3);处理间不同小写字母a、b和c分别表示相同重金属不同处理间的差异显著(P<0.05) 图 2 猪粪沼渣及其水热炭中溶解态重金属含量及比例 Figure 2 The amount of dissolved heavy metals and their leaching ratios from digested swine manure and their hydrochars |
重金属在不同pH条件下的溶液中,通过溶解、沉淀、凝聚、络合等反应形成不同的赋存形态,直接影响着重金属的生物有效性和毒性[32-33]。对于农田而言,除了施肥外,其pH值主要与灌溉水或降水有关;而对于工业污水,其pH值因处理工艺条件不同差异很大。因此,研究不同pH条件下猪粪沼渣水热炭中重金属的浸出特征,有助于评估其农田利用或工业废水处理过程中可能产生的环境风险。
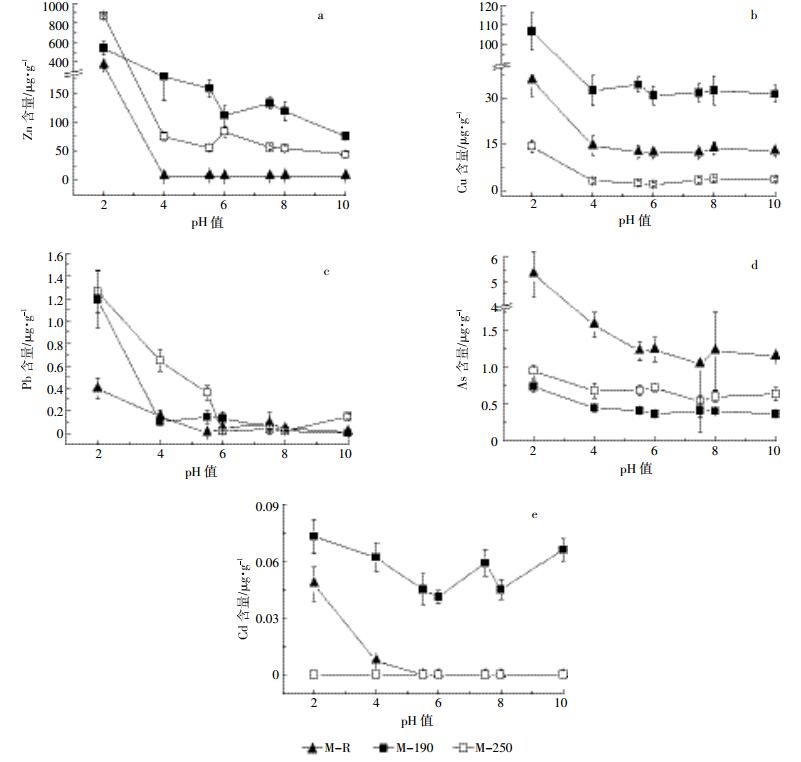
不同pH条件下猪粪沼渣及其水热炭中重金属的浸出量如图 3所示。可以看出,在模拟雨水(pH 5.50)和灌溉水(pH 7.50)这两个pH条件下,猪粪沼渣生物炭中重金属的溶出量变化不大。在其他pH条件下,不同重金属的浸出特征差异较大。pH为2时,各处理中重金属的浸出量均最高,说明强酸条件有利于增加重金属的溶解态含量,这与何绪文等[34]研究的镍渣中重金属浸出结果相一致。随着pH值的升高,水热炭中各重金属的浸出量呈现不同程度下降。各pH条件下,水热炭中Zn和Pb的浸出量均高于其在M-R中的浸出量(图 3a和图 3c),说明HTC可能增加二者的环境风险;M-190中Cu的浸出量虽有增加,但其在M-250中却明显低于M-R(图 3b),这说明增加HTC温度可显著降低沼渣水热炭中Cu的生物有效性;水热炭中As在各pH条件下的进出量均低于M-R(图 3d),说明HTC过程中形成的砷化合物在强酸或强碱条件下较为稳定;M-190中Cd在强酸或强碱条件下的浸出量最高(图 3e),这与其他重金属明显不同,主要是由于矿物质(如CO32-、PO43-)含量降低导致Cd与其结合不紧密[35-36],进而造成M-190中Cd的浸出量相对较高。而M-250中Cd总含量仅有0.009 0 μg·g-1,其在不同pH条件下的浸出量已低于仪器检测下限(0.005 0 μg·g-1),故M-250中Cd浸出量几乎为零。总体来看,猪粪沼渣中As、Pb和Cd在各pH条件下的浸出量极低,均满足农用污泥中污染物控制标准。
|
| 图 3 不同pH条件下猪粪沼渣及其水热炭中重金属的浸出量 Figure 3 The amount of heavy metal leaching of digested swine manure and its hydrochars at different pH |
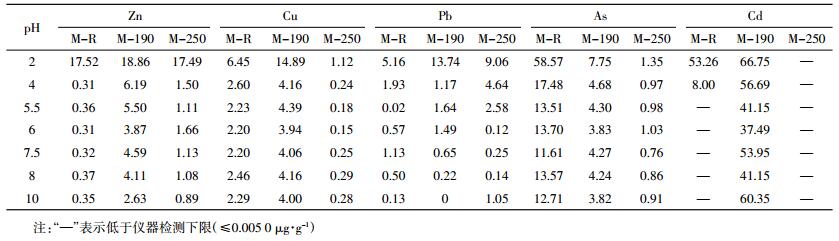
不同pH条件下,沼渣水热炭中重金属Zn、Cu、Pb、As、Cd的溶出率如表 3所示。可以看出,pH为2时溶出率均处于较高水平,也进一步验证图 3中重金属在pH为2时浸出量较高的结论。Zn和Cu在M-190中浸出率高于M-R(增幅1.34%~8.44%),而As在M-190中浸出率低于M-R(降幅7.43%~50.82%)。同时,除了pH为4时,Pb在M-190的浸出率略高于M-250,其余条件下M-250中Zn、Cu、Pb、As和Cd的浸出率均低于M-190。说明猪粪沼渣经HTC后会影响溶解态重金属比例,其中250 ℃炭化比190 ℃炭化后溶解态重金属比例低。
|
(1)水热炭化对猪粪沼渣中的Zn、Cu和As有浓缩作用,且HTC温度越高浓缩程度越大。与原料相比,增幅分别为4.12%~18.99%、7.00%~14.00%和26.57%~289.70%;但Pb和Cd却有少量损失。
(2)猪粪沼渣水热炭中溶解态Zn含量增加10.18~21.74倍,而溶解态As含量却降低0.52~1.45倍,而Cu、Pb在M-250中溶解态含量比M-190分别降低95.50%和64.47%;HTC温度增加可显著(P < 0.001)降低水热炭中溶解态重金属含量。
(3)pH为2时,猪粪沼渣水热炭中重金属的浸出量最大,随着pH的增加,其浸出量急剧下降;pH在4~10范围内,重金属浸出量的变化维持在相近水平。
| [1] |
Wang F H, Ma W Q, Dou Z X, et al. The estimation of the production amount of animal manure and its environmental effect in China[J]. China Environmental Science, 2006, 26(5): 614-661. |
| [2] |
2015年中国统计年鉴[M]. 北京: 国家统计局, 2015. China statistical yearbook 2015[M]. Beijing: National Bureau of Statistics, 2015. |
| [3] |
Jiang X Y, Sommer S G, Christensen K V. A review of the biogas industry in China[J]. Energy Policy, 2011, 39(10): 6073-6081. DOI:10.1016/j.enpol.2011.07.007 |
| [4] |
全国农村沼气发展"十三五"规划[EB/OL]. [2017-06-19]. http://ghs.ndrc.gov.cn/ghwb/gjjgh/201706/t20170607_850194.html. The 13th "Five-Year" Plan for National rural biogas development[EB/OL]. [2017-06-19]. http://ghs.ndrc.gov.cn/ghwb/gjjgh/201706/t20170607_850194.html. |
| [5] |
武深树, 谭美英, 刘伟. 沼气工程对畜禽粪便污染环境成本的控制效果[J]. 中国生态农业学报, 2012, 20(2): 247-252. WU Shen-shu, TAN Mei-ying, LIU Wei. Environmental cost control of livestock and poultry fecal pollution via biogas project[J]. Chinese Journal of Eco-Agriculture, 2012, 20(2): 247-252. |
| [6] |
葛振, 魏源送, 刘建伟, 等. 沼渣特性及其资源化利用探究[J]. 中国沼气, 2014, 32(3): 74-82. GE Zhen, WEI Yuan-song, LIU Jian-wei, et al. Characteristics of digestate and utilization[J]. China Biogas, 2014, 32(3): 74-82. |
| [7] |
吴根义, 廖新俤, 贺德春, 等. 我国畜禽养殖污染防治现状及对策[J]. 农业环境科学学报, 2014, 33(7): 1261-1264. WU Gen-yi, LIAO Xin-di, HE De-chun, et al. Current situation and countermeasures of livestock industry pollution control in China[J]. Journal of Agro-Environment Science, 2014, 33(7): 1261-1264. DOI:10.11654/jaes.2014.07.001 |
| [8] |
Cang L, Wang Y J, Zhou D M, et al. Heavy metals pollution in poultry and livestock feeds and manures under intensive farming in Jiangsu Province, China[J]. Journal of Environmental Sciences, 2004, 16(3): 371-374. |
| [9] |
靳红梅, 付广青, 常志州. 猪粪及奶牛粪中温厌氧发酵对Cu和Zn的影响[J]. 环境科学研究, 2015, 28(3): 474-480. JIN Hong-mei, FU Guang-qing, CHANG Zhi-zhou, et al. Effects of mesophilic anaerobic digestion of pig and dairy manures on Cu and Zn[J]. Research of Environmental Sciences, 2015, 28(3): 474-480. |
| [10] |
靳红梅, 付广青, 常志州, 等. 猪, 奶牛粪厌氧发酵中Pb的形态转化及其分布特征[J]. 农业工程学报, 2013, 29(22): 218-225. JIN Hong-mei, FU Guang-qing, CHANG Zhi-zhou, et al. Distribution of Pb and its chemical fractions in liquid and solid phases of digested pig and dairy slurries[J]. Transactions of the Chinese Society of Agricultural Engineering, 2013, 29(22): 218-225. DOI:10.3969/j.issn.1002-6819.2013.22.026 |
| [11] |
仇焕广, 廖绍攀, 井月, 等. 我国畜禽粪便污染的区域差异与发展趋势分析[J]. 环境科学, 2013, 34(7): 2766-2774. QIU Huan-guang, LIAO Shao-pan, JING Yue, et al. Regional differences and development tendency of livestock manure pollution in China[J]. Environmental Science, 2013, 34(7): 2766-2774. |
| [12] |
Hoekman S K, Broch A, Robbins C, et al. Hydrothermal carbonization(HTC) of selected woody and herbaceous biomass feedstocks[J]. Biomass Conversion and Biorefinery, 2013, 3(2): 113-126. DOI:10.1007/s13399-012-0066-y |
| [13] |
吴艳姣, 李伟, 吴琼, 等. 水热炭的制备、性质及应用[J]. 化学进展, 2016, 28(1): 121-130. WU Yan-jiao, LI Wei, WU Qiong, et al. Preparation, properties and applications of hydrochar[J]. Progress in Chemistry, 2016, 28(1): 121-130. DOI:10.7536/PC150745 |
| [14] |
Mumme J, Eckervogt L, Pielert J, et al. Hydrothermal carbonization of anaerobically digested maize silage[J]. Bioresource Technology, 2011, 102(19): 9255-9260. DOI:10.1016/j.biortech.2011.06.099 |
| [15] |
Berge N D, Ro K S, Mao J, et al. Hydrothermal carbonization of municipal waste streams[J]. Environmental Science & Technology, 2011, 45(13): 5696-5703. |
| [16] |
Dicke C, Lanza G, Mumme J, et al. Effect of hydrothermally carbonized char application on trace gas emissions from two sandy soil horizons[J]. Journal of Environmental Quality, 2014, 43(5): 1790-1798. DOI:10.2134/jeq2013.12.0513 |
| [17] |
Jin H M, Arazo R O, Gao J, et al. Leaching of heavy metals from fast pyrolysis residues produced from different particle sizes of sewage sludge[J]. Journal of Analytical & Applied Pyrolysis, 2014, 109: 168-175. |
| [18] |
Gao Y, Wang X H, Wang J, et al. Effect of residence time on chemical and structural properties of hydrochar obtained by hydrothermal carbonization of water hyacinth[J]. Energy, 2013, 58: 376-383. DOI:10.1016/j.energy.2013.06.023 |
| [19] |
杨金钰, 马雪琴, 唐光木, 等. 土壤研磨粒径和硫酸钾浸提浓度对可溶性有机碳测定的影响[J]. 新疆农业科学, 2015, 1: 151-156. YANG Jin-yu, MA Xue-qin, TANG Guang-mu, et al. Effects of particle size and leaching solution concentration on the analytical methods of soil dissolved organic carbon[J]. Xinjiang Agricultural Sciences, 2015, 1: 151-156. |
| [20] |
World Health Organization(WHO). Guidelines for drinking-water quality[M]. Geneva: WHO, 2004.
|
| [21] |
Smith A M, Ross A B. Production of bio-coal, bio-methane and fertilizer from seaweed via hydrothermal carbonisation[J]. Algal Research, 2016, 16: 1-11. DOI:10.1016/j.algal.2016.02.026 |
| [22] |
侯建伟, 索全义, 梁桓, 等. 炭化条件对黑沙蒿生物炭产率的影响[J]. 西北农林科技大学学报(自然科学版), 2015, 43(1): 169-174. HOU Jian-wei, SUO Quan-yi, LIANG Huan, et al. Effects of carbonization conditions on biochar yield from Artemisia ordosica[J]. Journal of Northwest A&F University(Nat Sci Ed), 2015, 43(1): 169-174. |
| [23] |
Reza M T, Mumme J, Ebert A. Characterization of hydrochar obtained from hydrothermal carbonization of wheat straw digestate[J]. Biomass Conversion and Biorefinery, 2015, 5(4): 425-435. DOI:10.1007/s13399-015-0163-9 |
| [24] |
Ghanim B M, Pandey D S, Kwapinski W, et al. Hydrothermal carbonisation of poultry litter:Effects of treatment temperature and residence time on yields and chemical properties of hydrochars[J]. Bioresource Technology, 2016, 216: 373-380. DOI:10.1016/j.biortech.2016.05.087 |
| [25] |
Mumme J, Eckervogt L, Pielert J, et al. Hydrothermal carbonization of anaerobically digested maize silage[J]. Bioresource Technology, 2011, 102(19): 9255-9260. DOI:10.1016/j.biortech.2011.06.099 |
| [26] |
Sun L, Wan S G, Luo W S. Biochars prepared from anaerobic digestion residue, palm bark, and eucalyptus for adsorption of cationic methylene blue dye:Characterization, equilibrium, and kinetic studies[J]. Bioresource Technology, 2013, 140: 406-413. DOI:10.1016/j.biortech.2013.04.116 |
| [27] |
李蜜. 水生植物基生物炭的酸碱性、碱(土)金属浸出性及对Cu(Ⅱ)的吸附效应[D]. 上海大学, 2014. LI Mi. Acid-base property, alkali and alkaline earth metallic species leaching and Cu(Ⅱ)sorption by aquatic plant-derived biochar[D]. Shanghai University, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10280-1015574466.htm |
| [28] |
赵秋, 孙毅, 吴迪, 等. 猪粪堆制过程中铅、镉、铜、锌的变化[J]. 黑龙江农业科学, 2007, 3(5): 50-52. ZHAO Qiu, SUN Yi, WU Di, et al. Change of Pb, Cd, Cu and Zn during the pig manure composting[J]. Heilongjiang Agricultural Sciences, 2007, 3(5): 50-52. |
| [29] |
韩张雄, 王龙山, 郭巨权, 等. 土壤修复过程中重金属形态的研究综述[J]. 岩石矿物学杂志, 2012, 31(2): 271-278. HAN Zhang-xiong, WANG Long-shan, GUO Ju-quan, et al. Heavy metal forms in the process of soil remediation[J]. Acta Petrologica et Mineralogica, 2012, 31(2): 271-278. |
| [30] |
Jackson B P, Bertsch P M, Cabrera M L, et al. Trace element speciation in poultry litter[J]. Journal of Environmental Quality, 2003, 32(2): 535-540. DOI:10.2134/jeq2003.5350 |
| [31] |
黄永炳, 王丽丽, 李晓娟, 等. 砷形态转化及其环境效应研究[J]. 环境污染与防治, 2013, 35(1): 16-19. HUANG Yong-bing, WANG Li-li, LI Xiao-juan, et al. Transformation of arsenic species and its environmental effect[J]. Environmental Pollution and Control, 2013, 35(1): 16-19. |
| [32] |
Méndez A, Gómez A, Paz-Ferreiro J, et al. Effects of sewage sludge biochar on plant metal availability after application to a mediterranean soil[J]. Chemosphere, 2012, 89(11): 1354-1359. DOI:10.1016/j.chemosphere.2012.05.092 |
| [33] |
刘晶晶, 杨兴, 陆扣萍, 等. 生物质炭对土壤重金属形态转化及其有效性的影响[J]. 环境科学学报, 2015, 35(11): 3679-3687. LIU Jing-jing, YANG Xing, LU Kou-ping, et al. Effect of bamboo and rice straw biochars on the transformation and bioavailability of heavy metals in soil[J]. Acta Scientiae Circumstantiae, 2015, 35(11): 3679-3687. |
| [34] |
何绪文, 石靖靖, 李静, 等. 镍渣的重金属浸出特性[J]. 环境工程学报, 2014, 8(8): 3385-3389. HE Xu-wen, SHI Jing-jing, LI Jing, et al. Leaching characteristics of heavy metals from nickel slag[J]. Chinese Journal of Environmental Engineering, 2014, 8(8): 3385-3389. |
| [35] |
Xu X Y, Cao X D, Zhao L, et al. Removal of Cu, Zn, and Cd from aqueous solutions by the dairy manure-derived biochar[J]. Environmental Science & Pollution Research International, 2013, 20(1): 358-368. |
| [36] |
夏广洁, 宋萍, 邱宇平. 牛粪源和木源生物炭对Pb(Ⅱ)和Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2014, 33(3): 569-575. XIA Guang-jie, SONG Ping, QIU Yu-ping. Sorption of Pb(Ⅱ) and Cd(Ⅱ) by manure and wood derived biochars[J]. Journal of Agro-Environment Science, 2014, 33(3): 569-575. DOI:10.11654/jaes.2014.03.025 |
 2018, Vol. 37
2018, Vol. 37