文章信息
- 舒小华, 张倩, 杨琛, 许子夫, 韦惠华, 梁英, 莫德清
- SHU Xiao-hua, ZHANG Qian, YANG Chen, XU Zi-fu, WEI Hui-hua, LIANG Ying, MO De-qing
- 泰乐菌素的超声波降解效果及机制
- The efficiency and mechanism of ultrasonic tylosin degradation
- 农业环境科学学报, 2018, 37(2): 323-331
- Journal of Agro-Environment Science, 2018, 37(2): 323-331
- http://dx.doi.org/10.11654/jaes.2017-1098
文章历史
- 收稿日期: 2017-08-13
- 录用日期: 2017-11-06
2. 桂林电子科技大学生命与环境科学学院, 广西 桂林 541006;
3. 华南理工大学环境与能源学院, 广州 510006
2. School of Life and Environmental Science, Guilin University of Electronic Technology, Guilin 541006, China;
3. College of Environment and Energy, South China University of Technology, Guangzhou 510006, China
细菌对抗生素的耐药性及超级细菌的出现危害了生态环境的平衡、威胁人体的健康[1-2]。高达60%~90%的兽药抗生素会以母体或代谢产物的形式随粪尿和冲洗栏舍废水一起排入水体中,导致水体、土壤,甚至自来水中都检测到了抗生素的存在[3]。为了减少抗生素对生态环境和人体健康的威胁,必须对含抗生素污水进行处理。
常见的传统生化污水处理技术(厌氧折流板、SBR、MBR等)被尝试用于处理抗生素污水[4-6]。尽管生化法对抗生素污水的处理有一定的效果,但由于抗生素对微生物产生的抑制作用,去除效果并不理想。为了改进传统生化法存在的缺陷和不足,一系列新的污水处理技术被研究并应用于抗生素污水的处理。其中超声空化技术因降解条件温和、无二次污染而被广泛关注[7-8]。目前国内外主要研究该技术对卤代烃、酚类、芳香烃、农药、染料、焦化废水等有毒性、难降解的有机废水的处理[9]。鉴于其显著的去除效果,一些研究也开始将超声空化技术用于抗生素废水的处理。Naddeo等[10]利用超声波工艺处理了水中包括阿莫西林在内的3种抗生素,发现超声波对抗生素的降解具有很好的潜力,它可以提高抗生素废水的可生化性,降低废水的生物毒性。郭喜峰等[11]报道了超声波降解四环素类抗生素的最佳条件;银仁莉[12]报道了超声波联合臭氧氧化降解磺胺类抗生素的效果和机制;喹诺酮类抗生素(左旋氧氟沙星、环丙沙星等)的超声波降解也有相关报道[13-14]。
尽管国内外对抗生素污水的超声空化降解研究取得了一定的成果,但是国内对该技术的研究尚处在摸索阶段。研究对象主要集中在四环素、磺胺类和喹诺酮类抗生素,而对大环内酯类抗生素超声波降解的相关研究报道比较少。大环内酯类兽药抗生素,因为良好的治疗和促生长作用被广泛用于畜牧养殖业。它们通过动物粪便等途径进入环境中,对微生物及其周边生态环境产生重要影响,甚至威胁人类健康。和四环素、磺胺类及喹诺酮类抗生素相比,大环内酯类抗生素分子量大,具有典型的内酯环结构。因此此类抗生素的超声波降解效果、降解机理可能不同。超声空化降解有机物的主要理论有3种:自由基氧化、热点理论和超临界水氧化理论。相关文献对四环素类抗生素、磺胺类抗生素及喹诺酮类抗生素的超声波降解研究显示,基于·OH等活性自由基的氧化是去除抗生素的主要机制[11-12, 14-16]。由于超声空化是一个极其复杂的物理化学过程,抗生素的超声空化降解过程中自由基氧化和热解效应可能同时进行,如何通过有效的手段对不同的超声空化机制进行定性或定量分析,是抗生素超声波降解机制研究的重要内容。
此外,目前超声空化降解抗生素研究内容主要集中在超声波对单一抗生素的降解及其影响因素的研究[11, 14-15]、超声波联合其他高级氧化技术处理模拟抗生素废水的研究等[12-13, 17-18]。其中联合超声波降解抗生素主要思路是将超声波与有利于提高自由基氧化的物质或技术联合,如超声波/双氧水(H2O2)[17]、超声波/臭氧[19]、超声波/硫酸根自由基[13],超声波/氯代甲烷等[20]。H2O2是最常见的氧化剂。除了自身具有的氧化作用之外,其在超声波作用下能迅速分解为羟基自由基,有效提高有机污染物的降解效果[21]。但H2O2与超声波协同降解大环内酯类抗生素效果的相关文献不多。
粘土矿物在自然介质中广泛存在。这类矿物不仅能吸附有机物,而且还具有稳定有机自由基、抑制电荷复合的作用[22]。因此粘土矿物在一定条件下会促进有机污染物的自由基氧化过程,一些文献也报道了富铁粘土矿物对有机污染物光降解的促进作用[23-24]。然而对抗生素环境行为有明显影响的粘土矿物在超声波降解抗生素过程中所产生的影响却鲜见报道。
在前人研究的基础上,本实验以使用量较大的典型大环内酯类兽药抗生素泰乐菌素(TYL)为研究对象,考察了超声波功率、超声波处理时间、初始浓度及溶液pH值等对TYL超声波降解效果的影响,在此基础上通过联合超声波法(添加H2O2或蒙脱石)提高超声波降解效果,并探讨TYL超声波降解机制,从而为超声波处理城市供水和养殖废水中的抗生素提供参考。
1 材料与方法 1.1 仪器与试剂BILON92-IID超声波细胞破碎仪(频率范围是20~25 kHz;具有频率自动跟踪功能;功率20~900 W连续可调),上海比朗仪器有限公司;Water HPLC 515高效液相色谱仪,美国Waters公司;RF-5301PC荧光分光光度计,日本岛津公司。
TYL(纯度>95%),购自Sigma试剂公司;甲醇、乙腈为色谱纯,购自Fisher试剂公司;双氧水、蒙脱土-K10、正丁醇、磷酸二氢钾、氢氧化钠等试剂为分析纯,购自国药集团试剂有限公司。分析纯试剂对苯二甲酸和二羟基对苯二甲酸购自阿拉丁试剂有限公司。蒙脱土-K10化学组成如下:73.0%SiO2、14.0%Al2O3、2.2% Fe2O3、0.5%CaO、1.3%MgO、0.6%Na2O和1.9%K2O。
1.2 实验方法 1.2.1 超声波处理TYL水溶液取30 mL一定浓度的TYL水溶液,置于50 mL烧杯中,超声过程中变幅杆(超声探头)入水深度约为1.5 cm左右,超声波处理时间和超声波间隙时间设为超声1 s、间隙1 s。开启冷却水,控制温度为(20±0.1)℃。设置超声功率及作用时间。打开超声波反应器,超声结束后,取样测定反应液中TYL的浓度。实验中所有的样品均设置3个平行样。
1.2.2 TYL超声波降解效率的影响因素取30 mL的TYL水溶液在设定的超声波功率(280 W)、超声波处理时间(90 min)、溶液pH值(pH=7)和初始浓度(10 mg·L-1)条件下进行超声,超声结束后取样待测。实验在考察一个影响因素时,均固定其他3个影响因素不变。不同影响因素的梯度设置如下:超声波功率分别为100、150、200、250、300、330、400 W;处理时间分别为0、5、15、30、60、120、180、240 min;溶液pH值分别为3、5、7、8.36、9、11;初始浓度分别为0.5、1、5、10、30、50、100 mg·L-1。
1.2.3 正丁醇添加量对TYL降解效果影响取10 mg·L-1、30 mL的TYL溶液(pH=7)分别加入一定量的正丁醇,使其浓度分别为0、0.5、1、2.5、5 mmol·L-1,在超声波功率为280 W的条件下超声90 min,超声结束后取样分析溶液的TYL浓度。
1.2.4 H2O2/蒙脱石联合超声降解TYL效果在10 mg·L-1、30 mL的TYL溶液(pH=7)中添加一定浓度的H2O2或蒙脱石后,280 W功率下超声。然后在不同超声时间取样分析。H2O2浓度设为0.1、1、10 mmol·L-1;蒙脱石的质量浓度设为33.3、166.7、333.3、1 666.7 mg·L-1。
1.2.5 羟基自由基含量测定采用荧光分光光度法测定羟基自由基含量,具体方法参考文献[12]:用超纯水配制对苯二甲酸(TA)与NaOH混合溶液(混合液中TA浓度为0.2 mmol·L-1、NaOH浓度为5 mmol·L-1)、150 μmol·L-1 2-羟基对苯二甲酸(HTA)溶液(逐级稀释配成浓度为0 ~1.0 μmol·L-1的HTA标准溶液)。在10 mg·L-1、30 mL的TYL溶液中加入0.5 mL、0.2 mmol·L-1 TA溶液。分别在不同超声波条件下超声,设置未超声样品为对照样,超声结束后测定样品的荧光强度。超声波条件考虑因素包括超声波功率、超声波处理时间和溶液pH值,实验在考察一个影响因素时,均固定其他2个影响因素不变。
1.3 检测方法 1.3.1 TYL浓度的检测高效液相色谱条件:Luna,C18(2)色谱柱(250×4.6 mm,5 μm);流动相pH=2的0.01 mol·L-1 KH2PO4:乙腈=65:35;流速0.5 mL·min-1;进样量为100 μL;检测波长为290 nm。
1.3.2 羟基自由基浓度检测用RF-5301PC荧光分光光度计测定HTA的浓度。固定激发波长为310 nm,测定样品在426 nm处的荧光强度。
1.4 数据处理 1.4.1 TYL降解率TYL的降解率根据超声前后溶液中的TYL浓度差进行计算,计算公式如下:
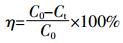 (1)
(1) 式中:C0和Ct分别指初始和t时刻的TYL的质量浓度,mg·L-1。
1.4.2 羟基自由基含量TA是一种自由基捕获剂,可以与羟基自由基反应生成稳定的HTA。
·OH+TA→HTA
TA本身不具有荧光或者无法检测出荧光,但是HTA却能发出强度较大的荧光。由于超声过程中产生的羟基自由基可以与TA反应生成HTA。故可用超声过程中HTA的浓度反映羟基自由基的含量,即:
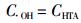 (2)
(2) 式中:C·OH和CHTA分别为羟基自由基和HTA的摩尔浓度,μmol·L-1。
2 结果与讨论 2.1 超声波降解效果影响因素探讨 2.1.1 超声波功率和时间对TYL降解的影响不同超声波功率和超声波处理时间下TYL的降解率见图 1。结果显示TYL的降解率随着超声波功率和超声波处理时间的增加而增加,表明提高超声波功率、增加超声波处理时间有利于TYL的降解。

|
| 图 1 TYL超声波降解率随超声波功率和时间的变化曲线 Figure 1 The effect of ultrasonic power and time on the degradation rate of TYL |
超声过程形成空化气泡是有机物降解的重要阶段。当超声波功率和时间增加时会形成更多空化泡。空化泡在破裂瞬间产生的高温和高压使得进入空化泡中的水和氧分子发生分裂及链式反应[5, 8],从而产生更多的自由基。相关研究认为,超声过程中亲水非挥发性有机物的降解很大程度上取决于羟基自由基的氧化[11, 16]。作为两性物质的TYL,其辛醇-水分配系数logKow=3.5,溶解度为5 g·L-1 [25]。可见溶液中自由基浓度的增加可能是TYL降解率增大的重要原因。当超声功率大于280 W时,TYL的降解率增加并不显著。田凯勋等[26]研究发现,在溶液pH=3、实验温度为30 ℃、实验时间为30 min条件下,将超声波功率从总功率的60%上升到100%时,对氯硝基苯的降解率从91.52%上升到94.47%,降解率增加幅度不大。郭照冰等[15]对四环素的超声波降解研究也发现随着超声功率(100~500 W)的增加,四环素的去除率先增大后缓慢减小。这可能是由于超声波功率达到一定程度时,空化泡会在声波负压相阶段长得过大而形成声屏障[7],这种声屏障使得空化泡在随后的声波压缩阶段不能瞬间完全崩溃,致使系统利用超声能量的效率降低,不能明显促进TYL的超声波降解。
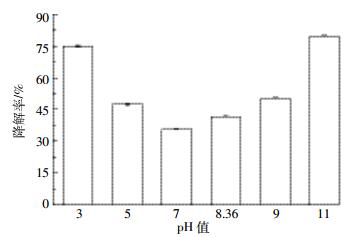
2.1.2 pH值对TYL降解的影响pH值对TYL降解效果的影响结果见图 2。在溶液pH值显酸性或碱性时其降解率明显增高,而在溶液呈中性时降解效果较差。碱性条件和酸性条件有利于水中TYL的降解。pH值对超声波降解有机物的影响比较复杂。有些研究发现酸性溶液有利于超声波降解[27],另外也有学者认为pH值增大有利于超声波降解[16-17]。
|
| 图 2 TYL超声波降解率随pH值的变化 Figure 2 The effect of pH on the degradation rate of TYL |
在酸性或中性条件时,溶液中有大量H+与羟基自由基反应,消耗掉一定量的自由基[28],其反应如下:
H++·OH+e→H2O
上述反应会使羟基自由基的浓度降低,使得TYL的降解率减小。魏红等[17]研究左氧氟沙星的超声波降解时也认为H+对·OH的捕获作用是pH值为3.00时左氧氟沙星降解率低的原因。而在碱性条件下羟基自由基的量比中性或酸性条件下多,因此碱性条件下TYL的超声波降解效果较好。
然而实验结果显示酸性条件(pH=3)时,TYL的超声降解效果也比较好,这可能与TYL在此pH值下的存在形态相关。有研究表明离子态的有机物很难进入空化泡内部,反应只能发生在空化泡的气液界面区[29]。尽管空化泡的气液界面温度不如其内部高,但这一区域存在高浓度的·OH[30]。TYL在酸性条件下带正电,TYL+进入空化气泡气液界面,更容易受到·OH的攻击,因此酸性条件下TYL的降解效果较好。随着pH值的增加,进入空化气泡气液界面的TYL+逐渐减少,其竞争羟基自由基的能力减弱,故在酸性范围内,TYL的降解率随pH值增加而减小。
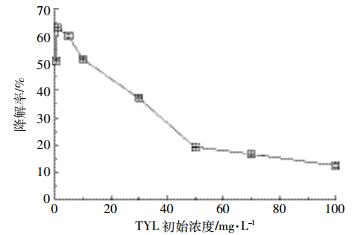
2.1.3 TYL初始浓度对TYL降解的影响图 3结果显示,TYL的降解率在初始浓度较低时表现出增加的趋势。当初始浓度大于1 mg·L-1时,TYL的降解率随着初始浓度的增加而降低。大量研究结果显示超声波降解有机物的效率随有机物浓度的增加而减小,相关研究者认为,当超声频率一定时,反应体系中产生氧化性物质(如羟基自由基)的量是一定的,因此当初始浓度增加时,去除率势必下降[14-17]。TYL降解率在初始浓度小于1 mg·L-1时表现出的增加趋势,可能是因为初始浓度较低时产生的氧化性物质足以氧化所有能被氧化的TYL。此外,溶液的浓度影响黏度,黏度通过影响空化阈、吸收声能两方面来影响空化效果[27],浓度越高,空化越困难,空化效果随之减弱。而且高浓度TYL降解过程会产生更多的中间产物,这些中间产物相互碰撞可能会消耗一部分超声能量,弱化空化效应,从而使TYL降解率减小。
|
| 图 3 TYL超声波降解率随TYL初始浓度的变化曲线 Figure 3 The effect of initial concentration of TYL on the ultrasonic degradation rate |
一般来说,超声波降解有机物的机理有以下两种[21]:一种是热解,即超声波产生的极高温度使有机物降解;另一种是羟基自由基的氧化,即由超声波产生的羟基自由基氧化有机物使其降解。为了排除热解的影响,实验中设置了冷凝水装置,控制实验温度为(20±1)℃。而且TYL作为亲水性物质其降解可能主要是羟基自由基的氧化作用[16]。为了验证这一说法,实验将正丁醇加入到TYL溶液中同时进行超声。由于正丁醇是一种自由基清除剂,可以有效地消除溶液中的羟基自由基,如果TYL的降解率随着正丁醇的加入量而减小,则可间接证明TYL的降解主要是由羟基自由基的氧化引起的。其他学者也采用该方法研究抗生素的超声波降解机理[11, 17]。
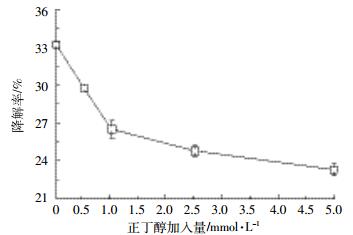
如图 4所示,随着正丁醇加入量的增多,TYL的降解率急剧减小后缓慢下降。这表明当正丁醇的浓度增多时,确实对TYL的降解有较大影响。正丁醇浓度越高,消耗溶液中羟基自由基越多,剩余能氧化TYL的羟基自由基的浓度就越少。当正丁醇浓度过高,即羟基自由基浓度过低时,TYL的降解率变化幅度减小,逐渐趋于稳定。因此可以推测TYL的降解主要通过自由基氧化途径进行。值得提出的是,当正丁醇的浓度为5 mmol·L-1时,在消耗掉溶液超声过程中产生的自由基后,TYL的降解率仍可达到23%。因此在确定自由基在TYL超声降解过程中的重要作用之后,如何定量地分析自由基氧化对超声降解的贡献率,以及可能存在的其他降解机制还需要进一步深入研究。
|
| 图 4 TYL超声波降解率随正丁醇加入量的变化曲线 Figure 4 The effect of concentration of butyl alcohol on the degradation rate of TYL |
此外,实验测定了超声过程中羟基自由基的浓度(表 1)。从表 1中可见,在超声波功率从100 W增加到400 W时,羟基自由基的浓度从0.294 μmol·L-1增加至0.801 μmol·L-1,表明超声波强度的增加确实使得水中羟基自由基的浓度升高,而正是由于羟基自由基量的增加,导致TYL在超声波强度增加时更容易被降解。在超声波功率和溶液pH值不变条件下,水中羟基自由基的量与超声时间呈正相关,因此适当延长超声波处理时间有利于TYL的降解。

|
在相同超声波功率和超声波处理时间下,羟基自由基的浓度随着pH的增高而逐渐增大(表 1),且在酸性条件下羟基自由基的浓度最低。这也说明在酸性条件下H+的存在会消耗溶液中的羟基自由基。当溶液中存在TYL时,TYL+进入空化气泡气液界面,更容易受到·OH的攻击[29-30],因此该条件下超声对TYL仍然有较好的降解效果。碱性条件下TYL降解效率的增加是由于碱性条件下能生成更多的羟基自由基。
从以上分析可见,羟基自由基的浓度变化能较好地说明TYL在不同超声波条件下的降解规律。
2.3 超声联合降解效果探讨研究表明,超声波对疏水性的难降解有机污染物的降解效果明显[31],但对亲水性、难挥发的有机污染物的降解效率却不高[32]。通过以上超声波降解条件的探讨可以得出,TYL在最佳超声条件(初始浓度为10 mg·L-1,pH值为11,超声波功率280 W,超声波处理时间90 min)下降解率为72%。为了进一步提高TYL(两性物质)的降解效果,实验选取了常见的氧化剂H2O2和粘土矿物蒙脱石与超声波结合,分别考察两种不同物质的联合超声波降解效果。
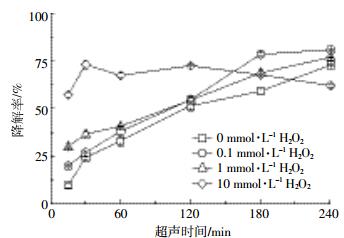
2.3.1 H2O2联合超声波降解图 5是不同浓度H2O2联合超声波的降解效果对比图。从图 5中可以看出,超声前120 min,TYL的降解率随着H2O2浓度的增加而逐渐升高。H2O2浓度为0.1和1 mmol·L-1时,其降解率提高幅度不大;而H2O2浓度为10 mmol·L-1时,TYL的超声波降解率与不添加H2O2相比,从51.4%升高至72.5%。超声120 min后,H2O2浓度为0.1 mmol·L-1和1 mmol·L-1时,TYL降解率仍缓慢增加,到240 min时,提高至80.9%(0.1 mmol·L-1 H2O2);而H2O2浓度为10 mmol·L-1时,TYL的降解率开始下降。添加H2O2后,TYL降解率增加的原因可能是超声促进H2O2的分解,增加溶液中的·OH的产生量,从而提高TYL超声波降解效果。但是H2O2作为强氧化剂,也可能与TYL直接发生氧化反应而使其降解。魏红等[17]也认为H2O2能够直接引起左氧氟沙星的降解,但受到反应条件的影响,H2O2对左氧氟沙星的氧化分解有限。
|
| 图 5 H2O2添加浓度对TYL超声波降解效果的影响 Figure 5 The effect of H2O2 adding concentration on TYL ultrasonic degradation rate |
为了查找TYL超声波降解率增加原因,实验考察了10 mmol·L-1 H2O2在不超声条件下对TYL降解效果的影响,实验结果见图 6。从图 6可以看出,添加H2O2后,即使不超声,TYL的降解率在60 min到达平衡,240 min的降解率为41.5%,此时TYL的降解可能是由H2O2直接氧化TYL引起的。和不添加H2O2直接超声效果相比,直接超声的降解率随时间增加而缓慢增加,240 min时的降解率为72.8%,显然超声波可以促进H2O2的分解,增加溶液中·OH的产生量,提高TYL超声波降解效果。添加H2O2在超声条件下,TYL的降解率在15 min迅速达到57.2%,120 min时达到72.5%,之后开始出现下降趋势,这可能是由于H2O2本身捕获了溶液中的·OH[33]。

|
| 图 6 不同实验条件下TYL降解效果 Figure 6 The degradation of TYL at different experiment conditions |
由此可见,H2O2直接氧化降解TYL的效果不及超声波处理,超声波/H2O2联合后可加快TYL的降解。直接氧化和·OH氧化均参与降解TYL的过程,但直接氧化对TYL的分解有限,超声促进H2O2分解产生·OH可能是超声波/H2O2协同降解TYL的控制步骤。
2.3.2 蒙脱石联合超声波降解图 7是蒙脱石添加量对TYL超声降解效果的影响,从图 7中可以看出,TYL超声降解率随着超声溶液中蒙脱石浓度的增加而增大。蒙脱石浓度在33.3~333.3 mg·L-1时,TYL降解率与直接超声效果相比增加幅度不大。然而蒙脱石浓度增加至1 666.7 mg·L-1后,TYL降解率15 min时迅速增加至54.9%,120 min时增大到93.1%,之后降解率基本达到平衡,240 min时降解率为93.3%。可见添加适量的蒙脱石,可以显著提高TYL的超声降解效果。

|
| 图 7 蒙脱石添加浓度对TYL超声降解效果的影响 Figure 7 The effect of montmorillonite adding concentration on TYL ultrasonic degradation rate |
由于蒙脱石是典型的粘土矿物,对TYL具有很好的吸附效果[34],因此不超声情况下直接添加蒙脱石(质量浓度1 666.7 mg·L-1),TYL的降解率在60 min就基本达到平衡,240 min时为75.4%(图 8)。直接对TYL溶液进行超声,TYL降解率随超声时间增加而增大,240 min达到72.8%。两者相比,添加蒙脱石不超声能迅速降低溶液中TYL的浓度。蒙脱石/超声波联合处理TYL的效果比单独处理效果好,TYL的去除率可达到93.9%,蒙脱石对TYL超声降解具有协同作用。这种协同作用产生的原因可能有两种:第一,添加蒙脱石超声,促进溶液中·OH的产生。理论上,蒙脱石中含有的少量铁,尤其是表面的自由铁,在一定的条件下会部分进入反应液中[35]。这些进入溶液中的Fe3+/Fe2+可能发生芬顿反应或类芬顿反应,促进溶液中·OH的产生;第二,蒙脱石对TYL的吸附作用。

|
| 图 8 添加蒙脱石超声与不超声对TYL降解效果的影响 Figure 8 The effect of montmorillonite adding on TYL ultrasonic/no-ultrasonic degradation rate |
实验检测了不同浓度蒙脱石在超声240 min后溶液中的·OH浓度,结果见表 2。从表 2中可以看出,添加少量的蒙脱石(33.3 mg·L-1)进行超声,溶液中的·OH浓度不变。但随着蒙脱石加入量的增加,·OH浓度降低。溶液中·OH浓度并没有因为含铁蒙脱石(含2.2% Fe2O3)浓度的增加而增大。芬顿体系需要在pH值2.5~6.0范围内进行,而类芬顿体系的反应pH值是2.8~3.8[36]。实验中不同浓度蒙脱石超声波处理溶液的初始pH值为7,该pH值条件可能限制了芬顿或类芬顿反应的发生。可见蒙脱石/超声协同降解TYL的过程中,·OH的氧化起了一部分作用,但主要原因可能是蒙脱石对TYL的吸附。超声过程中,溶液中·OH含量随蒙脱石浓度增加而减少可能也是因为蒙脱石对·OH产生了吸附。

|
(1)超声能有效降解水溶液中的TYL,不同超声条件及环境条件会影响水溶液中TYL的降解效果。TYL超声降解机理主要是超声过程产生的羟基自由基的氧化作用。
(2)超声联合H2O2及蒙脱石处理TYL水溶液,能加快TYL的降解并提高其降解效果,尤其是蒙脱石联合超声可使TYL的去除率达到93.9%。
(3)添加H2O2或蒙脱石对超声波降解TYL的降解效果和降解机制与其性质密切相关。不能简单归因于羟基自由基的氧化。H2O2可以直接氧化TYL,促进·OH生成甚至捕获溶液中的·OH;蒙脱石的吸附性能及含有的少量铁均可能影响溶液中·OH含量。含铁蒙脱石对超声波降解TYL的影响还需要进一步深入研究。
(4)在含抗生素废水的处理过程中,可以考虑用超声法对其进行预处理减少抗生素的浓度,从而有利于含抗生素废水进一步的生化处理。
| [1] |
Ma Y J, Wilson C A, Novak J T, et al. Effect of various sludge digestion conditions on sulfonamide, macrolide, and tetracycline resistance genes and class Ⅰ integrons[J]. Environmental Science & Technology, 2011, 45(18): 7855-7861. |
| [2] |
Gao P P, Mao D Q, Luo Y, et al. Occurrence of sulfonamide and tetracycline-resistant bacteria and resistance genes in aquaculture environment[J]. Water Research, 2012, 46(7): 2355-2364. DOI:10.1016/j.watres.2012.02.004 |
| [3] |
梁惜梅, 施震, 黄小平. 珠江口典型水产养殖区抗生素的污染特征[J]. 生态环境学报, 2013, 22(2): 304-310. LIANG Xi-mei, SHI Zhen, HUANG Xiao-ping. Occurrence of antibiotics in typical aquaculture of the Pearl River Estuary[J]. Ecology and Environmental Sciences, 2013, 22(2): 304-310. |
| [4] |
Yin X W, Qian Z M, Ben W W, et al. Biodegradation of sulfamethazine by activated sludge:Lab-scale study[J]. Journal of Environmental Engineering, 2014, 140(7): 3769-3774. |
| [5] |
Prado N, Ochoa J, Amrane A. Biodegradation by activated sludge and toxicity of tetracycline into a semi-industrial membrane bioreactor[J]. Bioresource Technology, 2009, 100(15): 3769-3774. DOI:10.1016/j.biortech.2008.11.039 |
| [6] |
Yang S F, Lin C F, Wu C J, et al. Fate of sulfonamide antibiotics in contact with activated sludge sorption and biodegradation[J]. Water Research, 2012, 46(4): 1301-1308. DOI:10.1016/j.watres.2011.12.035 |
| [7] |
张军, 曾新吾, 陈聃, 等. 水下强声波脉冲负压的产生和空化气泡运动[J]. 物理学报, 2012, 61(18): 268-278. ZHANG Jun, ZENG Xin-wu, CHEN Dan, et al. Generation of negative pressure of underwater intensive acoustic pulse and cavitation bubble dynamics[J]. Acta Physica Sinica, 2012, 61(18): 268-278. |
| [8] |
Bremner D H, Burgess A E, Chand R. The chemistry of ultrasonic degradation of organic compounds[J]. Current Organic Chemistry, 2011, 15(2): 168-177. DOI:10.2174/138527211793979862 |
| [9] |
Chowdhury P, Viraraghavan T. Sonochemical degradation of chlorinated organic compounds, phenolic compounds and organic dyes:A review[J]. Science of the Total Environment, 2009, 407(8): 2474-2492. DOI:10.1016/j.scitotenv.2008.12.031 |
| [10] |
Naddeo V, Meric S, Kassinos D, et al. Fate of pharmaceuticals in contaminated urban wastewater effluent under ultrasonic irradiation[J]. Water Research, 2009, 43(16): 4019-4027. DOI:10.1016/j.watres.2009.05.027 |
| [11] |
郭喜丰, 肖广全, 马丽莉, 等. 超声波降解四环素类抗生素废水[J]. 环境工程学报, 2014, 8(4): 1503-1509. GUO Xi-feng, XIAO Guang-quan, MAO Li-li, et al. Ultrasonic degradation of tetracyclines in aqueous solution[J]. Chinese Journal of Environmental Engineering, 2014, 8(4): 1503-1509. |
| [12] |
银仁莉. 超声联合臭氧技术降解磺胺甲恶唑的研究[D]. 哈尔滨: 哈尔滨工业大学, 2014. YIN Ren-li. Study on sulfamethoxazole degradation by ultrasound/ozone oxidation process[D]. Harbin: Harbin Institute of Technology, 2014. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D592016 |
| [13] |
魏红, 杨虹, 高扬, 等. 超声/K2S2O8体系降解水中左旋氧氟沙星的研究[J]. 西北农林科技大学学报(自然科学版), 2015, 43(3): 169-174. WEI Hong, YANG Hong, GAO Yang, et al. Degradation of levofloxacin in aqueous soluiton using US/K2S2O8[J]. Journal of Northwest A&F Univesity(Natural Science Edition), 2015, 43(3): 169-174. |
| [14] |
葛鑫, 郭照冰, 祝胜男, 等. 水中盐酸环丙沙星的超声降解[J]. 环境工程学报, 2015, 9(12): 5745-5749. GE Xin, GUO Zhao-bing, ZHU Sheng-nan, et al. Ultrasonic degradtion of ciprofloxacin hydrochloride in aqueous solution[J]. Chinese Journal of Environmental Engineering, 2015, 9(12): 5745-5749. DOI:10.12030/j.cjee.20151216 |
| [15] |
郭照冰, 周飞, 张超智, 等. 水中四环素的超声辐照降解[J]. 环境化学, 2012, 31(8): 1215-1221. GUO Zhao-bing, ZHOU Fei, ZHANG Chao-zhi, et al. Degradation of tetracyclines in aqueous solution by ultrasonic irraddiation[J]. Environmental Chemistry, 2012, 31(8): 1215-1221. |
| [16] |
马艳, 高乃云, 姚娟娟, 等. 水中盐酸四环素的超声辐照降解[J]. 华南理工大学学报(自然科学版), 2010, 38(8): 147-152. MAO Yan, GAO Nai-yun, YAO Juan-juan, et al. Degradation of tetracycline hydrochloride in aqueous solution by ultrasonic irraddiation[J]. Journal of South China University of Technology(Natural Science Edition), 2010, 38(8): 147-152. |
| [17] |
魏红, 李娟, 李克斌, 等. 左氧氟沙星的超声/H2O2联合降解研究[J]. 中国环境科学, 2013, 33(2): 257-262. WEI Hong, LI Juan, LI Ke-bin, et al. Degradation of levofloxacin by sonolysis-assisted H2O2 in aqueous solution[J]. China Environmental Science, 2013, 33(2): 257-262. |
| [18] |
Ji G D, Zhang B L, Wu Y C. Combined ultrasound/ozone degradation of carbazole in APG1214 surfactant solution[J]. Journal of Hazardous Materials, 2012, 225/226: 1-7. DOI:10.1016/j.jhazmat.2012.02.044 |
| [19] |
Guo W Q, Yin R L, Zhou X J, et al. Sulfamethoxazole degradation by ultrasound/ozone oxidation process in water:Kinetics, mechanisms, and pathways[J]. Ultrasonics Sonochemistry, 2015, 22: 182-187. DOI:10.1016/j.ultsonch.2014.07.008 |
| [20] |
魏红, 李娟, 李克斌, 等. CCl4对左旋氧氟沙星超声降解的影响[J]. 高等学校化学学报, 2012, 33(7): 1438-1443. WEI Hong, LI Juan, LI Ke-bin, et al. Effect of CCl4 on antibiotics levofloxacin's ultrasonic degradation[J]. Chemical Journal of Chinese University, 2012, 33(7): 1438-1443. DOI:10.3969/j.issn.0251-0790.2012.07.013 |
| [21] |
乔冠磊. 环丙沙星的超声波辐照降解研究[D]. 郑州: 郑州大学, 2013. QIAO Guan-lei. The study on ultrasonic degradation of ciprofloxacin[D]. Zhengzhou: Zhengzhou University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10459-1013255389.htm |
| [22] |
田浩廷. 蒙脱石促进下水合电子对有机污染物的降解研究[D]. 南京: 南京大学, 2016. TIAN Hao-ting. Ehanced degradation of organic contaminants by hydrated electrons on montmorillonite[D]. Nanjing: Nanjing University, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10284-1016131413.htm |
| [23] |
Tong M, Yuan S H, Ma S C, et al. Production of abundant hydroxyl radicals from oxygenation of subsurface sediments[J]. Environmental Science & Technology, 2016, 50(1): 214-221. |
| [24] |
Liu X X, Yuan S H, Tong M, et al. Oxidation of trichloroethylene by the hydroxyl radicals produced from oxygenation of reduced nontronite[J]. Water Research, 2017, 113: 72-79. DOI:10.1016/j.watres.2017.02.012 |
| [25] |
张倩, 杨琛, 莫德清, 等. 水溶液性质对泰乐菌素光降解的影响[J]. 农业环境科学学报, 2014, 33(12): 2444-2449. ZHANG Qian, YANG Chen, MO De-qing, et al. Effect of aqueous solution properities on tylosin photolysis[J]. Journal of Agro-Environment Science, 2014, 33(12): 2444-2449. DOI:10.11654/jaes.2014.12.023 |
| [26] |
田凯勋, 戴友芝, 张良长. 超声波/零价铁降解对氯苯胺性能及机理研究[J]. 环境工程学报, 2008, 2(2): 166-169. TIAN Kai-xun, DAI You-zhi, ZHANG Liang-chang. Research on properties and mechanism of pchloroaniline degradated by ultrasound/Fe0[J]. Chinese Journal of Environmental Engineering, 2008, 2(2): 166-169. |
| [27] |
孙仁超, 田凯勋, 杨广超, 等. 超声波-空气体系对溶液中五氯酚的降解[J]. 环境工程学报, 2016, 10(7): 3682-3686. SUN Ren-chao, TIAN Kai-xun, YANG Guang-chao, et al. Degradation of pentachlorophenol in aqueous solutions by ultrasonic-air system[J]. Chinese Journal of Environmental Engineering, 2016, 10(7): 3682-3686. DOI:10.12030/j.cjee.201502111 |
| [28] |
Huang Y H, Huang Y F, Huang C I, et al. Efficient decolorization of azo dye Reactive Black B involving aromatic fragment degradation in buffered Co2+/PMS oxidative processes with a ppb level dosage of Co2+-catalyst[J]. Journal of Hazardous Materials, 2009, 170(2/3): 1110-1118. |
| [29] |
Iida Y, Yasui K, Tuziuti T, et al. Sonochemistry and its dosimetry[J]. Microchemical Journal, 2005, 80(2): 159-164. DOI:10.1016/j.microc.2004.07.016 |
| [30] |
Adewuyi Y G. Sonochemistry in environmental remediation. 1. Combinative and hybrid sonophotochemical oxidation processes for the treatment of pollutants in water[J]. Environmental Science & Technology, 2005, 39(10): 3409-3420. |
| [31] |
Song W H, Delacruz A A, Rein K, et al. Ultrasonically induced degradation of microcystin-LR and -RR:Identification of products, effect of pH, formation and destruction of peroxides[J]. Environmental Science & Technology, 2006, 40(12): 3941-3946. |
| [32] |
Mahamuni N N, Pandit A B. Effect of additives on ultrasonic degradation of phenol[J]. Ultrasonics Sonochemistry, 2006, 13(2): 165-174. DOI:10.1016/j.ultsonch.2005.01.004 |
| [33] |
Shriwas A K, Gogate P R. Ultrasonic degradation of methyl parathion in aqueous solutions:Intensification using additives and scale up aspects[J]. Separation and Purification Technology, 2011, 79(1): 1-7. DOI:10.1016/j.seppur.2011.02.034 |
| [34] |
Zhang Q, Yang C, Huang W L, et al. Sorption of tylosin on clay minerals[J]. Chemosphere, 2013, 93(9): 2180-2186. DOI:10.1016/j.chemosphere.2013.07.081 |
| [35] |
Liang L Y, Hofmann A, Gu B H. Ligand-induced dissolution and release of ferrihydrite colloids[J]. Geochimica et Cosmochimica Acta, 2000, 64(12): 2027-2037. DOI:10.1016/S0016-7037(00)00349-5 |
| [36] |
Jiang C C, Pang S Y, Ouyang F, et al. A new insight into Fenton and Fenton-like processes for water treatment[J]. Journal of Hazardous Materials, 2010, 174(1/2/3): 813-817. |
 2018, Vol. 37
2018, Vol. 37