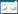文章信息
- 邓金环, 郜礼阳, 周皖婉, 杜伟庭, 蔡昆争, 陈桂葵, 黄飞
- DENG Jin-huan, GAO Li-yang, ZHOU Wan-wan, DU Wei-ting, CAI Kun-zheng, CHEN Gui-kui, HUANG Fei
- 不同温度制备香根草生物炭对Cd2+的吸附特性与机制
- Adsorption characteristics and mechanisms of Cd2+ in biochar derived from vetiver grass under different pyrolysis temperatures
- 农业环境科学学报, 2018, 37(2): 340-349
- Journal of Agro-Environment Science, 2018, 37(2): 340-349
- http://dx.doi.org/10.11654/jaes.2017-1066
文章历史
- 收稿日期: 2017-08-03
- 录用日期: 2017-09-27
2. 农业部华南热带农业环境重点实验室, 广州 510642;
3. 重庆大学城市建设与环境工程学院, 重庆 400045
2. Key Laboratory of Tropical Agro-Environment, Ministry of Agriculture, Guangzhou 510642;
3. College of Urban Construction and Environmental Engineering, Chongqing University, Chongqing 400045
香根草(Vetiveria zizanioides L.)作为我国南方普遍生长的一种禾本科的多年生大型草本植物,生长快且生物量大,近年来被广泛用于生态环境治理和退化生态系统恢复[1-4]。夏汉平等[1]研究了香根草对铅锌尾矿土壤重金属的吸收性能,发现香根草对尾矿中重金属有一定的生物净化作用,富集能力顺序为Zn>Cu>Pb;Pang等[2]和Aibibu等[3]研究了不同重金属Cu、Zn、Cd和Pb对香根草生长、生理和生化特性的影响,发现香根草对不同重金属均具有一定的耐受性;马文超等[4]研究Cd在土壤-香根草系统中的迁移和转化特征,发现处理90 d后香根草根部Cd累积量达241.54 mg·kg-1。而且,Zhang等[5]进一步研究不同Cd2+浓度胁迫下香根草的生理代谢情况发现,当土壤Cd2+浓度在15~100 mg·kg-1范围时,香根草地下根部Cd2+积累量是地上部积累量的41~44倍,转移系数(Translocation factor,TF)范围为0~0.023,两者积累量分别为167~396 mg·kg-1和0.13~9.0 mg·kg-1;Ng等[6]在评价香根草对土壤重金属污染修复效果时,发现4种不同重金属处理下香根草的TF系数范围为0~0.038;同样地,其他学者[7-9]在香根草修复重金属污染的研究中,也发现香根草积累重金属的部位主要是根部(TF均远远小于1)。这些研究以及其他报道[10-12]表明,香根草在重金属污染土壤的修复方面具有较大的潜力,能吸收重金属离子并将其绝大部分储存于根部。然而,修复完之后收割的大量香根草秸秆造成了极大的浪费(株高1~2 m),而且有关香根草修复重金属污染的研究,目前往往集中于土壤环境方面,在水体环境治理方面研究较少。本文拟以香根草为原材料制备生物炭并研究其吸附Cd2+的特性与机制,既是对有关香根草研究方面的一个补充,也是对香根草秸秆资源化利用途径的一个探索。
生物炭是不同生物质(秸秆和畜禽粪便等)在限氧或缺氧条件下,采用相对较低温度(< 700 ℃)热解后得到的富碳产物,具有发达的孔隙结构、巨大的比表面积和丰富的含氧官能团,可作为环境中重金属污染治理的材料之一[13-14]。但是,不同热解温度制备的生物炭对重金属的吸附性能往往存在较大的差异[15-16]。戴静等[15]以木屑、米糠、稻秆、玉米秸秆为原料,研究5种热解温度(300~700 ℃)下制备的生物炭对水中Cd2+的吸附特性,发现700 ℃下制备的4种不同原材料类型生物炭对Cd2+吸附效果最佳。类似地,Li等[16]、李力等[17]和楚颖超等[18]分别发现700 ℃高温热解制备的凤眼莲秸秆、玉米秸秆和椰纤维等生物炭对水中重金属吸附去除效果最佳。但是,也有报道[19-21]表明低温300 ℃制备生物炭对水溶液中重金属的吸附效果最好。以上这些研究以及其他报道[22-23]说明,何种温度范围内(高温、中温、低温)制备的生物炭吸附重金属的性能最佳,尚存在争议,这是因为不同热解温度导致生物炭表面性质和结构不同,从而决定生物炭吸附性能的差异。而且,Cui等[24]在研究不同热解温度制备美人蕉秸秆生物炭对水中Cd2+的吸附机制中,发现无机盐离子浓度与吸附性能关系显著,其中无机盐离子与Cd2+的沉淀作用对高温生物炭(≥500 ℃)吸附的贡献较大;Wang等[25]研究不同热解温度生物炭对水中Pb2+的吸附特性,认为高温生物炭(≥500 ℃)特性中更完备的π共轭芳香结构增加了对吸附的贡献。这些报道表明不同温度下制备生物炭的理化性质与其吸附特性之间的相互关系尚不明确,值得进一步探究。
本文采用限氧控温热解法,分别在不同温度下(300、500 ℃和700 ℃)制备香根草生物炭,并对生物炭的性质进行表征分析,研究了三种生物炭(BC300、BC500和BC700)对Cd2+的吸附特性与机制,以期为香根草秸秆资源化利用提供一种新思路,并为水体重金属污染的治理提供理论参考。
1 材料与方法 1.1 生物炭的制备香根草秸秆取自华南农业大学生态农场,将原材料烘干粉碎后填满于密闭的热解盒中,放入马弗炉中通入10~20 min氮气,分别在300、500 ℃和700 ℃三种温度下热解2 h,冷却至室温后取出研磨过筛(60目),储存于干燥器中备用。原材料与生物炭分别标记为CK和BC300、BC500、BC700。
1.2 生物炭的表征生物炭的产率通过制备前后的质量损失来计算,灰分由灼烧法测定,pH由pH计测定,固液比为1:20(g·mL-1)。表面电荷采用Zeta电位分析仪(Nano-ZS90,英国Malvern)测定,元素组成由元素分析仪(Vario EL cube,德国Elementar)测得,比表面积及孔径分布采用物理化学吸附仪(ASIQACIV200-2,美国Quantachrome)测定。原材料与生物炭吸附前后的表面形貌,通过电镜能谱(SEM-EDS)仪(Nova Nano SEM 430,荷兰FEI)进行表面形态和成分分析;原材料与生物炭吸附前后的表面官能团变化情况,利用傅立叶变换红外光谱(FTIR)仪(VERTEX 70,德国Bruker)进行测试,采用KBr压片制样,扫描区域为500~4000 cm-1。
1.3 吸附试验 1.3.1 吸附等温线本课题组前期实验结果发现,生物炭最佳吸附条件:固液比1 g·L-1,pH 6.0,转速150 r·min-1。分别称取0.02 g生物炭于含不同Cd2+浓度(10、20、30、50、80、100、120、150、180、200、250 mg·L-1)的20 mL溶液中,并调节pH为6.0,室温条件下在摇床中进行吸附试验(150 r·min-1,12 h),取样过滤后上清液采用原子吸收光谱仪(AAS)测定Cd2+浓度。
生物炭的吸附量及去除率(η)的计算公式为:
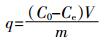 (1)
(1) 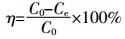 (2)
(2) 式中:q为生物炭吸附量,mg·g-1;C0、Ce分别为溶液中Cd2+的初始浓度和平衡浓度,mg·L-1;V为溶液体积,L;m为生物炭的质量,g。
吸附等温线分别用Langmuir模型(式3)和Freundlich模型(式4)进行拟合,公式[26]如下:
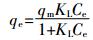 (3)
(3) 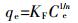 (4)
(4) 式中:qe和qm分别为平衡吸附量和最大吸附量,mg·g-1;KL为Langmuir常数,L·g-1,与吸附强度有关;KF(mg1-1/n·L1/n·g-1)和n为Freundlich常数,分别与吸附容量和吸附强度有关。
1.3.2 吸附动力学准确称取0.02 g生物炭于两种初始Cd2+浓度(20、100 mg·L-1)的20 mL溶液中,调节pH为6.0,在转速150 r·min-1下进行吸附试验,并于12 h内进行取样,并用AAS测定上清液中Cd2+的浓度。
采用准一级动力学方程(式5)和准二级动力学方程(式6)对吸附过程进行模拟,公式[27]如下:
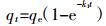 (5)
(5) 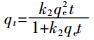 (6)
(6) 式中:qe、qt分别为吸附平衡和吸附时间为t时的吸附容量,mg·g-1;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g·mg-1·min-1。
2 结果与分析 2.1 热解温度对生物炭性质的影响三种热解温度制备的生物炭主要理化性质见表 1。随着热解温度的升高,香根草生物炭的产率明显下降,而pH和灰分则逐渐增加。BC700的灰分含量为24.45%,分别比BC500和BC300增加了2.53%和8.76%。三种生物炭均呈碱性,BC300、BC500和BC700分别为8.13、9.64和10.62,热解温度越高,碱性越强,这与灰分含量有相似的变化趋势。同时,相对原材料CK,生物炭中C元素含量显著增加,O和H元素含量显著减少(表 1)。随着热解温度的升高,生物炭中H/C原子比逐渐减小,芳香性增强。此外,三种生物炭(BC300、BC500和BC700)的Zeta电位分别为-25.00、-28.07 mV和-30.33 mV,可见生物炭表面均带负电且电荷量随温度升高而增加,这可能有利于Cd2+等重金属污染物通过静电作用吸附于其表面。
三种生物炭(BC300、BC500和BC700)的比表面积分别是3.37、42.89 m2·g-1和227.04 m2·g-1,分别是原材料的1.02、12.99倍和68.8倍(表 1)。随着热解温度的升高,比表面积显著增大,总孔容逐渐增大,但平均孔径下降,这表明升高温度有利于生物炭孔隙结构的发育,从而为吸附重金属等污染物质提供了更多的位点。SEM的观察结果也可以验证这一点(图 3)。
|
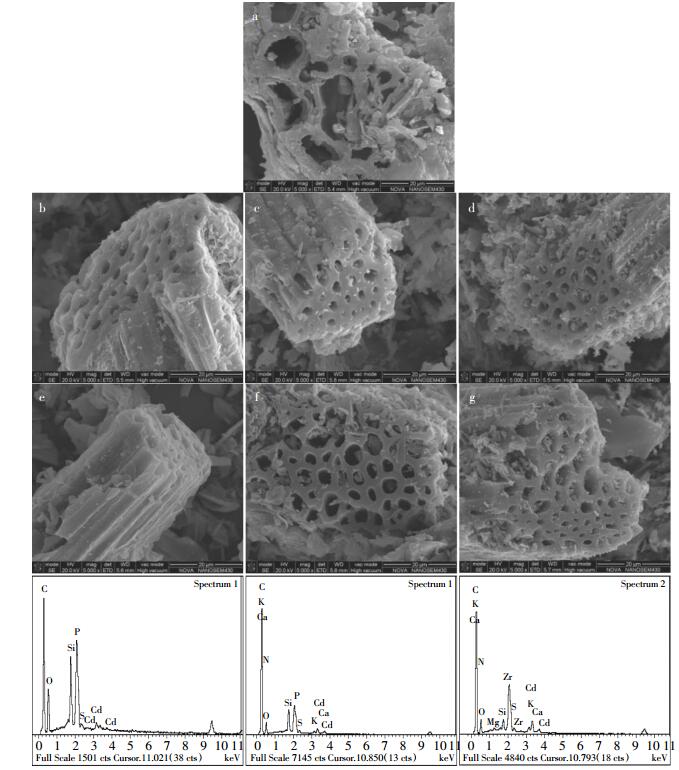
| a:CK;b:BC300;c:BC500;d:BC700;e:BC300+Cd;f:BC500+Cd;g:BC700+Cd 图 3 生物炭吸附前后的电镜能谱图(×5000倍) Figure 3 SEM-EDS images of biochar before and after adsorption(×5000 times) |
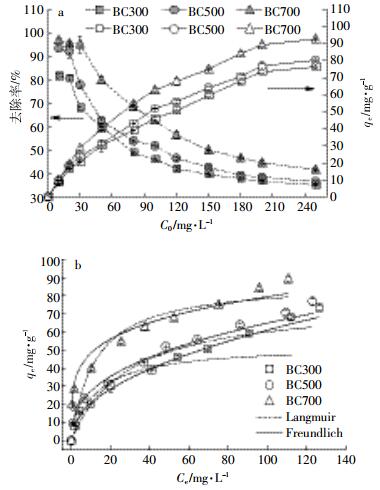
不同初始Cd2+浓度对生物炭吸附的影响如图 1a所示。从中可以看出,三种生物炭的吸附量均随Cd2+浓度的增大而不断增加,并最终趋于稳定,达到吸附平衡,但去除率却呈下降趋势。值得注意的是,三种生物炭最大吸附量顺序依次是BC700(92.65 mg·g-1)> BC500(80.17 mg·g-1)> BC300(76.29 mg·g-1)。而且,当初始Cd2+浓度为10 mg·L-1时,生物炭达到最大去除率,三者的大小依次为BC700(96.77%)>BC500(93.40%)>BC300(81.44%),可见三者吸附能力的顺序为BC700>BC500>BC300。
|
| 图 1 不同Cd2+初始浓度对生物炭吸附的影响(a)和等温线的拟合(b) Figure 1 Effect of initial Cd2+ concentration on adsorption(a) and isotherm model fitting(b) |
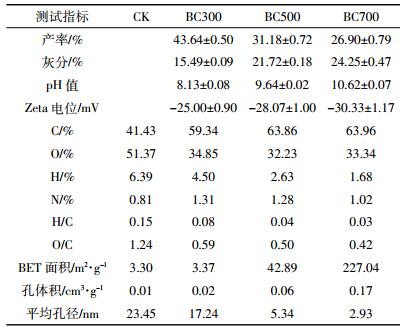
采用Langmuir和Freundlich模型对等温吸附特征进一步描述(图 1b),其模型参数见表 2。两种模型均能较好地描述三种生物炭的吸附行为,但Freundlich模型拟合度相对较高(R2>0.98),且Freundlich模型参数n>1,说明生物炭对Cd2+的吸附是有利吸附。此外,KF和n值均随温度升高而不断增大,表明BC700具有较强的吸附能力,且优于其他两种生物炭BC300和BC500。
生物炭吸附Cd2+的动力学过程如图 2所示。在初始Cd2+浓度为20 mg·L-1条件下,BC700对Cd2+的吸附开始较快,当吸附5 min时,吸附量已达到饱和吸附量的87.50%,随后增幅减缓,并在80 min时达到动态平衡。BC500和BC300也有相似的变化趋势,分别在180 min和240 min达到平衡,因此,平衡时间顺序为BC700(80 min) < BC500(180 min) < BC300(240 min)。类似地,在初始Cd2+浓度为100 mg·L-1条件下,BC700、BC500和BC300达到平衡的时间也相应地延长,分别为150、360 min和360 min。

|
| 图 2 吸附时间对吸附的影响 Figure 2 Effect of time on Cd2+ adsorption |
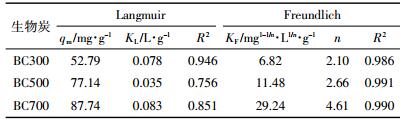
为进一步反映生物炭吸附动力学特性,采用准一级和准二级动力学模型进行拟合(表 3)。对比R2值,发现准二级动力学模型拟合效果明显较好(R2值均大于0.98),且理论吸附量更接近实际平衡吸附量(qexp),平均相对误差分别为2.18%、1.71%和3.79%,这表明生物炭吸附符合准二级动力学模型。两种初始Cd2+浓度(20、100 mg·L-1)下,从速率常数k2可以看出,k2(BC700)>k2(BC500)>k2(BC300),说明BC700的吸附速率最大,能较早达到吸附平衡,这与图 2观察到的现象相吻合。
SEM图谱显示,与原材料相比,香根草秸秆经热解后均形成了明显的孔隙结构(图 3b、图 3c、图 3d),表面粗糙,切面出现较规则的孔状结构。当温度升至500 ℃和700 ℃时,生物炭表面出现了排列规则且致密的孔状结构,这使高温生物炭具有较大的比表面积,从而增大吸附潜能,这与表 1中的BET结果相吻合。另外,采用EDS对吸附后的生物炭进行分析发现,吸附后的生物炭表面可能附着含Cd化合物(图 3e、图 3f、图 3g)。
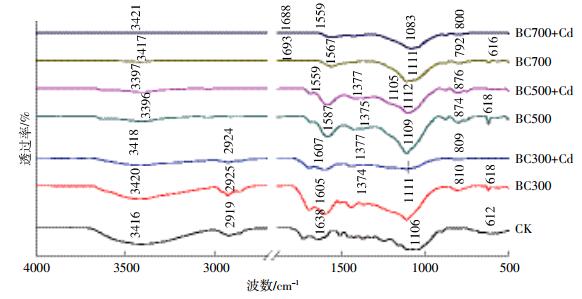
2.4 FTIR分析对比原材料与生物炭的FTIR光谱图(图 4a),热解后的三种生物炭表面均具有较丰富的官能团。对于BC300,在3420 cm-1的-OH吸收峰、1700~1600 cm-1之间羧基和醛基上的C=O伸缩振动峰、1110 cm-1处酯基C-O伸缩振动峰和618 cm-1的-OH吸收峰,表明BC300具有丰富的含氧官能团[28-29]。但对于BC500和BC700,上述特征峰减弱或消失,而与芳环结构相关的特征峰1600~1400 cm-1处的芳环C=C和900~700 cm-1的芳环C-H弯曲振动变化较为显著,表明热解温度升高促进了生物炭芳香性和稳定性的提高[30],这与生物炭元素分析的结果相吻合(表 2)。
|
| 图 4 原材料与生物炭的红外光谱图 Figure 4 FTIR spectra of the biochar and raw materials |
对比分析生物炭吸附前后的FTIR谱图发现,BC300含氧官能团特征吸收峰(3 420.37、1 605.55、1 374.63、1 111.56 cm-1和618.03 cm-1)明显减弱,表明-OH、C-O、C=O等官能团参加了生物炭对Cd2+的吸附作用;对于BC500和BC700,除了含氧官能团发生作用外,芳环的特征吸收峰也产生了明显的变化,尤其是BC700在1 567.22 cm-1和792.95 cm-1发生了较大幅度的位移。以上这些表明三种生物炭吸附Cd2+的主要官能团分别为-OH、C-O、C=O(BC300),-OH、C-O、C=C、C-H(BC500),-OH、C=O、C-O、C=C、C-H(BC700)。由此可见,BC700有较多的官能团参与了吸附过程。
3 讨论 3.1 不同热解温度对香根草生物炭理化性质的影响热解温度是影响生物炭理化性质的主要因素之一。Al-Wabel等[31]、Chen等[32]和Wang等[33]的研究均发现生物炭呈现碱性且随着温度升高而增加,本研究中制备的香根草生物炭也得到了这一规律(表 1)。原因在于随着热解温度升高,无机盐离子被熔结形成以灰分形式存在的固体碱性物质,从而导致生物炭具有较强的碱性[34]。而且,本试验中灰分含量随热解温度升高而增大,可能是固体碱性物质以灰分的形式存在,进而增大pH值,也能较好地解释这一现象。但是,张千丰等[35]、卢欢亮等[36]和Zhang等[22]研究者却发现低温(300~400 ℃)下产生的污泥和稻壳等生物炭均呈酸性,这表明生物炭的pH与热解温度有关。另外,升高温度有利于生物炭孔隙结构的发育,形成更大的比表面积和孔径更小的孔结构,安增莉等[37]、郎印海等[38]和Cui等[24]的研究也证实了这一点。其中,安增莉等[37]在试验中发现当热解温度从300 ℃升至600 ℃时,水稻秸秆生物炭比表面积从9.45 m2·g-1升至121.32 m2·g-1,但平均孔径由48.40 nm降至24.24 nm。
根据热解温度和生物炭制备特性的相关性分析(表 4),表明热解温度与灰分、pH等有极显著的正相关关系(P<0.01),相关系数r分别为0.970和0.992;相反,热解温度与生物炭的产率、Zeta电位、H含量及表征芳香性的H/C等有极显著负相关关系(P<0.01),相关系数r分别为-0.960、-0.957、-0.995和-0.974。这表明热解温度对生物炭的产率、灰分、pH、Zeta电位、H含量和H/C等特性的影响显著。同样地,简敏菲等[39]研究不同热解温度(300、400、500、600 ℃和700 ℃)对稻秆生物炭特性的影响,发现热解温度与产率、灰分、挥发分、pH值、元素含量(C、H、O、N)、H/C和O/C等生物炭性质有显著的相关性。

|
本研究中,三种生物炭均符合Langmuir和Freundlich模型,其中Freundlich模型拟合效果更好,表明生物炭对Cd2+的吸附过程为多分子层吸附为主[40],最大吸附量顺序依次为BC700(92.65 mg·g-1)> BC500(80.17 mg·g-1)>BC300(76.29 mg·g-1)。王俊超等[21]、林宁等[41]和Zhu等[42]在研究生物炭对重金属吸附作用时均发现Freundlich模型能较好地描述吸附过程。另外,准二级动力学模型能很好地模拟生物炭的吸附过程(表 3),说明其吸附过程是以化学吸附为主[27]。大多数学者[29, 43-44]在研究生物炭吸附重金属过程中,发现准二级动力学模型能较好地模拟吸附过程,但是,也有部分学者发现吸附过程符合准一级动力学模型[45]。
目前,有关生物炭对重金属Cd2+的吸附机制主要包括:(1)生物炭中无机矿物离子(PO43-、CO32-等)与Cd2+的沉淀作用,形成碳酸盐或磷酸盐沉淀[22, 46-47];(2)无机盐离子(K+、Ca2+、Na+、Mg2+等)或部分官能团(-COOM、-R-O-M等)与Cd2+的离子交换机制[48-49];(3)生物炭表面含氧官能团与Cd2+的螯合机制[50-51];(4)π电子(C=C、C≡C等)与Cd2+的配键作用[19, 22]。本研究中,三种生物炭的Zeta电位都低于-25 mV,表面负电荷量较大,为生物炭以静电吸附形式吸附Cd2+提供了较大的潜能。Inyang等[52]、Xu等[53]和Zhang等[22]也发现生物炭可以通过表面的负电荷与重金属产生静电吸附,这种吸附是由生物炭表面带负电荷基团与溶液中带正电荷的重金属离子之间产生静电作用,从而去除重金属离子。同时,对三种生物炭的吸附过程分析发现,-OH、C-O、C=O等含氧官能团的吸收峰发生了明显的变化(图 3),这说明大量含氧官能团参与了生物炭对重金属的吸附络合过程。Cao等[19]研究奶牛粪生物炭去除Pb2+时,发现对Pb2+的去除主要是由于生物炭上的官能团(如羧基)与Pb2+发生络合反应生成沉淀,Lu等[54]和徐楠楠等[55]研究者也同样发现了这一规律。此外,王俊超等[21]分析认为在垫料生物炭对Cd2+的吸附作用中,阳离子-π作用占主要地位,这可能是本研究中BC500和BC700吸附后在芳环特征吸收峰1600~1400 cm-1和900~700 cm-1处发生较大位移的原因。值得注意的是,很多学者在探讨生物炭对Cd2+的吸附机制时,发现生物炭灰分中的无机盐离子(PO43-和CO32-)与Cd2+的沉淀作用是重要机制之一[22, 46-47, 52],其中Zhang等[22]进一步推断沉淀物可能是CdCO3或者Cd3(PO4)2,本试验中三种生物炭的灰分含量也较高(15.49%~24.25%),在吸附Cd2+的过程中也有可能发生沉淀作用。而且,三种生物炭具有较强的碱性(pH范围为8.13~10.62),也有可能会产生Cd(OH)2沉淀物,Kim等[46]在研究不同热解温度制备芒草生物炭对水中Cd2+吸附机制时,发现沉淀作用发生程度随着水体pH值不同而变化,并用模拟方程(MINTEQ program)推算沉淀物的化学形式为Cd(OH)2。综合以上分析,香根草生物炭的吸附机制主要包括多分子层的静电吸附和络合作用,同时也可能存在沉淀作用。
本试验还发现生物炭BC700对Cd2+的吸附效果明显优于BC500和BC300,结合表 4可知热解温度与灰分、pH值和Zeta电位等表现为显著的相关性,推断原因可能是:BC700在吸附过程中发生了较强的沉淀作用、具有较多的负电荷量、较大的比表面积和较多的官能团参与了Cd2+的络合作用。而且,王震宇等[20]认为热解温度越高,生物炭的芳香性越强,供电子能力也越强,阳离子-π作用对吸附的贡献就越大,这也可能是BC700的吸附性能优于BC500和BC300的原因之一。
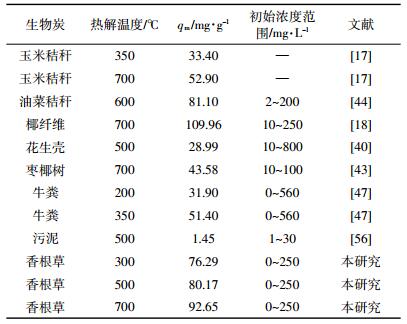
3.3 不同热解温度和原材料制备的生物炭对Cd2+的吸附能力差异不同热解温度和生物质原料制备的生物炭对Cd2+的吸附能力,往往存在着较大的差异(表 5)。李力等[17]利用农业废弃物(玉米秸杆)在350 ℃和700 ℃制备的生物炭,发现其对Cd2+的吸附量分别为33.40 mg·g-1和52.90 mg·g-1;Usman等[43]采用林业废弃物(枣椰树)制备生物炭,发现700 ℃生物炭最大吸附量43.58 mg·g-1;郑凯琪等[56]以工业废弃物(污泥)为原材料制备生物炭,发现500 ℃生物炭最大吸附量为1.45 mg·g-1。同时,一些研究者以其他废弃物为材料制备生物炭,均发现热解温度对生物炭吸附Cd2+有较为显著的影响[18, 43, 47]。本研究中,三种生物炭(BC700、BC500和BC300)对Cd2+的最大吸附量分别为92.65、80.17 mg·g-1和76.29 mg·g-1,表明香根草生物炭具有较好的重金属吸附能力,可作为一种具有应用潜力的吸附材料。
(1)随着热解温度升高,三种生物炭(BC300、BC500和BC700)的产率逐步下降,灰分含量、pH值和表面负电荷量升高,芳香性增强,比表面积逐渐增大而孔径减小。其中,温度对产率、灰分、pH、Zeta电位、H含量和H/C等生物炭特性的影响尤为显著。
(2)Freundlich模型与Langmuir模型均能较好地描述三种生物炭对Cd2+的吸附过程,但Freundlich模型更符合。其中,吸附量顺序为BC700(92.65 mg·g-1)>BC500(80.17 mg·g-1)>BC300(76.29 mg·g-1),平衡时间顺序为BC700(80 min) < BC500(180 min) < BC300(240 min),均符合准二级动力学方程,以化学吸附为主。
(3)结合SEM-EDS和FTIR等分析结果,香根草生物炭对Cd2+的吸附机制主要包括多分子层的表面静电吸附和络合作用。三种生物炭中,高温条件下制备的香根草生物炭BC700对Cd2+的吸附性能最佳,在水体重金属污染治理方面具有较强的应用潜力。
| [1] |
夏汉平, 束文圣. 香根草和百喜草对铅锌尾矿重金属的抗性与吸收差异研究[J]. 生态学报, 2001, 21(7): 1121-1129. XIA Han-ping, SHU Wen-sheng. Resistance to and uptake of heavy metals by Vetiveria zizanioides and Paspalum notatum from lead/zinc mine tailings[J]. Acta Ecologica Sinica, 2001, 21(7): 1121-1129. |
| [2] |
Pang J, Chan G S Y, Zhang J, et al. Physiological aspects of vetiver grass for rehabilitation in abandoned metal liferous mine wastes[J]. Chemosphere, 2003, 52(9): 1559-1570. DOI:10.1016/S0045-6535(03)00496-X |
| [3] |
Aibibu N, Liu Y G, Zeng G M, et al. Cadmium accumulation in Vetiveria zizanioides and its effects on growth, physiological and biochemical characters[J]. Bioresource Technology, 2010, 101(16): 6297-6303. DOI:10.1016/j.biortech.2010.03.028 |
| [4] |
马文超, 刘媛, 孙晓灿, 等. 镉在土壤-香根草系统中的迁移及转化特征[J]. 生态学报, 2016, 36(11): 3411-3418. MA Wen-chao, LIU Yuan, SUN Xiao-can, et al. Transfer and transformation characteristics of cadmium from soil to Vetiveria zizanioide[J]. Acta Ecologica Sinica, 2016, 36(11): 3411-3418. |
| [5] |
Zhang X F, Gao B, Xia H P. Effect of cadmium on growth, photosynthesis, mineral nutrition and metal accumulation of bana grass and vetiver grass[J]. Ecotoxicology and Environmental Safety, 2014, 106: 102-108. DOI:10.1016/j.ecoenv.2014.04.025 |
| [6] |
Ng C C, Law S H, Amru N B, et al. Phyto-assessment of soil heavy metal accumulation in tropical grasses[J]. Journal of Animal & Plant Sciences, 2016, 26(3): 686-696. |
| [7] |
Yang B, Shu W S, Ye Z H, et al. Growth and metal accumulation in vetiver and two Sesbania species on lead/zinc mine tailings[J]. Chemosphere, 2003, 52(9): 1593-1600. DOI:10.1016/S0045-6535(03)00499-5 |
| [8] |
Banerjee R, Goswami P, Pathak K, et al. Vetiver grass:An environment clean-up tool for heavy metal contaminated iron ore mine-soil[J]. Ecological Engineering, 2016, 90: 25-34. DOI:10.1016/j.ecoleng.2016.01.027 |
| [9] |
Gautam M, Agrawal M. Phytoremediation of metals using vetiver(Chrysopogon zizanioides(L) Roberty) grown under different levels of red mud in sludge amended soil[J]. Journal of Geochemical Exploration, 2017, 182: 218-227. DOI:10.1016/j.gexplo.2017.03.003 |
| [10] |
努扎艾提·艾比布, 刘云国, 曾光明, 等. 香根草对镉毒害的生理耐性和积累特性[J]. 环境科学学报, 2009, 29(9): 1958-1963. NUZA'AITI·Aibibu, LIU Yun-guo, ZENG Guang-ming, et al. Cadmium tolerance and accumulation characteristic of Vetiveria zizanioides[J]. Acta Scientiae Circumstantiae, 2009, 29(9): 1958-1963. |
| [11] |
徐德聪, 詹婧, 陈政, 等. 种植香根草对铜尾矿废弃地基质化学和生物学性质的影响[J]. 生态学报, 2012, 32(18): 5683-5691. XU De-cong, ZHAN Jing, CHEN Zheng, et al. Effects of Vetiveria zizanioides L. growth on chemical and biological properties of copper mine tailing wastelands[J]. Acta Ecologica Sinica, 2012, 32(18): 5683-5691. |
| [12] |
Attinti R, Barrett K R, Datta R, et al. Ethylenediaminedisuccinic acid(EDDS) enhances phytoextraction of lead by vetiver grass from contaminated residential soils in a panel study in the field[J]. Environmental Pollution, 2017, 225: 524-533. DOI:10.1016/j.envpol.2017.01.088 |
| [13] |
Lehmann J, Gaunt J, Rondon M. Biochar sequestration in terrestrial ecosystems:A review[J]. Mitigation and Adaptation Strategies for Global Change, 2006, 11(2): 395-419. |
| [14] |
马锋锋, 赵保卫, 钟金魁, 等. 牛粪生物炭对磷的吸附特性及其影响因素研究[J]. 中国环境科学, 2015, 35(4): 1156-1163. MA Feng-feng, ZHAO Bao-wei, ZHONG Jin-kui, et al. Characteristics phosphate adsorption onto biochars derived from dairy manure and its influencing factors[J]. China Environmental Science, 2015, 35(4): 1156-1163. |
| [15] |
戴静, 刘阳生. 四种原料热解产生的生物炭对Pb2+和Cd2+的吸附特性研究[J]. 北京大学学报(自然科学版), 2013, 49(6): 1075-1082. DAI Jing, LIU Yang-sheng. Adsorption of Pb2+ and Cd2+ onto biochars derived from pyrolysis of four kinds of biomasses[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2013, 49(6): 1075-1082. |
| [16] |
Li M, Lou Z J, Wang Y, et al. Alkali and alkaline earth metallic(AAEM) species leaching and Cu(Ⅱ) sorption by biochar[J]. Chemosphere, 2015, 119: 778-785. DOI:10.1016/j.chemosphere.2014.08.033 |
| [17] |
李力, 陆宇超, 刘娅, 等. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2012, 31(11): 2277-2283. LI Li, LU Yu-chao, LIU Ya, et al. Adsorption mechanisms of cadmium(Ⅱ) on biochars derived from corn straw[J]. Journal of Agro-Environment Science, 2012, 31(11): 2277-2283. |
| [18] |
楚颖超, 李建宏, 吴蔚东. 椰纤维生物炭对Cd(Ⅱ), As(Ⅲ), Cr(Ⅲ)和Cr(Ⅵ)的吸附[J]. 环境工程学报, 2015, 9(5): 2165-2170. CHU Ying-chao, LI Jian-hong, WU Wei-dong, et al. Adsorption of Cd(Ⅱ), As(Ⅲ), Cr(Ⅲ) and Cr(Ⅵ)by coconut fiber-derived biochars[J]. Chinese Journal of Environmental Engineering, 2015, 9(5): 2165-2170. DOI:10.12030/j.cjee.20150523 |
| [19] |
Cao X D, Ma L Q, Gao B, et al. Dairy-manure derived biochar effectively sorbs lead and atrazine[J]. Environmental Science & Technology, 2009, 43(9): 3285-3291. |
| [20] |
王震宇, 刘国成, MonicaXing, 等. 不同热解温度生物炭对Cd(Ⅱ)的吸附特性[J]. 环境科学, 2014, 35(12): 4735-4744. WANG Zhen-yu, LIU Guo-cheng, Monica Xing, et al. Adsorption of Cd(Ⅱ)varies with biochars derived at different pyrolysis temperatures[J]. Environmental Science, 2014, 35(12): 4735-4744. |
| [21] |
王俊超, 郑凯琪, 俞筱妍, 等. 垫料生物炭对Cd2+的吸附性能[J]. 环境工程学报, 2016, 10(11): 6655-6661. WANG Jun-chao, ZHENG Kai-qi, YU Xiao-yan, et al. Adsorption properties of Cd2+ by bedding materials derived-biochar[J]. Chinese Journal of Environmental Engineering, 2016, 10(11): 6655-6661. DOI:10.12030/j.cjee.20156028 |
| [22] |
Zhang F, Wang X, Yin D X, et al. Efficiency and mechanisms of Cd removal from aqueous solution by biochar derived from water hyacinth(Eichornia crassipes)[J]. Journal of Environmental Management, 2015, 153: 68-73. |
| [23] |
Kolodyńska D, Krukowska J, Thomas P. Comparison of sorption and desorption studies of heavy metal ions from biochar and commercial active carbon[J]. Chemical Engineering Journal, 2017, 307: 353-363. DOI:10.1016/j.cej.2016.08.088 |
| [24] |
Cui X Q, Fang S Y, Yao Y Q, et al. Potential mechanisms of cadmium removal from aqueous solution by Canna indica derived biochar[J]. Science of the Total Environment, 2016, 562: 517-525. DOI:10.1016/j.scitotenv.2016.03.248 |
| [25] |
Wang Z Y, Liu G C, Zheng H, et al. Investigating the mechanisms of biochar's removal of lead from solution[J]. Bioresource Technology, 2015, 177: 308-317. DOI:10.1016/j.biortech.2014.11.077 |
| [26] |
Azouaou N, Sadaoui Z, Djaafri A, et al. Adsorption of cadmium from aqueous solution onto untreated coffee grounds:Equilibrium, kinetics and thermodynamics[J]. Journal of Hazardous Materials, 2010, 184(1/2/3): 126-131. |
| [27] |
Hu X J, Wang J S, Liu Y G, et al. Adsorption of chromium(Ⅵ) by ethylenediamine-modified cross-linked magnetic chitosan resin:Iso-therms, kinetics and thermodynamics[J]. Journal of Hazardous Materials, 2011, 185(1): 306-314. DOI:10.1016/j.jhazmat.2010.09.034 |
| [28] |
Wang X S, Tang Y P, Tao S R. Removal of Cr(Ⅵ) from aqueous solutions by the nonliving biomass of Alligator weed:Kinetics and equilibrium[J]. Adsorption, 2008, 14(6): 823-830. DOI:10.1007/s10450-008-9145-6 |
| [29] |
吴晴雯, 孟梁, 张志豪, 等. 芦苇秸秆生物炭对水体中重金属Ni2+的吸附特性[J]. 环境化学, 2015, 34(9): 1703-1709. WU Qing-wen, MENG Liang, ZHANG Zhi-hao, et al. Adsorption behaviors of Ni2+ onto reed straw biochar in the aquatic solutions[J]. Environmental Chemistry, 2015, 34(9): 1703-1709. DOI:10.7524/j.issn.0254-6108.2015.09.2015031108 |
| [30] |
Tan X F, Liu Y G, Zeng G M, et al. Application of biochar for the removal of pollutants from aqueous solutions[J]. Chemosphere, 2015, 125: 70-85. DOI:10.1016/j.chemosphere.2014.12.058 |
| [31] |
Al-Wabel M, Al-Omran A, El-Naggar A H, et al. Pyrolysis temperature induced changes in characteristics and chemical composition of biochar produced from conocarpuswastes[J]. Bioresource Technology, 2013, 131(3): 374-379. |
| [32] |
Chen T, Zhang Y X, Wang H T, et al. Influence of pyrolysis temperature on characteristics and heavy metal adsorptive performance of biochar derived from municipal sewage sludge[J]. Bioresource Technology, 2014, 164(7): 47-54. |
| [33] |
Wang S S, Gao B, Zimmerman A R, et al. Physicochemical and sorptive properties of biochars derived from woody and herbaceous biomass[J]. Chemosphere, 2015, 134: 257-262. DOI:10.1016/j.chemosphere.2015.04.062 |
| [34] |
Yuan J H, Xu R K, Zhang H. The forms of alkalis in the biochar produced from crop residues at different temperatures[J]. Bioresource Technology, 2011, 102(3): 3488-3497. DOI:10.1016/j.biortech.2010.11.018 |
| [35] |
张千丰, 孟军, 刘居东, 等. 热解温度和时间对三种作物残体生物炭pH值及碳氮含量的影响[J]. 生态学杂志, 2013, 32(9): 2347-2353. ZHANG Qian-feng, MENG Jun, LIU Ju-dong, et al. Effects of pyrolysis temperature and duration time on pH, carbon and nitrogen contents of biochars produced from three crop residues[J]. Chinese Journal of Ecology, 2013, 32(9): 2347-2353. |
| [36] |
卢欢亮, 叶向东, 汪永红, 等. 热解温度对污泥生物炭的表面特性及重金属安全性的影响[J]. 环境工程学报, 2015, 9(3): 1433-1439. LU Huan-liang, YE Xiang-dong, WANG Yong-hong, et al. Effects of pyrolysis temperature on surface properties and heavy metal safety of sludge-derived biochar[J]. Chinese Journal of Environmental Engineering, 2015, 9(3): 1433-1439. DOI:10.12030/j.cjee.20150373 |
| [37] |
安增莉, 侯艳伟, 蔡超, 等. 水稻秸秆生物炭对Pb(Ⅱ)的吸附特性[J]. 环境化学, 2011, 30(11): 1851-1857. AN Zeng-li, HOU Yan-wei, CAI Chao, et al. Lead(Ⅱ) adsorption characteristics on different biochars derived from rice straw[J]. Environmental Chemistry, 2011, 30(11): 1851-1857. |
| [38] |
郎印海, 刘伟, 王慧. 生物炭对水中五氯酚的吸附性能研究[J]. 中国环境科学, 2014, 34(8): 2017-2023. LANG Yin-hai, LIU Wei, WANG Hui. Adsorption efficiencies of pentachlorophenol from aqueous solution onto biochars[J]. China Environmental Science, 2014, 34(8): 2017-2023. |
| [39] |
简敏菲, 高凯芳, 余厚平. 不同裂解温度对水稻秸秆制备生物炭及其特性的影响[J]. 环境科学学报, 2016, 36(5): 1757-1765. JIAN Min-fei, GAO Kai-fang, YU Hou-ping. Effects of different pyrolysis temperatures on the preparation and characteristics of biochar from rice straw[J]. Acta Scientiae Circumstantiae, 2016, 36(5): 1757-1765. |
| [40] |
程启明, 黄青, 刘英杰, 等. 花生壳与花生壳生物炭对镉离子吸附性能研究[J]. 农业环境科学学报, 2014, 33(10): 2022-2029. CHENG Qi-ming, HUANG Qing, LIU Ying-jie, et al. Adsorption of cadmium(Ⅱ)on peanut shell and its biochar[J]. Journal of Agro-Environment Science, 2014, 33(10): 2022-2029. DOI:10.11654/jaes.2014.10.020 |
| [41] |
林宁, 张晗, 贾珍珍, 等. 不同生物质来源生物炭对Pb(Ⅱ)的吸附特性[J]. 农业环境科学学报, 2016, 35(5): 992-998. LIN Ning, ZHANG Han, JIA Zhen-zhen, et al. Adsorption of Pb(Ⅱ)by biochars derived from three types of biomass[J]. Journal of Agro-Environment Science, 2016, 35(5): 992-998. DOI:10.11654/jaes.2016.05.025 |
| [42] |
Zhu Q H, Wu J, Wang L L, et al. Adsorption characteristics of Pb2+ onto wine lees-derived biochar[J]. Bulletin of Environmental Contamination and Toxicology, 2016, 97(2): 294-299. DOI:10.1007/s00128-016-1760-4 |
| [43] |
Usman A, Sallam A, Zhang M, et al. Sorption process of date palm biochar for aqueous Cd(Ⅱ) removal:Efficiency and mechanisms[J]. Water, Air, & Soil Pollution, 2016, 227(12): 449. |
| [44] |
Li B, Yang L, Wang C Q, et al. Adsorption of Cd(Ⅱ) from aqueous solutions by rape straw biochar derived from different modification processes[J]. Chemosphere, 2017, 175: 332-340. DOI:10.1016/j.chemosphere.2017.02.061 |
| [45] |
陈再明, 方远, 徐义亮, 等. 水稻秸秆生物炭对重金属Pb2+的吸附作用及影响因素[J]. 环境科学学报, 2012, 32(4): 769-776. CHEN Zai-ming, FANG Yuan, XU Yi-liang, et al. Adsorption of Pb2+ by rice straw derived-biochar and its influential factors[J]. Acta Scientiae Circumstantiae, 2012, 32(4): 769-776. |
| [46] |
Kim W K, Shim T, Kim Y S, et al. Characterization of cadmium removal aqueous solutions by biochar produced from a giant Miscanthus at different pyrolytic temperatures[J]. Bioresource Technology, 2013, 138(2): 266-270. |
| [47] |
Xu X Y, Cao X, Zhao L, et al. Removal of Cu, Zn, and Cd from aqueous solutions by the dairy manure-derived biochar[J]. Environmental Science and Pollution Research, 2013, 20(1): 358-368. DOI:10.1007/s11356-012-0873-5 |
| [48] |
Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+ sorption mechanisms by sludge-derived biochar[J]. Water Research, 2012, 46(3): 854-862. DOI:10.1016/j.watres.2011.11.058 |
| [49] |
Ahmad M, Rajapaksha A U, Lim J E, et al. Biochar as a sorbent for contaminant management in soil and water:A review[J]. Chemosphere, 2014, 99(3): 19-33. |
| [50] |
Sun J K, Lian F, Liu Z Q, et al. Biochars derived from various crop straws:Characterization and Cd(Ⅱ) removal potential[J]. Ecotoxicology and Environmental safety, 2014, 106(2): 226-231. |
| [51] |
Wan S L, Ma Z Z, Xue Y, et al. Sorption of lead(Ⅱ), cadmium(Ⅱ), and copper(Ⅱ) ions from aqueous solutions using tea waste[J]. Industrial & Engineering Chemistry Research, 2014, 53(9): 3629-3635. |
| [52] |
Inyang M, Gao B, Wenchuan D, et al. Enhanced lead sorption by biochar derived from anaerobically digested sugarcane bagasse[J]. Separation Science & Technology, 2011, 46(12): 1950-1956. |
| [53] |
Xu X Y, Schierz A, Xu N, et al. Comparison of the characteristics and mechanisms of Hg(Ⅱ) sorption by biochars and activated carbon[J]. Journal of Colloid and Interface Science, 2016, 463: 55-60. DOI:10.1016/j.jcis.2015.10.003 |
| [54] |
Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+ sorption mechanisms by sludge-derived biochar[J]. Water Research, 2011, 46(3): 854-862. |
| [55] |
徐楠楠, 林大松, 徐应明, 等. 玉米秸秆生物炭对Cd2+的吸附特性及影响因素[J]. 农业环境科学学报, 2014, 33(5): 958-964. XU Nan-nan, LIN Da-song, XU Ying-ming, et al. Adsorption of aquatic Cd2+ by biochar obtained from corn stover[J]. Journal of Agro-Environment Science, 2014, 33(5): 958-964. DOI:10.11654/jaes.2014.05.019 |
| [56] |
郑凯琪, 王俊超, 刘姝同, 等. 不同热解温度污泥生物炭对Pb2+, Cd2+的吸附特性[J]. 环境工程学报, 2016, 10(12): 7277-7282. ZHENG Kai-qi, WANG Jun-chao, LIU Shu-tong, et al. Adsorption characteristic of Pb2+ and Cd2+ with sludge biochars derived at different pyrolysis temperatures[J]. Chinese Journal of Environmental Engineering, 2016, 10(12): 7277-7282. DOI:10.12030/j.cjee.201507083 |
 2018, Vol. 37
2018, Vol. 37