文章信息
- 刘锦嫦, 熊双莲, 马烁, 高菲, 涂书新
- LIU Jin-chang, XIONG Shuang-lian, MA Shuo, GAO Fei, TU Shu-xin
- 硒砷交互作用对水稻幼苗生理特性及砷硒累积的影响
- Interactive effects of selenite and arsenite on physiological characteristics and accumulation of arsenic and selenium in rice seedlings
- 农业环境科学学报, 2018, 37(3): 423-430
- Journal of Agro-Environment Science, 2018, 37(3): 423-430
- http://dx.doi.org/10.11654/jaes.2017-1157
文章历史
- 收稿日期: 2017-08-24
- 录用日期: 2017-12-01
2. 华中农业大学微量元素研究中心, 武汉 430070;
3. 土壤环境与污染修复湖北省重点实验室, 武汉 430070
2. Research Centre of Trace Elements, Huazhong Agricultural University, Wuhan 430070, China;
3. Hubei Key Laboratory of Soil Environment and Pollution Remediation, Wuhan 430070, China
硒(Se)是人和动物必需的营养元素,世界上大约有10亿的人口缺硒,中国约72%的土地缺硒[1]。谷物及其产品是人体摄入硒的主要来源之一,通过施用外源硒肥生产富硒大米是解决人体缺硒的有效措施[2]。硒亦为植物生长的有益元素,适量硒可以提高植物抵抗逆境胁迫的能力,降低植物对重金属的吸收累积[3-4]。
砷(As)是环境中普遍存在的一种毒性较强的致癌物质,对动植物均具有毒害作用。水稻是我国主要的粮食作物之一,较其他谷物具有更强的吸收累积砷的能力[5]。我国南方一些矿区周边稻田中存在不同程度的土壤砷污染[6-8]。有调查表明砷污染稻田稻米中硒含量与砷含量呈负相关[9];将富硒土壤上生长的芥菜施入到土壤中降低了水稻植株及稻米中砷的含量,但对稻米硒含量的影响不清楚[10]。关于水稻硒砷交互作用对水稻砷和硒吸收累积的影响已有少量报道[11-12],但砷或硒处理浓度比较单一、研究结论不一致[12-13]。例如Hu等[13]研究了1 μmol·L-1硒与1 μmol·L-1砷的交互作用,表明硒或砷处理仅降低水稻地上部砷或硒含量,对根中两元素含量有促进作用;而Kumar等[12]对25 μmol·L-1硒和25 μmol·L-1砷交互作用的研究则表明硒降低水稻根和地上部砷的含量,砷则提高根和地上部硒的含量。硒对植物生长表现出双重作用,即低浓度促进、高浓度抑制[14]。目前虽有研究探讨了硒缓解水稻砷毒害的机理[12, 15],但均是在高砷(25 μmol·L-1)和高硒(25 μmol·L-1)条件下,如此高的硒水平在单独施用时已对作物产生了毒害[12],在实际生产中并不可取。因此系统研究不同浓度的硒与砷交互作用对水稻生长和砷、硒累积的影响及机理对于水稻富硒、降砷有十分重要的意义。
淹水条件下,土壤中砷和硒主要以三价砷和四价硒的形态存在[16]。本文系统研究了不同水平的三价砷和四价硒处理条件下,硒和砷单独及联合处理对水稻幼苗砷和硒累积及抗氧化系统的影响,探讨硒砷相互作用的机理,旨在为水稻降砷、富硒提供参考。
1 材料与方法 1.1 供试材料及幼苗培养供试水稻品种为广两优272,由湖北省农业科学院粮食作物研究所选育。水稻种子经消毒(10%过氧化氢)、清洗、浸泡、萌发后,置于可控光培养室培育5 d,其培养液用1/4国际水稻研究所(IRRI)推荐的配方营养液。选择长势一致的水稻幼苗移栽到塑料盒中(规格28 cm×20 cm×8 cm),每盒移植48株水稻幼苗,用100%水稻营养液培育10 d。用KOH和HCl调节pH为5.5~6.0。可控光生长室条件:14 h的光照(260~350 μmol·m-2·s-1),白天温度为28 ℃,夜间为20 ℃,相对湿度为60%~70%。
1.2 试验方法考虑生产实际中硒的施用浓度不宜过高,硒的试验浓度设计原则为单独处理时对作物生长不产生毒害作用。砷的试验浓度设计则考虑了低砷水平(不产生毒害作用)和高砷水平(产生明显毒害作用)。在参考文献[12]和[15]并进行预备试验的基础上,本研究砷浓度设为0、5、25 μmol·L-1 As(NaAsO2),硒浓度设为0、1、5、10 μmol·L-1 Se(Na2SeO3),采用随机完全区组设计,共12个处理,分别用CK、As5、As25、Se1、Se5、Se10、As5Se1、As5Se5、As5Se10、As25Se1、As25Se5、As25Se10表示,每处理3次重复。选择生长一致的幼苗进行砷和硒处理,期间每周更换2次营养液,处理2周后进行收获。水稻幼苗先用自来水冲洗,再用去离水冲洗3遍,将地上部与根部剪开,分别测量根部和地上部鲜重。然后将根和叶片平均分成两份,取一份根和叶片放在-80 ℃超低温冰箱保存,用于测定抗氧化系统等指标,另一份样品在105 ℃杀青15 min,70 ℃烘干、研磨后,用于测定砷和硒的含量,并计算转运系数(水稻地上部As或Se含量与根中As或Se含量的比值)。
1.3 测定方法砷和硒含量测定:植物样品经硝酸-高氯酸(4:1)消解后,用原子荧光光度计(AFS8220,北京吉天仪器公司,中国)检测[17]。采用标准物质灌木枝叶GBW 07602(GSV-1)进行分析质量控制。
超氧化物歧化酶(SOD)活性测定采用氮蓝四唑(NBT)光还原比色法,过氧化物酶(POD)活性测定采用愈创木酚比色法,过氧化氢酶(CAT)活性测定采用过氧化氢分解法,丙二醛(MDA)含量测定采用TBA比色法[18]。谷胱甘肽过氧化物酶(GPx)活性测定参考黄爱缨等[19]的方法。谷胱甘肽(GSH)、非蛋白巯基物质(NPT)及植物络合素(PCs)含量测定采用比色法[20]。
1.4 数据分析采用Genstat 18th Edition统计软件对试验数据进行双因素方差分析及多重比较。采用Sigma Plot 10.0进行绘图。
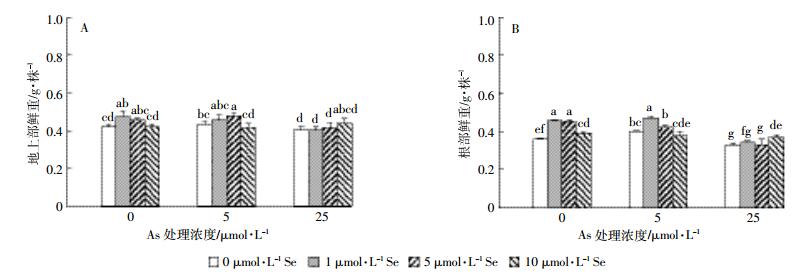
2 结果与分析 2.1 硒砷交互作用对水稻幼苗生长的影响图 1结果表明砷处理显著影响了水稻的生长(P < 0.05),表现为低浓度促进、高浓度抑制:As5处理地上部和根部鲜重分别较对照增加了3.1%和10.8%,As25处理较对照分别降低了4.8%和8.3%。低浓度硒处理显著促进了水稻幼苗的生长(P < 0.05):Se1处理地上部和根部鲜重分别比对照增加了11.9%和27.8%,Se5则分别增加了9.5%和25%(图 1)。
|
| 不同字母表示不同处理间差异显著(P<0.05),下同 Different letters indicate significant differences among the treatment(P < 0.05). The same below 图 1 砷和硒处理14 d水稻幼苗地上部(A)和根部(B)鲜重 Figure 1 The fresh weight of shoots(A) and roots(B) of rice seedlings treated with different level of As and Se for 14 d |
砷和硒对水稻根部(P < 0.01)和地上部(P < 0.01)鲜重的影响有显著交互作用。低浓度砷处理(5 μmol·L-1)条件下,≤5 μmol·L-1低硒处理对水稻幼苗生长有协同促进作用,其地上部和根部鲜重约是不加硒处理的1.05~1.18倍。高浓度砷处理(25 μmol·L-1)条件下地上部和根部鲜重随着硒处理浓度增加而升高,到10 μmol·L-1硒处理时达到最大值,是不加硒处理的1.09倍和1.12倍,由此说明高硒处理可以拮抗高砷胁迫对水稻生长的抑制作用。
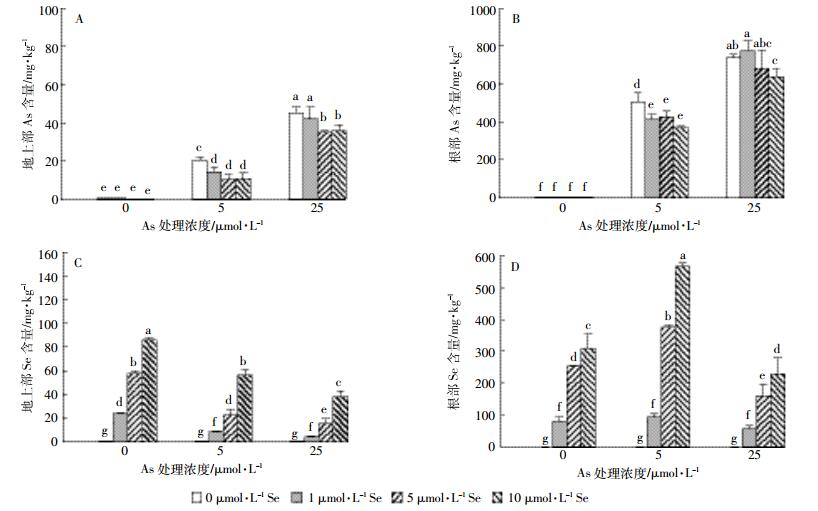
2.2 硒砷交互作用对水稻幼苗砷和硒吸收累积的影响图 2A、图 2B结果表明,除As25Se1处理外,添加硒处理显著降低了地上部和根部砷含量(P<0.05),由此说明适宜浓度的硒对水稻砷吸收存在拮抗作用。水稻地上部和根部砷含量As5Se1、As5Se5、As5Se10处理分别是As5处理的69.3%、49.4%、52.7%和81.8%、84.1%、72.5%;As25Se10处理分别是As25处理的79.1%和86.3%(图 2A、图 2B)。添加硒使低砷和高砷处理水稻砷的转运系数由0.041和0.062分别降至0.024~0.034和0.053~0.057,由此说明硒处理抑制了砷向地上部的转运。
|
| 图 2 砷和硒处理14 d水稻幼苗地上部和根部砷(A、B)和硒(C、D)的含量 Figure 2 The As(A, B) and Se(C, D) content in shoots and roots of rice seedlings treated with different level of As and Se for 14 d |
砷处理对水稻地上部硒的含量产生了拮抗作用(图 2C、图 2D)。低砷(5 μmol·L-1As)和高砷(25 μmol·L-1 As)处理水稻地上部硒的含量仅分别为不加砷处理的35.8%~65.3%和17.2%~44.3%(图 2C)。与地上部不同,水稻根部硒的含量则是随着砷浓度的增加呈现先升高后降低的趋势:低砷(5 μmol·L-1As)处理水稻根部硒含量为不加砷处理的1.16~1.77倍,高砷(25 μmol·L-1 As)处理则为不加砷处理的63.2%~74.1%(图 2D)。砷处理同样抑制了硒向水稻地上部的转移:Se1、Se5和Se10处理水稻硒的转运系数分别为0.30、0.25和0.28,添加砷处理分别为不加砷处理的25%~30%、26%~42%和36%~60%。
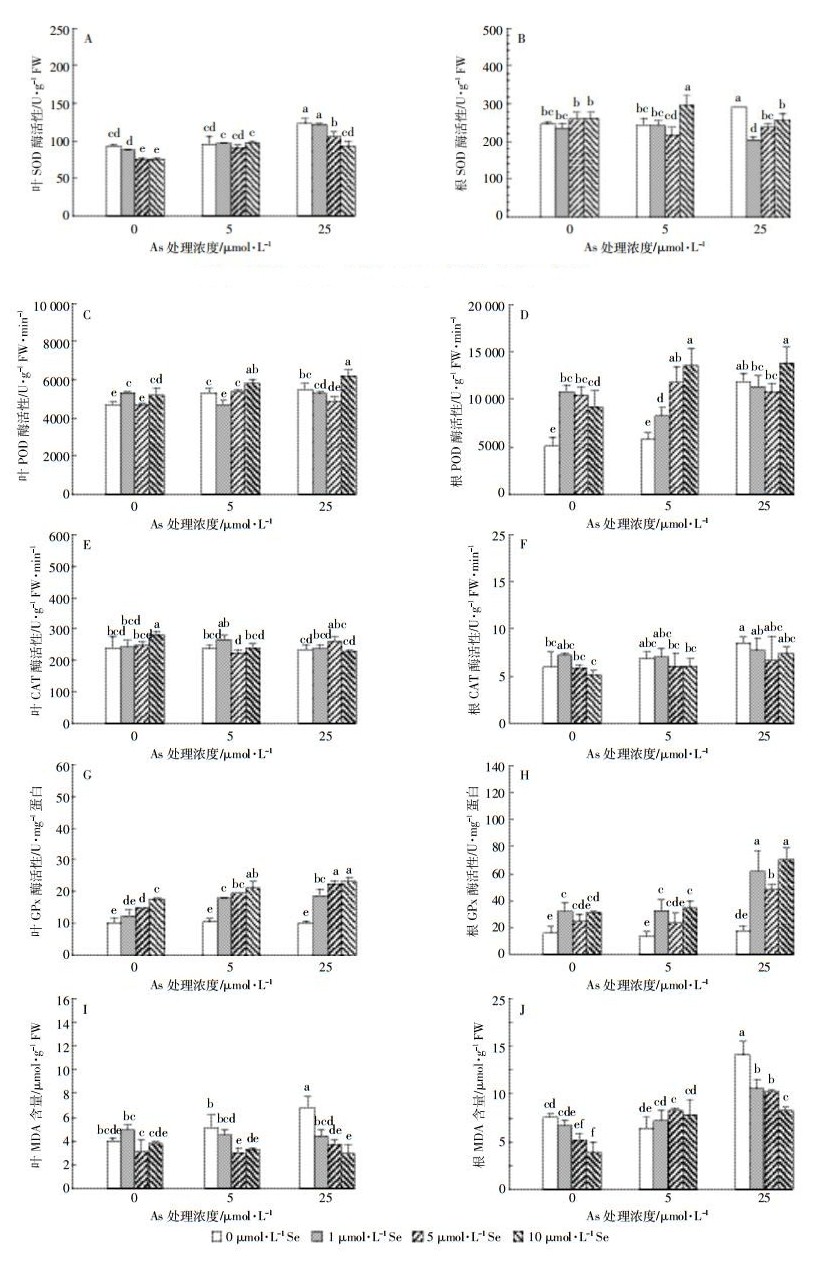
2.3 硒砷交互作用对水稻幼苗抗氧化系统及巯基化合物含量的影响图 3结果表明单独砷处理条件下,低浓度砷(5 μmol·L-1)处理对水稻抗氧化酶活性和MDA含量均无显著影响(P>0.05);高浓度砷(25 μmol·L-1)处理则显著提高了水稻叶片和根中SOD酶、POD酶活性及MDA含量(P < 0.05),分别是不加砷处理的1.32倍和1.18倍(图 3A、图 3B)、2.23倍和1.17倍(图 3C、图 3D)及1.71倍和1.87倍(图 3E、图 3F)。
|
| 图 3 砷和硒处理14 d水稻幼苗叶(A、C、E、G、I)和根(B、D、F、H、J)中SOD、POD、CAT、GPx酶活性及MDA含量 Figure 3 The activities of SOD, POD, CAT and GPx as well as the content of MDA in leaves(A, C, E, G, I) and roots(B, D, F, H, J) of rice seedlings treated with different level of As and Se for 14 d |
硒和砷处理对水稻幼苗抗氧化酶活性和MDA含量产生了显著的交互作用。同一砷水平下,硒处理显著提高了水稻幼苗叶和根中GPx活性,且叶中GPx活性随着硒处理浓度增加而升高;砷与硒交互作用对水稻根部和叶片中GPx活性具有显著的协同促进作用(P<0.05)(图 3G、图 3H)。低砷条件下,硒显著降低了叶中MDA含量(图 3I),但对根中MDA含量无显著影响(图 3J)。高砷条件下,硒处理降低了水稻叶片和根中SOD酶活性,约为不加硒处理的70%~89%(图 3A、图 3B);水稻叶和根中POD酶活性随着硒处理浓度的增加先降低后增高,在Se10时达到最大值,显著高于无Se和低Se处理(图 3C、图 3D)。添加硒亦显著降低高砷处理水稻叶片和根中MDA含量,且随着硒处理浓度的增加MDA含量逐渐降低。As25Se1、As25Se5、As25Se10处理叶片和根中MDA含量分别是As25处理的64.7%、54.7%、43.6%(图 3I)和75.1%、72.1%、58.4%(图 3J)。
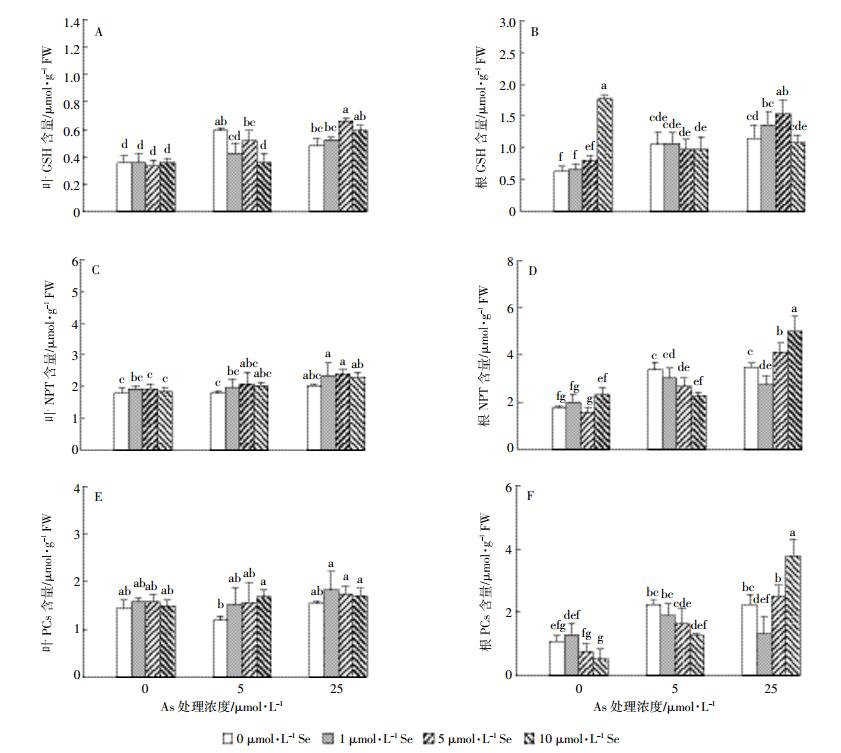
图 4结果表明,单独砷处理显著增加了水稻根中GSH、NPT、PCs及叶中GSH的含量(P<0.05),但对叶中NPT和PCs含量无显著影响(P>0.05)。低砷处理(5 μmol·L-1)下,加硒降低了水稻叶片GSH含量、但对根部无显著影响;高砷处理(25 μmol·L-1)下,水稻叶和根部GSH含量随着硒处理浓度的增加呈现先升高后降低趋势,在Se5达到最大值(图 4A,图 4B)。水稻根中NPT和PCs含量在低砷条件下随着硒处理浓度的增加而降低,高砷条件下则随着硒浓度的增加呈先降低后升高趋势,在10 μmol·L-1硒处理时达到最大值(图 4D,图 4F)。
|
| 图 4 砷和硒处理14 d水稻幼苗叶(A、C、E)和根(B、D、F)GSH、NPT和PCs含量 Figure 4 The GSH, NPT and PC scontent in leaves(A, C, E) and roots(B, D, F) of rice seedlings treated with different level of As and Se for 14 d |
三价砷和四价硒均可通过硅转运蛋白OsNIP2;1进入水稻植株[21-22],因此理论上硒和砷交互对水稻砷和硒的累积存在拮抗作用。我们的结果也证实适量的硒或砷可以拮抗水稻对砷或硒的吸收和转运,且砷处理浓度越高,产生显著抑制作用所需硒的浓度亦越高(图 2)。Chauhan等[15]研究表明25 μmol·L-1 As处理条件下5~20 μmol·L-1 Se处理显著抑制了水稻对砷的吸收,本研究的结果(≥5 μmol·L-1 Se)与其相类似。
砷处理抑制水稻地上部的硒含量,但低浓度砷(5 μmol·L-1 As)处理显著增加幼苗根部硒的含量(图 2),这一结果与Hu等[13]1 μmol·L-1 As处理的研究结果相类似,其原因可能是一方面四价硒除了利用硅转运蛋白OsNIP2;1外,还可以通过磷酸转运体被植物吸收[23],导致低浓度砷对水稻吸收硒的抑制作用有限;另一方面低砷处理显著促进了根系生长(图 1),从而可能提高了根对硒的吸收能力。四价硒被植物吸收后通常在根部转化为有机硒而留在根部,Hu等[13]研究发现砷处理提高了水稻根部SeMet的含量,这可能是导致硒在水稻幼苗根部累积及地上部降低的另一个原因。具体原因还需要从砷对硒的吸收动力学及硒转运蛋白基因表达等方面进一步深入研究。
砷对植物生长的影响与其剂量有关。高砷处理抑制了水稻生长,对其造成了氧化胁迫、提高了细胞膜脂过氧化产物MDA含量(图 1、图 3)。SOD、POD、CAT及GPx是一类重要的抗氧化酶,它们在清除重金属诱导产生的氧自由基和过氧化物、抑制膜质过氧化、保护细胞免遭伤害等方面起着重要的作用。硫醇化合物在植物缓解砷的毒害及耐受性中发挥重要作用:GSH是一种抗氧化剂,同时As(Ⅲ)与GSH、PC等多肽的巯基络合后贮存在液泡中可以降低砷对植物的毒害作用[24-25]。Kumar等[12]研究发现高硒处理(25 μmol·L-1 Se)提高了砷胁迫处理水稻幼苗抗坏血酸过氧化物酶(APX)、CAT和GPx的活性及GSH和PCs的含量,硒通过调节抗氧化酶活性及巯基化合物的含量来缓解砷诱导的氧化胁迫。我们的研究发现1~10 μmol·L-1 Se处理均可显著缓解高砷诱导的氧化胁迫,且随硒处理浓度增加,缓解作用增强(图 3)。与Kumar等[12]研究结果稍有不同的是,高砷胁迫下,低硒处理(1~5 μmol·L-1 Se)仅显著增加了幼苗GPx活性和GSH含量,对POD和CAT酶活性及NPT和PCs含量无显著影响。硒是GPx的成分,相关分析表明硒与叶中GPx活性有正相关(r=0.373*),由此推测加硒后水稻幼苗GPx活性的显著增加在缓解砷诱导的氧化胁迫中发挥着重要作用。随着硒处理浓度提高,10 μmol·L-1 Se处理不仅显著提高了GPx活性,还显著增加了POD酶活性及NPT和PCs含量,进一步增强了抑制高砷诱导的氧化胁迫的作用,降低砷的毒害作用。
综上所述,适量的硒可以促进水稻的生长、且硒与砷交互作用对水稻地上部砷和硒累积存在拮抗作用,因此在砷污染的农田可以考虑使用硒肥来降低砷的含量、提高硒的含量。由于本研究是在溶液培养条件下进行的,还需要进一步进行全生育期盆栽和大田试验,并进行安全评估,以确定不同砷污染程度的土壤中硒肥的最佳用量,达到既可以降低稻米砷含量、提高硒含量,又不会产生负面影响(如稻米中硒含量过高)的目的。
4 结论(1)低硒(≤5 μmol·L-1 Se)和低砷(5 μmol·L-1 As)交互作用对水稻生长有协同促进作用;高硒(10 μmol·L-1 Se)处理可以显著拮抗高砷(25 μmol·L-1 As)胁迫对水稻生长的抑制作用。
(2)硒对水稻砷的吸收和转运有拮抗作用,但高砷胁迫下产生显著抑制作用所需的硒浓度相应提高;砷显著抑制硒向水稻地上部转运和累积,但对根部硒的含量影响表现为低砷促进、高砷抑制。
(3)高砷胁迫下,硒显著抑制了水稻幼苗细胞膜的过氧化作用,且抑制作用随着硒处理水平提高而增强;硒砷交互对水稻幼苗谷胱甘肽过氧化物酶活性有协同促进作用。
| [1] |
Chen L, Yang F, Xu J, et al. Determination of selenium concentration of rice in China and effect of fertilization of selenite and selenate on selenium content of rice[J]. Journal of Agricultural and Food Chemistry, 2002, 50(18): 5128-5130. DOI:10.1021/jf0201374 |
| [2] |
Boldrin P F, Faquin V, Ramos S J, et al. Soil and foliar application of selenium in rice biofortification[J]. Journal of Food Composition and Analysis, 2013, 31(2): 238-244. DOI:10.1016/j.jfca.2013.06.002 |
| [3] |
Liao G J, Xu Y, Chen C, et al. Root application of selenite can simultaneously reduce arsenic and cadmium accumulation and maintain grain yields, but show negative effects on the grain quality of paddy rice[J]. Journal of Environmental Management, 2016, 183(Pt3): 733-741. |
| [4] |
Wan Y A, Yu Y, Wang Q, et al. Cadmium uptake dynamics and translocation in rice seedling:Influence of different forms of selenium[J]. Ecotoxicology and Environmental Safety, 2016, 133: 127-134. DOI:10.1016/j.ecoenv.2016.07.001 |
| [5] |
Williams P N, Villada A, Deacon C, et al. Greatly enhanced arsenic shoot assimilation in rice leads to elevated grains levels compared to wheat and barley[J]. Environmental Science & Technology, 2017, 42(19): 6854-6859. |
| [6] |
Fu Y G, Chen M L, Bi X Y, et al. Occurrence of arsenic in brown rice and its relationship to soil properties from Hainan Island, China[J]. Environmental Pollution, 2011, 159(7): 1757-1762. DOI:10.1016/j.envpol.2011.04.018 |
| [7] |
Lu X W, Zhang X L. Environmental geochemistry study of arsenic in Western Hunan mining area, P. R. China[J]. Environmental Geochemistry and Health, 2005, 27(4): 313-320. DOI:10.1007/s10653-004-5735-8 |
| [8] |
Wei C Y, Wang C, Yang L S. Characterizing spatial distribution and sources of heavy metals in the soils from mining-smelting activities in Shuikoushan, Hunan Province, China[J]. Journal of Environmental Sciences, 2009, 21(9): 1230-1236. DOI:10.1016/S1001-0742(08)62409-2 |
| [9] |
Williams P N, Islam S, Islam R, et al. Arsenic limits trace mineral nutrient(selenium, zinc, and nickel) in Bangladesh rice grain[J]. Environmental Science & Technology, 2009, 43(21): 8430-8436. |
| [10] |
Kaur S, Singh D, Singh K. Effect of selenium application on arsenic uptake in rice(Oryza sativa L.)[J]. Environmental Monitoring and Assessment, 2017, 189(9): 430. DOI:10.1007/s10661-017-6138-5 |
| [11] |
胡莹, 黄益宗, 刘云霞. 砷-硒交互作用对水稻吸收转运砷和硒的影响[J]. 环境化学, 2013, 32(6): 952-958. HU Ying, HUANG Yi-zong, LIU Yun-xia. Interactions between arsenic and selenium uptake and translocation in rice(Oryza sativa L.) seedlings[J]. Environmental Chemistry, 2013, 32(6): 952-958. DOI:10.7524/j.issn.0254-6108.2013.06.005 |
| [12] |
Kumar A, Singh R P, Singh P K, et al. Selenium ameliorates arsenic induced oxidative stress through modulation of antioxidant enzymes and thiols in rice(Oryza sativa L.)[J]. Ecotoxicology, 2014, 23(7): 1153-1163. DOI:10.1007/s10646-014-1257-z |
| [13] |
Hu Y, Duan G L, Huang Y Z, et al. Interactive effects of different inorganic As and Se species on their uptake and translocation by rice(Oryza sativa L.) seedlings[J]. Environmental Science and Pollution Research International, 2014, 21(5): 3955-3962. DOI:10.1007/s11356-013-2321-6 |
| [14] |
Feng R W, Tu S X. The roles of selenium in protecting plants against abiotic stresses[J]. Environmental and Experimental Botany, 2013, 87: 58-68. DOI:10.1016/j.envexpbot.2012.09.002 |
| [15] |
Chauhan R, Awasthi S, Tripathi P, et al. Selenite modulates the level of phenolics and nutrient element to alleviate the toxicity of arsenite in rice(Oryza sativa L.)[J]. Ecotoxicology and Environmental Safety, 2017, 138(2): 47-55. |
| [16] |
张均华, 朱练峰, 禹盛苗, 等. 稻田硒循环转化与水稻硒营养研究进展[J]. 应用生态学报, 2012, 23(10): 2900-2906. ZHANG Jun-hua, ZHU Lian-feng, YU Sheng-miao, et al. Selenium cycling and transformation in paddy field and selenium nutrition of rice:A review[J]. Chinese Journal of Applied Ecology, 2012, 23(10): 2900-2906. |
| [17] |
Han D, Xiong S L, Tu S X, et al. Interactive effects of selenium and arsenic on growth, antioxidant system, arsenic and selenium species of Nicotianatabacum L[J]. Environmental and Experimental Botany, 2015, 117: 12-19. DOI:10.1016/j.envexpbot.2015.04.008 |
| [18] |
王学奎. 植物生理生化实验原理和技术[M]. 二版. 北京: 高等教育出版社, 2006, 167-173, 280. WANG Xue-kui. Plant physiological and biochemical experimental principles and techniques[M]. The second edition. Beijing: Higher Education Press, 2006, 167-173, 280. |
| [19] |
黄爱缨, 吴珍龄. 水稻谷胱甘肽过氧化物酶的测定法[J]. 西南农业大学学报, 1999, 21(4): 324-327. HUANG Ai-ying, WU Zhen-ling. Determination of glutathione peroxidase in rice seedlings[J]. Journal of Southwest Agricultural University, 1999, 21(4): 324-327. |
| [20] |
梁程, 林匡飞, 张雯, 等. 不同浓度硫处理下硒镉交互胁迫对水稻幼苗的生理特性影响[J]. 农业环境科学学报, 2012, 31(5): 857-866. LIANG Cheng, LIN Kuang-fei, ZHANG Wen, et al. Effects of sulfur and selenium treatment on plant growth and some physiological characteristics of rice under cadmium stress[J]. Journal of Agro-Environmental Science, 2012, 31(5): 857-866. |
| [21] |
Ma J F, Yamaji N, Mitani N, et al. Transporters of arsenite in rice and their role in arsenic accumulation in rice grain[J]. Proceedings of the National Academy Science U S A, 2008, 105(29): 9931-9935. DOI:10.1073/pnas.0802361105 |
| [22] |
Zhao X Q, Mitani N, Yamaji N, et al. Involvement of silicon influx transporter OsNIP2;1 in selenite uptake in rice[J]. Plant Physiology, 2010, 153(4): 1871-1877. DOI:10.1104/pp.110.157867 |
| [23] |
Li H F, McGrath S P, Zhao F J. Selenium uptake, translocation and speciation in wheat supplied with selenate or selenite[J]. New Phytologist, 2008, 178(1): 92-102. DOI:10.1111/j.1469-8137.2007.02343.x |
| [24] |
刘艳丽, 徐莹, 杜克兵, 等. 无机砷在植物体内的吸收和代谢机制[J]. 应用生态学报, 2012, 23(3): 842-848. LIU Yan-li, XU Ying, DU Ke-bing, et al. Absorption and metabolism mechanisms of inorganic arsenic in plants:A review[J]. Chinese Journal of Applied Ecology, 2012, 23(3): 842-848. |
| [25] |
Srivastava S, Mishra S, Tripathi R D, et al. Phytochelatins and antioxidant systems respond differentially during arsenite and arsenate stress in Hydrillaverticillata(L. f.) Royle[J]. Environmental Science & Technology, 2007, 41(8): 2930-2936. |
 2018, Vol. 37
2018, Vol. 37




