2. 农业农村部环境保护科研监测所, 天津 300191;
3. 农业农村部农产品质量安全环境因子控制重点实验室, 天津 300191;
4. 济南市农产品质量检测中心, 济南 250316
2. Agro-Environmental Protection Institute of Ministry of Agriculture and Rural Affairs, Tianjin 300191, China;
3. Key Laboratory for Environmental Factors Control of Agro-product Quality Safety, Ministry of Agriculture and Rural Affairs, Tianjin 300191, China;
4. Test Center for Agri-products Quality of Ji′nan, Ji′nan 250316, China
设施蔬菜田土壤中农药残留是影响我国产地环境健康及可持续发展的重要问题。2013年我国设施蔬菜种植面积和总产量分别达370万hm2和2.5亿t, 占蔬菜种植面积的18%和蔬菜总产量的34%以上[1]。番茄和黄瓜是我国设施蔬菜的主要品种, 其产量均位居世界首位。联合国粮农组织2017年统计数据显示, 我国黄瓜种植面积为123.7万hm2, 产量为0.65亿t, 占世界总产量的77%;我国番茄种植面积为103.3万hm2, 产量为0.60亿t, 占世界总产量的33%。
近年来, 由于设施蔬菜田复种指数高、温湿度高及病虫草害产生抗药性等因素, 农业有害生物危害日益严重, 为保证蔬菜的稳产和高产, 农药使用频次不断升高、用量增大[2]。这种情况导致农药在土壤中的蓄积, 并且直接威胁蚯蚓等土壤动物的生存, 进而影响农田的可持续利用[3]。蚯蚓是农田生态系统土壤物质循环中的重要一环, 其对农药残留的敏感性使得它可以作为陆生生态系统危害程度的理想指示生物, 给土壤环境质量退化提供早期预警[4]。蚯蚓作为指示生物可表征农药对土壤中非靶标生物的影响[5]。
为保障重要土壤生物生存和繁殖、土壤生态价值和功能不受影响, 确保土壤生态系统中土壤资源的可持续性, 我国于2017年发布农药对土壤生物的环境风险评估指南(NY/T 2882.8—2017), 实现农药施用对包括蚯蚓和土壤微生物在内的土壤生物的急性和慢性风险评估。该指南采用风险商值(RQ)法对土壤残余农药作用于蚯蚓的急性风险进行表征[6]。风险商值(Risk Quotient, RQ)法是表征农药对蚯蚓风险的重要方法, 根据效应评价阶段得到的毒性终点值和暴露评价阶段得到的暴露浓度值进行风险商值计算[7]。风险商值法是评估农药对蚯蚓急性风险的有效方法, 已在欧盟[8]、OECD[7]和我国[6]农药管理及对蚯蚓的风险评价中得到认可和应用。然而, 目前在表征风险时, 多使用预测暴露浓度(Predicted exposure concentration, PEC, 通过保守假设模型计算获得)与预测无效浓度(Predicted no-effect concentrations, PNEC)进行比较。而更接近于真实情况的研究方法正在兴起, 如应用实测田间土壤农药残留浓度对蚯蚓风险进行评价。在捷克, 已用土壤实测农药残留浓度结合PNEC计算风险商值, 继而表征农药对蚯蚓的风险[8], 这更接近于田间实际风险, 结果表明35%的监测点位中耕地土壤农药残留对蚯蚓的风险不可接受(RQ≥1)。
噻虫嗪、噻虫胺、噻唑膦、吡虫啉、多菌灵、阿维菌素是我国设施蔬菜田常用农药品种, 高毒农药克百威(代谢物三羟基克百威)和甲基异柳磷虽已被禁止在蔬菜田使用[9], 然而目前产地环境土壤中仍有克百威检出[10], 并且甲基异柳磷也存在非法隐性添加的情况[11]。为了表征上述农药土壤残留对蚯蚓的危害风险, 本研究在山东省选择代表性设施蔬菜种植区, 在作物产中、产后、后茬产中取样监测黄瓜和番茄土壤中上述农药残留水平, 并通过风险商值法评估其对蚯蚓的影响。
1 材料与方法 1.1 材料及试剂岛津8050超快速液相色谱-串联质谱(UFLCMS/MS, 日本SHIMADZU公司);色谱柱为Waters T3 C18柱(1.8 μm, 2.1×100 mm);恒温培养振荡器(天津市欧诺仪器仪表有限公司);离心机(德国SIGMA离心机有限公司)。克百威(99.5%)、多菌灵(99.5%)、甲基异柳磷(98.4%)、吡虫啉(99.5%)、阿维菌素(96.6%)、噻虫嗪(99.5%)、噻虫胺(99.5%)、噻唑膦(95.3%)均购自美国ChemService公司, 三羟基克百威(98%)购自Dr. Ehrenstorfer公司。乙腈(色谱纯, Fisher), 实验用水由Milli-Q净水系统制备(Millipore公司), 氯化钠(优级纯)购自天津市科密欧化学试剂有限公司, 乙酸铵(98%)购自Acros Organics公司。
1.2 土壤样品的采集土壤样品采自山东省济南市济阳县。济阳县是设施蔬菜主产区, 番茄和黄瓜单品种种植规模大。本研究选择济阳县13个设施番茄种植基地和10个设施黄瓜种植基地, 其种植时间均在10年以上。选择的番茄和黄瓜大棚均为常年单品种蔬菜种植, 不换茬。番茄田土壤取样时间为:当季产中(2017.06.27)、当季产后(2017.09.30)、后茬产中(2017.11.14), 每个取样时间分别采集13个土壤样品, 合计39个土样。黄瓜田土壤取样时间为:当季产中(2017.06.27)、当季产后(2017.09.30)、后茬产中(2017.11.20), 每个取样时间分别采集10个土壤样品, 合计30个土样。采集土壤样品时, 使用不锈钢土钻按垂直柱状法进行, 采样深度0~20 cm, 剔除土壤中大粒径石砾、杂草、植物根系等杂物。每个蔬菜大棚土壤采用梅花点采样法进行, 混合、缩分形成1个土壤样品, 样品重量不少于500 g。将所采集的土壤样品风干后研磨, 过60目筛, 充分混匀后, 放入样品袋中-20 ℃储存待测。
1.3 土壤样品中农药残留检测方法 1.3.1 标准溶液的配制准确称取噻虫嗪、噻虫胺、多菌灵、吡虫啉、阿维菌素、噻唑膦、甲基异柳磷、克百威和三羟基克百威的标准物质, 用色谱纯乙腈配制成1000 mg·L-1的标准储备液。将9种目标物的标准储备液混合, 用色谱纯乙腈稀释成浓度为0.1、0.5、1、5、10、20、50、100、200、500 μg·L-1的混合标准溶液。混合标准溶液中各个目标化合物的浓度一致。以目标物的浓度(x)为横坐标、相对应的色谱峰面积(y)为纵坐标, 绘制标准曲线。
1.3.2 样品前处理称取10.00 g样品于250 mL锥形瓶中, 加入10 mL水, 水化1 h, 加入20 mL乙腈, 摇床200 r·min-1振荡1 h, 倒出上清液至含5~7 g NaCl的100 mL离心管中, 土壤中再加入20 mL乙腈再次200 r·min-1摇床振摇1 h, 合并两次上清液, 5000 r·min-1离心机离心5min, 取2 mL上清液过0.22 μm滤膜上机检测。
1.3.3 色谱条件流动相A为2 mmol·L-1乙酸铵水溶液, 流动相B为乙腈, 流速0.35 mL·min-1, 柱温40 ℃, 进样量为1 μL, 梯度洗脱程序:0 min, 90%A;0.00~0.50 min, 90%A~40%A;0.50~2.00 min, 40%A;2.00~5.00 min, 5%A;5.00~9.00 min, 5%A;9.00~11.50 min, 5%A~ 90%A;13.00 min, 90%A。
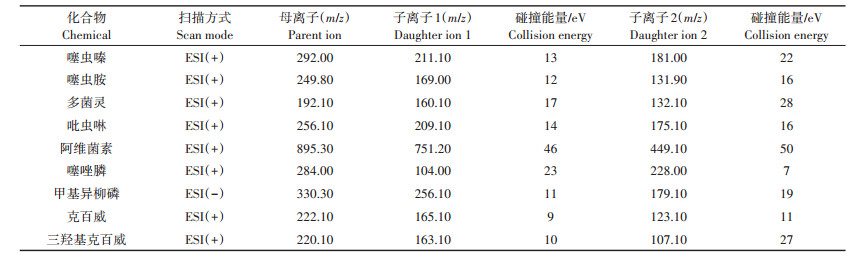
1.3.4 质谱条件采用多反应监测模式(MRM), 各个化合物定性定量离子对如下(表 1)。雾化气流速为3 L·min-1, 加热气流速为10 L·min-1, 干燥气流速为10 L·min-1。
|
|
表 1 9种化合物的串联质谱条件 Table 1 MS/MS parameters for nine chemicals |
取10.00 g空白土壤样品, 分别向其中添加含有9种目标物的混合标准溶液, 添加水平分别为0.04、0.4、2 mg·kg-1, 每个添加水平设置4个重复。按照上述样品前处理方法进行提取和仪器分析, 计算土壤样品的平均添加回收率和相对标准偏差(Relative standard deviation, RSD)。
1.5 环境风险评估根据NY/T 2882.8—2017, 按照以下公式计算风险商值。
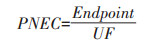
|
(1) |
式中:PNEC为预测无效应浓度, mg·kg-1 dw;Endpoint为目标物对蚯蚓的半数致死浓度(LC50, mg·kg-1 dw)。UF为不确定因子, 对于急性风险评估, 默认值为10。目标化合物对蚯蚓的半致死浓度(LC50), 噻虫嗪、噻虫胺、多菌灵、吡虫啉、噻唑膦、阿维菌素、克百威、三羟基克百威的LC50分别为1000[12]、5.93[12]、5.4[13]、10.7[14]、209[15]、16.5[16]、226.6[17]、226.6 mg·kg-1 dw(假设三羟基克百威与克百威对蚯蚓的急性毒性相当)。
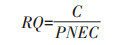
|
(2) |
式中:RQ为风险商值, 无量纲;C代表暴露浓度, 在本研究中为土样样品中目标物的检测浓度, mg·kg-1 dw;对于未检出的农药, 以其检出限的一半作为暴露浓度开展RQ计算。当风险商值RQ>1时, 表示土壤残留农药对蚯蚓存在不可接受急性风险, 数值越大, 风险越大;RQ≤1时, 表示土壤残留农药对蚯蚓的急性风险可接受, 数值越小, 风险越小。

|
(3) |
式中:C阈值为对蚯蚓急性风险可接受的土壤安全阈值浓度(mg·kg-1 dw)。当RQ=1时, 根据公式(2)可推算C阈值=PNEC。
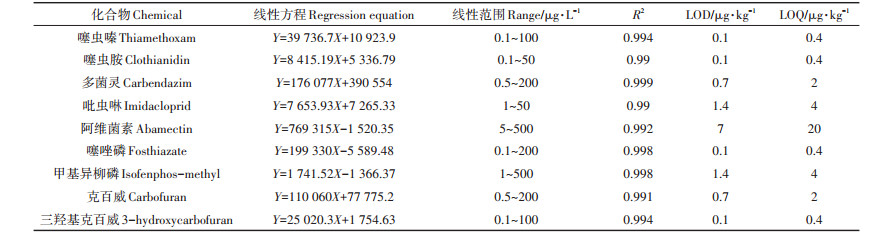
2 结果与讨论 2.1 方法的线性范围、准确度及精密度以目标化合物的浓度(x)与相对应的色谱峰面积(y)作标准曲线, 用外标法定量分析9种化合物的含量。研究中以混合标准溶液进样, 测定9种化合物的校准曲线回归方程如表 2所示。校准曲线呈良好的线性关系。吡虫啉的线性范围在1~50 μg·L-1之间, 其余8种化合物的线性范围都在3个数量级以上。以3倍信噪比计算目标化合物的检出限(Limit of detection, LOD), 其LOD在0.1~7 μg·kg-1之间;以10倍信噪比计算目标化合物的定量限(Limit of quantification, LOQ), 其LOQ在0.4~20 μg·kg-1之间。由此可见, 本方法的检出限和定量限均较低, 满足分析需要。
|
|
表 2 目标化合物的校准曲线方程相关参数 Table 2 Linear regression parameters of the calibration curve for the nine chemicals |
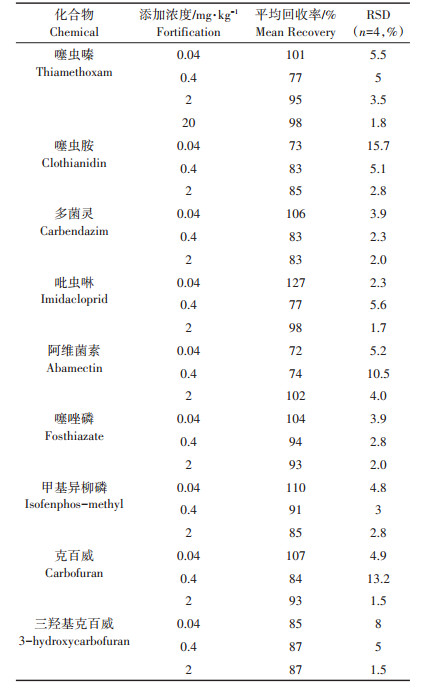
本研究选择空白土壤, 对其进行3个浓度水平的添加回收实验, 9种化合物的平均回收率在72%~ 127%之间, 相对标准偏差(Relative standard deviation, RSD)在1.5%~15.7%之间, 表明本方法的准确度和精密度均较好, 稳定可靠(表 3)。此外, 由于在实际监测中个别土样中噻虫嗪的检出浓度已超出添加回收浓度范围, 因此, 本研究增加了20 mg·kg-1噻虫嗪的添加回收实验, 该水平下的回收率结果也满足研究需要(表 3)。
|
|
表 3 土壤中目标化合物的添加回收率 Table 3 Recoveries of nine chemicals in soil analysis |
在39个设施番茄田土样中, 各化合物的检出率范围在0%~90%之间, 其中噻虫嗪、噻虫胺和吡虫啉的检出率较高, 分别为90%、79%和49%。上述3种农药的最大检出浓度分列目标化合物的前三位, 分别是吡虫啉(2.344 mg·kg-1)、噻虫胺(1.656 mg·kg-1)和噻虫嗪(0.884 mg·kg-1)。在检出的7种化合物中, 检出浓度均值由高到低的顺序为吡虫啉(0.233 mg· kg-1)、阿维菌素(0.133 mg·kg-1)、噻虫嗪(0.107 mg· kg-1)、噻虫胺(0.100 mg·kg-1)、三羟基克百威(0.079 mg·kg-1)、多菌灵(0.009 mg·kg-1)和克百威(0.003 mg· kg-1)。蔬菜田禁用农药克百威及其代谢物三羟基克百威的检出率均为5%, 并且三羟基克百威检出最大值达0.116 mg·kg-1;另一蔬菜田禁用农药甲基异柳磷在番茄田土壤中未检出。
在30个设施黄瓜田土样中, 各农药的检出率范围在0~63%之间, 其中噻虫嗪、噻虫胺、多菌灵和吡虫啉检出率较高, 分别为63%、30%、42%和57%。在检出的8种化合物中, 检出浓度均值由高到低的顺序为噻虫嗪(1.177 mg·kg-1)、吡虫啉(0.126 mg·kg-1)、三羟基克百威(0.122 mg·kg-1)、噻虫胺(0.039 mg·kg-1)、阿维菌素(0.029 mg·kg-1)、多菌灵(0.014 mg·kg-1)、克百威(0.009 mg·kg-1)和噻唑膦(0.003 mg·kg-1)。在土壤中最大检出浓度分列前三位的目标化合物分别是噻虫嗪(16.32 mg·kg-1)、噻虫胺(0.244 mg·kg-1)和吡虫啉(1.66 mg·kg-1)。蔬菜田禁用农药克百威及其代谢物三羟基克百威的检出率均为3%, 并且三羟基克百威检出最大值可达0.122 mg·kg-1;另一蔬菜田禁用农药甲基异柳磷在黄瓜田土壤中未检出。
图 1中列出设施番茄田和黄瓜田土壤中农药检出率和检出均值。噻虫嗪、噻虫胺、多菌灵和吡虫啉在两种设施蔬菜田中的检出率高于其余5种化合物的检出率。将检出率及检出浓度综合分析表明, 在番茄土壤中高检出的3种农药噻虫嗪、噻虫胺、吡虫啉的残留浓度也较高, 推测可能存在近期用药的可能性;阿维菌素虽然检出率较低, 但检出浓度较高, 推测在部分种植基地有近期施药的情况;三羟基克百威检出浓度较高, 推测可能是土壤中残留的克百威降解产生的[18]。在黄瓜土壤中高检出的农药中只有噻虫嗪和吡虫啉的残留浓度较高, 推测其在近期使用。然而, 其他农药不论检出率高或低, 其检出浓度均较低, 推测为历史用药残留。

|
图 1 设施番茄和黄瓜田土壤中目标农药的检出率及检出浓度均值 Figure 1 Detection frequency and the mean detected level of the target chemicals in soil samples of greenhouse tomato and cucumber fields |
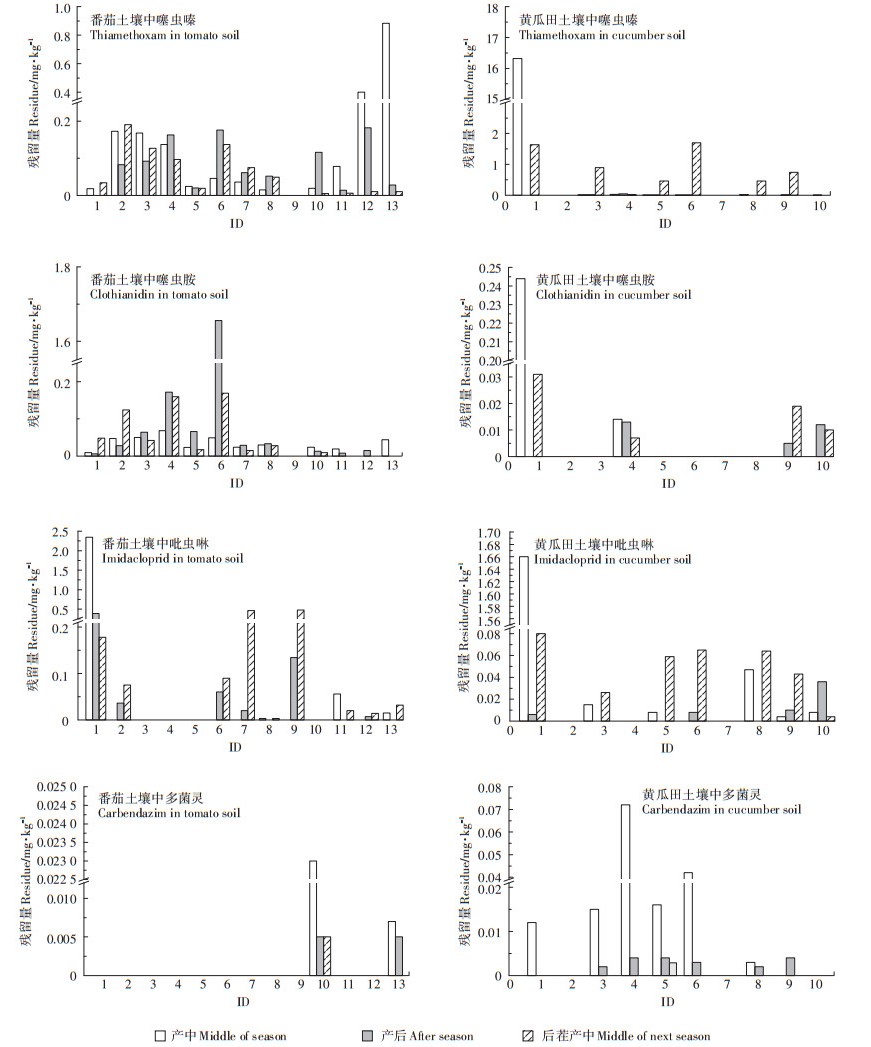
图 2给出了13个设施番茄种植基地不同时期(产中、产后、后茬产中)土壤中噻虫嗪、噻虫胺、吡虫啉、多菌灵的残留浓度。在设施番茄田土壤中, 不同取样点位的噻虫嗪在不同时期的残留趋势存在差异, 取样点2~3在3个时期的土壤噻虫嗪残留趋势呈现出先降低后升高的现象, 这表明, 随着后茬作物种植过程中噻虫嗪的再次使用造成了土壤中其残留浓度上升的现象, 提示存在产中及后茬产中两次用药的情况;取样点4、6、10可能由于后茬产前用噻虫嗪进行土壤处理造成土壤残留浓度趋势为先升高(当季产后)再下降(后茬产中);取样点12~13应为当季产中施药后逐步消散过程, 造成其在后茬种植期间残留浓度的下降。噻虫胺在取样点6后茬产前浓度高于1.5 mg· kg-1, 提示其为直接施药过程;其余取样点中噻虫胺在土壤中的残留可能是噻虫嗪在土壤中降解转化而成[19]。取样点位1在当季产中施用吡虫啉, 吡虫啉在当季产中施药后发生降解或者转化行为, 随产后及后茬产中浓度逐步降低;取样点位7和9在后茬产中阶段也存在使用吡虫啉的情况;其余点位为历史残留。
|
图 2 设施番茄和黄瓜田土壤中噻虫嗪、噻虫胺、吡虫啉、多菌灵的检出浓度 Figure 2 Residue levels of thiamethoxam, clothianidin, imidacloprid, and carbendazim in soil samples of greenhouse tomato and cucumber fields |
在黄瓜土壤中, 噻虫嗪在取样点位1、3、5、6、8、9均在后茬产中施药, 且取样点1还在当季产中施药, 噻虫胺为噻虫嗪施药后代谢产生。当季产中在取样点位1还使用过吡虫啉, 其余点位吡虫啉为历史残余。多菌灵的土壤残留浓度较低, 且降解速度较快。
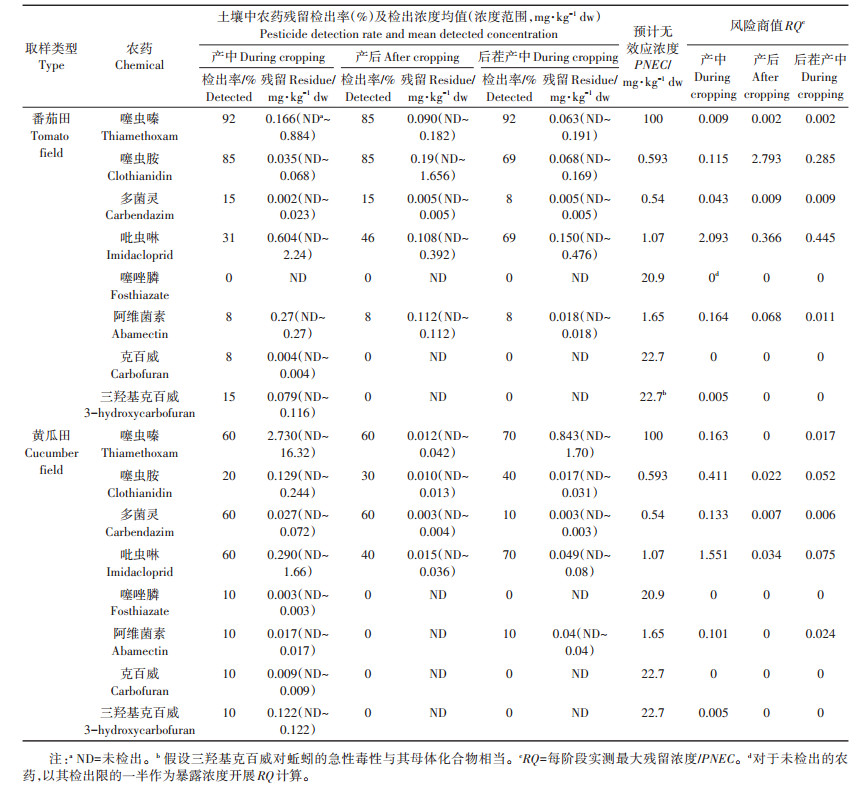
2.3 产前、产中、产后土壤中农药残留对蚯蚓的急性毒性评估本研究中, 番茄土壤中检出的目标物为噻虫嗪、噻虫胺、多菌灵、吡虫啉、阿维菌素、克百威、三羟基克百威;黄瓜土壤检出的化合物为噻虫嗪、噻虫胺、多菌灵、吡虫啉、噻唑膦、阿维菌素、克百威、三羟基克百威, 将对其开展蚯蚓的急性毒性风险评估。由于甲基异柳磷在所有土壤样品中未检出, 并且番茄田土壤中噻唑膦未检出, 以其检出限的一半作为暴露浓度开展其对蚯蚓的急性风险评估。根据《农药登记环境风险评估指南第8部分:土壤生物》(NY / T2882.8— 2017), 通过目标化合物对蚯蚓的LC50, 结合蚯蚓急性毒性的不确定因子(UF=10), 计算出预测无效应浓度PNEC(公式1);继而通过在监测中得到的目标化合物土壤残留浓度, 根据公式(2)算出各个化合物对蚯蚓急性毒性的风险商值(RQ)。表 4为各化合物对蚯蚓的急性毒性风险评估结果。
|
|
表 4 目标化合物对蚯蚓急性风险评估 Table 4 Acute risk assessment for targeted chemicals to earthworm |
在番茄田土壤中, 取样点位1当季产中吡虫啉残留对蚯蚓的急性风险不可接受(RQ=2.093);取样点位6后茬产前噻虫胺残留对蚯蚓的急性毒性不可接受(RQ=2.793);其余点位不同时间的土壤样品中目标农药对蚯蚓的急性毒性风险商值均低于1。在黄瓜田土壤中, 取样点位1当季产中吡虫啉残留对蚯蚓的急性风险不可接受(RQ=1.551), 其余点位不同时间的土壤样品中目标农药对蚯蚓的急性毒性风险商值均低于1。上述数据表明, 研究区域内上述农药对蚯蚓的风险总体较低;在39个番茄土壤样品中, 目标农药对蚯蚓的急性风险评估RQ < 1的比率高达95%;在30个黄瓜土壤样品中, 目标农药对蚯蚓的急性风险评估RQ < 1的比率高达97%。在3例土壤中发现RQ>1, 包括2例吡虫啉和1例噻虫胺, 根据公式(3)计算吡虫啉和噻虫胺对蚯蚓的急性风险可接受的土壤安全阈值浓度分别为1.07 mg·kg-1 dw和0.593 mg· kg-1 dw。
本研究明确了新烟碱类农药吡虫啉和噻虫胺对蚯蚓的急性风险高, 已报道的研究表明上述农药对蚯蚓的机能及繁殖力均存在显著危害。针对本研究中锁定的高风险农药吡虫啉, 当其浓度为1.6 mg·kg-1时对蚯蚓生长有抑制作用, 并降低了蚯蚓体腔细胞溶酶体膜稳定性[5];并且经吡虫啉淋溶后的土壤会使蚯蚓体内的乙酰胆碱及酶原蛋白含量升高[20];当土壤中吡虫啉浓度达到2.0 mg·kg-1时, 会使蚯蚓的繁殖力降低84.0%[21]。本研究中, 吡虫啉土壤残留最高可达2.344 mg·kg-1, 可能具有潜在的抑制蚯蚓生长、繁殖及体内生化过程的危险。在所有目标化合物中, 噻虫胺对蚯蚓的急性毒性最高;且本研究中发现1例噻虫胺土壤残留对蚯蚓的急性风险不可接受。有研究表明, 当土壤中噻虫胺浓度达到0.5 mg·kg-1及以上时, 蚯蚓体内的活性氧(ROS)水平极大增加, 引起抗氧化酶活性的变化, 生物大分子的损伤和功能基因的异常表达[22]。当土壤中噻虫胺浓度为2.0 mg·kg-1时, 会严重影响蚯蚓的繁殖, 蚯蚓的繁殖力降低45.7%[21]。本研究中, 噻虫胺的最大土壤残留浓度为1.656 mg·kg-1, 可能引起蚯蚓体内的ROS升高, 引起蚯蚓体内生物生化过程异常。
3 结论(1) 在设施番茄和黄瓜种植土壤中广泛检出噻虫嗪、噻虫胺和吡虫啉, 除个别点位外, 检出浓度均低于0.5 mg·kg-1 dw。
(2) 根据风险商值法评估, 土壤残留农药对蚯蚓的急性风险总体较低, 超过90%的土壤样品中, 目标农药对蚯蚓的急性风险可接受。
(3) 高风险农药吡虫啉和噻虫胺对蚯蚓的急性风险可接受的土壤安全阈值浓度分别为1.07 mg·kg-1 dw和0.593 mg·kg-1 dw。
| [1] |
董静, 赵志伟, 梁斌, 等. 我国设施蔬菜产业发展现状[J]. 中国园艺文摘, 2017, 33(1): 75-77. DONG Jing, ZHAO Zhi-wei, LIANG Bin, et al. Development status of greenhouse vegetable industry in China[J]. Chinese Horticulture Abstracts, 2017, 33(1): 75-77. DOI:10.3969/j.issn.1672-0873.2017.01.030 |
| [2] |
王文桥. 我国设施蔬菜农药减施增效展望[J]. 中国蔬菜, 2016(5): 1-3. WANG Wen-qiao. Prospect of reducing pesticide application and increasing efficiency in greenhouse vegetables in China[J]. China Vegetables, 2016(5): 1-3. DOI:10.3969/j.issn.1000-6346.2016.05.002 |
| [3] |
陈晓玲, 苗娟娟, 徐挺, 等. 基于土壤微生物指标和蚯蚓的生物效应评估太湖流域农田土壤的污染状况[J]. 广东化工, 2017, 44(4): 1-3. CHEN Xiao-ling, MIAO Juan-juan, XU Ting, et al. Ecological risk assessment of pesticide residues in soil combining soil microbiological parameters and biomarker responses in earthworms from Taihu Lake, China[J]. Guangdong Chemical Industry, 2017, 44(4): 1-3. DOI:10.3969/j.issn.1007-1865.2017.04.001 |
| [4] |
梁继东, 周启星, 孙福红. 蚯蚓在环境安全研究中的应用[J]. 生态学杂志, 2006(5): 581-586. LIANG Ji-dong, ZHOU Qi-xing, SUN Fu-hong. Application of earthworm in environmental safety study[J]. Chinese Journal of Ecology, 2006(5): 581-586. DOI:10.3321/j.issn:1000-4890.2006.05.022 |
| [5] |
冯磊, 张兰, 张燕宁, 等. 三种新烟碱类农药对蚯蚓体重及溶酶体膜的影响[J]. 植物保护, 2015, 41(3): 35-39. FENG Lei, ZHANG Lan, ZHANG Yan-ning, et al. Effects of three neonicotinoids on the weight and neutral red retention time of earthworm (Eisenia fetida)[J]. Plant Protection, 2015, 41(3): 35-39. DOI:10.3969/j.issn.0529-1542.2015.03.007 |
| [6] |
中华人民共和国农业部.农药登记环境风险评估指南第8部分: 土壤生物NY/T 2882. 8-2017[S].北京: 中国农业出版社, 2017. Ministry of Agriculture of PRC. Guidance on environmental risk assessment for pesticide registration Part 8: Soil organism NY/T 2882. 8- 2017[S]. Beijing: China Agriculture Press, 2017. |
| [7] |
姜锦林, 程燕, 卜元卿, 等. 农药对蚯蚓的生长和繁殖毒性及其在生态风险评价中的应用[J]. 农药科学与管理, 2014, 35(9): 23-32. JIANG Jin-lin, CHENG Yan, BU Yuan-qin, et al. Effects of pesticides on the growth and reproduction of earthworm and its application in ecological risk assessment[J]. Pesticide Science and Administration, 2014, 35(9): 23-32. DOI:10.3969/j.issn.1002-5480.2014.09.006 |
| [8] |
Vašíčková J, Hvězdová M, Kosubová P, et al. Ecological risk assessment of pesticide residues in arable soils of the Czech Republic[J]. Chemosphere, 2019, 216: 479-487. DOI:10.1016/j.chemosphere.2018.10.158 |
| [9] |
中华人民共和国农业部公告第199号.农药登记公告[R]. 2002. Ministry of Agriculture. No. 199 Announcement on pesticide registration[R]. 2002. |
| [10] |
张劲强, 董元华, 安琼, 等. 不同种植方式下土壤和蔬菜中氨基甲酸酯类农药残留状况研究[J]. 土壤学报, 2006(5): 772-779. ZHANG Jin-qiang, DONG Yuan-hua, AN Qiong, et al. Residues of carbamate pesticides in soils and vegetables under different vegetation systems[J]. Acta Pedologica Sinica, 2006(5): 772-779. DOI:10.3321/j.issn:0564-3929.2006.05.010 |
| [11] |
袁善奎, 刘亮, 王以燕, 等. 农药非法添加隐性成分及其风险分析[J]. 农药, 2016, 55(7): 480-482. YUAN Shan-kui, LIU Liang, WANG Yi-yan, et al. Situation of illegal hidden ingredients in pesticides from market and its risk analysis[J]. Agrochemicals, 2016, 55(7): 480-482. |
| [12] |
European Food Safety Authority. Review report for the active substance thiamethoxam[R]. 2006.
|
| [13] |
European Food Safety Authority. Conclusion on the peer review of the pesticide risk assessment of the active substance carbendazim[J]. EFSA Journal, 2010, 8(5): 1598. DOI:10.2903/j.efsa.2010.1598 |
| [14] |
European Food Safety Authority. Conclusion regarding the peer review of the pesticide risk assessment of the active substance imidacloprid[J]. EFSA Journal, 2008, 6(7): 148. |
| [15] |
University of Hertfordshire. THE PPDB pesticide properties database[DB/OL].[2019-03-11]. http://sitem.herts.ac.uk/aeru/iupac/atoz.htm.
|
| [16] |
European Food Safety Authority. Conclusion regarding the peer review of the pesticide risk assessment of the active substance abamectin[J]. EFSA Journal, 2008, 6(7): 147. |
| [17] |
European Food Safety Authority. Conclusion regarding the peer review of the pesticide risk assessment of the active substance carbofuran[J]. EFSA Journal, 2006, 4(8): 90. DOI:10.2903/j.efsa.2006.90r |
| [18] |
谢恩平, 林亲铁, 杨仁斌. 克百威丙硫克百威和丁硫克百威的残留与降解研究进展[J]. 农药科学与管理, 2002(3): 18-20. XIE En-ping, LIN Qin-tie, YANG Ren-bin. The research development of residue and degredation for carbofuran, fenfuracarb and carbosulfan[J]. Pesticide Science and Administration, 2002(3): 18-20. DOI:10.3969/j.issn.1002-5480.2002.03.008 |
| [19] |
蒋梦云, 巩文雯, 刘庆菊, 等. 噻虫嗪及其代谢产物在盆栽辣椒和土壤中的残留动态和膳食风险评估[J]. 农药, 2018, 57(9): 662-665. JIANG Meng-yun, GONG Wen-wen, LIU Qing-ju, et al. Residue dynamics and dietary risk assessment of thiamethoxam and its metabolites in potted peppers and soil[J]. Agrochemicals, 2018, 57(9): 662-665. |
| [20] |
王萌, 杨叶, 吉哲蓉, 等. 吡虫啉和阿维菌素淋溶土壤对蚯蚓及其淋出液对浮萍急性毒性和生理生化指标的影响[J]. 农药, 2017, 56(6): 437-442. WANG Meng, YANG Ye, JI Zhe-rong, et al. Effects of imidacloprid and abamectin leaching soil on earthworm and these leaching solution on the physiological and biochemical indices of duckweed[J]. Agrochemicals, 2017, 56(6): 437-442. |
| [21] |
Wang K, Pang S, Mu X, et al. Biological response of earthworm, Eisenia fetida, to five neonicotinoid insecticides[J]. Chemosphere, 2015, 132: 120-126. DOI:10.1016/j.chemosphere.2015.03.002 |
| [22] |
Liu T, Wang X, You X, et al. Oxidative stress and gene expression of earthworm(Eisenia fetida)to clothianidin[J]. Ecotoxicology and Environmental Safety, 2017, 142: 489-496. DOI:10.1016/j.ecoenv.2017.04.012 |
 2019, Vol. 38
2019, Vol. 38