2. 中国科学院大学, 北京 100049
2. University of Chinese Academy of Science, Beijing 100049, China
邻苯二甲酸二丁酯(DnBP)是一类广泛使用的添加剂,主要应用于树脂以及PVC聚合材料中以增加材料的柔韧性和延展性[1],DnBP还常应用于墨水、胶水以及化妆品和药品行业中[2]。有研究表明DnBP还被应用于化肥和农药中[3]。由于自然流失、污水灌溉,以及固体废弃物管理不当等原因[4-6],目前DnBP在土壤环境中被广泛检测到[7-8]。如,Chen等[7]的研究表明我国大棚土壤中DnBP的含量从0.16~0.96 mg·kg-1不等,李艳等[8]研究了北京近郊灌区表层土中DnBP含量浓度从0.55~10.8 mg·kg-1不等。
DnBP是由邻苯二甲酸和正丁醇酯化生成的一类人工合成物,其基本的理化性质如表 1所示。研究表明,DnBP具有内分泌干扰性,是一类环境类激素,具有一定的生态毒性[9]。例如,Carruthers等[10]对怀孕的SD大鼠进行为期20 d的DnBP剂量为500 mg·kg-1·d-1的暴露实验,结果表明暴露2 d时,雄性胎儿的生殖器官发育可受到最大伤害,而暴露10—18 d会直接影响胎儿生殖器性状的改变。Mccarthy等[11]的研究表明,DnBP暴露量为1.8 mg·L-1时,大型蚤和呆鲦鱼(Pimephales promelas)的生殖能力和早期生存能力会受到影响,1 mg·L-1的暴露剂量则会引起两种生物繁殖后代数量的减少。鉴于DnBP具有生态毒性,近年来对DnBP降解的报道逐年增加[2, 12-13]。而对于土壤的DnBP污染,研究主要集中在利用微生物代谢降解DnBP上。例如,DnBP可受到巨大芽孢杆菌菌株(YJB3)代谢的影响而发生降解,逐步分解为邻苯二甲酸单丁酯(MnBP)、邻苯二甲酸(PA)、原儿茶酸(PCA)等代谢产物[13]。然而,对于铁含量高的土壤,表层的土壤在接受光照时会产生各种各样的自由基反应[14-17],DnBP可能被产生的自由基所降解,而经由这一途径发生的DnBP的降解研究却比较少。
土壤环境因素可影响DnBP在红壤中的物理化学降解。例如,草酸、柠檬酸等是土壤中常见的小分子脂肪酸[19]。铁的(水合)氧化物会与脂肪酸的羧基发生络合,形成表面络合的小分子有机酸-铁(水合)氧化物复合物(如草酸-针铁矿、柠檬酸-赤铁矿等),这些复合体在接受紫外-可见光的照射下,可以原位生成H2O2。在铁矿或某些持久性自由基的作用下,H2O2会分解产生氧化性极高的羟基自由基·OH(EH = 2.8 V),从而降解有机污染物[20]。土壤pH则可以改变土壤中铁的形态,而且H+的浓度变化通常是土壤发生各种铁溶出以及(光)类芬顿反应高效进行的重要因素。NO3-是常见的无机阴离子,研究表明在紫外-可见光照射下,水溶液中的NO3-可以转化为·NO2和·OH,存在潜在的降解DnBP的能力[21]。此外,近年来,有机-无机复合污染的土地常有报道[22]。以Cu2+污染为例,矿区农田由于铜矿开采,导致土壤铜污染严重,例如湖北大冶地区土壤中铜污染最高浓度可达630.39 mg·kg-1[23]。而其余地区普通的农田土壤铜的污染主要来自于复合肥和含铜农药的累积施用以及污水灌溉[24]。例如,北京的蔬菜基地土壤Cu2+污染在6~65.2 mg·kg-1波动。研究表明大棚土壤中的DnBP和Cu2+浓度均与大棚年限呈显著的正相关[25-27]。报道还指出,Cu2+的存在还可以影响光类芬顿反应过程,因此复合污染的结果可能致使有机污染物的降解受到影响[28]。我国幅员辽阔,昼夜变化以及季节变化均可引起光照强度在同一地点具有显著差异。因此研究DnBP在300~400 nm的紫外光照射下在红壤中的降解,对我们理解土壤中的有机污染物由物理化学反应引起的归趋变化具有重要环境意义。本文将重点考虑DnBP在紫外光(300~400 nm)照下(对照暗环境)的降解,并讨论环境条件对土壤DnBP降解的影响。
1 材料与方法 1.1 供试土壤供试土壤为采集自江西鹰潭的农田土壤,经过通风避光干燥后,磨细过100目筛。经测量,受试土壤的DnBP背景含量低于方法检出限,故制备100 mg·kg-1 DnBP污染土壤样品时,不考虑背景DnBP污染浓度。制备的大致步骤:配制200 mg·L-1 DnBP正己烷溶液500 mL,分5次倒入200 g过100目的风干土样中。均匀搅拌后,放于通风避光处,待正己烷完全挥发即可得到均匀的DnBP污染含量为100 mg·kg-1的土壤。老化30 d后进行试验。取不同质量的污染土,对其进行DnBP的提取实验。结果表明,所提取的DnBP含量与称量土壤之间具有很好的的线性关系(R2= 0.99),说明制备的DnBP污染土为均匀污染的土壤。
1.2 实验设计在光照和暗环境下,分别观察在土壤溶液pH为5.5时,以下因素对DnBP降解的影响:土壤中草酸和柠檬酸浓度、土壤中Cu2+浓度、土壤中NO3-浓度以及土壤pH的影响。为了更好地对比说明,本文对纯水溶液中NO3-对DnBP降解的影响也做了考察。在有和无50 mmol·L-1草酸存在于土壤溶液中的条件下,考察土壤溶液中Cu2+浓度对DnBP降解的影响实验。具体实验设计如表 2所示。实验结果通过SPSS 22软件中的One-way ANOVA分析相同处理不同水平之间的显著性差异。
|
|
表 2 影响DnBP降解的不同影响因素实验条件设计 Table 2 Experimental design of different factors influencing DnBP degradation |
所有光化学反应在XPA-7型光反应器中进行(南京胥江机电厂,中国南京)。反应器内部竖直放置一500 W的高压汞灯,经过滤光片(300~400 nm)后获得照射于光反应管上强度为2.5 mW·cm-2的UV光。反应试管为60 mL石英试管,竖直均匀放置于围绕灯做周转的小圆盘槽中,其距离中心灯6 cm。反应过程中,40 mL土水比为1:20的悬浊液在石英光反应管中持续搅拌的同时围绕汞灯做周转。反应前溶液和土混合体系先在暗环境下搅拌平衡12 h,在开启光照前取1 mL搅拌均匀的悬浊液,反应5 h后再取1 mL搅拌均匀的悬浊液(对照的暗反应进行相同操作,无光照),将所取样品冷冻干燥待测。
1.3 测定方法土壤pH测量通过电位法,即1:2.5的土水比混合搅拌30 min,静置测量上清液pH值[29]。土壤有机质通过重铬酸钾氧化法测定[29]。土壤全氮采用半微量凯氏法测定[29]。土壤无定型铁采用草酸-草酸铵提取-邻菲罗啉比色法测定,结晶铁含量采用连二亚硫酸钠-柠檬酸钠-重碳酸钠浸提(DCB法)-邻菲罗啉比色法测定[30]。土壤机械组成采用吸管法测定[29]。
土壤中的DnBP测量方法如下:向冷冻干燥后的土壤样品中加入1 mL甲醇,在35 ℃下超声提取40 min,所得浑浊甲醇溶液过0.22 μm的有机系滤膜,滤液即为DnBP提取液,通过HPLC测定(安捷伦1260 infinity)。经测试,此方法DnBP回收率为95.14%。HPLC测定所使用的色谱柱为安捷伦SB-C18色谱柱(4.6 mm × 250 mm,5 μm)。测定条件为:进样量20 μL,以纯甲醇和超纯水(体积比为80:20)为流动相;流速设置为1.0 mL·min-1;检测波长为224 nm,柱温设置为35 ℃。仪器检出限确定为0.041 9 mg·L-1,方法检出限确定为0.121 4 mg·L-1。仪器测定相对偏差为2.93%。
2 结果与讨论 2.1 受试土壤的理化性质如表 3所示,采自江西鹰潭的红壤为黏土质地,0.002~0.05 mm大小的颗粒占总量的41.72%。土壤背景铜浓度为27.41 mg·kg-1,这与之前文献[24-25]报道的结果在相同的数量级。这些背景铜是通过完全消解土壤矿物得到,与外源性污染的铜对催化反应的可利用性具有很大差别。因此实验仍然只以外加铜作为铜浓度影响的变量。土壤有机质含量为1.01%,偏低。土壤中游离铁的含量,即结晶态铁(包括各种铁的水合氧化矿,如针铁矿、纤铁矿、磁铁矿、赤铁矿等)和无定型铁(包括水铁矿、氢氧化铁以及与有机物络合的铁)含量很高,这也使得江西鹰潭的土壤呈现砖红色。由于高铁的土壤中铁交换了H+,因此土壤溶液的pH值为酸性(4.91)。
|
|
表 3 江西鹰潭红壤的理化性质 Table 3 Physicochemical properties of high iron content soil of Yingtan, Jiangxi Province |
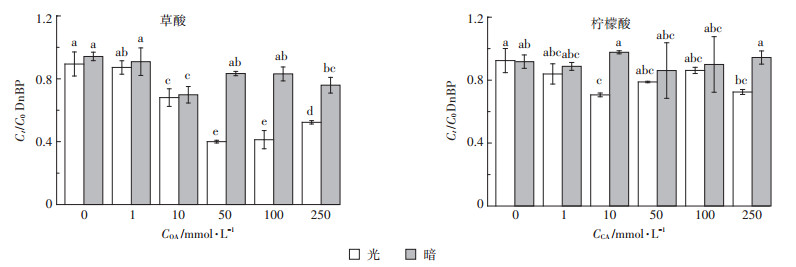
本文采用两种常见的小分子有机酸,草酸(OA)和柠檬酸(CA),分别在光照和黑暗下对DnBP降解进行测定。实验结果如图 1所示。在光照下,当悬浊液pH为5.5,草酸浓度为50 mmol·L-1时,DnBP的降解率为60.00%;当草酸浓度低于50 mmol·L-1时,DnBP的降解率随着草酸浓度的增加而增加;当草酸浓度高于50 mmol·L-1时,DnBP的降解率随着草酸浓度的增加而降低。光照下,柠檬酸浓度对DnBP的降解没有显著性影响。在无光的条件下,草酸的存在会影响DnBP的降解,其中最佳浓度为10 mmol·L-1,此浓度下DnBP可以发生30.14%的降解;而无光条件下,柠檬酸不仅对DnBP降解没有作用,而且在所有柠檬酸浓度下DnBP均未发生降解。整体而言,草酸对DnBP发生光降解的影响要大于柠檬酸。
|
图中Ct表示反应结束后土壤中DnBP的浓度,C0表示初始时土壤中DnBP的浓度。柱上不同英文字母表示处理间差异显著(P < 0.05)。下同 Ct and C0 denote the concentrations of DnBP in soils at the end and start of the reactions respectively.Different letters indicate significant differences among treatments (P < 0.05). The same below 图 1 草酸(OA)和柠檬酸(CA)在光照(300~400 nm)和暗环境下对DnBP降解的影响 Figure 1 DnBP degradation under 300~400 nm light irradiation and in dark as a function of oxalic and citric acid concentrations |
光照下之所以会发生DnBP的降解,主要与光照下悬浊液中存在光类芬顿反应有关。研究表明,在有铁的(水合)氧化矿存在下,小分子有机羧酸会通过其羧基与铁矿发生表面络合反应,如方程式1所示[20]。在光照下,小分子有机酸作为配体失去电子,传递给铁矿表面的三价铁离子,生成表面二价铁≡Fe2+和小分子有机酸自由基LMWOA*(方程式2)。当与氧气接触时,≡Fe2+和LMWOA*可分别传递电子给氧气生成超氧自由基O2-·,自身分别被氧化为≡Fe3+以及小分子有机酸的分解产物DLMWOA(方程式3和方程式4)。在酸性条件下,O2-·可以和氢离子结合,产生H2O2(方程式5)。H2O2在光照和≡Fe2+的催化作用下均可分解为羟基自由基(方程式6和方程式7),而羟基自由基具有无选择性降解有机污染物的作用。在10mmol·L-1草酸单独存在的暗环境下,DnBP可以发生30.14%的降解,这主要是因为草酸具有一定的还原性[31],可以还原铁氧化物表面的≡Fe3+,生成表面≡Fe2+,再经过方程式3、5、7形成类芬顿体系降解DnBP。

|
(1) |

|
(2) |

|
(3) |
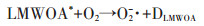
|
(4) |
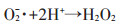
|
(5) |

|
(6) |
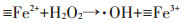
|
(7) |
本研究中,红壤的无定型铁含量为3.45 g·kg-1,结晶态铁的含量为23.04 g·kg-1(换算成铁元素为16.13 g·kg-1)。这说明,大部分铁均以结晶良好的铁矿(土壤中常见的结晶态铁矿有针铁矿、赤铁矿、纤铁矿以及菱铁矿等)存在,无定型铁(土壤中常见的形态为水铁矿以及络合离子形态的铁)含量略低。在前期的研究中,作者发现均相溶液中草酸发生光催化的作用要强于柠檬酸,然而,在异相催化中,柠檬酸的作用要强于草酸[32]。本文反应中既存在均相铁也会存在异相铁,而草酸对DnBP的降解要强于柠檬酸,这就说明了在本研究中,起主要光活性成分的铁为还原溶解或络合溶解的均相铁。
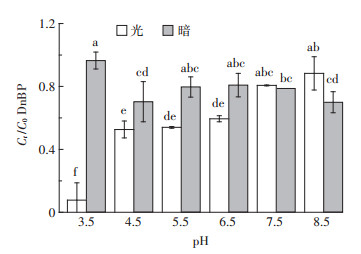
2.3 pH对草酸光照下降解DnBP的影响当草酸浓度为50 mmol·L-1时,由图 2可以观察到,光照下,pH为3.5时DnBP降解率达到95%,而在pH 4.5~6.5时,约50%的DnBP发生降解且无显著性差异。当pH为碱性时,有20%的DnBP发生降解。暗环境下DnBP发生降解主要由草酸的还原性引起,且在pH从4.5~8.5变动期间,DnBP发生约80%的降解,不同pH之间差异不显著。pH对DnBP降解的影响主要有两方面原因:一方面,对于红壤中无定型铁,低pH容易诱导铁矿的溶出,从而增加水溶液中Fe3+与草酸的络合。从方程式1~方程式3以及方程式7可以得出,铁的存在可以引起体系产生类芬顿反应,从而有效地降解DnBP。另一方面,如方程式5所示,H+的增多有利于H2O2的生成,从而促进·OH的生成,因此酸性环境有利于DnBP的降解。
|
图 2 pH对土壤中DnBP在50 mmol·L-1草酸存在条件下降解的影响 Figure 2 Effects of pH on the degradation of DnBP in the presence of 50 mmol·L-1 oxalic acid |
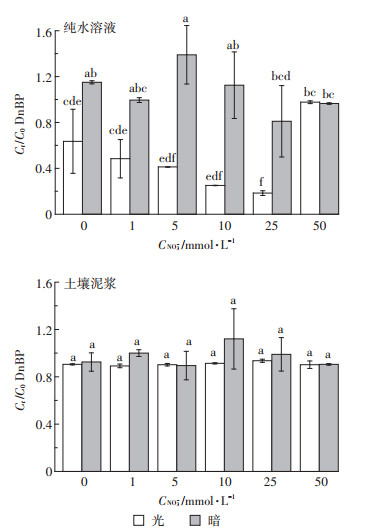
如图 3所示,在纯水溶液中0~25 mmol·L-1的NO3-存在时,光照下随着NO3-浓度的增加,DnBP的降解率逐渐从37.5%增加至78%。当NO3-浓度从25 mmol·L-1增加到50 mmol·L-1时,DnBP的降解受到抑制。暗环境中,DnBP无降解发生。在土壤中,光照条件下NO3-的存在对土壤中DnBP降解无影响,且无DnBP的降解。暗环境下,土壤悬浊液中亦无DnBP降解的发生,且NO3-对DnBP的降解无影响。DnBP在纯水溶液中的这一降解行为主要是由于,NO3-在接受紫外光照射时,可生成激发态的硝酸根离子NO3-*。在酸性条件下,NO3-*可以分解为·OH和二氧化氮自由基NO2·[21],如方程式8和方程式9所示。NO3-的这一光催化降解作用,在对全氟辛酸的研究中也得到了证明。例如Li等[33]的研究指出,在有NO3-存在的水溶液中全氟辛酸在254 nm的紫外光照下可以发生降解直至矿化,起主要作用的是在紫外光的照射下NO3-转化成的·NO2。而NO -浓度继续增加之所以会抑制DnBP的降解,主要是因为NO3-与体系中的O之间发生反应降低了·NO2的产率(方程式10),这一过程称为自抑制过程。
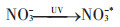
|
(8) |
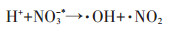
|
(9) |
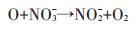
|
(10) |
|
图 3 NO3-浓度对DnBP在土壤溶液和纯水溶液中降解的影响 Figure 3 DnBP degradation in water solution and soil solution as a function of NO3- concentration |
由于纯体系中可供·NO2自由基攻击氧化的有机物质只有DnBP,因此DnBP会得到降解。然而土壤成分相对要复杂很多,尤其是土壤中的有机组分可以作为还原剂猝灭·NO2,从而降低土壤中DnBP的降解作用。此外,NO3-并没有对土壤中DnBP的降解产生影响还与DnBP的水溶性差有关系。对于草酸体系,矿物表面吸附的DnBP可以被因草酸吸附而在矿物表面原位生成的自由基所降解。或者低pH下矿物溶解使得DnBP缓慢释放入水相有利于DnBP接受均相体系自由基的降解。在硝酸盐体系中,DnBP与水溶液中生成的自由基接触反应的几率显著受到DnBP在土壤上黏附作用的影响,相对不易降解。
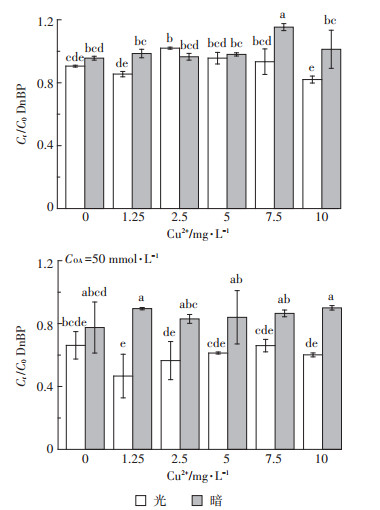
2.5 Cu2+浓度对DnBP降解的影响如图 4所示,在无草酸作用下,Cu2+浓度在0~10 mg·L-1变动时,光照和暗环境下DnBP在5 h内均未发生降解,且不同浓度的Cu2+对DnBP降解影响无显著性差异。在加入50 mmol·L-1草酸时,暗环境下DnBP发生20%左右的降解,而在光照下发生30%左右的降解。且存在50 mmol·L-1 DnBP的条件下,Cu2+浓度无论是光照还是暗环境下对DnBP的降解均无显著性影响。在光照下草酸的加入主要是发生了方程式1~方程式7所示的反应,形成了光类芬顿体系,在暗环境下草酸的加入引起了DnBP的降解,主要是因为暗环境下发生了草酸直接还原铁矿,发生方程式1~方程式3以及方程式7的类芬顿反应。而相较于之前的研究报道,即在光照下,Cu2+可以接受配体(此处为草酸)的电子而生成亚铜离子Cu+,Cu+传递电子给氧气生成O-·,影响光芬顿反应的过程。本文在有50 mmol·L-1草酸存在的条件下,Cu2+浓度变化对DnBP降解没有影响。这可能与环境中Cu污染浓度相对于红壤中铁含量严重偏低(Cu:Fe=1:97.9),(光照下)配体(草酸)-金属(Cu2+)电子传递下生成的Cu+浓度相较于≡Fe2+的含量要少得多有关[34]。
|
图 4 Cu2+浓度对DnBP在土壤中无草酸和有50 mmol·L-1草酸存在条件下降解的影响 Figure 4 DnBP degradation as a function of Cu2+ concentration in the presence and absence of 50 mmol·L-1 oxalic acid |
(1)当红壤溶液pH为5.5时,草酸浓度变化对DnBP降解的影响呈不同趋势。在草酸浓度低于50 mmol·L-1时,草酸浓度的增加促进DnBP的降解,而当草酸浓度高于50 mmol·L-1时,草酸浓度的增加会减少DnBP的降解。草酸在暗环境下的存在有助于DnBP的降解。
(2)柠檬酸在光照下对红壤中DnBP的降解影响没有草酸强,且柠檬酸在暗环境下没有促进DnBP降解的作用。
(3)在50 mmol·L-1草酸存在的条件下,pH为3.5时,DnBP的降解率可达95%,pH升高对DnBP的降解不利。
(4)环境中的NO3-可以对纯水体系中DnBP产生光催化降解作用,说明在地表水中NO3-能促进DnBP降解。然而由于红壤成分的复杂性,NO3-对红壤中DnBP的降解没有显著作用。本研究中,Cu2+污染对DnBP在红壤中的降解无影响。
| [1] |
Stringer R, Labunska I, Santillo D, et al. Concentrations of phthalate esters and identification of other additives in PVC children's toys[J]. Environmental Science & Pollution Research, 2000, 7(1): 27-36. |
| [2] |
Koch H M, Christensen K L Y, Harth V, et al. Di-n-butyl phthalate (DnBP) and diisobutyl phthalate (DiBP) metabolism in a human volunteer after single oral doses[J]. Archives of Toxicology, 2012, 86(12): 1829. |
| [3] |
Mo C H, Cai Q Y, Li Y H, et al. Occurrence of priority organic pollutants in the fertilizers, China[J]. Journal of Hazardous Materials, 2008, 152(3): 1208-1213. |
| [4] |
Ito M, Nagai K. Analysis of degradation mechanism of plasticized PVC under artificial aging conditions[J]. Polymer Degradation & Stability, 2007, 92(2): 260-270. |
| [5] |
Zhang Y, Liang Q, Gao R, et al. Contamination of phthalate esters (PAEs) in typical wastewater-irrigated agricultural soils in Hebei, north China[J]. PLoS One, 2015, 10(9): e0137998. |
| [6] |
唐丽霞, 左停. 中国农村污染状况调查与分析:来自全国141个村的数据[J]. 中国农村观察, 2008(1): 31-38. TANG Li-xia, ZUO Ting. Investigation and analysis of pollution situation in rural China:Data from 141 villages in China[J]. Rural Observation, 2008(1): 31-38. |
| [7] |
Chen N, Shuai W, Hao X, et al. Contamination of phthalate esters in vegetable agriculture and human cumulative risk assessment[J]. Pedosphere, 2017, 27(3): 439-451. DOI:10.1016/S1002-0160(17)60340-0 |
| [8] |
李艳, 刘洪禄, 顾华, 等. 北京市东南郊灌区土壤和农产品酞酸酯污染风险评估[J]. 农业工程学报, 2017, 33(18): 203-212. LI Yan, LIU Hong-lu, GU Hua, et al. Assessment of soils and crops of irrigation district located at southeastern suburb contamination risk of PAEs Beijing[J]. Transactions of the CSAE, 2017, 33(18): 203-212. DOI:10.11975/j.issn.1002-6819.2017.18.027 |
| [9] |
Tan W, Zhang Y, He X, et al. Distribution patterns of phthalic acid esters in soil particle-size fractions determine biouptake in soil-cereal crop systems[J]. Scientific Reports, 2016, 6: 31987. |
| [10] |
Carruthers C M, Foster P M. Critical window of male reproductive tract development in rats following gestational exposure to di-n-butyl phthalate[J]. Birth Defects Research Part B Developmental & Reproductive Toxicology, 2010, 74(3): 277-285. |
| [11] |
Mccarthy J F, Whitmore D K. Chronic toxicity of di-n-butyl and din-octyl phthalate to Daphnia magna and the fathead minnow[J]. Environmental Toxicology & Chemistry, 1985, 4(2): 167-179. |
| [12] |
Shailaja S, Ramakrishna M, Mohan S V, et al. Biodegradation of di-nbutyl phthalate (DnBP) in bioaugmented bioslurry phase reactor[J]. Bioresource Technology, 2007, 98(8): 1561-1566. DOI:10.1016/j.biortech.2006.06.009 |
| [13] |
Feng N X, Yu J, Mo C H, et al. Biodegradation of di-n-butyl phthalate(DBP) by a novel endophytic Bacillus megaterium strain YJB3[J]. Science of the Total Environment, 2018, 616/617: 117-127. DOI:10.1016/j.scitotenv.2017.10.298 |
| [14] |
洪瑞.淹水条件下红壤中五氯酚的降解[D].武汉: 华中农业大学, 2013. HONG Rui. Degradation of pentachlorophenol in red soil under flooded[D]. Wuhan: Huazhong Agricultural University, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10504-1013336123.htm |
| [15] |
杨俊, 徐仁扣. 阴离子对As(Ⅲ)在砖红壤与TiO2混合体系中的光催化氧化/吸附的影响[J]. 环境科学学报, 2009, 29(2): 367-372. YANG Jun, XU Ren-kou. Influence of anions on photocatalytic oxidation and adsorption of As(Ⅲ) on an oxisol with TiO2[J]. Acta Scientiae Circumstantiae, 2009, 29(2): 367-372. DOI:10.3321/j.issn:0253-2468.2009.02.021 |
| [16] |
Fang G D, Gao J, Liu C, et al. Key role of persistent free radicals in hydrogen peroxide activation by biochar:Implications to organic contaminant degradation[J]. Environmental Science & Technology, 2014, 48(3): 1902-1910. |
| [17] |
Fang G D, Zhu C Y, Dionysiou D D, et al. Mechanism of hydroxyl radical generation from biochar suspensions:Implications to diethyl phthalate degradation[J]. Bioresource Technology, 2015, 176: 210-217. |
| [18] |
Lincoln J, Lucas D. Commercial fishing deaths:United States, 2000-2009[J]. Morbidity & Mortality Weekly Report, 2010, 59(27): 842-845. |
| [19] |
Fox T R, Comerford N B. Low-molecular-weight organic acids in selected forest soils of the southeastern USA[J]. Soil Science Society of America Journal, 1990, 54: 1139-1144. |
| [20] |
Benhamouda K, Belaidi S, Sehili T, et al. Catalytic photodegradation of rhodamine B in the presence of natural iron oxide and oxalic acid under artificial and sunlight radiation[J]. International Journal of Chemical Reactor Engineering, 2017, 15(2): 1-9. |
| [21] |
Wagner I, Strehlow H, Busse G. Flash photolysis of nitrate ions in aqueous solution[J]. Zeitschrift Für Physikalische Chemie, 1980, 123(1): 1-33. |
| [22] |
蔡轩, 龙新宪, 种云霄, 等. 无机-有机混合改良剂对酸性重金属复合污染土壤的修复效应[J]. 环境科学学报, 2015, 35(12): 3991-4002. CAI Xuan, LONG Xin-xian, ZHONG Yun-xiao, et al. Inorganic-organic amendments for immobilization of metal contaminants in an acidic soil[J]. Acta Scientiae Circumstantiae, 2015, 35(12): 3991-4002. |
| [23] |
邹佳佳, 孟梅, 张云, 等. 农田土壤铜污染评价和油菜铜积累特征研究[J]. 土壤通报, 2015, 46(3): 621-627. ZOU Jia-jia, MENG Mei, ZHANG Yun, et al. Evaluation of copper pollution status of soil and copper accumulation features of rapes in farmland[J]. Soil Bulletin, 2015, 46(3): 621-627. |
| [24] |
邢艳帅, 罗婧晗, 汪磊.苯并三唑与铜复合污染对赤子爱胜蚓的铜富集和毒性效应研究[C].中国土壤学会土壤环境专业委员会山东省土壤污染防控与修复技术研讨会. 2017. XING Yan-shuai, LUO Jing-han, WANG Lei. Study on the copper and benzotriazole enrichment on the toxicity of the Eisenia vermis[C]. Soil science society of China, specialized committee, Shandong specialized committee seminar on soil pollution control and remediation technology. 2017. http://cpfd.cnki.com.cn/Article/CPFDTOTAL-TRHJ201708001092.htm |
| [25] |
李见云, 侯彦林, 化全县, 等. 大棚设施土壤养分和重金属状况研究[J]. 土壤, 2005, 37(6): 626-629. LI Jian-yun, HOU Yan-lin, HUA Quan-xian, et al. Variation of soil nutrient and heavy metal concentrations in greenhouse soils[J]. Soils, 2005, 37(6): 626-629. DOI:10.3321/j.issn:0253-9829.2005.06.009 |
| [26] |
曾路生, 高岩, 李俊良, 等. 寿光大棚菜地酸化与土壤养分变化关系研究[J]. 水土保持学报, 2010, 24(4): 157-161. ZENG Lu-sheng, GAO Yan, LI Jun-liang, et al. Changes of acidification and nutrient accumulation in greenhouse vegetable soils in Shouguang[J]. Soil and Water Conservation Information, 2010, 24(4): 157-161. |
| [27] |
Chai C, Cheng H, Wei G, et al. Phthalic acid esters in soils from vegetable greenhouses in Shandong peninsula, east China[J]. PLoS One, 2014, 9(4): e95701. DOI:10.1371/journal.pone.0095701 |
| [28] |
Fujihira M, Satoh Y, Osa T. Heterogeneous photocatalytic reactions on semiconductor materials. Ⅲ. Effect of pH and Cu2+ ions on the photo-Fenton type reaction[J]. Journal of Electroanalytical Chemistry & Interfacial Electrochemistry, 1981, 126(1/2/3): 277-281. |
| [29] |
刘光崧. 土壤理化分析与剖面描述[M]. 北京: 中国标准出版社, 2000. LIU Guang-song. Soil physico chemical analyses and description of soil profiles[M]. Beijing: China Standard Press, 2000. |
| [30] |
鲁如坤. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社, 2000. LU Ru-kun. Agrochemical analysis methods of soil[M]. Beijing: China Agricultural Science and Technology Press, 2000. |
| [31] |
Panias D, Taxiarchou M, Paspaliaris I, et al. Mechanisms of dissolution of iron oxides in aqueous oxalic acid solutions[J]. Hydrometallurgy, 1996, 42(2): 257-265. |
| [32] |
Shuai W J, Liu C, Fang G D, et al. Nano-α-Fe2O3 enhanced photocatalytic degradation of diethyl phthalate ester by citric acid/UV(300~400 nm):A mechanism study[J]. Journal of Photochemistry & Photobiology A:Chemistry, 2018, 360: 78-85. |
| [33] |
Li A, Zhang Z, Li P, et al. Nitrogen dioxide radicals mediated mineralization of perfluorooctanoic acid in aqueous nitrate solution with UV irradiation[J]. Chemosphere, 2017, 188: 367-374. DOI:10.1016/j.chemosphere.2017.08.170 |
| [34] |
Seraghni N, Ghoul I, Lemmize I, et al. Use of oxalic acid as inducer in photocatalytic oxidation of cresol red in aqueous solution under natural and artificial light[J]. Environmental Technology, 2018, 39(22): 2908-2915. |
 2019, Vol. 38
2019, Vol. 38





