2. 广东省地质局, 广州 510080;
3. 中国地质大学(北京), 北京 100083
2. Guangdong Geological Bureau, Guangzhou 510080, China;
3. China University of Geosciences, Beijing 100083, China
近几十年来,NO3--N作为世界范围内地下水中最为普遍的污染因子[1-3],对人体健康造成了一定威胁和危害[4]。地下水具有一定的自净能力,其中净化NO3--N的主要机制为反硝化作用[5]。含水层中的反硝化作用是NO3--N在微生物作用下转化为N2O或N2的过程[6]。反硝化作用强度越大,地下水中硝酸盐的自净能力越强。因此,掌握含水层中的反硝化作用强度及其影响因素,可为地下水硝酸盐污染防控和修复提供重要理论依据。
反硝化作用强度可由反硝化速率或反硝化潜力表征。国内外地下水中的反硝化作用强度研究一直以人为添加硝态氮的控制性试验为主,因此目前研究成果以反硝化潜力为主,反硝化速率的测定研究相对较少。地下水反硝化作用强度的测定研究相比于土壤要少得多,且在国外研究较多,国内仍处于起步阶段。目前国内外研究者大多通过培养或模拟含水层材料等室内试验[7-10]或利用地下水井原位试验[11-12]等方式来实现。反硝化作用试验以野外原位试验居多,其中地下水井抽注试验最为常见[13-14]。原位抽注试验通过对比NO3--N消耗过程与Br-、SF6[15-16]等普通示踪剂穿透曲线之间的关系[17-20],或利用15N同位素示踪计算反硝化产物速率等方式[11, 21]得到反硝化强度值。试验过程中涉及的研究方法包括乙炔抑制法[22]、同位素稀释法和气压过程分离法等[16]。用于野外原位反硝化试验的地下水井包括传统常规监测井、多级监测井[23]以及有水力联系的多个循环井[24]等类型。
水文地质条件普遍存在明显的垂向变化,不同含水介质类型和不同取样深度上发生反硝化作用的水化学环境不同,这些条件对反硝化作用强度有着重要影响。深层地下水的水文地质条件更复杂(如断层构造导致的高渗透性或优先流)[25],且进行无扰动采样试验的难度很大,导致开展反硝化作用试验研究的难度非常大。因此,目前地下水反硝化作用的垂向空间分布规律尚不明了。Korom[26]曾对经典的室内外试验测定的反硝化速率结果进行了简单总结,研究成果截止到上世纪90年代初,因此也缺乏全面的含水介质类型下的反硝化强度统计分析。
整合分析是在同一研究主题下对不同研究成果的数据进行汇总和综合分析[27-28]。本研究拟通过对目前国内外已有的地下水反硝化强度的研究成果进行整合分析,从宏观上掌握不同含水介质和不同深度上地下水反硝化强度的取值范围和分布规律,从微观上明确不同含水层环境因子对地下水反硝化强度的影响程度。研究结果可为地下水中硝酸盐转化过程机理研究、地下水硝酸盐污染防控与修复等领域提供重要的理论依据。
1 材料与方法 1.1 数据来源和质量控制同时以“地下水”和“反硝化”为主题,在中国知网、维普科技期刊数据库、Web of Science(核心库)中对1957—2017年间发表的论文进行检索,共获得论文3185篇,其中与地下水反硝化强度有关的论文有740篇,包括中文论文485篇,英文论文255篇。筛选得到与地下水反硝化强度研究密切相关的文献共38篇,涉及国内外22个研究区,文献筛选标准为(1)具有明确的反硝化速率或反硝化潜力数据,或包括可解析计算反硝化作用强度的图片或表格;(2)含有含水介质类型、试验取样地点、采样深度、溶解氧等地下水背景理化性质等信息。从这些文献中共提取获得80组地下水反硝化强度数据以及相应的地下水理化性质参数,统计信息见表 1。所选文献涉及的反硝化强度单位以μg·kg-1·d-1为主,个别单位为mg·kg-1·a-1,后者乘以(365/1000)即可统一标准化为前者。反硝化强度单位意义指单位时间内在单位质量含水介质中硝态氮发生反硝化作用的净减量。
|
|
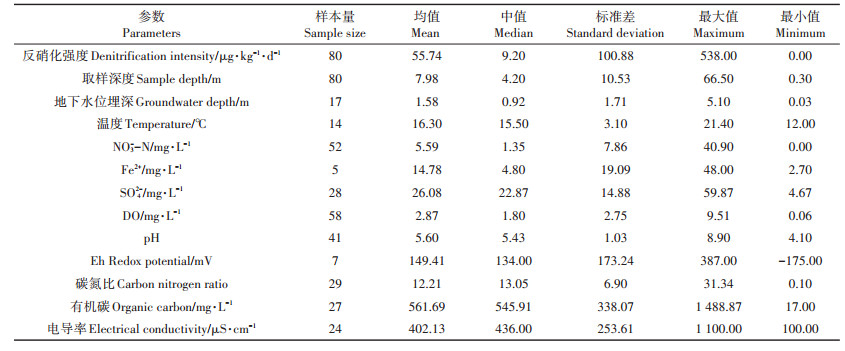
表 1 所获数据的统计信息 Table 1 Statistics of the data related to denitrification |
本次研究的技术路线见图 1。首先对已获得的地下水反硝化强度与理化性质数据集进行整理和标准化。其次,总结各类典型含水介质中的反硝化强度取值范围。然后,对不同取样深度的反硝化强度统计分析,总结反硝化强度的垂向空间分布规律。最后,重点探讨不同取样深度和溶解氧(Dissolved oxygen,DO)浓度分级条件下反硝化强度的影响因素。

|
图 1 技术路线图 Figure 1 Technical flowchart |
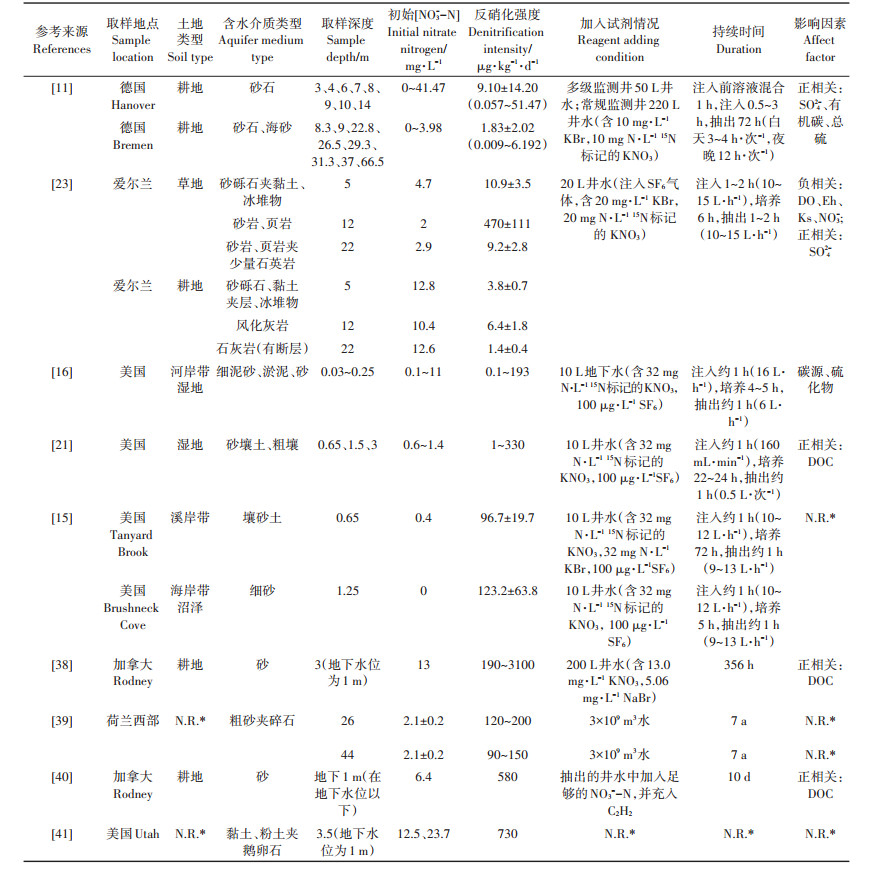
本研究在Korom总结基础上,完善统计了室内和野外原位不同试验条件下不同含水介质中的反硝化强度试验结果,见表 2和表 3。对典型含水介质类型下的反硝化强度进行归类后可知,黏土和粉土约730 μg·kg-1·d-1;砂壤土和壤砂土为1~330 μg·kg-1·d-1;细砂为0.1~193 μg·kg-1·d-1;粗砂为9~200 μg·kg-1·d-1;砂为190~3100 μg·kg-1·d-1;砂砾石为1.83~283.6 μg·kg-1·d-1,甚至可达到7646 μg·kg-1·d-1[29];砂卵石层中的反硝化强度为4~82 μg·kg-1·d-1;碎石夹黏土为100~440 μg·kg-1·d-1;砂岩和页岩为9.2~470 μg·kg-1·d-1;灰岩为1.4~6.4 μg·kg-1·d-1。部分研究表明,不同的含水介质有着不同的颗粒大小和粒间孔隙,孔隙过小可能会抑制反硝化微生物的生长,并影响其运移[30];也有学者认为小孔隙(大约50 μm)不会对微生物的生长造成影响,而地下水流速才是抑制微生物膜生长的原因[31]。因此,粒间孔隙对于反硝化强度的影响还不确定,含水介质类型与反硝化强度之间未呈现明显的规律性。
|
|
表 2 室内实验测定的地下水反硝化强度 Table 2 Groundwater denitrification intensity measured by laboratory experiment |
|
|
表 3 野外抽注实验测定的地下水反硝化强度 Table 3 Groundwater denitrification intensity measured by field experiment |
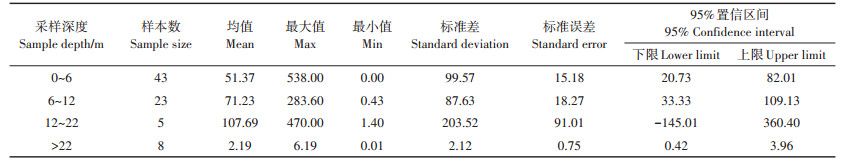
不同取样深度下地下水中反硝化强度统计分析结果见表 4。结果表明,反硝化强度值在12~22 m区间内达到峰值107.69 μg·kg-1·d-1,高于0~12 m和 > 22 m区间内的反硝化强度,反硝化强度沿含水层垂向上先逐渐增大后大幅减小,在某深度处存在峰值。Jahangir等[23]的反硝化试验研究得出下层土与基岩接触带的地下水反硝化强度高于该深度的下层土及低于该深度的基岩所对应的反硝化强度;Weymann等[9]开展的室内试验观察到自养区(地面以下6.5~7 m)的NO3-去除强度明显高于浅层区域(地面以下1.5~4 m)。这均与本研究结论基本一致。
|
|
表 4 不同取样深度下的地下水反硝化强度统计表(μg·kg-1·d-1) Table 4 Statistical of groundwater denitrification intensity under different sampling depths(μg·kg-1·d-1) |
含水层反硝化强度的影响因素包括NO3--N浓度、DO浓度、营养物质和微量元素、Eh、pH、温度、含水介质孔隙、微生物活性、盐度和抑制物质等[42]。含水层中不同深度的水文地球化学环境不同,对于使反硝化作用发生的DO浓度限值的认识也并不一致[23, 43-45]。因此,本研究根据不同取样深度和DO浓度分级研究了反硝化作用强度的影响因素。参照某一反硝化试验场地[23]的情况,取样深度分为0~6、6~12、12~22 m和 > 22 m四个等级。结合前人的研究成果将DO浓度分成0~0.2、0.2~2、2~6 mg·L-1和 > 6 mg·L-1四个等级。
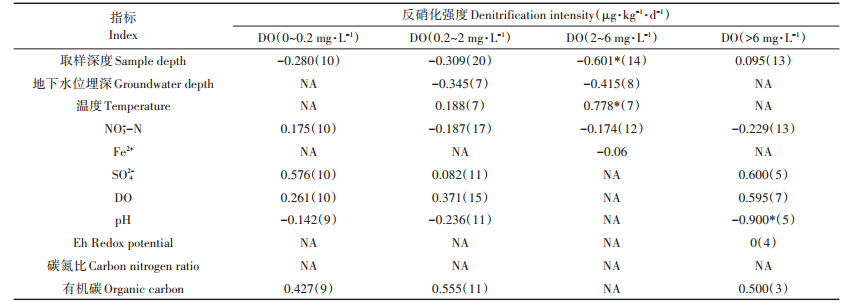
2.3.1 不同取样深度反硝化作用强度的影响因素为识别不同深度下的地下水反硝化强度的主要影响因素,采用Spearman等级相关性系数法进行统计分析,计算结果见表 5。结果表明,取样深度为0~6 m时,反硝化强度与地下水位埋深(0.03~4.2 m)、NO3--N浓度(0.40~27.59 mg·L-1)、DO浓度(0.60~9.51 mg·L-1)呈显著负相关关系,与温度(12.0~21.4 ℃)和有机碳浓度呈显著正相关关系。推测对于浅层含水层,以异养反硝化作用为主,有机碳浓度是影响反硝化强度的主导因素,有机碳为反硝化微生物的生长和新陈代谢提供了足够的能量,其含量越高,反硝化强度越大。地下水位埋深越大,淋滤进入地下水的有机碳含量越低,不利于反硝化作用的进行。NO3--N浓度过高时,会抑制N2的生成而导致N2O不断累积,不利于反硝化作用的进行[46]。当DO浓度较高时,分子态氧成为NO3--N的竞争性电子受体氧化分解有机物,不利于反硝化作用的进行。温度主要通过影响反硝化微生物的活性来影响反硝化强度,12.0~21.4 ℃处于微生物生存的适宜范围。取样深度为6~12 m时,有机碳浓度(437.95~1 488.87 mg·L-1)仍是影响反硝化强度的主导因素,二者呈显著正相关关系。取样深度为12~ 22 m时,反硝化强度与NO3--N浓度(0.63~12.6 mg·L-1)呈显著负相关。当取样深度大于22 m时,Eh(-24~ 276 mV)通过影响地下水中可溶性离子的存在形式成为影响反硝化强度的主导因素,二者呈显著负相关关系。
|
|
表 5 不同取样深度下反硝化强度和理化性质之间的Spearman相关性分析 Table 5 Spearman correlation analysis between denitrification intensity and physicochemical properties at different sampling depths |
表 6统计了不同DO浓度等级下的地下水反硝化强度。结果表明,DO浓度为0.2~2 mg·L-1时反硝化强度最大,均值可达90.94 μg·kg-1·d-1;浓度为2~6 mg·L-1时反硝化强度次之,可达51.26 μg·kg-1·d-1;DO浓度大于6 mg·L-1时反硝化强度值明显降低,均值为10.60 μg·kg-1·d-1。这三个DO浓度范围的反硝化强度符合两者之间为负相关关系的普遍规律。但当DO浓度小于0.2 mg·L-1时,反硝化强度值最低,均值为5.91 μg·kg-1·d-1,与前人[45]研究得到的该浓度下的反硝化强度最为理想的结论不一致。原因是DO浓度为0~0.2 mg·L-1的10个样本的采样深度由5 m变化至66.5 m,跨度较大,数据的代表性可能不强。
|
|
表 6 不同DO浓度下的地下水反硝化强度统计表(μg·kg-1·d-1) Table 6 Statistics of groundwater denitrification intensity under different DO concentrations(μg·kg-1·d-1) |
为进一步了解在不同DO浓度下,影响反硝化强度的主要环境因素,本文分析了其他理化性质与反硝化强度的相关性,统计分析结果见表 7。结果表明,DO浓度为0~0.2 mg·L-1时反硝化强度与SO42-(5.10~ 52.03 mg·L-1)呈不显著正相关关系,可能以自养反硝化作用为主;DO浓度为0.2~2 mg·L-1时反硝化强度与取样深度、地下水位埋深、NO3--N浓度和Eh均呈不显著负相关关系;DO浓度介于2~6 mg·L-1时,反硝化强度与取样深度(0.65~3 m)呈显著负相关关系,与温度(12~18.6 ℃)呈显著正相关;DO浓度大于6 mg·L-1时地下水属强氧化环境,反硝化强度与Eh(163~387 mV)之间呈显著负相关关系。
|
|
表 7 不同DO浓度下反硝化强度和其他理化性质之间的Spearman相关性 Table 7 Spearman correlation between denitrification intensity and other physicochemical properties at different DO concentrations |
本次研究统计结果存在一定不确定性,主要来自于试验方法、计算方法和统计过程等方面。
(1)不同研究区所采用的反硝化强度测定方法不同。本文所统计的反硝化强度数据来自于室内试验和野外试验。其中,室内试验易创造严格的厌氧环境而使反硝化强度被高估[26],相比来说,野外试验得到的反硝化强度结果更接近真实值。由于不同水文地质条件下地下水水流速度的差异,不同类型的反硝化微生物对于外加硝酸盐溶液的适应能力的不同,大多野外试验均开展预试验以确定反硝化试验溶液在地下水井的培养时间,过早或过晚抽出都会影响试验结果,培养时间几小时到几天不等[23]。
(2)不同研究区所采用的反硝化强度计算方法不同。一是本文所统计的反硝化强度测定试验多以反硝化作用产物N2O和N2进行反算,而忽略了中间产物NO2-和NO,使得反硝化强度被低估[16]。不同研究者采用的N2O收集方法有所差异,其操作规范程度[47]以及产物N2和空气中N2的区分情况也都可能影响计算结果。二是部分文献忽略了含水层中存在的稀释、平流和弥散等物理过程,使得反硝化强度被低估[48]。三是计算反硝化强度常采用15N同位素示踪法或基于Br-、SF6等示踪剂的浓度穿透曲线法,两种计算精度不同,其中15N方法高于Br-和SF6方法[7, 11]。15N同位素示踪法是将地下水反硝化作用最终产物生成速率表征为反硝化强度,如下式所示[23]。
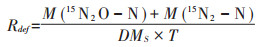
|
式中:Rdef表示地下水反硝化强度,μg·kg-1·d-1;M(15N2O-N)+M(15N2-N)表示反硝化反应后单位体积水中含有的产物N2O和N2的总质量,μg;DMS表示单位体积含水介质的干质量,kg;T表示反硝化反应时间,d。
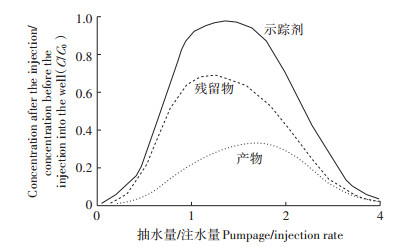
浓度穿透曲线计算法是通过测定示踪剂Br-或SF6浓度、反应物的残留量(NO3-)和可能产物(如NO2-、NO、N2O、N2)的浓度,绘制成浓度穿透曲线[20](图 2)。惰性离子或气体示踪剂用于计算C/C0,其中C表示注入井水后不同时间段的示踪剂浓度,C0表示注入井水前的示踪剂浓度。
|
图 2 用于计算反硝化强度的浓度穿透曲线图 Figure 2 Concentration breakthrough curve for calculating the denitrification intensity |
(3)取样深度和DO浓度所采用的划分方法具有一定的主观性。
3 结论(1)大多含水介质中的反硝化强度处于10-1~102 μg·kg-1·d-1量级范围内,个别砂、砂砾石含水介质可以达到103 μg·kg-1·d-1量级范围。含水介质粒间孔隙大小与反硝化强度未呈明显相关关系。
(2)反硝化强度沿含水层垂向上先逐渐增大后显著减小,在某深度处存在峰值。但由于含水介质等的不同,峰值对应的深度存在明显的区域差异。对于浅层含水层有机碳丰富的区域,以异养反硝化作用为主。反硝化强度主要受有机碳浓度影响,同时受NO3--N浓度、DO浓度、地下水位埋深、温度等因素影响较大。在深层含水层中,反硝化强度主要受Eh值影响。
(3)DO浓度与反硝化强度值整体符合负相关关系。当DO浓度介于2~6 mg·L-1时,反硝化强度与取样深度呈显著负相关,与温度呈显著正相关;当DO浓度大于6 mg·L-1时,Eh是反硝化强度的主导因素。
4 展望目前,含水介质结构、实际水文地质状况和水化学环境复杂、采样过程难度大等原因造成国内外含水层中反硝化强度研究成果相对较少。近十年,随着同位素技术、微生物技术和地下水采样技术的提升以及分子生物学、污染水文地质学等学科的发展,研究重心从室内试验转向野外原位定量试验。基于该领域当前发展水平下获取的数据和认识还比较有限,很多问题仍需进一步研究:
(1)当前的反硝化强度研究以控制性试验为主,测定的反硝化潜力是在添加外源硝态氮的条件下获得的,为了能够更加客观确定含水层中反硝化强度,需加强直接测定反硝化速率的试验研究。
(2)目前在野外原位反硝化强度测定试验中多以单井抽注试验为主,为了更好地揭示含水层中硝酸盐衰减规律,需加强开展多井抽注试验。
(3)含水层中硝酸盐发生反硝化作用的必备条件有三个,一是存在硝酸盐、反硝化微生物和电子供体(如有机碳、还原性铁/硫等),二是厌氧或半厌氧状态,三是有利的环境条件,如适宜的温度、pH、盐度、硝酸盐浓度、含水介质等[42]。因此,应加强含水介质孔隙、阻碍反硝化作用的其他物质(如重金属、杀虫剂和农药等[49])和微生物活性[50]对地下水中反硝化强度的影响研究。特别是,对于反硝化作用中有效微生物的代谢途径和特定微生物的特性仍不清楚[51],加强反硝化微生物试验有利于探索影响反硝化作用的更深层次的因素。
(4)随着全球范围内对粮食和能源日益增长的需求,人为投入的氮极大地改变了氮的生物地球化学循环,过量的氮素投入导致地下水硝酸盐含量超标等环境问题,因此量化研究地下水中的氮循环过程是区域环境和人类健康的重要议题[52]。含水层反硝化过程是全球氮循环过程中的重要组成部分,反硝化过程产生的N2、NO和N2O是氮支出比例最高的去向[53],因此加强含水层反硝化强度精确定量研究,进一步研究地下水氮素输出量,对保护水生态环境、保持大尺度及全球氮循环动态平衡具有重要意义。
| [1] |
Bailey R T, Ahmadi M, Gates T K, et al. Spatially distributed influence of agro-environmental factors governing nitrate fate and transport in an irrigated stream-aquifer system[J]. Hydrology and Earth System Sciences, 2015, 19(12): 4859-4876. DOI:10.5194/hess-19-4859-2015 |
| [2] |
Gilmore T E, Genereux D P, Solomon D K, et al. Quantifying the fate of agricultural nitrogen in an unconfined aquifer:Stream-based observations at three measurement scales[J]. Water Resources Research, 2016, 52(3): 1961-1983. DOI:10.1002/2015WR017599 |
| [3] |
Nakagawa K, Amano H, Asakura H, et al. Spatial trends of nitrate pollution and groundwater chemistry in Shimabara, Nagasaki, Japan[J]. Environmental Earth Sciences, 2016, 75(3): 1-17. |
| [4] |
Su X, Wang H, Zhang Y. Health risk assessment of nitrate contamination in groundwater:A case study of an agricultural area in Northeast China[J]. Water Resources Management, 2013, 27(8): 3025-3034. DOI:10.1007/s11269-013-0330-3 |
| [5] |
Iribar A, Hallin S, Pérez J M S, et al. Potential denitrification rates are spatially linked to colonization patterns of nosZ genotypes in an alluvial wetland[J]. Ecological Engineering, 2015, 80: 191-197. DOI:10.1016/j.ecoleng.2015.02.002 |
| [6] |
陈建耀, 王亚, 张洪波, 等. 地下水硝酸盐污染研究综述[J]. 地理科学进展, 2006, 25(1): 34-44. CHEN Jian-yao, WANG Ya, ZHANG Hong-bo, et al. Overview on the studies of nitrate pollution in groundwater[J]. Process in Geography, 2006, 25(1): 34-44. DOI:10.3969/j.issn.1007-6301.2006.01.004 |
| [7] |
Clague J C, Stenger R, Clough T J. Denitrification in the shallow groundwater system of a lowland catchment:A laboratory study[J]. Catena, 2015, 131: 109-118. DOI:10.1016/j.catena.2015.03.012 |
| [8] |
Eschenbach W, Well R. Predicting the denitrification capacity of sandy aquifers from shorter-term incubation experiments and sediment properties[J]. Biogeosciences, 2013, 10(2): 1013-1035. DOI:10.5194/bg-10-1013-2013 |
| [9] |
Weymann D, Geistlinger H, Well r, et al. Kinetics of N2O production and reduction in a nitrate-contaminated aquifer inferred from laboratory incubation experiments[J]. Biogeosciences, 2010, 7(6): 1953-1972. DOI:10.5194/bg-7-1953-2010 |
| [10] |
何晓锋.地下水饱和带硝酸盐迁移转化的试验研究[D].合肥: 合肥工业大学, 2007: 21-45. HE Xiao-feng. Experimental study of nitrate transportation and reduction in saturated zone[D]. Hefei: Hefei Industrial University, 2007: 21-45. http://cdmd.cnki.com.cn/Article/CDMD-10359-2007102554.htm |
| [11] |
Eschenbach W, Well R, Walther W. Predicting the denitrification capacity of sandy aquifers from in situ measurements using push-pull 15N tracer tests[J]. Biogeosciences, 2015, 12(8): 2327-2346. DOI:10.5194/bg-12-2327-2015 |
| [12] |
程东会.北京城近郊区地下水硝酸盐氮和总硬度水文地球化学过程及数值模拟[D].北京: 中国地质大学(北京), 2007: 12. CHENG Dong-hui. Study on the hydrogeochemical process and numerical model of nitrate and total hardness in Beijing urban[D]. Beijing: China University of Geosciences(Beijing), 2007: 12. http://cdmd.cnki.com.cn/Article/CDMD-82501-2007066929.htm |
| [13] |
Cho Y, Han K, Kim N, et al. Estimating in situ biodegradation rates of petroleum hydrocarbons and microbial population dynamics by performing single-well push-pull tests in a fractured bedrock aquifer[J]. Water, Air, & Soil Pollution, 2013, 224(2): 1364. |
| [14] |
Warneke S, Schipper L A, Bruesewitz D A, et al. A comparison of different approaches for measuring denitrification rates in a nitrate removing bioreactor[J]. Water Research, 2011, 45(14): 4141-4151. DOI:10.1016/j.watres.2011.05.027 |
| [15] |
Addy K, Kellogg D Q, Gold A J, et al. In situ push-pull method to determine ground water denitrification in riparian zones[J]. Journal of Environmental Quality, 2002, 31(3): 1017-1024. DOI:10.2134/jeq2002.1017 |
| [16] |
Harrison M D, Groffman P M, Mayer P M, et al. Denitrification in alluvial wetlands in an urban landscape[J]. Journal of Environment Quality, 2011, 40(2): 634-646. DOI:10.2134/jeq2010.0335 |
| [17] |
Istok J D, Humphrey M D, Schroth M H, et al. Single-well, "pushpull" test for in situ determination of microbial activities[J]. Ground Water, 1997, 35(4): 619-631. DOI:10.1111/gwat.1997.35.issue-4 |
| [18] |
Schroth M H, Istok J D, Conner G T, et al. Spatial variability in in situ aerobic respiration and denitrification rates in a petroleum-contaminated aquifer[J]. Ground Water, 1998, 36(6): 924-937. DOI:10.1111/gwat.1998.36.issue-6 |
| [19] |
Clough T J, Addy K, Kellogg D Q, et al. Dynamics of nitrous oxide in groundwater at the aquatic-terrestrial interface[J]. Global Change Biology, 2007, 13(7): 1528-1537. DOI:10.1111/gcb.2007.13.issue-7 |
| [20] |
郇环.松花江吉林段地下水脆弱性评价研究[D].北京: 北京师范大学, 2012: 36. HUAN Huan. Groundwater vulnerability assessment in Jilin section of the Songhua River[D]. Beijing: Beijing Normal University, 2012: 36. |
| [21] |
Kellogg D Q, Gold A J, Groffman P M, et al. In situ ground water denitrification in stratified, permeable soils underlying riparian wetlands[J]. Journal of Environmental Quality, 2005, 34(2): 524-533. DOI:10.2134/jeq2005.0524 |
| [22] |
Sgouridis F, Stott a, Ullah S. Application of the 15N gas-flux method for measuring in situ N2 and N2O fluxes due to denitrification in natural and semi-natural terrestrial ecosystems and comparison with the acetylene inhibition technique[J]. Biogeosciences, 2016, 13(6): 1821-1835. DOI:10.5194/bg-13-1821-2016 |
| [23] |
Jahangir M M R, Johnston P, Addy K, et al. Quantification of in situ denitrification rates in groundwater below an arable and a grassland system[J]. Water, Air, & Soil Pollution, 2013, 224(9): 1693. |
| [24] |
Burbery L F, Flintoft M J, Close M E. Application of the re-circulating tracer well test method to determine nitrate reaction rates in shallow unconfined aquifers[J]. Journal of Contaminant Hydrology, 2013, 145: 1-9. DOI:10.1016/j.jconhyd.2012.11.006 |
| [25] |
Buss S R, Rivett M O, Morgan P, et al. Attenuation of nitrate in the subsurface environment[R]. England: Environment Agency Science Group Report, SC030155/2, 2005.
|
| [26] |
Korom S F. Natural denitrification in the saturated zone:A review[J]. Water Resources Research, 1992, 28(6): 1657-1668. DOI:10.1029/92WR00252 |
| [27] |
Niu B, Loáiciga H A, Wang Z, et al. Twenty years of global groundwater research:A science citation index expanded-based bibliometric survey(1993-2012)[J]. Journal of Hydrology, 2014, 519: 966-975. DOI:10.1016/j.jhydrol.2014.07.064 |
| [28] |
宋长青, 谭文峰. 基于文献计量分析的近30年国内外土壤科学发展过程解析[J]. 土壤学报, 2015, 52(5): 957-969. SONG Chang-qing, TAN Wen-feng. The historical venation of soil cience in the past 30 years-based on the bibliometric analysis[J]. Acta Pedologica Sinica, 2015, 52(5): 957-969. |
| [29] |
Sánchez-pérez J M, Bouey C, Sauvage S, et al. A standardised method for measuring in situ denitrification in shallow aquifers:Numerical validation and measurements in riparian wetlands[J]. Hydrology and Earth System Sciences, 2003, 7(1): 87-96. DOI:10.5194/hess-7-87-2003 |
| [30] |
West J M, Chilton P J. Aquifers as environments for microbiological activity[J]. Quarterly Journal of Engineering Geology and Hydrogeology, 1997, 30(2): 147-154. DOI:10.1144/GSL.QJEGH.1997.030.P2.06 |
| [31] |
Seiler Seiler K, Vomberg I. Denitrification in a karst aquifer with matrix porosity[J]. Nitrates in Groundwater:IAH Selected Papers on Hydrogeology, 2004(5): 87. |
| [32] |
Lind A M. Nitrate reduction in the subsoil[M]//Denitrification in the nitrogen cycle. Boston, MA:Springer, 1985:145-156.
|
| [33] |
Slater J M, Capone D G. Denitrification in aquifer soil and nearshore marine sediments influenced by groundwater nitrate[J]. Applied and Environmental Microbiology, 1987, 53(6): 1292-1297. |
| [34] |
Morris J T, Whiting G J, Chapelle F H. Potential denitrification rates in deep sediments from the southeastern coastal plain[J]. Environmental Science & Technology, 1988, 22(7): 832-836. |
| [35] |
Smith R L, Duff J H. Denitrification in a sand and gravel aquifer[J]. Applied and Environmental Microbiology, 1988, 54(5): 1071-1078. |
| [36] |
Francis A J, Slater J M, Dodge C J. Denitrification in deep subsurface sediments[J]. Geomicrobiology Journal, 1989, 7(1/2): 103-116. |
| [37] |
Smith R L, Howes B L, Duff J H. Denitrification in nitrate-contaminated groundwater:Occurrence in steep vertical geochemical gradients[J]. Geochimica et Cosmochimica Acta, 1991, 55(7): 1815-1825. DOI:10.1016/0016-7037(91)90026-2 |
| [38] |
Trudell M R, Gillham R W, Cherry J A. An in-situ study of the occurrence and rate of denitrification in a shallow unconfined sand aquifer[J]. Journal of Hydrology, 1986, 83(3/4): 251-268. |
| [39] |
Beek C, Puffelen V J. Changes in the chemical composition of drinking water after well infiltration in an unconsolidated sandy aquifer[J]. Water Resources Research, 1987, 23(1): 69-76. DOI:10.1029/WR023i001p00069 |
| [40] |
StarR R C, Gillham R W. Controls on denitrification in shallow unconfined aquifers[J]. Contaminant Transport in Groundwater. Kobus & Kinzelbach, Rotterdam, 1989, 51-56. |
| [41] |
Korom S F. Denitrification in the unconsolidated deposits of the Heber Valley aquifer[D]. Logan: Utah State University, Dept of Civil and Environmental Engineering, 1991: 65.
|
| [42] |
Rivett M O, Buss S R, Morgan P, et al. Nitrate attenuation in groundwater:A review of biogeochemical controlling processes[J]. Water Research, 2008, 42(16): 4215-4232. DOI:10.1016/j.watres.2008.07.020 |
| [43] |
Skerman V B D, Macrae I C. The influence of oxygen availability on the degree of nitrate reduction by seudomonas denitrificans[J]. Canadian Journal of Microbiology, 1957, 3(3): 505-530. DOI:10.1139/m57-055 |
| [44] |
Gillham R W, Cherry J A. Field evidence of denitrification in shallow groundwater flow systems[J]. Water Quality Research Journal, 1978, 13(1): 53-72. DOI:10.2166/wqrj.1978.006 |
| [45] |
Desimone L A, Howes B L. Nitrogen transport and transformations in a shallow aquifer receiving wastewater discharge:A mass balance approach[J]. Water Resources Research, 1998, 34(2): 271-285. DOI:10.1029/97WR03040 |
| [46] |
Blackmer A M, Bremner J M. Inhibitory effect of nitrate on reduction of N2O to N2 by soil microorganisms[J]. Soil Biology and Biochemistry, 1978, 10(3): 187-191. DOI:10.1016/0038-0717(78)90095-0 |
| [47] |
Jurado A, Borges A V, BROUYÈRE S. Dynamics and emissions of N2O in groundwater:A review[J]. Science of the Total Environment, 2017(584/585): 207-218. |
| [48] |
Green C T, Böhlke J K, Bekins B A, et al. Mixing effects on apparent reaction rates and isotope fractionation during denitrification in a heterogeneous aquifer[J]. Water Resources Research, 2010, 46(8). DOI:10.1029/2009WR008903 |
| [49] |
Hunter W J. Accumulation of nitrite in denitrifying barriers when phosphate is limiting[J]. Journal of Contaminant Hydrology, 2003, 66(1/2): 79-91. |
| [50] |
Zhang D, Li G, Yang Y S, et al. Bio-geological processes of nitrogen transport and transformation in the aeration zone and aquifer[J]. Hydrological Sciences Journal, 2009, 54(2): 316-326. DOI:10.1623/hysj.54.2.316 |
| [51] |
李发东, 张妍, 李静. 地下水硝酸盐去除中反硝化微生物的研究进展[J]. 中国生态农业学报, 2013, 21(1): 110-118. LI Fa-dong, ZHANG Yan, LI Jing. Research review of denitrifying microorganisms of groundwater to nitrate denitrification[J]. Chinese Journal of Eco-Agriculture, 2013, 21(1): 110-118. |
| [52] |
谷保静.人类-自然耦合系统氮循环研究-中国案例[D].杭州: 浙江大学, 2011: 1-2. GU Bao-jing. Nitrogen Cycle of coupled human and natural systemA case study of China[D]. Hangzhou: Zhejiang University, 2011: 1-2. http://cdmd.cnki.com.cn/Article/CDMD-10335-1012338326.htm |
| [53] |
遆超普.不同空间尺度区域氮素收支[D].南京: 南京农业大学, 2010: 111-112. TI Chao-pu. Regional nitrogen budget at different spatial scales[D]. Nanjing: Nanjing Agricultural University, 2010: 111-112. http://cdmd.cnki.com.cn/Article/CDMD-10307-1012271465.htm |
 2019, Vol. 38
2019, Vol. 38