2. 重庆市农业资源与环境研究重点实验室, 重庆 400716;
3. 三峡库区生态环境教育部重点实验室, 重庆 400716
2. Chongqing Key Laboratory of Agricultural Resources and Environment, Chongqing 400716, China;
3. China Key Laboratory of the Three Gorges Reservoir Region's Eco-Environment, Ministry of Education, Chongqing 400716, China
随着我国经济的发展和城市化进程的加快,我国耕地土壤重金属污染问题日趋突出。据估计,我国目前受重金属污染的耕地面积近2000万hm2,约占总耕地面积的1/5[1]。土壤中的重金属可被作物吸收累积,最终通过食物链进入人体,对人体健康构成极大的威胁。其中,以Cd污染最为普遍,其点位超标率达到7%,在几种重金属中位居第一[2-3],全国不少地区(如湖南、广西等)土壤Cd含量已经远远超过我国土壤环境质量标准三级标准[4],同时土壤中的Cd移动性强、生物累积性较高,对人体心、肝、肾等多个器官存在严重损害且具有“三致”效应,被列为优先控制重金属之一[5]。人体Cd超标不仅会影响人类的新陈代谢与身体机能,还会造成胎儿发育畸形、生殖障碍等,人群Cd接触暴露的主要途径是食物的摄入,土壤、污泥、灌溉污水和大气沉降颗粒物等各种介质中的Cd,通过食物链形成“从土壤到餐桌”的污染[6-7]。
Cd在土壤中的吸附-解吸过程是控制其生物有效性的关键过程。天然有机质(Natural organic matter,NOM)广泛存在于土壤、沉积物等环境介质,由于其复杂的分子结构和所带的多种功能基团,具有极高的反应活性,作为污染物的络合剂和吸附剂,对土壤吸附-解吸性能有着重要的影响,从而制约重金属形态转化和生物有效性[8-10]。NOM对Cd吸附-解吸的效应与其组成和性质关系密切。对于NOM组分与效应的研究,经典的方法是按照NOM的溶解特性区分为胡敏素(HM)、胡敏酸(HA)和富里酸(FA)等,并认为HA和FA是NOM的主要活性组分,围绕两者对土壤重金属环境行为的影响开展了大量研究,如王青清[11]、王俊[12]研究比较了HA和FA对紫色土Pb、As吸附-解吸行为的影响,表明HA可有效促进土壤Pb、As的吸附,FA则降低了土壤Pb、As吸附能力。李光林等[13]研究了溶液体系中HA和FA对Cu、Cd吸附-解吸特征的影响,表明Cu、Cd吸附容量FA>HA,吸附强度HA>FA,解吸量FA>HA。Yang等[14]从单一土壤沉积物中依次提取四个HA组分,结果显示较早提取的HA组分对Cu2+亲和力更好。有研究表明官能团是影响NOM对金属离子吸附的主要因素[15-16]。从垃圾渗滤液中提取的HA对Cd的吸附与其羧基数量成正相关[17]。而从土壤中提取的NOM对重金属吸附效果,则受其pH和羧基、酚羟基的离子强度影响[18]。含氮和含硫基团也在结合重金属方面发挥着重要作用[19]。这些研究反映出NOM对重金属的调控效应确实随其组成、来源的不同而异,但是在实际的环境介质中NOM不同组分分子量应该是连续分布,很难区分为HA和FA。事实上,NOM中的HA和FA组分在基本分子构成单元上并无本质区别,而分子大小可能是其影响土壤重金属环境行为的关键,不同NOM的影响差异是其不同组分综合作用所体现的表观效应,但目前对NOM影响重金属吸附-解吸行为的研究较少,特别是对于NOM的效应与其分子组成和性质的关系缺乏深入研究。
为此,本研究以污染危害大、污染范围广的重金属Cd为对象,采用切向超滤连续分级方法,将NOM区分为不同分子量组分,研究比较NOM及其不同分子量组分对紫色土Cd吸附-解吸的影响,分析NOM不同分子量组分元素组成、活性功能基团含量与其对土壤Cd吸附-解吸行为影响效应之间的关系,探究各组分不同浓度NOM对土壤吸附Cd的影响。以期深化对NOM调控重金属土壤环境行为的认识,同时为利用含NOM材料进行土壤Cd污染修复提供科学依据。
1 材料和方法 1.1 供试材料 1.1.1 供试土壤供试土壤为西南地区广泛分布的紫色土——灰棕紫泥(Grey-brown purplish soil,GPS),采集自重庆市涪陵区耕地土壤表层(0~20 cm)。所采土样去除砾石及植物残体,自然风干后磨细过2 mm标准筛,用于后续的土壤培养试验。供试土壤的基本理化性质结果见表 1。
|
|
表 1 供试土壤基本理化性质 Table 1 Basic physicochemical properties of soil sample |
供试NOM提取自重庆市北碚区缙云山国家自然保护区森林土壤腐殖质层(A0)。该自然保护区植物种类丰富,分246科992属1966种。取样点位于保护区核心区,受人为活动影响较少,A0层厚度10~50 cm,植被类型为混交林。
1.2 试验方法 1.2.1 NOM的提取和组分分级与性质表征按照国际腐植酸学会(IHSS)推荐的方法,土样过2.00 mm筛,室温下1 mol·L-1 HCl在pH 1~2范围内振荡平衡土样。用0.1 mol·L-1 HCl来调整土样悬浊液的液体体积,液:土=10:1(V/W)。悬浊液振荡1 h后低速离心分离,移除上清液,保留剩余土样。用1 mol·L-1 NaOH调整剩余土样pH至中性(pH=7.0),N2氛围中,按液:土=10:1(V/W)添加0.1 mol·L-1 NaOH溶液,间歇性振荡4 h后,将碱性悬浊液静置过夜,然后离心分离获得上清液,碱溶重复三次。提取NOM粗样后,采用0.1 mol·L-1 HCl和0.3 mol·L-1 HF纯化,直到灰分含量低于1%。将纯化后的溶液pH调至7,并过0.45 μm滤膜。采用Amicon Ultrafiltration Stirred Cell 8400(Beverley,MA,USA)将纯化提取到的NOM样品超滤分级,滤膜截留分子量为5000、10 000、30 000,获得四个不同分子量的组分:组分F1,分子量 < 5000;组分F2,5000~10 000;组分F3,10 000~30 000;组分F4,>30 000。同时保留一份未分级NOM(原NOM),记为F0,不同组分冷冻干燥获得固体样品备用。对不同分子量组分进行元素组成测定、活性功能基团的测定等,表征各分子组分特征,用于后续研究。
1.2.2 NOM对Cd的等温吸附-解吸的影响试验称取上述供试土壤50 g备16份,按土质量0.1%、0.2%、0.5%的C含量分别添加未分级NOM(F0)及其不同分子量组分(F1、F2、F3、F4),留一份不添加NOM的原土作为对照(CK)。NOM以水溶液形式加入,并人工充分搅拌均匀,风干备用。称取上述土样各1.000 g于50 mL塑料离心管中,按水土比20:1加入不同浓度的CdCl2溶液(0、1、5、10、20、30、40、50 mg· L-1 Cd),支持电解质为0.01 mol·L-1 Na(NO)3,在摇床中以转速220 r·min-1恒温25 ℃振荡24 h后,以4000 r·min-1离心10 min,取上清液分别测Cd浓度,根据吸附平衡前后上清液Cd浓度差值,计算吸附量。每组试验设三个平行。
吸附试验完成后,倾去上清液,用去离子水轻轻洗净土壤表层,在残留土壤中加入20 mL 0.01 mol· L-1 Na(NO)3溶液,搅拌均匀,在相同条件下振荡24 h,4000 r·min-1离心10 min。测定上清液Cd浓度,计算土壤Cd解吸量。
1.3 分析方法土壤pH、有机质含量、可溶性有机碳(DOC)、全氮等基本理化性质的测定参照《土壤农化分析与环境监测》 [20]。其中,pH采用pH测量仪测定;土壤DOC采用超纯水提取,碳氮分析仪进行测定;土壤全氮测定采用凯式定氮法;全磷采用HClO4-H2SO4消化,钼锑抗比色法测定,全钾采用火焰光度法。土壤有机质采用重铬酸钾容量法-外加热法测定。吸附解吸上清液中Cd采用火焰原子吸收分光光度法测定(TAS-900,北京普析)。NOM及其不同组分的C、H、O、N、S等主要元素含量采用元素分析仪(Vario EL Cube)测定,计算H/C、O/H、O/C、C/N。采用Ba(OH)2和(CH3COO)2Ca间接滴定法测定不同分子量NOM酸性功能基团的含量[21]。
1.4 数据处理采用Microsoft Excel 2007进行数据整理,Origin Pro 8进行数据分析作图。
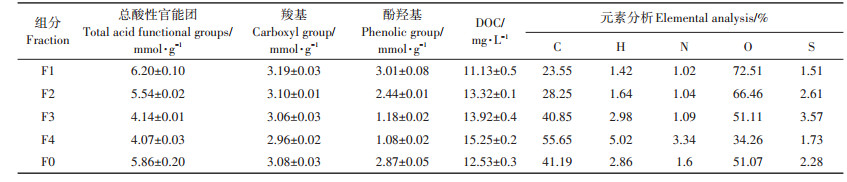
2 结果与讨论 2.1 NOM及其不同分子量组分的元素组成与功能基团含量特征NOM及其不同分子量组分元素和主要功能基团含量如表 2所示。由表 2可见,NOM各分子组分元素组成具有一定规律性,其中C、H含量随着NOM组分分子量的增大而增大,而O元素则相反。N元素含量虽随着NOM分子量增加而增大,但组分F1、F2、F3相差不大(1.02%~1.09%),组分F4中N元素含量明显上升,约为组分F3的3倍。组分F0(未分级NOM)C、N元素含量均介于F3和F4之间,其中C元素含量与F3接近,N元素含量大于F3。
|
|
表 2 元素组成和酸性官能团分析 Table 2 Elemental compositions and acidic functional groups of HA fractions |
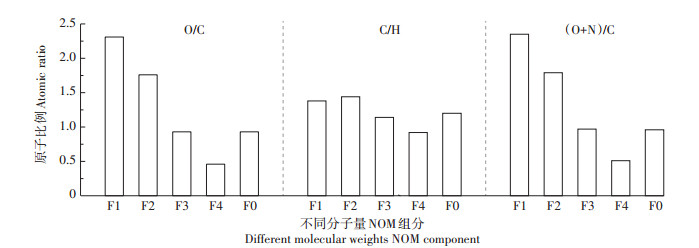
腐植酸中的O/C、H/C等原子比通常可以用来描述腐植酸的结构和性质差异[22-24]。NOM各组分原子比例如图 1所示。其中,O/C通常代表腐植酸中羧酸等含氧官能团含量和氧化程度[25],随着分子量的增加,此比值降低。C/H可以标志有机质的来源和结构[26]。组分F2的C/H较高(1.44),说明F2含有更多的芳香烃结构,而组分F4的C/H较低(0.92),说明F4组分脂肪化程度较高。(O+N)/C作为极性指标,随着各组分分子量的增加,此比值逐渐降低。综上所述,分子量越大,NOM组分氧化程度越低,极性越弱。分子量>5000时,分子量越大,NOM的缩合程度越低,芳香结构物质含量减少,脂肪性物质增加。Chen等[27]从泥炭土中提取HA分为不同分子量级后,也发现低分子量HA具有极性和芳香结构。总酸性基团、羧基、酚羟基均随着分子量的增大而减小,与O/C顺序一致。其中羧基的变化并不明显(2.96~3.19 mmol·g-1),可见酚羟基的减少是总酸性官能团含量降低的原因。组分F0的O/C和(O+N)/C值与F3相接近,但C/H值介于F2与F3之间。和其余组分相比,F0羧基变化也并不明显,酚羟基和总酸性官能团含量介于组分F1与F2之间。
|
图 1 不同分子量NOM组分O/C、C/H、(O+N)/C比值 Figure 1 The atomic ratio of different molecular weights NOM |
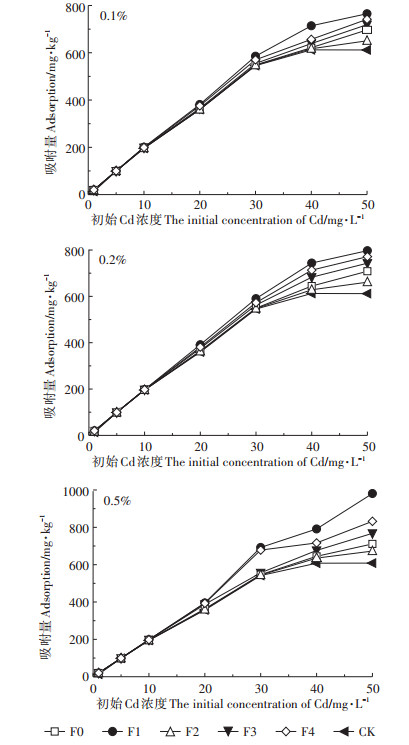
不同NOM处理土壤Cd吸附量随Cd添加浓度的变化如图 2所示。NOM不同组分对土壤Cd吸附的影响与其添加量有关:当土壤中NOM组分添加量在0.2%(以C计)以下时,只有土壤Cd初始浓度达到30 mg·L-1,土壤Cd的吸附量才表现出明显差异,而当NOM组分添加量为0.5%时,土壤Cd浓度在20 mg·L-1时不同处理之间即表现明显差异。说明在低NOM用量或较低Cd水平下,Cd的吸附主要受土壤自身性质的影响,随NOM或Cd初始浓度水平的增加,NOM对土壤Cd吸附性能的影响越明显。有研究表明,随着NOM溶液中重金属质量浓度的增加,二者之间的结合大致可分为三个阶段[28-30]:一是重金属离子主要与NOM中的强官能团结合;二是重金属离子开始与NOM中的弱官能团结合;三是重金属离子与NOM中所有可利用的官能团结合。因此当Cd初始质量浓度逐渐增加,NOM中官能团利用率逐步提升,NOM对土壤Cd吸附性能影响也越明显。同时,NOM对土壤Cd吸附量的影响与NOM组分分子量有关,在0.1%、0.2% C和Cd≥30 mg·L-1以及0.5% C和Cd≥20 mg·L-1添加量条件下,不同组分处理土壤Cd吸附量大小顺序均表现为F1>F4>F3>F0>F2>CK。说明NOM及其组分的添加均增加了土壤对Cd的表观吸附能力。当添加0.5% C组分F1时,Cd吸附量(987.3 mg·kg-1)较CK(612.4 mg·kg-1)增加了61.22%。当添加0.1% C组分F2时,Cd吸附量(650.7 mg·kg-1)较CK增加6.25%。未添加NOM的对照(CK)处理在Cd初始添加浓度为40 mg·kg-1时,吸附基本达到饱和,而添加NOM及其组分的土壤Cd吸附量还在持续上升。这表明NOM及其组分的增加提高了土壤对Cd的吸附容量;但不同组分对土壤Cd吸附能力的影响方向和程度存在差异:添加组分F1、F3、F4的土壤与未分级NOM(F0)处理的土壤相比,土壤对Cd的吸附能力明显提高,其中添加组分F1的土壤对Cd的吸附量与添加F0土壤相比,增加了约9.8%~37.98%,而添加组分F2的土壤Cd的吸附量与F0相比反而降低了约5.35%~6.68%。可见NOM组分对土壤Cd吸附的影响随其分子量大小的变化不存在线性依存关系,反映出NOM组分对土壤Cd吸附影响的复杂性。
|
图 2 添加不同浓度不同分子量NOM的土壤对Cd吸附量的影响 Figure 2 Effects of the adsorption amount of Cd in soil with different fractions and molecular weight NOM |
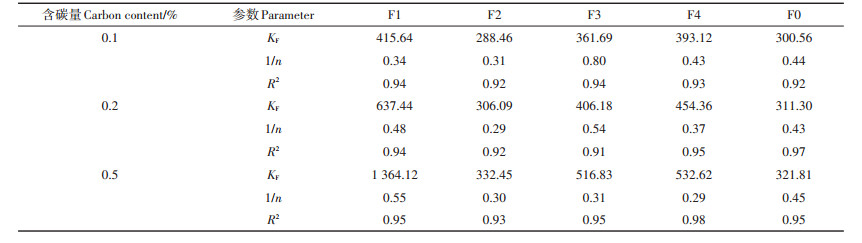
为进一步探讨NOM及其不同分子组分对土壤吸附能力的改变,采用Langmuir、Freundlich等几种常用等温吸附方程对NOM不同组分影响下的吸附数据进行拟合,结果表明Freundlich方程拟合效果最好,能很好地描述NOM各组分在不同浓度下Cd的吸附行为,决定系数R2>0.92(表 3)。
|
|
表 3 添加不同浓度不同分子量NOM的土壤Freundlich模型等温吸附参数 Table 3 Isothermal adsorption parameters of Freundlich model with different fractions and molecular weight of NOM |
Freundlich模型表达式为:Qe=KF×Ce1/n。
式中:Qe为土壤Cd吸附浓度,mg·L-1;Ce为吸附平衡液Cd浓度,mg·L-1;KF为和吸附能力有关的常数,KF值越高,则吸附剂对吸附质的吸附能力越强。据表 3可知,吸附能力大小为F1>F4>F3>F0>F2>CK。和图 2分析结果一致。等温吸附模型拟合结果进一步证明,NOM及其各组分的添加改变了土壤对Cd的吸附性能,且各组分对土壤吸附性能的影响差异明显。同样,由常数KF可知,同种NOM组分C添加越高,NOM及其不同组分处理的土壤对Cd吸附能力的影响越明显。
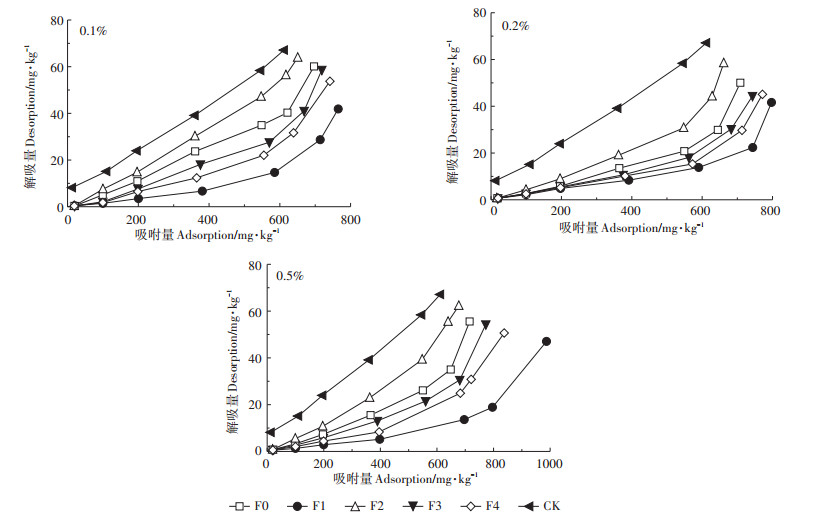
2.3 NOM及其不同分子量组分影响下土壤吸附Cd的解吸特征土壤吸附重金属离子的解吸特性与其释放能力密切相关,解吸量直接影响土壤溶液以及农作物吸收重金属的含量。不同NOM处理土壤Cd解吸量随Cd吸附量的变化如图 3所示:NOM各单一组分解吸量均随吸附量的增大而增大。这一结论与李灵等[31]的研究结果相似。其中,未添加NOM的对照(CK)处理Cd的解吸量最多,解吸率约为10.97%,其余组分中F2解吸率最高为9.19%,相比CK降低16.22%;F1解吸率最低为4.77%,相比CK降低56.52%,可见CK对Cd的吸持强度最弱;NOM及其组分添加后均提高了土壤对Cd的吸持强度,降低了土壤Cd释放的环境风险。但添加不同分子量NOM土壤对Cd的吸持强度的影响方向和强度存在差异。在0.1%、0.2%和0.5%添加量下,不同组分处理土壤Cd解吸量大小顺序均表现为CK>F2>F0>F3>F4>F1。其顺序与吸附量相反。以含碳量0.5%的NOM为例,F0、F1、F2、F3、F4各组分最大吸附量分别为715.5、987.3、677.2、772.7 mg·kg-1和837.7 mg · kg-1时,解吸量分别为55.56、47.05、62.24、54.32 mg·kg-1和50.64 mg·kg-1,由此可得解吸率分别为7.77%、4.77%、9.19%、7.03%、6.05%。与F0组分相比,添加组分F1的土壤对Cd吸持强度增强,解吸率降低38.63%,而F2处理的土壤对Cd吸持强度降低,土壤Cd解吸率较F0增加了18.02%。结合图 2可知,同等条件下(以含碳量计)NOM土壤对Cd吸持强度大小为F1>F4>F3>F0>F2。NOM不同组分对土壤Cd吸持强度的影响与其对吸附量大小的影响作用顺序一致。可见NOM组分对土壤Cd解吸的影响随其分子量大小的变化亦不存在线性依存关系。
|
图 3 添加不同浓度不同分子量NOM的土壤Cd吸附量与解吸量的关系 Figure 3 Relationship between the desorption and absorption amount of Cd in soil with different fractions and molecular weight NOM |
前述分析结果表明,本试验中分子量 < 5000的F1组分对土壤Cd吸附的促进作用最大,而分子量5000~ 10 000的F2组分则低于未分级NOM(F0),当组分分子量>10 000时,则随组分分子量的增加,对土壤Cd吸附的促进作用增强(F4>F3),各组分对土壤Cd吸附影响与其分子量之间存在非线性依存关系。这一现象与以往的认识不完全一致,以往研究普遍认为中低分子量组分如简单有机酸、富里酸等可降低土壤重金属的吸持能力,提高其移动性和植物有效性,高分子组分如腐植酸对土壤重金属则主要起吸持和固定作用,从而降低重金属的移动性和生物活性[32-35]。
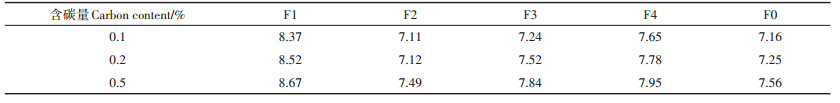
NOM对土壤重金属吸附的可能的途径包括NOM作为天然吸附剂或络合剂的直接吸附作用、在土壤溶液中与重金属离子络合而改变其在土壤固相的吸附性能[36]、或通过影响土壤pH和有机-无机复合体状态等理化性质,进而影响其对金属离子的吸附过程[37]。本试验中,NOM以溶液形式先加入土壤,待土壤风干后进行吸附试验,在此过程中(约2周)NOM已经对土壤性质产生了影响,其中,以土壤pH的变化最为明显(表 4),而pH是影响土壤Cd吸附的众多因素中的关键因素。添加不同组分NOM土壤pH值高低顺序为F1>F4>F3>F0>F2,与NOM影响下土壤Cd吸附量、吸持强度顺序一致。与CK(8.13)相比,除F1组分处理的土壤pH值升高外,其余组分pH值均降低。其中,组分F2处理pH值相比F0有所降低,而组分F3、F4 pH值相比F0升高。有研究表明,在pH为中性到碱性的条件下,pH升高,生成Cd的沉淀物反应增强[38-40]。杨毅等[41]研究也证明了土壤对Cd的吸附性与pH有关。随着pH值增大,腐植酸与Cd2+作用后Zeta电位绝对值增大而粒径逐渐减小,且腐植酸与Cd2+的结合稳定性和结合量逐渐增强。单瑞娟等[42]研究表明,随着pH升高,腐植酸对土壤重金属Cd的解吸量降低,对土壤Cd吸持作用加强。本试验研究中,F2组分加入土壤中后,土壤pH(7.11~7.12)远小于添加F1组分的土壤pH(8.52~8.73),且添加组分F2的土壤对Cd的吸附能力最弱,该结果也表明pH的升高加强了土壤对Cd的吸附能力。当pH较低时,溶液中H+会与Cd2+产生竞争吸附,吸附-解吸在溶液中是一个动态平衡的过程,这可能也是添加组分F2的土壤解吸率最高的原因。因此,不同分子量大小的NOM对土壤Cd的吸附-解吸能力的影响,可能主要是通过改变土壤pH值实现的。
|
|
表 4 添加不同浓度不同分子量NOM的土壤pH值 Table 4 pH of different concentrations and molecular weight NOM |
此外,NOM组分对土壤Cd吸持性能的影响可能还与其结构复杂性及功能基团数量等性质有关。Garcia-Mina[43]研究发现胡敏酸对重金属的络合能力可能存在两种形式的络合过程,一种在中偏酸条件下,羧化物起了主要作用,另一种是在碱性条件下,羧化物、酚类官能团都会发挥作用。由表 4可见,经不同分子量NOM处理后土壤呈中偏碱性,在此条件下,酚羟基可能对Cd的吸持发挥主要作用,而由表 2可知,NOM各分子组分羧基变化不大,而酚羟基随着分子量的增加而降低。因此,NOM分子量 < 5000时,土壤对Cd的吸附能力最强可能还与组分F1中酚羟基含量最高,对Cd络合作用强有关。同时,本试验中按照等量碳添加的NOM各组分,F1的碳含量(23.55%)最低,因此土壤中F1组分的绝对添加量最多,含氧功能基团的绝对数量相应更多,从而表现出对Cd更强的吸附性能,Ni等[44]也发现沉积物中Cd对芳香化程度高的低分子量HA亲和能力强于高分子量HA。当NOM组分分子量进一步增加至>10 000时,土壤对Cd的吸持能力又随分子量增加而增大,Al-Reasi等[45]等和Kozyatnyk等[46]的研究也获得了类似的结果。本试验中当NOM组分分子量>10 000时,随着组分分子量的进一步增加,芳香化程度和缩合程度降低、脂族性增加,而对Cd的吸附量却增加,这一结果与李丽等[47]实验结果类似,但与以往的一般认知有所不同。有研究表明芳香族碳基团不能作为重金属离子的吸附位点,在含有大量芳香族环的碳纳米管上重金属离子的吸附可以忽略不计[48]。Salloum等[49]使用高分辨魔角旋转(HRMAS)1H HMR对土壤样品的研究结果也表明,土壤中NOM的芳香结构并不是存在于土壤-水的表面,而是被包埋在土壤胶体中,只有破坏了氢键作用,才使样品中的芳香结构暴露出来。因此,单纯从NOM结构芳香性并不能解释其对Cd吸附的能力,NOM的结构效应还与其对土壤有机-无机复合胶体性质的影响有关。试验过程中亦发现,NOM组分随其分子量的增加,相对色度逐步加深,其中F1组分呈米白色,F2呈棕黄色,F3呈棕黑色,F4呈黑褐色,这些高分子组分可能更利于与土壤无机胶体相互作用而影响其吸附性能[50-51]。可见NOM影响土壤重金属吸附的效应与机理十分复杂,NOM随其来源的不同,其分子组成必然有很大差异,其对土壤重金属环境行为的影响是各种组分共同作用所产生的表观现象,生产实践中施用有机物料修复土壤重金属污染常获得不一致的效果,正是源于其影响的复杂性,因此,NOM组成性质与结构效应的关系值得深入探讨。
3 结论(1)NOM不同分子量组分元素组成和性质有明显差异。C、H含量随着NOM分子量的增大而增大,而O元素则相反。表征腐植酸结构和性质的指标O/C、(N+O)/C随着分子量的增加而降低,反映出NOM高分子量组分氧化程度更低,极性更弱。分子量>5000时,高分子量组分缩合程度和芳香化程度更低。总酸性基团、酚羟基均随着分子量的增大而减小,与O/C比值顺序一致,而羧基含量随分子量的增加变化较小。
(2)NOM各组分均增加了土壤对Cd的表观吸附能力和吸持强度,但不同组分、不同添加量的影响程度存在差异。随NOM用量的增加,对土壤Cd吸附能力的促进作用增加;添加不同分子组分NOM土壤对Cd吸附量顺序表现为F1>F4>F3>F0>F2>CK。吸持强度顺序与其一致。等添加量下(以0.5%C),与组分F0相比,组分F1促进作用最大,而组分F2抑制了土壤对Cd的吸附。
(3)NOM组分对土壤Cd吸附-解吸的影响随其分子量大小的变化不存在线性依存关系。分子量 < 5000的NOM组分(F1)土壤对Cd吸附和吸持强度最高,而分子量>10 000时NOM对土壤Cd的吸附量和吸持强度随着分子量的增加而增大,低分子量组分可能主要通过影响土壤pH而改变其吸附性能,而高分子量组分还与其自身的吸附能力及分子结构有关。
| [1] |
王艳娜. 土壤重金属污染现状与防治方法[J]. 价值工程, 2014, 35(179): 311-312. WANG Yan-na. Pollution status and prevention methods of the soil heavy metal[J]. Value Engineering, 2014, 35(179): 311-312. |
| [2] |
环境保护部, 国土资源部. 全国污染土壤状况调查公报[J]. 中国环保产业, 2014(5): 10-11. Ministry of Environmental Protection, Ministry of Land and Resources. The report on the national general survey of soil contamination[J]. China Environmental Protection Industry, 2014(5): 10-11. |
| [3] |
杨冰雪, 方晨, 王宏, 等. 临安市底泥重金属污染特征及潜在生态危害评价[J]. 安徽农业科学, 2017, 45(29): 45-49. YANG Bing -xue, FANG Chen, WANG Hong, et al. Investigation of heavy metal pollution characteristics and potential ecological risk assessment in Lin' an City[J]. Journal of Anhui Agricultural Sciences, 2017, 45(29): 45-49. DOI:10.3969/j.issn.0517-6611.2017.29.016 |
| [4] |
Wang L, Cui X F, Cheng H G, et al. A review of soil cadmium contamination in China including a health risk assessment[J]. Environmental Science and Pollution Research, 2015, 22(21): 16441-16452. DOI:10.1007/s11356-015-5273-1 |
| [5] |
Chen C H, Teng Y G, Lu S J, et al. Contamination features and health risk of soil heavy metal in China[J]. Science of the Total Environment, 2015, 512/513: 143-153. DOI:10.1016/j.scitotenv.2015.01.025 |
| [6] |
李裕, 王刚. 有机农业与可持续发展[J]. 应用生态学报, 2004, 15(12): 2377-2382. LI Yu, WANG Gang. Organic agriculture and sustainable development[J]. Chinese Journal of Applied Ecology, 2004, 15(12): 2377-2382. DOI:10.3321/j.issn:1001-9332.2004.12.035 |
| [7] |
宋玉婷, 雷泞菲. 我国土壤镉污染的现状及修复措施[J]. 西昌学院学报(自然科学版), 2018, 32(3): 79-83. SONG Yu-ting, LEI Ning-fei. China's cadmium pollution land status and restoration measures[J]. Journal of Xichang University(Natural Science Edition), 2018, 32(3): 79-83. |
| [8] |
Xiong J, Koopal L K, Weng L, et al. Effect of soil fulvic and humic acid on binding of Pb to goethite-water interface:Linear additivity and volume fractions of HS in the stern layer[J]. Journal of Colloid and Interface Science, 2015, 457(1): 121-130. |
| [9] |
Xu J, Tan W, Xiong J, et al. Copper binding to soil fulvic and humic acids:NICA-Donnan modeling and conditional affinity spectra[J]. Journal of Colloid and Interface Science, 2016, 473(1): 141-151. |
| [10] |
Xu J, Koopal L, Fang L, et al. Proton and copper binding to humic acids analyzed by XAFS spectroscopy and isothermal titration calorimetry[J]. Environmental Science & Technology, 2018, 52(7): 4099-4107. |
| [11] |
王青清.腐植酸活性组分含量和比例对紫色潮土中铅的形态转化及生物有效性的影响[D].重庆: 西南大学, 2017. WANG Qing-qing. Effects of the content and proportion of humic acid active components on the speciation and bioavailability of Pb in purple alluvial soil[D]. Chongqing: Southwest University, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10635-1017846820.htm |
| [12] |
王俊.腐植酸对砷在土壤中形态转化和生物有效性的影响研究[D].重庆: 西南大学, 2017. WANG Jun. Effects of humic acid on the speciation and bioavailability of arsenic in soils[D]. Chongqing: Southwest University, 2017. |
| [13] |
李光林, 魏世强, 青长乐, 等. 镉在腐植酸上的吸附与解吸特征研究[J]. 农业环境科学学报, 2003, 22(1): 34-37. LI Guang-lin, WEI Shi-qiang, QING Chang-le, et al. Characteristics of adsorption and desorption of cadmium on humic acids[J]. Journal of Agro-Environment Science, 2003, 22(1): 34-37. DOI:10.3321/j.issn:1672-2043.2003.01.010 |
| [14] |
Yang K, Miao G F, Wu W H, et al. Sorption of Cu2+ on humic acids sequentially extracted from a sediment[J]. Chemosphere, 2015, 138: 657-663. DOI:10.1016/j.chemosphere.2015.07.061 |
| [15] |
Lee H H, Weng Y, Li K. Electro-ultrafiltration study on Aldrich humic substances with different molecular weights[J]. Separation and Purification Technology, 2008, 63(1): 23-29. DOI:10.1016/j.seppur.2008.03.030 |
| [16] |
Marsac R, Banik N L, Lützenkirchen J, et al. Modeling metal ionhumic substances complexation in highly saline conditions[J]. Applied Geochemisty, 2017, 79: 52-64. DOI:10.1016/j.apgeochem.2017.02.004 |
| [17] |
Wu J, Zhang H, He P, et al. Insight into the heavy metal binding potential of dissolved organic matter in MSW leachate using EEM quenching combined with PARAFAC analysis[J]. Water Research, 2011, 45(4): 1711-1719. |
| [18] |
He E, Lü C, He J, et al. Binding characteristics of Cu2+ to natural humic acid fractions sequentially extracted from the lake sediments[J]. Environment Science and Pollution Research, 2016, 23(22): 22667-22677. DOI:10.1007/s11356-016-7487-2 |
| [19] |
Jiang T, Wei S, Flanagan D C, et al. Effect of abiotic factors on the mercury reduction process by humic acids in aqueous systems[J]. Pedosphere, 2014, 24(1): 125-136. DOI:10.1016/S1002-0160(13)60087-9 |
| [20] |
杨剑虹, 王成林, 代亨林. 土壤农化分析与环境监测[M]. 北京: 中国大地出版社, 2008: 257-279. YANG Jian-hong, WANG Cheng-lin, DAI Heng-lin. Soil agrochemical analysis and environmental monitoring[M]. Beijing: China Land Press, 2008: 257-279. |
| [21] |
邬洪源, 黄海涛, 赵烨萍. 腐植酸中官能团的测定方法的研究[J]. 高师理科学刊, 2000, 20(1): 31-33. WU Hong-yuan, HUANG Hai-tao, ZHAO Ye-ping. Study on the determination of the functional group in humic acid[J]. Journal of Science of Teachers' College and University, 2000, 20(1): 31-33. |
| [22] |
Rice J A, Maccarthy P. Statisitical evaluation of the elemental composition of humic substances[J]. Organic Geochemistry, 1991, 17(5): 634-638. |
| [23] |
Hargital L. Biochemical of elemental characteristics of humic substances during humification related to their environmental functions[J]. Environmental International, 1994(20): 43-48. |
| [24] |
Kin J I, Buckau G, Li G H. Characterization of humic and fulvic acids from Gorleben groundwater[J]. Fresenius Journal of Analytical Chemistry, 1990, 338(3): 245-252. DOI:10.1007/BF00323017 |
| [25] |
赵楠, 吴贻忠. 不同施肥处理对潮土胡敏酸结构特性的影响[J]. 光谱学与光谱分析, 2012, 32(7): 1856-1859. ZHAO Nan, WU Yi-zhong. Effects of different fertilization treatments on soil humic acid structure characteristics[J]. Spectroscopy and Spectral Analysis, 2012, 32(7): 1856-1859. DOI:10.3964/j.issn.1000-0593(2012)07-1856-04 |
| [26] |
Gonzalez-Vila F J, Martin F, Del Rio J C, et al. Structure characteristics and geochemical significance of humic acids isolated from three Spanish lignite deposits[J]. Science of the Total Environment, 1992, 117/118(17): 355-343. |
| [27] |
Chen S Y, Huang S W, Chiang P N, et al. Influence of chemical compositions and molecular weights of humic acids on Cr(Ⅵ)photo-reduction[J]. Journal of Hazardous Materials, 2011, 197(15): 337-344. |
| [28] |
Yan M Q, Li M Y, Wang D S, et al. Optical property of iron binding to Suwannee River fulvic acid[J]. Chemosphere, 2013, 91(7): 1042-1048. DOI:10.1016/j.chemosphere.2013.01.069 |
| [29] |
Yan M Q, Wang D S, G V Korshin, et al. Quantifying metal ions binding onto dissolved organic matter using log-transformed absorbance spectra[J]. Water Research, 2013, 47(7): 2603-2611. DOI:10.1016/j.watres.2013.02.044 |
| [30] |
Xu H C, Yu G H, Yang L Y, et al. Combination of two-dimensional correlation spectroscopy and parallel factor analysis to characterize the binding of heavy metals with DOM in lake sediments[J]. Journal of Hazardous Materials, 2013, 263(2): 412-421. |
| [31] |
李灵, 唐辉, 张玉, 等. 南方酸性红壤区不同土地利用的土壤对镉(Cd)的吸附与解吸[J]. 三峡大学学报(自然科学版), 2017, 39(6): 104-108. LI Ling, TANG Hui, ZHANG Yu, et al. Characteristics of Cd adsorption-desorption of different land uses soils in acid red soils zone of south China[J]. Journal of China Three Gorges University(Natural Sciences), 2017, 39(6): 104-108. |
| [32] |
魏世强, 木志坚, 青长乐. 几种有机物对紫色土镉的溶出效应与吸附解吸行为影响的研究[J]. 土壤学报, 2003, 40(1): 110-117. WEI Shi-qiang, MU Zhi-jian, QING Chang-le. Effects of several organic substances on the solubility and adsorption-desorption behaviors of cadmium purplish soil[J]. Acta Pedologica Sinica, 2003, 40(1): 110-117. DOI:10.3321/j.issn:0564-3929.2003.01.015 |
| [33] |
何雨帆, 刘宝庆, 吴明文, 等. 腐植酸对小白菜吸收Cd的影响[J]. 农业环境科学学报, 2006, 25(增刊): 84-86. HE Yu-fan, LIU Bao-qing, WU Ming-wen, et al. Effect of humus on uptake of cadmium in pakchoi[J]. Journal of Agro-Environment Science, 2006, 25(Supplement): 84-86. |
| [34] |
陕红, 李书田, 刘荣乐. 秸秆和猪粪的施用对土壤镉有效性的影响和机理研究[J]. 核农学报, 2009, 23(1): 139-144. SHAN Hong, LI Shu-tian, LIU Rong-le. Availability and the related mechanisms of cadmium in soils as influenced by the application of straw or pig manure[J]. Journal of Nuclear Agricultural Sciences, 2009, 23(1): 139-144. |
| [35] |
An J, Jho E H, Nam K. Effect of dissolved humic acid on the Pb bioavailability in soil solution and its consequence on ecological risk[J]. Journal of Hazardous Materials, 2015, 286(9): 236-241. |
| [36] |
Senesi N, Dorazio V D, Miano T M. Adsorption mechanisms of s-triazine and bipyridylium herbicides on humic acids from hop field soils[J]. Geoderma, 1995, 66(3/4): 273-283. |
| [37] |
Matilainen A, Vepsalainen M, Sillanpaa M. Natural organic matter removal by coagulation during drinking water treatment:A review[J]. Advances in Colloid and Interface Science, 2010, 159(2): 189-197. DOI:10.1016/j.cis.2010.06.007 |
| [38] |
费宇红, 曹树堂, 张光辉, 等. 镉在土壤中吸附与沉淀的特征与界限[J]. 地球学报, 1998, 19(4): 409-414. FEI Yu-hong, CAO Shu-tang, ZHANG Guang-hui, et al. Characteristics and boundary line between adsorption and precipition cadmium in soil[J]. Acta Geoscientia Sinica, 1998, 19(4): 409-414. |
| [39] |
张光辉. 镉在包气带中的迁移与积累特征[J]. 西安地质学院学报, 1995, 17(2): 64-72. ZHANG Guang-hui. Migration and accumulation features of cadmium in the aeration zone[J]. Journal of Xi'an College of Geology, 1995, 17(2): 64-72. |
| [40] |
夏汗平. 土壤-植物系统中的镉研究进展[J]. 应用与环境生物学报, 1997, 3(3): 289-298. XIA Han-ping. Studies on cadmium in soil-plant system[J]. Chinese Journal of Application Environment Biology, 1997, 3(3): 289-298. DOI:10.3321/j.issn:1006-687X.1997.03.018 |
| [41] |
杨毅, 兰亚琼, 金鹏康, 等. 腐植酸与Cd2+的结合特性及其影响因素[J]. 环境化学, 2017, 36(6): 1198-1203. YANG Yi, LAN Ya-qiong, JIN Peng-kang, et al. Characteristic and influential factors of humic acid complexed with Cd2+[J]. Environment Chemistry, 2017, 36(6): 1198-1203. |
| [42] |
单瑞娟, 黄占斌, 柯超, 等. 腐植酸对土壤重金属镉的淋溶效果及吸附解吸机制研究[J]. 腐植酸, 2015(1): 12-17. SHAN Rui-juan, HUANG Zhan-bin, KE Chao, et al. Study on humic acid for leaching effect of cadmium in soil and its adsorption-desorption mechanism[J]. Humic Acid, 2015(1): 12-17. DOI:10.3969/j.issn.1671-9212.2015.01.005 |
| [43] |
Garcia-Mina J M. Stabilitysolubility and maximum metal binding capacity in metal humic complexes involving humic substances extracted from peat and organic compost[J]. Organic Geochemistry, 2006, 37(12): 1960-1972. DOI:10.1016/j.orggeochem.2006.07.027 |
| [44] |
Ni L, Su L, Wang P, et al. The characterization of dissolved organic matter extracted from different sources and their influence on cadmium uptake by microcystis aeruginosa[J]. Environmental Toxicology and Chemistry, 2017, 36(7): 1856-1863. DOI:10.1002/etc.3728 |
| [45] |
Al-Reasi H A, Smith D S. Evaluating the ameliorative effect of natural dissolved organic matter(DOM) quality on copper toxicity to Daphnia magna:Improving the BLM[J]. Ecotoxicology, 2012, 21(2): 524-537. DOI:10.1007/s10646-011-0813-z |
| [46] |
Kozyatnyk I, Bounchet S, Björn E, et al. Fractionation and size-distribution of metal and metalloid contaminants in a polluted groundwater rich in dissolved organic matter[J]. Journal of Hazardous Materials, 2016, 318(15): 194-202. |
| [47] |
李丽, 于志强, 盛国英, 等. 分子结构在腐植酸对菲吸附行为中的影响[J]. 环境化学, 2004, 23(4): 381-386. LI Li, YU Zhi-qiang, SHENG Guo-ying, et al. Effect of humic acid molecular structure on the sorption of phenanthrene[J]. Environment Chemistry, 2004, 23(4): 381-386. DOI:10.3321/j.issn:0254-6108.2004.04.005 |
| [48] |
Yang K, Wei W, Qi L, et al. Are engineered nanomaterials superior adsorbents for removal and pre-concentration of heavy metal cations from water?[J]. RSC Advances, 2014, 4: 46122-46125. DOI:10.1039/C4RA09375E |
| [49] |
Salloum M J, Dudas M J, McGill W B. Variation of 1-naphthol sorption with organic matter fractionation:The role of physical conformation[J]. Organic Geochemistry, 2001, 32(5): 709-719. DOI:10.1016/S0146-6380(01)00007-9 |
| [50] |
Huang G F, Wu Q T, Wong J W C, et al. Transformation of organic matter during co-composting of pig manure with sawdust[J]. Bioresource Technology, 2006, 97(15): 1834-1842. DOI:10.1016/j.biortech.2005.08.024 |
| [51] |
Pedra F, Plaza C, Garcia-Gil J C, et al. Effects of municipal waste compost and sewage sludge on proton binding behavior of humic acids from Portuguese sandy and clay loam soils[J]. Bioresource Technology, 2008, 99(7): 2141-2147. DOI:10.1016/j.biortech.2007.05.043 |
 2019, Vol. 38
2019, Vol. 38