2. 北京大学城市与环境学院, 地表过程分析与模拟教育部重点实验室, 北京 100871
2. Laboratory for Earth Surface Processes, College of Urban and Environmental Sciences, Peking University, Beijing 100871, China
生物炭是生物质在绝氧条件下经热解作用制取的富含碳的残余物[1],其性质稳定,可以改良土壤,增强土壤肥力;增加碳汇,缓解温室气体排放[2];同时作为低成本的高效吸附剂,在水土污染控制方面具有重要的应用价值[3-4]。研究表明,土壤矿物与土壤有机质的相互作用会屏蔽有机质中的吸附位点,显著降低其对有机污染物(如多环芳烃)的吸附[5-6]。因而生物炭中的矿物组分可能极大地影响其组成结构以及对有机污染物的吸附性能[7-8],从而影响污染物在土壤中的迁移和归趋。Sun等[9]和Ji等[10]发现相比于原始生物炭,典型多环芳烃菲和抗生素(四环素和磺胺甲恶唑)在去灰分生物炭上的吸附明显增强。而Li等[11]的研究结果却相反,其指出去灰分处理后,生物炭对双酚A的吸附减弱。何琦等[12]的研究同样发现,去灰分降低了生物炭对有机氯农药硫丹的吸附。最近的一项研究表明,去灰分对新烟碱类农药在低温生物炭(300 ℃)上的吸附无明显影响,但显著提高其在高温生物炭(500 ℃和700 ℃)上的吸附[13]。以上不一致的研究结果表明,去灰分对生物炭理化属性的改变将如何影响不同性质有机污染物的吸附行为及内在影响机制尚未完全明晰,亟待进一步深入探讨。鉴于生物炭的非均质性,相较于整体性质,生物炭的表面化学组成(如芳香碳和脂肪碳)和表面极性对有机污染物吸附的影响更显著[14],而目前关于去灰分对生物炭表面性质的改变影响有机污染物吸附过程和吸附能力的内在机理的研究相对有限[9]。另外,目前大多数研究仅关注去灰分对有机污染物在生物炭上热力学吸附平衡(包括吸附量和吸附强度)的影响,对其动力学吸附特征影响的研究鲜有报道。
本研究以不同炭化温度(300、400、500 ℃)下制得的小麦秸秆生物炭为对象,系统研究酸洗去灰分对生物炭表面积、孔隙度、极性官能团、整体和表面化学组成等理化属性的改变,以及对极性和非极性有机污染物(1-萘酚和萘)吸附动力学的影响和作用机制,分析矿物组分对有机污染物在生物炭上吸附过程的内在影响机制,为预测有机污染物的环境行为和评估生物炭在有机污染控制方面的应用提供科学依据。
1 材料与方法 1.1 生物炭的制备及去灰分处理以小麦秸秆为原材料制备生物炭。风干后的小麦秸秆切成10 cm小段置于炭化炉中,采用程序升温,以8.5 ℃·min-1分别升至300、400、500 ℃后,在绝氧条件下裂解炭化5 h,待冷却至室温,取出残余物。用0.1 mol·L-1HCl和超纯水洗至中性后于105 ℃干燥,研磨过0.25 mm(60目)筛,得到原始生物炭,标记为W300、W400和W500。
以1:5的固液比向原始生物炭样品中加入HCl/ HF(1.0 mol·L-1/3.0 mol·L-1)混合溶液,在40 ℃下,以140 r·min-1的转速水平振荡12 h,充分混合后以4 500 r·min-1的速度离心30 min,去除上清液。重复以上步骤5次,然后用超纯水清洗去除残留的HCl和HF,最后冷干、研磨、过0.25 mm(60目)筛,获得去灰分生物炭样品,标记为DW300、DW400和DW500。
1.2 生物炭理化性质表征原始和去灰分生物炭的C、H、N、S元素含量由美国PerkinElmer 2400 Ⅱ型元素分析仪测定,每个样品平行测定两次,取算术平均值表示整体元素含量。生物炭样品在900 ℃高温下灼烧4 h后测得灰分含量,氧含量根据质量平衡差减法计算得到。原始和去灰分生物炭的表面元素组成(C、N、O、Si)和含碳官能团分布由英国Kratos公司AXIS-UltraDLD型多功能成像X射线光电子能谱仪(XPS)测得。XPS测定使用带单色器的铝靶X射线源(hv=1 486.7 eV),功率约225 W(工作电压15 kV,发射电流15 mA)。C 1s峰中各含碳官能团结合能归属如下:284.8 eV为C—C,286.5 eV为C—OH,287.9 eV为C=O,289.1 eV为—COOH。固态交叉极化魔角自旋13C-核磁共振(NMR)谱图通过德国Bruker公司Advance Ⅲ型400 MHz核磁共振波谱仪测定得到,以分析生物炭样品的化学结构信息。
生物炭样品的表面积和孔隙度由美国Quantachrome公司Autosorb-1-MP型比表面积及孔隙度分析仪利用气体吸附法测得。将干燥的样品在105 ℃下脱气16 h,然后在77 K下测得N2的吸附-解吸曲线。其中样品的表面积通过相对压力P/P0在0.05~ 0.3范围内的吸附数据由多点Brunaer-Emmett-Teller (BET)方法计算得到;而样品的微孔(< 2 nm)体积通过P/P0≤0.05范围内的吸附数据由DubininRadushkevich(DR)方法计算得到,介孔(2~50 nm)和大孔(>50 nm)体积通过解吸数据由Barrett-JoynerHalenda(BJH)方法计算。
为了明确吸附剂对目标污染物的吸附机理,采用美国PerkinElmer公司Frontier型傅里叶变换红外(FTIR)光谱仪测定原始和去灰分生物炭以及吸附化合物后生物炭样品的FTIR谱图(以500 ℃生物炭为例)。化合物-生物炭复合物样品由吸附动力学实验达到平衡时的样品以4 500 r·min-1离心30 min,去除上清液,固体沉淀物用超纯水清洗以去除残余的化合物,然后冷干。
1.3 吸附动力学实验选取结构相同、极性不同的萘和1-萘酚为目标有机污染物,测定pH=7时的吸附动力学。准确称取一定量的萘和1-萘酚(纯度>99%,美国J&K科技有限公司),分别溶解于甲醇(色谱纯,百灵威科技有限公司)和超纯水中,然后用背景溶液稀释成初始浓度(C0)为目标化合物水溶解度50%的吸附初始溶液,控制pH为7。为避免共溶剂效应,溶液中甲醇的含量控制在0.1%(V/V)以下。背景溶液中含有0.01 mol· L-1的CaCl2以保持稳定的离子强度和200 mg·L-1的NaN3抑制微生物活动以排除微生物降解的干扰。按照预实验确定的固液比,向预先称好一定质量吸附剂样品的聚四氟乙烯螺纹盖玻璃小瓶中加入吸附初始溶液(C0=0.5Sw,Sw为吸附质的水溶解度),顶空体积保持最小以减少吸附质的蒸汽挥发。室温条件下,将所有样品瓶置于水平振荡器上以120 r·min-1避光振荡。在设置的每个时间点,取下样品瓶,以4 500 r·min-1的速度离心30 min,取2 mL上清液,使用0.45 μm聚四氟乙烯水相针式过滤器过滤,用配备紫外检测器的高效液相色谱仪(HPLC)测定上清液中吸附质的剩余浓度(C)。色谱柱为安捷伦ZORBAX Eclipse Plus C18分析柱(5 μm,4.6 mm × 250 mm),柱温为(26± 1)℃,流动相为乙腈:超纯水=80:20(V/V),流速为1 mL·min-1,进样量为10 μL,检测波长为275 nm。由未添加生物炭的空白对照组实验结果可知,吸附过程中萘和1-萘酚的质量损失可忽略不计(< 3%),原始和去灰分生物炭上目标化合物的吸附量通过液相中该化合物的C0与Ct之差计算得到。每个时间点的样品以及空白对照均设1个平行样品。
1.4 数据处理采用拟一级动力学模型、拟二级动力学模型和双室一级动力学模型对萘和1-萘酚在原始和去灰分生物炭上的吸附动力学曲线进行拟合。分别如下:
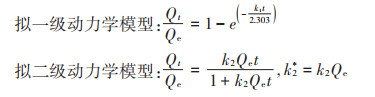
|
双室一级动力学模型:
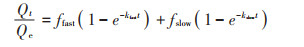
|
式中:Qe、Qt分别为吸附质在固相吸附剂上的平衡吸附量和t(h)时刻的吸附量,mg·kg-1;k1为拟一级吸附速率常数,h-1;k2为拟二级吸附速率常数,kg·mg-1·h-1;k2*为修正后的拟二级吸附速率常数,h-1;ffast、fslow分别为快、慢吸附单元的吸附速率常数,h-1;ffast、fslow分别为吸附平衡时,快、慢吸附占总吸附的比例,ffast+fslow=1。
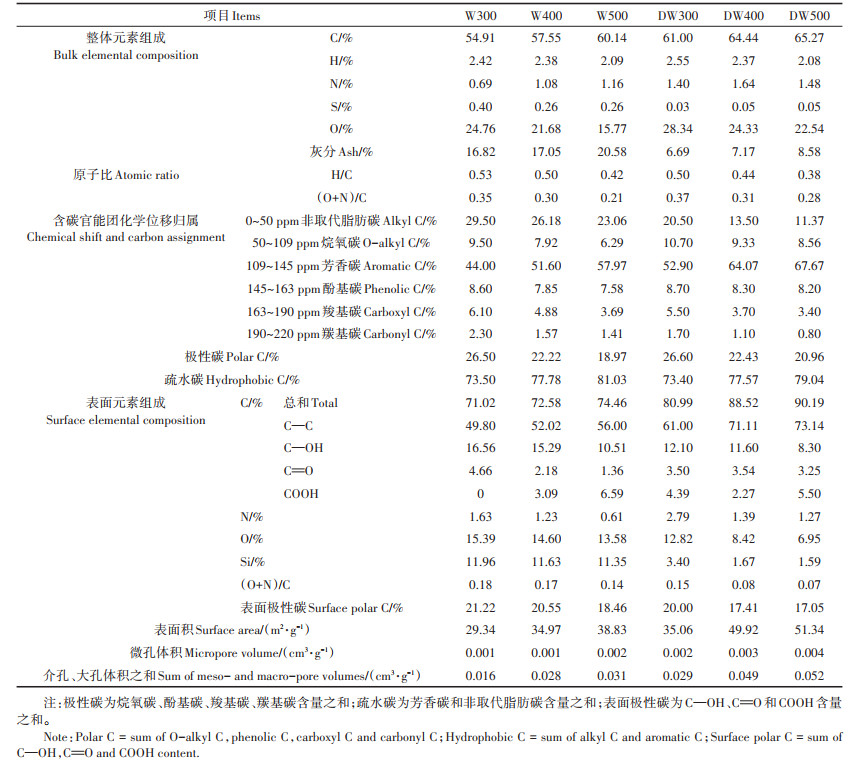
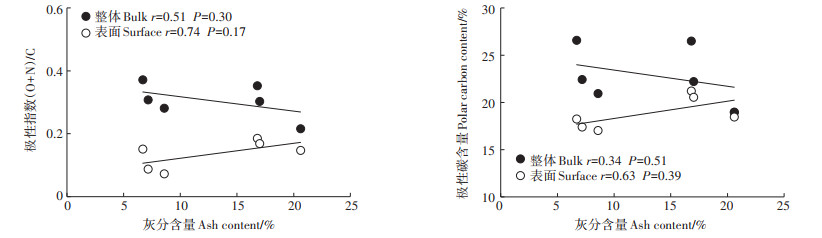
2 结果与讨论 2.1 去灰分对生物炭理化属性的改变生物炭的灰分含量随着炭化温度的升高而增加(表 1),这与多数文献报道结果一致[15-16]。酸洗处理后生物炭的灰分显著减少58.3%~60.7%,表明HCl/ HF混合酸洗去除无机矿物效果明显[9, 13]。表 1中XPS分析结果显示,表面矿物元素Si含量显著降低,说明HF的作用可以有效去除硅氧化物和硅酸盐。去灰分处理后,生物炭的整体C和表面C含量均增加,整体O含量增加而表面O含量减少;相应地,除灰后生物炭的整体极性指数(O+N)/C略有上升,但表面极性指数下降(表 1),该极性变化与Sun等[9]的研究结果一致,而与Yang等[5]考察去灰分对腐植酸理化性质影响的研究结果完全相反。与元素组成和极性指数的变化趋势相同,固相13C-NMR数据显示,生物炭的总极性碳含量在去灰分处理后略有升高,主要是源于烷氧碳组分的增多;而XPS数据显示,除灰后生物炭的表面极性碳含量降低,同样表现在烷氧碳含量的减少。并且由Pearson相关系数r和P可知,所有生物炭的灰分含量与其表面极性[包括(O+N)/C和极性碳含量]的相关性明显优于与整体极性的相关性(图 1)。
|
|
表 1 原始和去灰分生物炭的理化性质 Table 1 Physicochemical properties of the original and deashed biochars |
|
图 1 生物炭的灰分含量与整体和表面极性([O+N)/C指数和极性碳含量]的相关性 Figure 1 Relationships between the ash content of all biochars and their bulk or surface polarity including(O+N)/C index and polar carbon content |
研究表明生物炭的矿物组分影响生物炭中极性官能团的空间分布,有助于极性官能团在生物炭表面的向外暴露;而去灰分处理使得生物炭的表面极性减弱,尤其是烷氧基极性官能团向内分布,使原来被屏蔽的疏水有机组分外露。去灰分后,生物炭的芳香碳含量升高,H/C原子比值降低,说明其芳香性增强。除灰后生物炭的表面积和孔体积包括微孔、介孔及大孔体积均增大,表明去灰分使得生物炭外表面和孔内原来被矿物覆盖的吸附位点暴露出来[16]。以上结果表明,去灰分对生物炭的整体和表面化学组成及表面性质有显著影响。
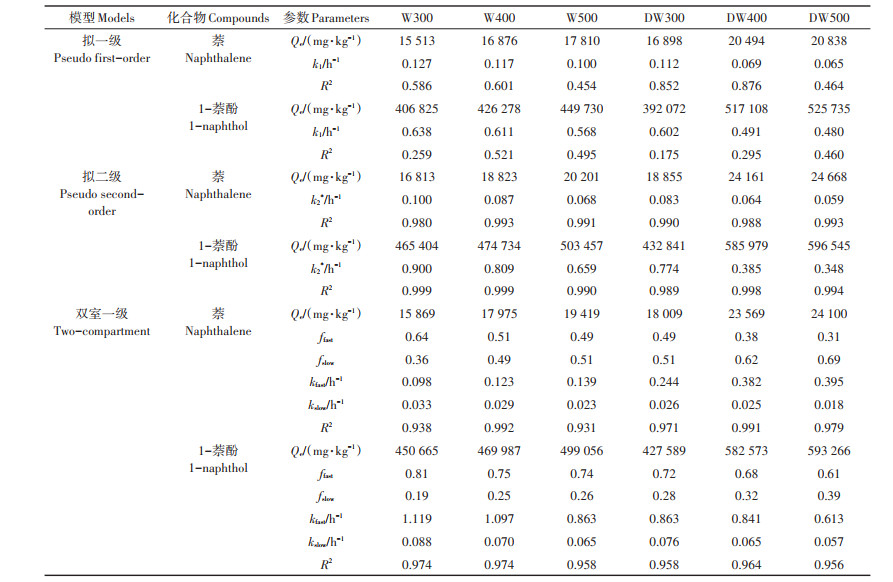
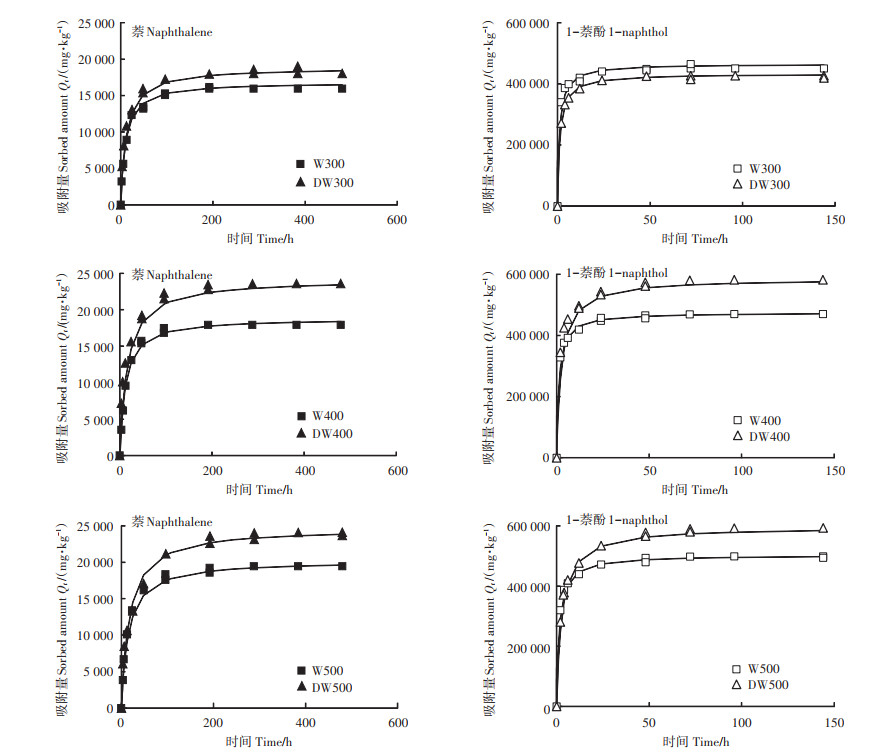
2.2 原始和去灰分生物炭上的吸附动力学萘和1-萘酚在原始和去灰分生物炭上的吸附量随时间的变化曲线如图 2所示,采用拟一级、拟二级和双室一级动力学模型对吸附动力学曲线进行拟合,拟合参数见表 2。结果表明,拟二级动力学模型能更好地描述目标有机污染物在所有生物炭样品上的动力学吸附过程(R2=0.980~0.999),与诸多研究生物炭对有机污染物如菲、萘和四环素的吸附动力学的结果一致[17-19]。其次是双室一级动力学模型(R2=0.938~ 0.992),Chen等[20]和陈建等[21]的研究也发现该模型可以精确描述萘和典型药品及个人护理用品(PPCPs)卡马西平在生物炭上的吸附动力学过程。因此,后续讨论将基于这两个模型的拟合结果。
|
图 2 萘和1-萘酚在原始和去灰分生物炭上的吸附动力学 Figure 2 Sorption kinetics of naphthalene and 1-naphthol on the original and deashed biochars |
|
|
表 2 萘和1-萘酚在原始和去灰分生物炭上吸附动力学的拟合参数 Table 2 Parameters for sorption kinetics of naphthalene and 1-naphthol on the original and deashed biochars fitted with three kinetic models |
由表 2可见,同一生物炭上1-萘酚的拟二级吸附速率常数大于萘,即其达到吸附平衡的时间比萘要短。有研究表明,吸附质分子从固液边界向吸附剂表面扩散为有机污染物(如萘)在生物炭上吸附的决速步[22]。1-萘酚比萘具有更大的水溶解度,固液界面上浓度更高,具有更大的吸附动力梯度,导致其吸附速率更快。去灰分使得目标污染物萘和1-萘酚在生物炭上的Qe增大(除DW300对1-萘酚),k2*降低。除灰后Qe和吸附平衡时间的增大与增大的表面积和孔体积一致,是产生更多有效吸附位点所致。诸多研究认为非取代脂肪碳可以通过疏水作用与芳香族化合物产生相互作用,这是影响其吸附的重要因素[23-24]。本研究中去灰分处理使得生物炭的非取代脂肪碳含量降低(表 1),然而其对芳香族化合物的Qe增大,表明生物炭样品中非取代脂肪碳吸附域不是控制其对萘和1-萘酚吸附的关键因素,或者是因为该组分被无机矿物(6.7%~20.6%)或烷氧基极性组分屏蔽,削弱了其对芳香族化合物的吸附作用。去灰分处理增大生物炭中芳香碳组分含量(表 1),增强其与芳香族化合物间的π-π和疏水作用[25],从而提高化合物的Qe,说明与非取代脂肪碳吸附域相比,生物炭样品中的芳香碳吸附域对萘和1-萘酚是更为有效的作用位点。
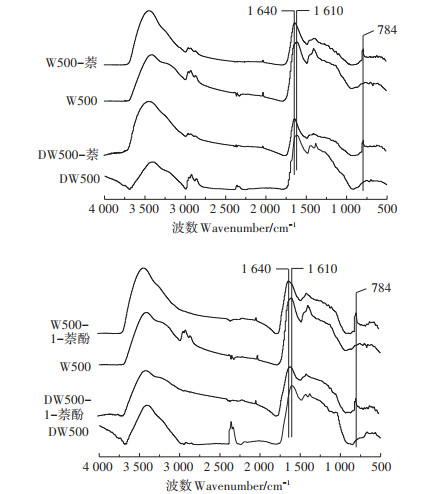
由图 3可见,吸附萘和1-萘酚分子后,原始和去灰分生物炭样品在784 cm-1处产生一个突出特征峰,该峰代表芳香环结构中C—H键的伸缩振动,说明两种化合物分子成功地被吸附到吸附剂上。并且,原始和去灰分生物炭样品在1 610 cm-1处有一明显的特征峰,该峰是由芳香环结构中C=C键的变形振动产生的,在吸附萘和1-萘酚分子后,该特征峰变得锐利并且向1 640 cm-1处发生偏移。以上发现证明了萘和1-萘酚分子与生物炭样品中的芳香组分之间的强相互作用。
|
图 3 原始和去灰分生物炭及其吸附化合物后样品的FTIR谱图 Figure 3 FTIR spectra of original biochar, deashed biochar and compound-sorbed sorbent sample |
矿物组分利于极性官能团外露,屏蔽生物炭上的疏水有机组分;而去灰分处理减少生物炭表面极性官能团的分布(表 1),使原来被掩盖的疏水碳吸附域(主要是芳香碳组分)暴露出来,促进其与芳香族化合物之间的疏水作用,进而提高生物炭对萘和1-萘酚的Qe(表 2)。DW300对1-萘酚的Qe小于W300,是因为1-萘酚结构中的极性官能团—OH能够与矿物含氧表面或者生物炭表面的极性官能团形成氢键作用,该作用对其在低温生物炭上的吸附有重要贡献,去灰分削弱氢键作用导致吸附量下降。诸多研究报道了矿物表面含氧组分容易通过氢键与极性有机污染物(如抗生素磺胺甲嘧啶和农药烟嘧磺隆)产生相互作用[16, 26-27]。因此,生物炭中的无机矿物组分一方面可以通过特定作用机制有效结合有机污染物,该作用对总吸附的贡献与污染物的性质、生物炭的制备温度和理化属性以及二者之间的主导作用机制有关;另一方面与有机碳复合,屏蔽有机组分中的疏水吸附位点,抑制吸附。酸洗去灰分对有机污染物在生物炭上吸附的影响取决于这两个方面的平衡。
2.3 去灰分对生物炭上快吸附和慢吸附的影响 2.3.1 对快、慢吸附贡献的影响萘和1-萘酚在所有生物炭样品上的吸附过程表现为明显的两阶段特征:初始24 h内,快吸附已达到平衡,占据主导地位,慢吸附对总吸附的贡献仅为19.7%~28.2%和16.7%~25.3%;随后直至吸附平衡,慢吸附贡献分别增加至36.0%~69.0%和18.7%~39.0%。
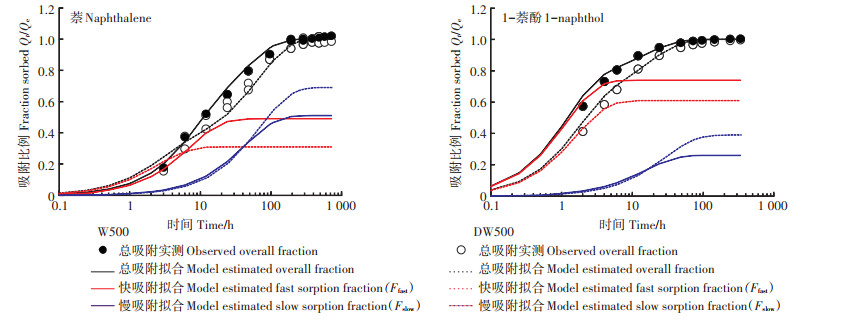
生物炭的芳香性随着炭化温度的升高而增强(表 1),萘和1-萘酚在生物炭上的慢吸附对总吸附的贡献(fslow)随之增大(表 2),说明高温增加的芳香碳组分主要贡献于慢吸附。相较于疏松、无定形的橡胶态软碳,芳香碳组分是紧实有序、高度芳香化的玻璃态硬碳,有机物相对难以扩散进入该致密结构,表现为慢吸附。有研究有机污染物在土壤、黑碳等地质吸附剂上吸附动力学的报道也提出,表面无定形碳上的吸附主要表现为快吸附,以分配作用为主;而内部致密的有机碳主要贡献于慢吸附[21, 28],说明快、慢吸附对总吸附的贡献与有机碳的炭化和致密程度有关。因此,去灰分处理提高生物炭的芳香碳含量(表 1),致密的芳香环结构增加,与原始生物炭相比fslow也明显增大(表 2和图 4)。同时,生物炭的脂肪碳含量在去灰分后减少,该组分的炭化度和致密度较芳香碳要低,相对利于快吸附的进行,快吸附贡献随之减小(表 1和表 2)。另外,有研究提出有机物分子扩散进入生物炭孔内的过程同样表现为慢吸附[29]。本实验中,去灰分后生物炭内部孔隙结构增多也是引起萘和1-萘酚在生物炭上慢吸附对总吸附的贡献fslow增大的一个因素。
|
图 4 由双室模型拟合的萘和1-萘酚在原始和去灰分生物炭上的快、慢吸附对总吸附的贡献(以500 ℃生物炭为例) Figure 4 The separated fast (Ffast)and slow(Fslow)sorption contributions to total sorption of naphthalene and 1-naphthol on W500 and DW500 derived from the two-compartment model |
萘和1-萘酚在所有生物炭样品上的吸附过程均包括初始的快吸附阶段,该阶段两种化合物的ffast分别为0.098~0.395 h-1和0.613~1.119 h-1;在后续的慢吸附阶段,萘的fslow为0.018~0.033 h-1,1-萘酚的fslow为0.057~0.088 h-1(表 2)。
有机污染物在生物炭上快吸附单元的吸附速率主要取决于其在生物炭表面水膜中的扩散以及吸附在外表面上的速度。去灰分对生物炭上两种目标污染物快吸附速率影响的不同,与生物炭表面含氧极性组分和化合物的极性有关。去灰分处理降低生物炭表面极性,减少表面含氧极性官能团的分布(表 1),减小空间位阻,提高生物炭表面疏水碳吸附域对化合物分子的可接近性。因此,去灰分后,非极性萘分子更易于向生物炭表面扩散,其ffast提高(图 4和表 2),而除灰后极性化合物1-萘酚的ffast降低。这是因为1-萘酚结构中的极性官能团—OH能够与生物炭表面极性官能团或矿物含氧表面形成氢键作用,这对快吸附有重要的贡献,而去灰分削弱了氢键作用。
去灰分后,萘和1-萘酚在生物炭上的慢吸附速率均下降(图 4和表 2)。这是由于去灰分增强生物炭的芳香性,提高内部有机碳的致密性,使得两种化合物分子相对较难扩散进入生物炭颗粒内部,另外,表面积和孔体积的增大延长了吸附平衡时间所致。
3 结论(1) 酸洗去灰分处理提高生物炭的芳香性、比表面积和孔隙度;除灰后生物炭的整体极性略有提高,而表面极性明显降低,表明矿物组分影响生物炭中极性官能团的空间分布,有助于极性官能团在生物炭表面的向外暴露。
(2) 与非取代脂肪碳相比,生物炭样品的芳香碳组分对萘和1-萘酚的吸附起着更重要的作用。去灰分增大化合物的平衡吸附量,主要是因为增加生物炭的芳香碳含量,促进其与萘和1-萘酚间的π-π和疏水作用;同时减少极性官能团(尤其是烷氧基官能团)在生物炭表面的分布,提高疏水碳吸附域的可达性。
(3) 致密的芳香碳和纳米级孔隙主要对萘和1-萘酚在生物炭上的慢吸附单元起作用,去灰分提高生物炭的芳香化程度和孔隙度,慢吸附对总吸附的贡献增大。
(4) 去灰分减少极性官能团在生物炭表面的暴露,促进萘分子向表面疏水吸附位点扩散,萘的快吸附速率常数升高;而1-萘酚结构中的—OH能够与表面极性官能团或矿物含氧表面形成氢键,对快吸附有重要贡献,去灰分削弱氢键作用,造成其快吸附速率常数下降。去灰分后两种化合物的慢吸附速率常数均降低。
| [1] |
Renner R. Rethinking biochar[J]. Environmental Science & Technology, 2007, 41(17): 5932-5933. |
| [2] |
Oliveira F R, Patel A K, Jaisi D P, et al. Environmental application of biochar:Current status and perspectives[J]. Bioresource Technology, 2017, 246: 110-122. |
| [3] |
Cao X D, Ma L N, Liang Y, et al. Simultaneous immobilization of lead and atrazine in contaminated soils using dairy manure biochar[J]. Environmental Science & Technology, 2011, 45(11): 4884-4889. |
| [4] |
Ahamd M, Rajapaksha A U, Lim J E, et al. Biochar as a sorbent for contaminant management in soil and water:A review[J]. Chemosphere, 2014, 99: 19-33. |
| [5] |
Yang Y, Shu L, Wang X L, et al. Impact of de-ashing humic acid and humin on organic matter structural properties and sorption mechanisms of phenanthrene[J]. Environmental Science & Technology, 2011, 45(9): 3996-4002. |
| [6] |
Guo X Y, Shen X F, Zhang M, et al. Sorption mechanisms of sulfamethazine to soil humin and its subfractions after sequential treatments[J]. Environmental Pollution, 2017, 221: 266-275. |
| [7] |
Li F Y, Cao X D, Zhao L, et al. Effects of mineral additives on biochar formation:Carbon retention, stability, and properties[J]. Environmental Science & Technology, 2014, 48(19): 11211-11217. |
| [8] |
王子莹, 邱梦怡, 杨妍, 等. 不同生物炭吸附乙草胺的特征及机理[J]. 农业环境科学学报, 2016, 35(1): 93-100. WANG Zi-ying, QIU Meng-yi, YANG Yan, et al. Sorption of acetochlor by biochars derived from wood dust and swine manure at different pyrolytic temperatures[J]. Journal of Agro-Environment Science, 2016, 35(1): 93-100. |
| [9] |
Sun K, Kang M J, Zhang Z Y, et al. Impact of deashing treatment on biochar structural properties and potential sorption mechanisms of phenanthrene[J]. Environmental Science & Technology, 2013, 47(20): 11473-11481. |
| [10] |
Ji L L, Wan Y Q, Zheng S R, et al. Adsorption of tetracycline and sulfamethoxazole on crop residue-derived ashes:Implication for the relative importance of black carbon to soil sorption[J]. Environmental Science & Technology, 2011, 45(13): 5580-5586. |
| [11] |
Li J, Liang N, Jin X Q, et al. The role of ash content on bisphenol A sorption to biochars derived from different agricultural wastes[J]. Chemosphere, 2017, 171: 66-73. |
| [12] |
何琦, 卢少勇, 陈方鑫, 等. 灰分对挺水植物生物炭吸附硫丹的影响[J]. 中国环境科学, 2018, 38(6): 2314-2320. HE Qi, LU Shao-yong, CHEN Fang-xin, et al. Influence of ash on adsorption of endosulfan by biochars derived from emergent plants[J]. China Environmental Science, 2018, 38(6): 2314-2320. |
| [13] |
Zhang P, Sun H W, Ren C, et al. Sorption mechanisms of neonicotinoids on biochars and the impact of deashing treatments on biochar structure and neonicotinoids sorption[J]. Environmental Pollution, 2018, 234: 812-820. |
| [14] |
Zhang M, Shu L, Shen X F, et al. Characterization of nitrogen-rich biomaterial-derived biochars and their sorption for aromatic compounds[J]. Environmental Pollution, 2014, 195: 84-90. |
| [15] |
张鹏, 武健羽, 李力, 等. 猪粪制备的生物炭对西维因的吸附与催化水解作用[J]. 农业环境科学学报, 2012, 31(2): 416-421. ZHANG Peng, WU Jian-yu, LI Li, et al. Sorption and catalytic hydrolysis of carbaryl on pig-manure-derived biochars[J]. Journal of AgroEnvironment Science, 2012, 31(2): 416-421. |
| [16] |
Zhang P, Sun H W, Li Y, et al. Adsorption and catalytic hydrolysis of carbaryl and atrazine on pig manure-derived biochars:Impact of structural properties of biochars[J]. Journal of Hazardous Materials, 2013, 244: 217-224. |
| [17] |
Hu E Z, Shang S Y, Wang N N, et al. Influence of the pyrolytic temperature and feedstock on the characteristics and naphthalene adsorption of crop straw-derived biochars[J]. Bioresources, 2019, 14(2): 2885-2902. |
| [18] |
Zhong Z W, Zhong J K, Yang Q Z, et al. Sorption of phenanthrene by biochar produced from potato straws[J]. Fresenius Environmental Bulletin, 2018, 27(3): 1814-1823. |
| [19] |
汪华, 方程冉, 王群, 等. 腐植酸对生物炭吸附四环素的影响[J]. 环境污染与防治, 2018, 40(4): 423-428. WANG Hua, FANG Cheng-ran, WANG Qun, et al. Effect of humic acid on the adsorption of tetracycline by biochar[J]. Environmental Pollution & Control, 2018, 40(4): 423-428. |
| [20] |
Chen Z M, Chen B L, Chiou C T. Fast and slow rates of naphthalene sorption to biochars produced at different temperatures[J]. Environmental Science & Technology, 2012, 46(20): 11104-11111. |
| [21] |
陈建, 王朋, 曹艳贝, 等. 生物炭的制备温度及酸处理对卡马西平的吸附动力学影响[J]. 环境化学, 2016, 35(7): 1461-1467. CHEN Jian, WANG Peng, CAO Yan-bei, et al. Impact of pyrolytic temperature and acid wash on adsorption kinetics of carbamazepine on biochar[J]. Environmental Chemistry, 2016, 35(7): 1461-1467. |
| [22] |
Zhang M, Shu L, Guo X Y, et al. Impact of humic acid coating on sorption of naphthalene by biochars[J]. Carbon, 2015, 94: 946-954. |
| [23] |
Sun K, Ro K, Guo M X, et al. Sorption of bisphenol A, 17 a-ethinyl estradiol and phenanthrene on thermally and hydrothermally produced biochars[J]. Bioresource Technology, 2011, 102(10): 5757-5763. |
| [24] |
Sun K, Jin J, Keiluweit M, et al. Polar and aliphatic domains regulate sorption of phthalic acid esters(PAEs) to biochars[J]. Bioresource Technology, 2012, 118: 120-127. |
| [25] |
Wang Z Y, Han L F, Sun K, et al. Sorption of four hydrophobic organic contaminants by biochars derived from maize straw, wood dust and swine manure at different pyrolytic temperatures[J]. Chemosphere, 2016, 144: 285-291. |
| [26] |
Teixido M, Pignatello J J, Beltran J L, et al. Speciation of the ionizable antibiotic sulfamethazine on black carbon(biochar)[J]. Environmental Science & Technology, 2011, 45(23): 10020-10027. |
| [27] |
Wang P P, Liu X G, Yu B C, et al. Characterization of peanut-shell biochar and the mechanisms underlying its sorption for atrazine and nicosulfuron in aqueous solution[J]. Science of the Total Environment, 2020, 702: 134767. |
| [28] |
Pignatello J J, Xing B S. Mechanisms of slow sorption of organic chemicals to natural particles[J]. Environmental Science & Technology, 1996, 30(1): 1-11. |
| [29] |
周尊隆, 卢媛, 孙红文. 菲在不同性质黑炭上的吸附动力学和等温线研究[J]. 农业环境科学学报, 2010, 29(3): 476-480. ZHOU Zun-long, LU Yuan, SUN Hong-wen. Sorption kinetics and isotherms of phenanthrene in charcoals with different properties[J]. Journal of Agro-Environment Science, 2010, 29(3): 476-480. |
 2020, Vol. 39
2020, Vol. 39