有机氯农药(OCPs)作为经济效益和实用价值并存的广谱杀虫剂,20世纪中后期曾被中国广泛应用于农业生产中。OCPs作为含有一个或几个苯环的氯衍生物,化学结构稳定,大部分单体具有共同的理化特征:半挥发性、高脂溶性和高毒性,在环境中迁移方式多样、影响范围广、降解时间长[1-2]。当OCPs通过大气沉降、地表径流等途径进入水环境后[3],大部分单体很快转移至沉积物的有机质和动物脂肪内,而水体-底泥系统受吸附解析作用影响时OCPs在各介质中相互转化,通过生物蓄积和放大作用后,影响周围居民和动植物安全[4]。
农田塌陷水域是在采煤活动影响下形成的一种特殊水体,此类水体底泥由原农田土壤垂直沉降形成,既保留塌陷前农田土壤的部分原有特性,又受采矿废水和上游水土流失带入的OCPs污染,同时还承担着和自然水体相同的养殖、灌溉等生产生活责任[5-6]。由于国内外学者多数集中在对河流、湖泊、海湾等普通水域的OCPs污染研究[7],而对此类因采煤沉陷形成的特殊水域研究极少。近年来随着地表塌陷情况加剧,部分潘集矿沉陷区受降雨及高潜水位影响成为积水区,当地居民还经常利用塌陷塘进行养殖、灌溉等生产活动,从而形成特殊的采煤沉陷区水生态环境。因此本文以潘集矿沉陷时间较长、面积较大的农田塌陷水体——杨庄塌陷区为研究对象,对水体-底泥中溶解态、悬浮态和沉积态OCPs的特征污染物六六六(HCHs)和滴滴涕(DDTs)的分布规律、来源及潜在生态风险进行探讨,从而为矿区农田塌陷水体污染防治及环境修复提供技术支撑。
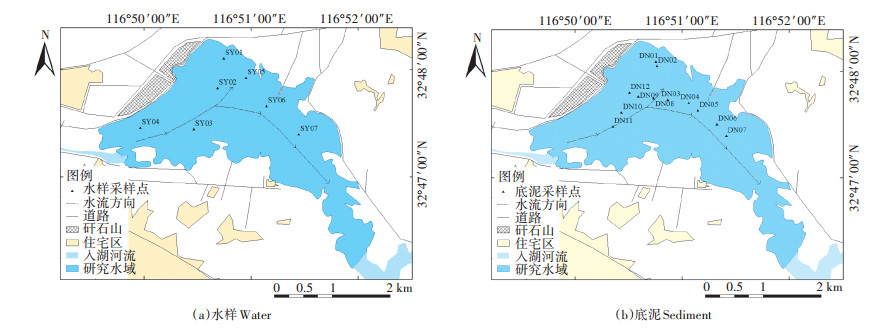
1 材料与方法 1.1 样品采集潘一矿杨庄采煤塌陷区的覆水时间约25 a[8],水域面积5.22 km2,平均水深3.6 m。根据《水质湖泊和水库采样技术指导》(GB/T 14581—1993)和《地表水环境质量标准》(GB 3838—2002)等标准,在保证总体布局比较均匀的情况下,结合研究区主要水流流向并兼顾周围如入河口、矸石山、住宅、稻田和水产养殖等关键区域进行采样点布设,于2016年7月17日布设水体采样点7个和底泥采样点12个,采样点分布情况见图 1。采集水样各4 L,使用BEEKER型柱状底泥采样器(荷兰BWT2-04.23.SB型)采集0~20 cm底泥,装入锡箔纸遮光包裹的棕色玻璃瓶中并用冰袋做冷藏处理后,立即送回实验室进行冷冻干燥。水样取1 L过0.45 μm滤膜,用锡纸将使用过的滤膜包好后与经筛分后的底泥样品一起放入-20 ℃冰箱保存,抽滤过的水样中加入10 mL甲醇固定剂和100 μL代标(2,4,5,6-四氯-间二甲苯)后于4 ℃冷藏并在7 d内完成检测。
|
图 1 杨庄采样点位分布图 Figure 1 Distribution of sampling points of Yangzhuang |
(1)水样:依次使用3 mL、CH2Cl2、3 mL CH3OH和3 mL超纯水对SPE(Solid-Phase Extraction)小柱活化,再将已抽滤过的待测水样过柱,控制流速在10 mL∙min-1,期间始终保持液面略高于柱内填充物且废液以滴落形态流出。待水样全部过柱,取5 mL超纯水淋洗小柱同时开启抽滤机进行干燥,待小柱干燥后向小柱中加入8 mL洗脱液[V(正己烷):V(CH2Cl2)=7:3]并浸泡,5 min后将小柱中洗脱液全量收集并通入已填好4 cm无水Na2SO4的层析柱进行脱水处理,再将收集液全量转移至氮吹仪中,缓慢浓缩至1.5 mL时加入2 mL正己烷进行洗涤,反复两次直至浓缩液近干后转移到GC-MS分析瓶中,加入100 μL五氯硝基苯为内标,用正己烷定容至1 mL待测。
(2)悬浮物和底泥:取(10±0.000 5)g底泥样品(处理悬浮物样品时需将附着有悬浮物的滤膜剪碎)与10 g Na2SO4混合再放入索氏提取器,另取200 mL萃取液[V(C6H14):V(CH2Cl2)=1:1]与100 μL代标混合,加2 g脱硫铜片,接入提取器进行提取;设置浴温50 ℃,将经24 h提取后的提取液过无水Na2SO4层析柱,在圆底烧瓶中旋转蒸发至约1 mL;再将浓缩液进行第二次过柱,该置换柱从上到下由无水Na2SO4:硅胶:Al2O3:无水Na2SO4=1:2:1:1组成,保持液面刚好淹没柱内填充物,取50 mL洗脱液进行冲洗,将第二次洗脱液旋转蒸发至1 mL左右,重复至柱内溶剂全为正己烷;最后将洗脱液全量转移至氮吹仪上浓缩置换近干,转移到GC-MS分析瓶中并加入100 μL内标(五氯硝基苯),用正己烷定容至1 mL待测。
1.2.2 仪器分析条件本试验选择PE公司的GC-MS,包括Clarus 580/680气质色谱仪和SQ8 MS质谱仪两个部分。GC参数:色谱柱选择Elite-5 MS;氦气流速1 mL∙min-1,不分流进样,进样量1 μL,入口温度250 ℃;初始温度80 ℃,以30 ℃∙min-1快速升温至160 ℃,再以3 ℃∙min-1缓慢升至265 ℃,其中每次升温至温度节点时均保温1 min后再进行下一阶段升温。MS参数:电子轰击能量70 eV,离子源温度250 ℃,传输线温度280 ℃,模式选择Scan全扫描(范围50~500 m/z),SIR(选择离子扫描)模式。工作曲线为测量前配制,标线范围为10~500 mg∙L-1OCPs混标,浓度梯度点设置为:10、20、50、100、200、500 mg∙L-1。待测样品定性分析时参照标准样品各色谱峰保存时间,定量分析采用内标法计算。
1.3 质量控制和保证(QA/QC)参照美国环保署(US-EPA)推荐的质控方法,采用方法空白、平行样设定和加标空白作为本次试验质控的主要方法。其中方法空白:每测4个样品后插入一个无水Na2SO4替换样并用相同测定步骤进行测定,以此保证正己烷无杂峰,试验结果响应值达到4.91e7;平行样设定:每组试验都设置一组平行样,并将相对标准误差控制在20%以下从而保证试验的可重复性;加标空白法:选择样品中不存在的代标物质可以对测定过程中的物质回收率进行测定,因此选择前处理实验前加入2,4,5,6-四氯-间二甲苯作为代标物,水样和底泥的平均回收率分别为70.14%~104.51%和76.28%~122.15%,符合EPA标准。
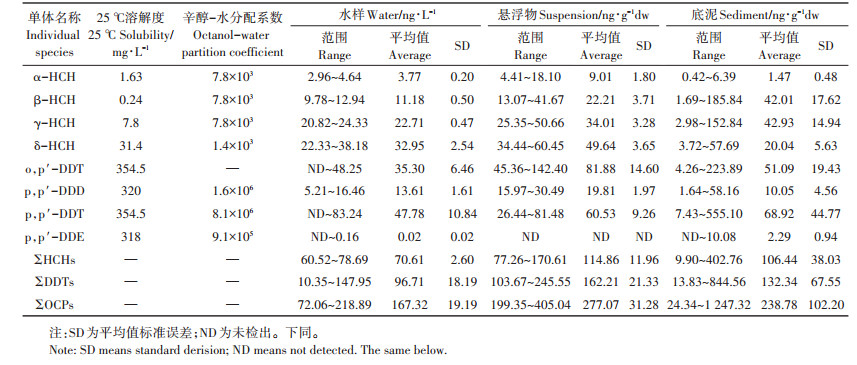
2 结果和讨论 2.1 杨庄沉陷区有机氯农药污染特征 2.1.1 六六六和滴滴涕的质量浓度特征由表 1可知,杨庄采煤沉陷区内除悬浮物未检出p,p′-DDE,其他7种OCPs单体(α-HCH、β-HCH、γ-HCH、δ-HCH和o,p′-DDT、p,p′ -DDD、p,p′-DDT)在3种介质中检出率达100%,证明该研究区域的OCPs在各介质中分布相当广泛。
|
|
表 1 杨庄沉陷区各介质OCPs质量浓度 Table 1 OCPs concentrations in various media in Yangzhuang subsidence area |
通过表 1对比各OCPs单体的水相溶解度和水样测量结果,发现检测结果总体偏低,符合OCPs疏水性较强的物理性质。杨庄水域悬浮态HCHs和DDTs平均值最高,分别达到114.86 ng∙g-1dw和162.21 ng∙g-1dw,沉积态HCHs和DDTs质量浓度分别为9.90~402.76 ng∙g-1dw和13.83~844.56 ng∙g-1dw,平均值均略低于悬浮态,由于底泥流动性低、混合性差和采样点差异性,造成数据离散程度高(SD=102.2)。此外经测定发现悬浮态TOC平均质量浓度为10.53 mg∙L-1,略高于沉积态TOC平均质量浓度9.08 mg∙L-1。排除测量误差后,根据Cornelissen等[9]和Per等[10]的研究结果,该现象可能是由于夏季水温较高,导致水体富营养化、浮游生物吸附及底泥OCPs释放速率加快。
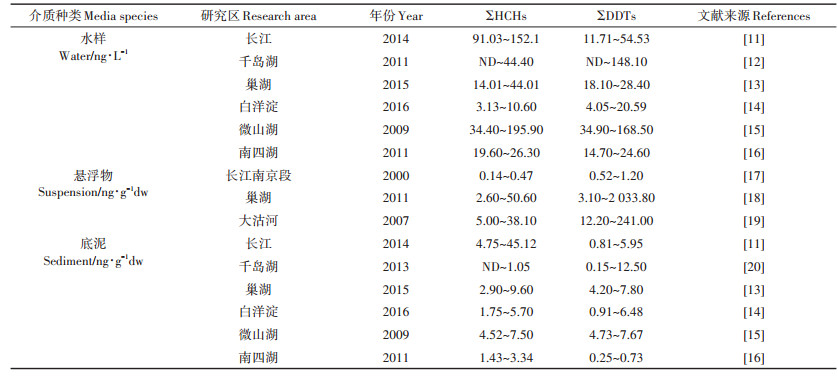
为了进一步了解OCPs的污染状况,与国内多个水域进行比较发现(表 2),研究区溶解态HCHs含量(60.52~78.69 ng∙L-1)低于长江,超过了千岛湖、巢湖、白洋淀和南四湖,略高于微山湖;DDTs含量(10.35~147.95 ng∙L-1)略低于大亚湾,与千岛湖及微山湖持平,部分点位略高于长江,远超巢湖、白洋淀和南四湖。悬浮态HCHs含量(77.26~170.61 ng∙g-1dw)超过长江南京段、巢湖和大沽河1~1000倍不等,DDTs含量(103.67~245.55 ng∙g-1dw)与巢湖和大沽河持平,超过南京段近千倍。沉积态HCHs含量(9.90~402.76 ng∙g-1dw)和DDTs含量(13.83~844.56 ng∙g-1dw)绝大部分点位均超过对照区域(长江、千岛湖、巢湖、白洋淀、微山湖和南四湖),据现场调查发现,该水域因地处煤炭运输主干道,受矸石山淋溶作用和上游水土流失带入的有机质影响,导致杨庄采煤沉陷区蓄积的OCPs含量较多,并超出一般水域的OCPs含量。综合对比结果发现:溶解态OCPs质量浓度略高于自然水域,悬浮态和沉积态OCPs质量浓度均大幅度超过自然水域,污染较严重,且夏季悬浮物污染程度大于底泥,因此该塌陷水域污染水平较高,建议进行生态修复。
|
|
表 2 中国各地水域的溶解态/悬浮态/沉积态HCHs和DDTs的质量浓度 Table 2 Concentrations of HCHs and DDTs in water, suspended solids and sediments in waters around China |
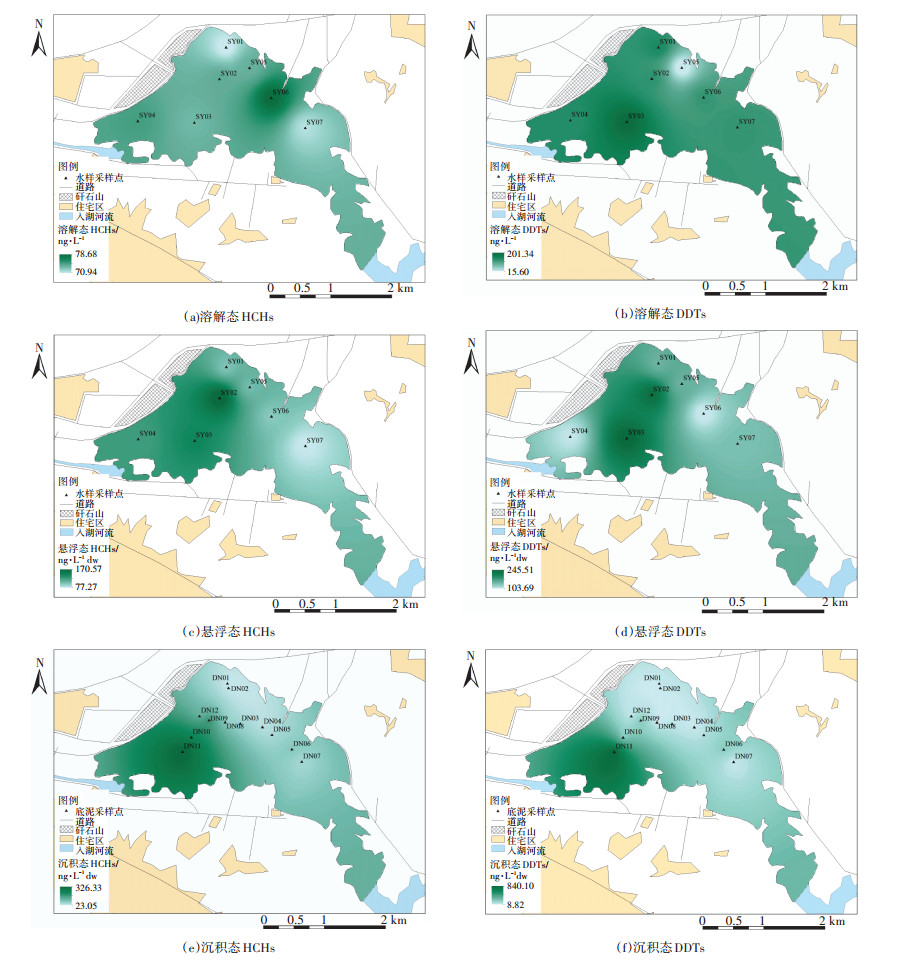
为了直观描述整个塌陷水域内DDTs和HCHs的空间分布特征,使用ArcGIS 10.2对各介质中DDTs和HCHs进行插值分析。由于采样时月降雨量达118.04 mm,环境中OCPs受地表径流作用及大气沉降作用进入研究区域。根据OCPs的高脂溶性特征,刚进入水体中的OCPs大部分吸附在悬浮颗粒上,小部分以溶解态的方式蓄存于水体[21]。因此溶解态DDTs和HCHs质量浓度分布较平均,部分点位受外界因素影响较大,如点SY05(图 2b)的溶解态DDTs含量较少,有研究表明水中浮游植物的生长可能会对溶解态DDTs含量有一定的拮抗作用[22],因此溶解态DDTs含量较少;而受降雨影响后入河口水流流量和流速上升,入湖口处悬浮态DDTs和HCHs的最高质量浓度点SY03和SY02偏离入河口向水域中心转移(图 2c、图 2d),质量浓度随水流走向呈现先升高后降低趋势;沉积态OCPs整体质量浓度分布特征则呈现随水流方向由西向东逐渐削减的趋势,该现象是由于夏季温度偏高,使得沉积态OCPs以解析释放为主要趋势,加上OCPs在底泥中迁移性较差,导致入湖OCPs主要沉积于底泥入河口处(图 2e、图 2f)。
|
图 2 3种介质中HCHs和DDTs的空间分布特征 Figure 2 Spatial distribution characteristics of HCHs and DDTs in three media |
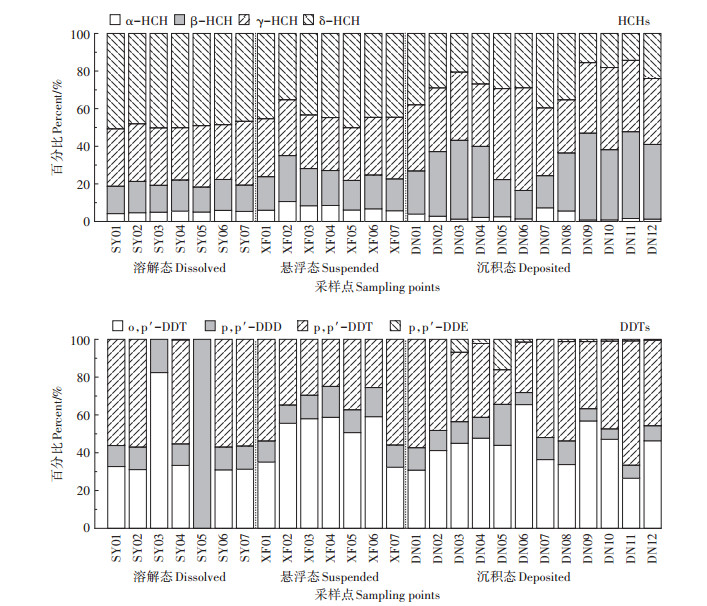
HCHs的来源通常分为两种,工业HCHs(α-HCH、β-HCH、γ-HCH、δ-HCH)和林丹(γ-HCH>99%)[23]。根据图 3a,溶解态和悬浮态中γ-HCH质量分数为30%左右,可能受林丹输入影响,沉积态γ-HCH质量分数明显高于溶解态和悬浮态。水流汇集处颗粒物和悬浮物沉降量增加使DN06点γ-HCH质量分数最高达到54.61%。由于各异构体稳定性不同,环境中HCHs降解速率为γ-HCH>α-HCH>δ-HCH>β-HCH[24],而溶解态和悬浮态中4种异构体的比例大小均为α-HCH < β-HCH < γ-HCH < δ-HCH,底泥中主要残留物为γ-HCH和β-HCH,均不符合降解规律,可能与短时间内新HCHs大量进入有关,影响到环境中各HCHs单体的质量浓度特征。
|
图 3 3种介质中HCHs和DDTs的组成特征 Figure 3 Composition characteristics of HCHs and DDTs in three medias |
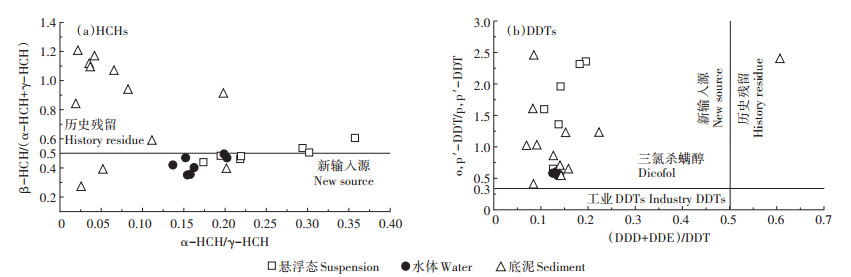
一般情况下,当β-HCH/(α-HCH+γ-HCH) < 0.5时,说明该区域存在新HCH输入,主要为林丹或大气源输入[25]。此外α-HCH和γ-HCH作为多种同分异构体中挥发性和持久性最强和最弱的物质,常常利用特征比值α-HCH/γ-HCH判别HCHs来源[26],当比值≤1时,HCHs主要来自林丹。由表 3中可见特征比值α-HCH/γ-HCH < 0.375,可知该地区的HCHs主要来自于林丹使用,且根据变异系数大小可见各介质受林丹影响的空间差异性顺序为沉积态>悬浮态>溶解态。通过各介质散点分布情况(图 4a),进一步说明各介质近期受林丹输入影响顺序为水体>悬浮物>底泥,底泥的原农田塌陷土壤HCHs正在降氯分解,而水体中新入林丹正由溶解态向沉积态转化。
|
|
表 3 各赋存形态中特征比值范围、平均值与变异系数对比 Table 3 The comparison of wherein the ratio range, the mean and CV in different medias |
|
图 4 3种介质中HCHs和DDTs的来源分析 Figure 4 Source analysis of HCHs and DDTs in three medias |
DDTs的来源也通常由工业DDTs(o,p′-DDT/p,p′-DDT=0.25)和农业三氯杀螨醇(o,p′-DDT/p,p′-DDT=7.0±2.2)组成,自然环境下,p,p′-DDT好氧代谢为p,p′-DDE,厌氧脱氢降解为p,p′-DDD,且降解物非常稳定[27]。研究区各介质中p,p′-DDE几乎未检测出,而p,p′-DDD的检出率为100%(图 3b),证明3种介质中溶解氧含量很低。
一般情况下,当DDT持续汇入自然环境时,降解产物DDD和DDE在总DDTs中占比相对较低。因此使用(DDD+DDE)/ΣDDTs来指示DDT的降解程度及来源,比值>0.5时表示沉积物中DDT主要来自土壤中长期分化残留,而 < 1时代表环境中存在DDT的新近输入[28-29]。考虑到本研究区域中除工业DDTs影响外可能还受农业三氯杀螨醇降解的影响,o,p′-DDT作为三氯杀螨醇最主要杂质,在该研究区域被大量检出(图 3b),因此本研究还选择o,p′-DDT/p,p′-DDT作为分辨DDTs来源的依据,一般来说,当比值≥ 0.3时,主要来源为三氯杀螨醇,当比例 < 0.2时,主要来源于工业DDTs[30]。根据图 3b,检测出3种介质中主要成分为p,p′-DDT和o,p′-DDT,且悬浮物中o,p′-DDT含量较高。图 4b中杨庄沉陷区仅个别底泥点位(DDD +DDE)/DDT>0.5,其余点位均 < 1,说明本地区绝大部分DDT来源于近期农业方面使用的三氯杀螨醇,符合周围农田进行稻谷生产时撒药杀虫的实际情况。并且从污染程度的空间变异性来看(表 3),各介质中DDTs特征比值的变异系数均超过15%,反映出各介质之间DDTs来源和受OCPs污染程度的空间差异性较大。
2.3 潜在生态风险分析目前,针对悬浮物的生态风险分析多使用和沉积物相同的标准[31],因此选用MacDonald等[32]提出的可应用于淡水背景的共识沉积物质量基准法(Consensus-based Sediment Quality Guidelines,CB-SQGs),对杨庄悬浮物和底泥中OCPs的潜在生态风险进行分析。该方法的OCPs毒性发生率与可能效应含量(Probable effect concentration,PECs)高度相关(R2=0.98),当ΣDDTs和ΣHCHs浓度高于PECs时,该地区水生生物的毒性发生率分别为100%和82.4%;当ΣDDTs和ΣHCHs浓度低于阈值效应浓度(Thresholdeffect concentration,TECs)时,水生生物毒性发生率分别为17.4%和28.1%;浓度介于TECs和PECs之间时,毒性发生率分别为100%和65.9%。
从表 4可见,在杨庄的7个水样点和12个底泥采样点中,溶解态DDTs和HCHs质量浓度均小于《地表水环境质量标准》(GB 3838—2002)中Ⅲ类水质标准中DDTs和HCHs标准限额0.001 mg∙L-1和0.005 mg∙L-1,对生物毒性小,处于低生态风险水平。其中悬浮态和沉积态中DDTs含量位于TECs和PECs间的点位概率分别为100%和91.67%,生物毒性发生率分别为100%和60.41%,说明这两种介质处于中高生态风险水平,尤其是悬浮态DDTs(p,p′-DDT+o,p′-DDT)的点位PECs超过率达100%,生态风险极高。γ-HCH在悬浮态和沉积态中质量浓度大于PECs的点位概率分别为100%和75%,且超过PECs限值几倍至几十倍不等,生物毒性发生率分别为82.4%和78.27%,生态风险水平较高。因此当前需要开展针对杨庄塌陷区OCPs底泥的污染修复行动,控制OCPs进入该水域,避免沉陷区周围生物受到更大影响。
|
|
表 4 杨庄沉陷区悬浮物和底泥中OCPs潜在生态风险分析 Table 4 Evaluation of potential ecological risks of OCPs in suspended matter and sediment in Yangzhuang subsidence area |
(1)杨庄农田塌陷区溶解、悬浮和沉积态的ΣOCPs质量浓度范围分别为72.06~218.89 ng∙L-1、199.35~405.04 ng∙g-1dw和24.34~1 247.32 ng∙g-1dw,其中溶解态OCPs污染程度略高于普通水域,悬浮态与沉积态OCPs污染程度大幅度超过自然水域,悬浮态OCPs略高于沉积态OCPs。
(2)溶解态OCPs各点位差异性较大,悬浮态和沉积态OCPs质量浓度分布特征呈现随水流方向从西向东依次递减的特征,且悬浮态OCPs相对沉积态OCPs的抗水流冲击能力较弱。
(3)水体-底泥系统受近期林丹输入影响顺序为水体>悬浮物>底泥,水体HCHs主要来自林丹,悬浮物和底泥都受历史残留HCHs和新入林丹影响,DDTs主要来自近期农业使用的三氯杀螨醇。
(4)溶解态OCPs对环境负面影响极小,处于低生态风险水平;悬浮态以及沉积态DDTs和γ-HCH各点位质量浓度全部超过阈值效应浓度TECs,处于中高生态风险水平,其中沉积态OCPs毒性发生率略低于悬浮态OCPs毒性发生率。
(5)针对采煤沉陷区的OCPs的污染特征,建议在入河口采取干扰措施,如建立水闸、降低水流速度、控制渔业养殖活动及周边农田的杀虫剂使用、适时进行湖底清淤工作等。
| [1] |
Feng J L, Zhai M X, Liu Q, et al. Residues of organochlorine pesticides (OCPs)in upper reach of the Huaihe River, East China[J]. Ecotoxicology and Environmental Safety, 2011, 74(8): 2252-2259. DOI:10.1016/j.ecoenv.2011.08.001 |
| [2] |
Zhi H, Zhao Z H, Zhang L, et al. The fate of polycyclic aromatic hydrocarbons(PAHs)and organochlorine pesticides(OCPs)in water from Poyang Lake, the largest freshwater lake in China[J]. Chemosphere, 2015, 119: 1134-1140. DOI:10.1016/j.chemosphere.2014.09.054 |
| [3] |
Tang Z W, Yang Z F, Shen Z Y, et al. Residues of organochlorine pesticides in water and suspended particulate matter from the Yangtze River catchment of Wuhan, China[J]. Environmental Monitoring and Assessment, 2008, 137(1/2/3): 427-439. |
| [4] |
Hu G, Luo X, Li F, et al. Organochlorine compounds and polycyclic aromatic hydrocarbons in surface sediment from Baiyangdian Lake, North China:Concentrations, sources profiles and potential risk[J]. Journal of Environmental Sciences, 2010, 22(2): 176-183. DOI:10.1016/S1001-0742(09)60090-5 |
| [5] |
邱浩然, 高良敏, 姚素平, 等. 淮南潘一采煤塌陷区土壤-底泥中多氯联苯(PCBs)分布特征[J]. 煤炭学报, 2015, 40(9): 2173-2180. QIU Hao-ran, GAO Liang-min, YAO Su-ping, et al. Distribution of PCBs in soil and sediment of subsidence water in Panji No. 1 coal mine of Huainan[J]. Journal of China Coal Society, 2015, 40(9): 2173-2180. |
| [6] |
Ouyang Z Z, Gao L M, et al. Distribution, sources and influence factors of polycyclic aromatic hydrocarbon at different depths of the soil and sediments of two typical coal mining subsidence areas in Huainan, China[J]. Ecotoxicology and Environmental Safety, 2018, 163: 255-265. DOI:10.1016/j.ecoenv.2018.07.024 |
| [7] |
Meng J, Wang T Y, Wang P, et al. Perfluorinated compounds and organochlorine pesticides in soils around Huaihe River:A heavily contaminated watershed in Central China[J]. Environmental Science and Pollution Research, 2013, 20(6): 3965-3974. DOI:10.1007/s11356-012-1338-6 |
| [8] |
谢凯, 张雁秋, 易齐涛, 等. 淮南潘一矿塌陷水域沉积物中磷的赋存和迁移转化特征[J]. 中国环境科学, 2012, 32(10): 1867-1874. XIE Kai, ZHANG Yan-qiu, YI Qi-tao, et al. Phosphorus fractions and migration in the sediments of a subsided water area in Panyi coal mine of Huainan[J]. China Environmental Science, 2012, 32(10): 1867-1874. DOI:10.3969/j.issn.1000-6923.2012.10.021 |
| [9] |
Cornelissen G, Noort P C M V, Parsons J R, et al. Temperature dependence of slow adsorption and desorption kinetics of organic compounds in sediments[J]. Environmental Science & Technology, 1997, 31(2): 454-460. |
| [10] |
Per L, Agdersson A, Dag B, et al. Persistent organic pollutants (POPs)in pelagic systems[J]. AMBIO, 2000, 29: 201-208. |
| [11] |
王静, 刘明丽, 张士超, 等. 沈抚新城不同土地利用类型多环芳烃含量、来源及人体健康风险评价[J]. 环境科学, 2016, 38(2): 703-710. WANG Jing, LIU Ming-li, ZHANG Shi-chao, et al. Concentration, sources and ecological risks of PAHs of different land use types in Shenfu New City[J]. Environmental Science, 2016, 38(2): 703-710. |
| [12] |
唐访良, 张明, 徐建芬, 等. 千岛湖库区及其主要入库河流水中有机氯农药残留污染特征及健康风险评价[J]. 环境科学, 2014, 35(5): 1735-1741. TANG Fang-liang, ZHANG Ming, XU Jian-fen, et al. Pollution characteristics and health risk assessment of organochlorine pesticides (OCPs)in the water of Lake Qiandao and its major input rivers[J]. Environmental Science, 2014, 35(5): 1735-1741. |
| [13] |
姜珊, 孙丙华, 徐彪, 等. 巢湖主要湖口水体和表层沉积物中有机氯农药的残留特征及风险评价[J]. 环境化学, 2016, 35(6): 1228-1236. JIANG Shan, SUN Bing-hua, XU Biao, et al. Characteristics and risk assessment of organochlorine pesticides in water and surface sediments from main estuaries of Chaohu Lake[J]. Environmental Chemistry, 2016, 35(6): 1228-1236. |
| [14] |
Dai G H, Liu X H, Liang G. Distribution of organochlorine pesticides (OCPs)and polychlorinated biphenyls(PCBs)in surface water and sediments from Baiyangdian Lake in north China[J]. Journal of Environmental Sciences, 2011, 23(10): 1640-1649. DOI:10.1016/S1001-0742(10)60633-X |
| [15] |
戴文婷, 安英莉, 葛冬梅, 等. 微山湖内源有机氯农药残留的生态风险评估[J]. 水生态学杂志, 2016, 37(5): 41-48. DAI Wen-ting, AN Ying-li, GE Dong-mei, et al. Ecological risk assessment of organochlorine pesticide residues in Weishan Lake[J]. Journal of Hydroecology, 2016, 37(5): 41-48. |
| [16] |
Zhang G Z, Pan Z K, Bai A Y, et al. Distribution and bioaccumulation of organochlorine pesticides(OCPs)in food web of Nansi Lake, China[J]. Environmental Monitoring and Assessment, 2014, 186(4): 2039-2051. DOI:10.1007/s10661-013-3516-5 |
| [17] |
许士奋, 蒋新, 冯建, 等. 气相色谱法测定长江水体悬浮物和沉积物中有机氯农药的残留量[J]. 环境科学学报, 2000, 20(4): 494-498. XU Shi-fen, JIANG Xin, FENG Jian, et al. Gas chromatographic method for the determination of organochlorine pesticides in suspended solids and sediments of the Yangtze River[J]. Journal of Environmental Sciences, 2000, 20(4): 494-498. DOI:10.3321/j.issn:0253-2468.2000.04.022 |
| [18] |
王卿梅, 何玘霜, 王雁, 等. 巢湖悬浮物中有机氯农药的分布、来源与风险[J]. 湖泊科学, 2014, 26(6): 887-896. WANG Qing-mei, HE Yan-shuang, WANG Yan, et al. Distribution, source identification and risk assessment of organochlorine pesticides (OCPs)in suspended particulate matter(SPM)from Lake Chao[J]. Lake Science, 2014, 26(6): 887-896. |
| [19] |
齐维晓, 刘会娟, 曲久辉, 等. 天津主要纳污及入海河流中有机氯农药的污染现状及特征[J]. 环境科学学报, 2010, 30(8): 1543-1550. QI Wei-xiao, LIU Hui-juan, QU Jiu-hui, et al. Characterization of organochlorine pesticides contamination in Tianjin rivers[J]. Journal of Environmental Science, 2010, 30(8): 1543-1550. |
| [20] |
陈峰, 唐访良, 徐建芬, 等. 千岛湖表层沉积物中有机氯农药的残留特征及生态风险评价[J]. 湖泊科学, 2014, 26(4): 111-117. CHEN Feng, TANG Fang-liang, XU Jian-fen, et al. Residue characteristics and ecological risk assessment of organochlorine pesticides (OCPs)in the surface sediments of Lake Qiandao[J]. Journal of Lake Science, 2014, 26(4): 111-117. |
| [21] |
Masahiro S, Kohji M. Wet and dry deposition fluxes of mercury in Japan[J]. Atmospheric Environment, 2005, 39: 3139-3146. DOI:10.1016/j.atmosenv.2005.01.049 |
| [22] |
王倩怡.富营养化水体中有机氯农药的污染及其与浮游植物间的响应关系[D].天津: 天津大学, 2007. WANG Qian-yi. Response of organochlorine pesticides pollution to phytoplankton dynamics in eutrophic water[D]. Tianjin: Tianjin University, 2007. http://d.wanfangdata.com.cn/Thesis/Y1357813 |
| [23] |
WillettI K L, Ulrich E M, Hites R A. Differential toxicity and environmental fates of hexachlorocyclohexane isomers[J]. Environmental Science & Technology, 1998, 32(15): 2197-2207. |
| [24] |
Kaushik K, Popp P. Persistence and metabolism of HCH and DDT under subtropical conditions[J]. Soil and Biology and Biochemistry, 1991, 23(2): 131-134. DOI:10.1016/0038-0717(91)90124-3 |
| [25] |
苏禹龙, 徐晓萌, 郭志勇, 等. 条子河中多环芳烃和有机氯农药的时空分布及来源解析[J]. 吉林大学学报(理学版), 2014, 52(3): 611-622. SU Yu-long, XU Xiao-meng, GUO Zhi-yong, et al. Temporospatial distribution and source identification of polycyclic aromatic hydrocarbons and organochlorine pesticides in Tiaozi River[J]. Journal of Jilin University (Science Edition), 2014, 52(3): 611-622. |
| [26] |
Kalantzi O I, Alcock R E, Johnston P A, et al. The global distribution of PCBs and organochlorine pesticides in butter[J]. Environmental Science & Technology, 2001, 35(6): 1013-1018. |
| [27] |
Yu H Y, Bao L J, Liang Y, et al. Field validation of anaerobic degradation pathways for Dichlorodiphenyltrichloroethane(DDT)and 13 metabolites in marine sediment cores from China[J]. Environmental Science & Technology, 2011, 45(12): 5245-5252. |
| [28] |
Li Y Y, Niu J F, Shen Z Y, et al. Spatial and seasonal distribution of organochlorine pesticides in the sediments of the Yangtze Estuary[J]. Chemosphere, 2014, 114(22): 233-240. |
| [29] |
Bosch C, Grimalt J O, Fernandez P. Enantiomeric fraction and isomeric composition to assess sources of DDT residues in soils[J]. Chemosphere, 2015, 138: 40-46. DOI:10.1016/j.chemosphere.2015.05.047 |
| [30] |
Aigner E J, Leone A D, Falconer R L. Concentrations and enantiomeric ratios of organochlorine pesticides in soils from the U. S. Corn Belt[J]. Environmental Science & Technology, 1998, 32: 1162-1168. |
| [31] |
Schubert B, Heiniger P, Keller M, et al. Monitoring of contaminants in suspended particulate matter as an alternative to sediments[J]. TracTrends in Analytical Chemistry, 2012, 36(SI): 58-70. |
| [32] |
MacDonald D D, Ingersoll C G, Berger T A. Development and evaluation of consensus-based sediment quality guidelines for fresh water ecosystems[J]. Archives of Environment Contamination and Toxicology, 2000, 39(1): 20-31. DOI:10.1007/s002440010075 |
 2020, Vol. 39
2020, Vol. 39