2. 青岛市生态环境局高新区分局, 山东 青岛 266000;
3. 澳门科技大学澳门环境研究院, 澳门 999078
2. High-tech Zone Branch of Qingdao Municipal Bureau of Ecology and Environment, Qingdao 266000, China;
3. Macao Environmental Research Institute, Macau University of Science and Technology, Macao 999078, China
铬(Cr)在自然界中普遍存在,在自然土壤中的浓度为10~150 mg·kg-1[1]。我国农田土壤中Cr的污染来源包括铬盐、电镀、制革、大气沉降和施用化肥等[2-4],其导致4.31%的农田调查点位超过《土壤环境质量农用地土壤风险管控标准(试行)》(GB 15618—2018)中Cr的筛选值[2]。Cr存在多种价态(-2~6),其在土壤环境中以Cr(Ⅲ)和Cr(Ⅵ)最为常见[5]。Cr(Ⅲ)是人类和动物健康所必需的微量元素,对脂质和糖代谢有重要影响[6];而Cr(Ⅵ)是一种强致癌物质,对生态环境和人体健康构成显著威胁[7],在土壤溶液中,Cr(Ⅲ)以阳离子(Cr3+)存在,其迁移性较差[8];与Cr(Ⅲ)不同,Cr(Ⅵ)常以HCrO4-、CrO42-和Cr2O72-等含氧阴离子形式存在,难以被固定,因此具有很强的活性[9]。鉴于Cr(Ⅲ)和Cr(Ⅵ)在毒性和物理化学性质方面的显著差异[10],土壤Cr(Ⅵ)污染受到广泛关注。
水溶性重金属进入土壤后,其可提取态、生物有效性和毒性随时间的推移逐渐降低,这个过程称为老化[11-13]。当水溶性的Cr(Ⅵ)进入土壤后,土壤组分和性质对其环境行为有很大影响。pH值的降低可以增加矿物表面的正电荷,从而增加对Cr(Ⅵ)的吸附能力[14]。铁氧化物能与Cr(Ⅵ)在球内表面形成络合,有利于Cr(Ⅵ)的吸附[15]。当酸性土壤中存在自由Cr(Ⅵ)时,有机质可以提供电子以促进Cr(Ⅵ)还原为Cr(Ⅲ)[16]。关于外源重金属在土壤中的老化过程已有较多研究[17]。Ma等[18]和Zhang等[19]认为外源Cu离子和Zn离子在土壤中的老化过程包括沉淀、有机质络合和微孔扩散,并利用土壤性质和时间构建了预测土壤中同位素可交换态Cu、Zn的半机理模型。郑顺安等[13]对Cr(Ⅲ)在我国22种典型土壤中的老化特征进行了研究,发现有机质对老化速率影响最大,其次是pH和活性氧化铁。受到土壤氧化还原条件的影响,Cr(Ⅵ)在土壤可以被还原成Cr(Ⅲ)。Xiao等[1]在7种土壤中对Cr(Ⅵ)进行了28 d的老化实验发现,Cr(Ⅵ)的还原速率受到溶解有机质、Fe(Ⅱ)、pH和土壤粒径分布的影响。Jardine等[20]在35种美国土壤中开展100 d老化实验发现,Cr(Ⅵ)的还原随土壤中总有机碳含量增加而增加。Yang等[21]通过105 d的老化实验发现,Cr(Ⅵ)在富含有机质和无定形Fe的水稻土中的老化和还原过程要快于潮土。目前,以上研究大多只注重单一价态Cr的老化,鲜有研究同时关注Cr(Ⅵ)及其还原产生的Cr(Ⅲ)的老化过程。
缓冲盐、稀酸和含螯合剂溶液可作为提取剂评估土壤重金属老化过程中毒性/有效性的变化[22]。例如,CaCl2溶液可通过离子交换提取出以弱静电作用吸附在土壤固体表面的重金属[13]。但缓冲盐溶液只能反映土壤中重金属对生物的直接作用,不能很好地评价重金属的潜在有效性[23]。稀酸溶液,如0.43 mol· L-1 HNO3,能部分溶解与有机物、碳酸盐、铁、锰氧化物结合的金属元素[24],也被用来评估金属元素的毒性。但是,稀酸溶液在石灰性土壤中不是理想的提取剂[25],也不能用于研究沉淀作用对老化作用的影响。络合剂(如EDTA),已广泛用于预测重金属元素的有效性[26]。Quevauviller等[27]提出当评估Cr的毒性/有效性时,用EDTA作为提取剂能够获得比较好的效果。因此,本研究选取EDTA作为提取剂,研究Cr(Ⅵ)在老化过程中的有效性变化。
我国农田土壤分布广泛,受气候、成土过程和土壤母质等多种因素的影响,农田土壤有多种类型[28]。鉴于我国土壤类型的复杂性,对于我国土壤中Cr(Ⅵ)的长时间老化过程缺乏系统的研究。在本研究中,选取了中国不同区域的12种农田土壤,以0.05 mol·L-1 EDTA作为有效态Cr(Ⅵ)提取剂,采用高效液相色谱(HPLC)和电感耦合等离子体质谱(ICP-MS)联用的方法对提取液中的Cr(Ⅲ)和Cr(Ⅵ)进行分析,研究外源Cr(Ⅵ)进入土壤后360 d内有效态Cr(Ⅲ)和Cr(Ⅵ)随时间的变化。本研究的目的是:探讨不同土壤性质对土壤中有效态Cr(Ⅵ)的影响;通过动力学模型对Cr(Ⅵ)的老化过程进行拟合并解析影响Cr(Ⅵ)老化的主控因子;探讨老化过程中Cr(Ⅵ)还原所产生的有效态Cr(Ⅲ)的动态变化过程。老化过程对土壤中Cr(Ⅵ)的生物有效性具有重要影响,本研究结果对于Cr(Ⅵ)生态风险评价和标准制定具有重要意义。
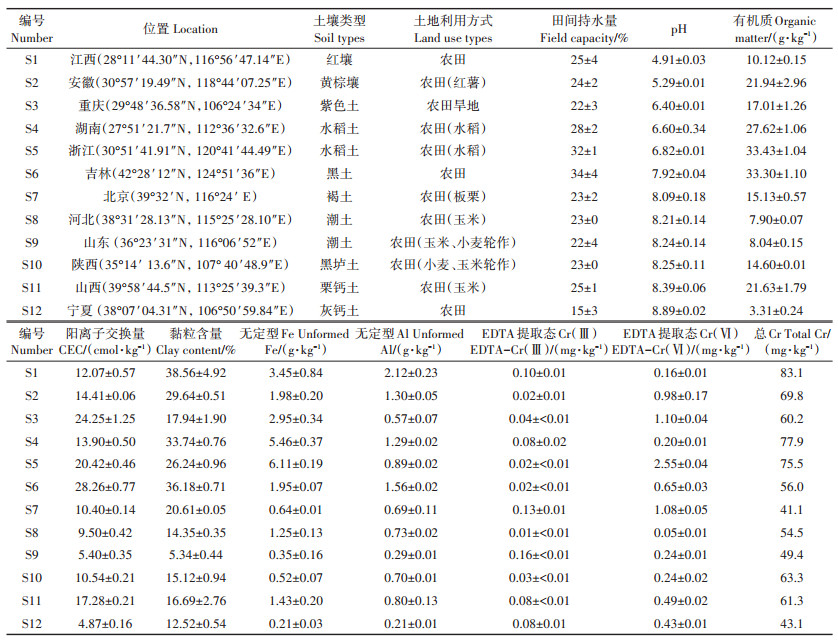
1 材料与方法 1.1 供试土壤及性质供试农田土壤样品(12种)分别采集于我国不同的区域,采样深度为(0~20 cm)。样品风干后,混匀,过2 mm的尼龙筛备用。土壤pH使用0.01 mol·L-1 CaCl2作为提取液(固液比为1:2.5),振荡提取1 h,静置30 min后,用pH计测定其酸度;土壤有机质使用重铬酸盐法测定;土壤阳离子交换量(CEC)用乙酸铵法测定;土壤中黏粒含量用移液管法测定;土壤无定形Fe、Al用草酸铵溶液提取,并用紫外可见分光光度计测定;土壤中的总Cr采用硝酸-高氯酸-氢氟酸(体积比为15:2:2)进行消解,并利用火焰原子吸收光谱法测定;土壤田间持水量用环刀法测定。在土壤基本性质分析过程中,土壤标准样品ASA-5A和GSS-7用于实验过程中的质量控制。标准样品中测定的pH、有机质、CEC及总Cr的含量分别为4.87、6.88 g·kg–1、10.3 cmol·kg–1和398 mg·kg–1,这与其认定值4.71± 0.09、7.30±0.50 g·kg–1、10.0±0.60 cmol·kg–1和410±23 mg·kg–1一致。
1.2 Cr老化实验称取2.00 kg土壤,利用喷壶均匀喷洒一定量的K2CrO4溶液,使土壤中外源添加Cr(Ⅵ)的初始浓度为50 mg·kg-1,然后把土壤充分混合均匀,放入塑料盆。加入适量去离子水,根据表 1,调节土壤含水量到田间最大持水量的80% ± 5%,并在室温下培养,同时设置不添加外源Cr(Ⅵ)的对照实验。每3 d通过称质量的方法保持土壤含水量稳定。分别在老化第2、5、15、30、60、180 d和360 d,利用柱状玻璃管,采集从表层到底部的土壤样品,冷冻干燥后,放入自封袋,供后续分析使用。每个处理设置两个平行。
|
|
表 1 供试土壤的理化性质 Table 1 Physical and chemical properties of the experimental soils |
称取1.00 g冻干的土壤于50 mL离心管中,加入10 mL 0.05 mol·L–1 EDTA(pH=10),摇床(40 ℃、180 r· min-1)中振荡12 h,离心10 min,取上清液过0.45 µm水相滤膜,暂存于4 ℃冰箱中待用。EDTA可与Cr(Ⅲ)形成Cr(Ⅲ)-EDTA络合物,防止提取液中Cr(Ⅲ)和Cr(Ⅵ)的相互转化[29]。提取液中的Cr(Ⅲ)和Cr(Ⅵ)采用高效液相色谱(HPLC)和电感耦合等离子体质谱(ICP-MS)联用的方法进行测定,具体操作条件及参数设置参考McSheehy等[30]的研究。EDTA提取的有效态Cr(Ⅵ或Ⅲ)浓度通过以下公式计算:

|
(1) |
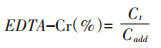
|
(2) |
式中:Ct为由于外源添加Cr(Ⅵ)而导致的第t d土壤中有效态Cr(Ⅲ)或Cr(Ⅵ)的浓度增加量,mg·kg-1;Cta为外源添加Cr(Ⅵ)土壤中第t d有效态Cr(Ⅲ)或Cr(Ⅵ)的浓度,mg·kg-1;Ct0为不添加外源Cr(Ⅵ)的对照土壤中的有效态Cr(Ⅲ)或Cr(Ⅵ)的浓度,mg·kg-1;Cadd为外源添加Cr(Ⅵ)的浓度,50 mg·kg-1。
1.4 动力学模型采用3种动力学模型对Cr(Ⅵ)老化的动力学过程进行拟合[28]。
二级动力学方程:
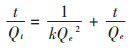
|
(3) |
Elovich方程:

|
(4) |
抛物线扩散方程:
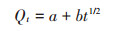
|
(5) |
式中:k为Cr(Ⅵ)老化速率常数,kg·mg-1·d-1;Qe为平衡时有效态Cr(Ⅵ)浓度,mg·kg-1;Qt为t时刻有效态Cr(Ⅵ)浓度,mg·kg-1;a和b都是常数,其中,b与Cr(Ⅵ)老化速率常数有关;t为老化时间,d。
通过比较标准误差(SE)和相关系数(R2)评价拟合程度。SE通过下列公式计算

|
(6) |
式中:q和q*分别为时间为t时土壤中Cr(Ⅵ)浓度的测定值和预测值,mg·kg-1;n为测定数据个数。
1.5 数据分析根据1.4中的3种动力学模型,用Origin 8.5将老化过程中有效态Cr(Ⅵ)实验数据进行动力学拟合,根据最优动力学模型确定Cr(Ⅵ)在不同土壤中的老化速率和老化平衡时间。利用SPSS 20.0将Cr(Ⅵ)老化速率和老化平衡时间分别与土壤性质进行多元逐步回归分析,确定Cr(Ⅵ)老化速率的主控因子。
2 结果与讨论 2.1 土壤性质依照pH由低到高的顺序,把12种土壤命名为S1~S12。如表 1所示,影响Cr(Ⅵ)环境化学行为的土壤物理化学性质(如pH、有机质等)存在差异显著[1]。土壤的pH范围为4.91~8.89,其中S1最低,S12最高。有机质含量由3.31 mg·kg–1(S12)增加到33.43 mg· kg–1(S5)。CEC的范围为4.87 cmol·kg–1(S12)~28.26 cmol · kg–1(S6)。土壤田间持水量的范围是15%~ 34%。除S9土壤(5.34%)外,各土壤黏粒含量均较高(12.52%~38.56%)。无定形Fe、Al分别在S9(0.35 g· kg–1)和S12(0.21 g·kg–1)中含量最低,在S5(6.11 g·kg–1)和S1(2.12 g·kg–1)中的含量最高。S7中总Cr含量最低(41.1 mg·kg–1),S1中的总Cr含量最高(83.1 mg·kg–1),12种土壤中总Cr含量均低于我国《土壤环境质量农用地土壤污染风险管控标准(试行)》(GB 15618—2018)中的筛选值。土壤中EDTA提取态Cr(Ⅵ)含量范围为0.05~2.55 mg·kg–1,EDTA提取态Cr(Ⅲ)含量范围为0.01~0.16 mg·kg–1,与总Cr含量相比,有效态Cr(Ⅵ)和Cr(Ⅲ)含量均较低,说明土壤中的Cr绝大多数以稳定形式存在。
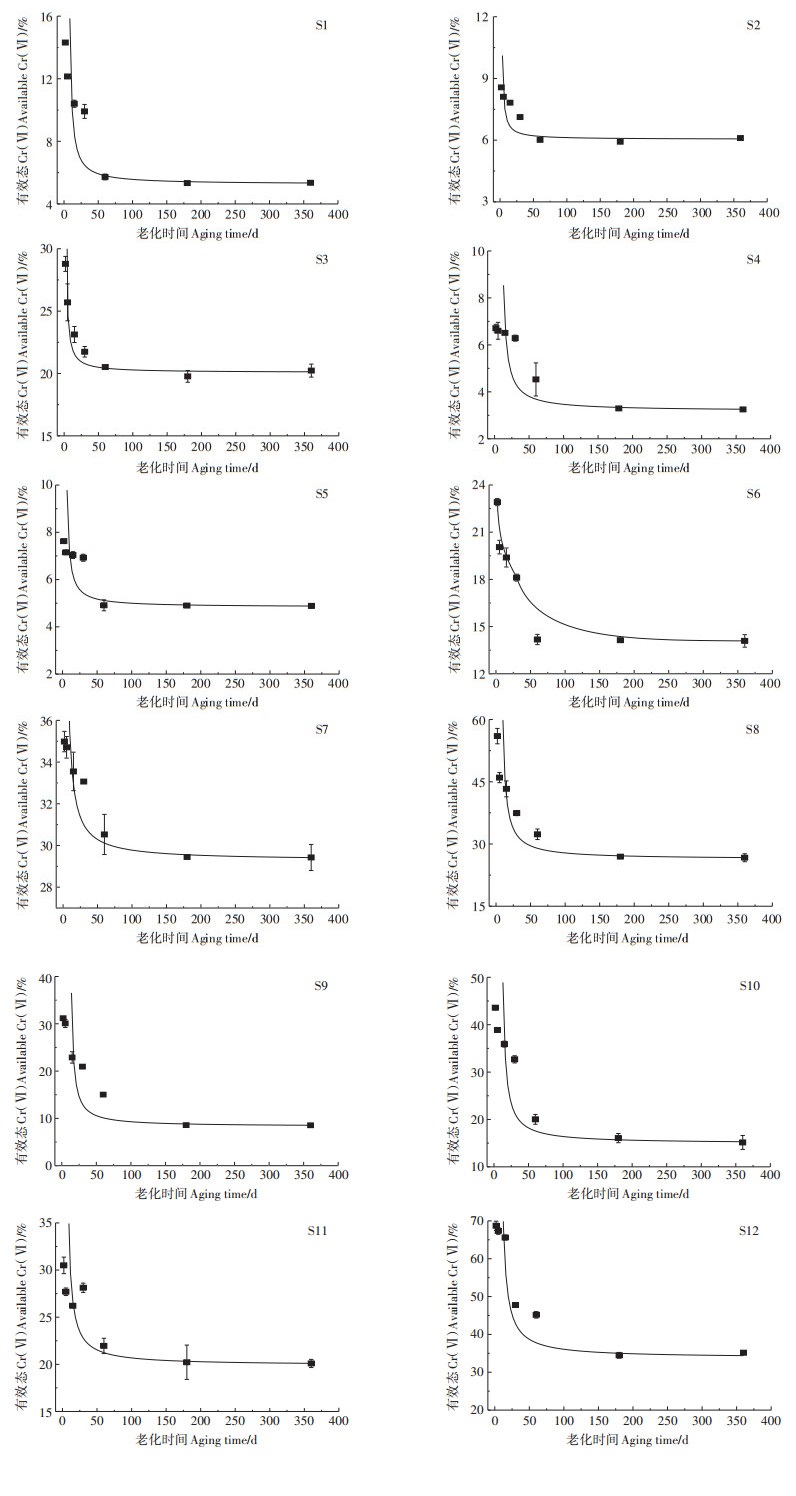
2.2 外源Cr(Ⅵ)在土壤中的老化过程 2.2.1 老化对有效态Cr(Ⅵ)的影响老化过程中12种土壤的有效态Cr(Ⅵ)逐渐降低(图 1)。老化2 d后,有效态Cr(Ⅵ)迅速降低至6.71%~68.71%,随着老化过程进行到第60 d,有效态Cr(Ⅵ)降低为4.53%~45.17%,此段时间内土壤中有效态Cr(Ⅵ)老化速度依然相对较快,降低幅度达2.18%~23.54%。180 d以后有效态Cr(Ⅵ)缓慢降低到3.29%~34.47%, 360 d后降低到3.25%~34.35%,降低量仅为1.24%~10.7%和1.28%~10.82%,本实验结果与文献报道一致。Stewart等[31]研究发现,Cr的生物有效性在老化前50 d显著下降,约100 d时在土壤中达到平衡。Yang等[21]对Cr(Ⅵ)的老化动力学研究发现,有效态Cr(Ⅵ)老化速率与老化达到平衡时间因土壤性质不同而存在较大差异(水稻土前20 d老化速率较快,约30 d到达平衡;潮土前40 d老化速率较快,约80 d达到平衡)。
|
误差线代表平行分析的标准误差 Error bars represent the standard error of duplicate analysis 图 1 老化过程中有效态Cr(Ⅵ)的变化趋势 Figure 1 Change of available Cr (Ⅵ) during the aging process |
有效态Cr(Ⅵ)的降低,与其进入土壤后发生的物理化学过程有紧密关系。土壤中的Cr(Ⅵ)可被带有正电荷的铁氧化物以静电吸引的方式吸附在表面,形成内圈或外圈络合物[32]。土壤中带有正电荷的有机质也可对Cr(Ⅵ)产生吸附作用[33]。伴随着快速的吸附过程,Cr(Ⅵ)可被有机质和Fe(Ⅱ)还原成Cr(Ⅲ)[7, 34]。未被还原的部分随时间的推移可进入到晶格内部[35]。这些过程都可固定土壤中的Cr(Ⅵ),从而使有效态Cr(Ⅵ)降低。
基于以上分析,土壤不同组分对Cr(Ⅵ)的老化可产生显著影响。已有研究显示,土壤对Cr(Ⅵ)的吸附与有机碳和铁氧化物含量呈正相关,与土壤pH呈负相关[36-38]。土壤中有机质和Fe(Ⅱ)含量与Cr(Ⅵ)还原速率存在显著正相关[1]。磁铁矿在高pH条件(pH= 13)下显著低于酸性(pH=1)和中性条件(pH=7)下对Cr(Ⅵ)的还原能力[39]。因此,pH对Cr(Ⅵ)老化过程中的吸附和还原过程起着非常重要的作用。
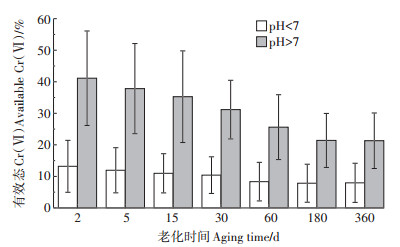
为了进一步讨论pH对有效态Cr(Ⅵ)的影响,根据pH值将土壤样品分为两组。S1、S2、S3、S4和S5为酸性土壤(pH < 7),其余的土壤为碱性土壤(pH>7)。由图 2可见,同一老化时间点有效态Cr(Ⅵ)在碱性土壤中平均含量(21.3%~41.1%)显著(P < 0.05)高于酸性土壤(8.0%~13.2%)。这意味着在pH值越高的土壤中,Cr(Ⅵ)有效态含量越高,进一步说明了pH值对有效态Cr(Ⅵ)的影响。在老化的第2 d,酸性和碱性土壤中有效态Cr(Ⅵ)含量分别为13.2%和41.1%,相差27.9个百分点。而随着时间的推移,酸性和碱性土壤中有效态Cr(Ⅵ)的含量逐渐降低为8.0%和21.3%,相差13.3个百分点。这可能是因为酸性土壤中Cr(Ⅵ)更容易被还原成Cr(Ⅲ)[21]。此外,其他土壤性质对有效态Cr(Ⅵ)的影响也不容忽视。例如S3土壤和S4土壤的pH相似,而S3土壤中有效态Cr(Ⅵ)的浓度远高于S4土壤,这可能与S3土壤中有机质和无定形Fe的含量较低有关[1]。
|
误差线表示每组土壤的标准误差 Error bars represent the standard error of soil in each group 图 2 pH < 7的土壤(n=5)与pH>7的土壤(n=7)老化过程中有效态Cr(Ⅵ)含量平均值比较 Figure 2 Comparison of the average available Cr(Ⅵ)contents between the pH < 7 soils (n=5)and pH>7 soils (n=7) during the aging process |
采用3种不同的动力学方程对老化过程中有效态Cr(Ⅵ)动态变化进行拟合(表 2),二级动力学方程拟合效果最好,相关系数为0.99~1.00(P < 0.01)。其次是Elovich方程(R2=0.83~0.97,P < 0.01),而抛物线方程(R2=0.51~0.75,P < 0.01)拟合效果较差。二级动力学模型中假定吸附的限制性过程是化学吸附。虽然该模型基于表面反应,但可以模拟由颗粒内部扩散驱动的吸附动力学[40]。因此,可以初步推测表面吸附可能是Cr(Ⅵ)老化过程中一个重要的过程。当土壤表面的结合位点被充分占据后,Cr(Ⅵ)可能扩散到土壤中吸附物质的孔隙,最后进入土壤矿物的晶格内[35]。抛物型扩散方程曲线并未穿过原点(a≠0),说明扩散作用不是Cr(Ⅵ)老化的唯一过程[41]。Elovich方程常用来描述土壤中养分和污染物的吸附和解吸动力学过程[42]。土壤中有效态Cr(Ⅵ)的变化可以用Elovich方程较好地拟合,说明土壤中Cr(Ⅵ)的老化可以看作是多个一级反应同时发生的过程[28]。
|
|
表 2 Cr(Ⅵ)老化过程的动力学拟合结果 Table 2 Kinetic fitting results of Cr(Ⅵ)aging process |
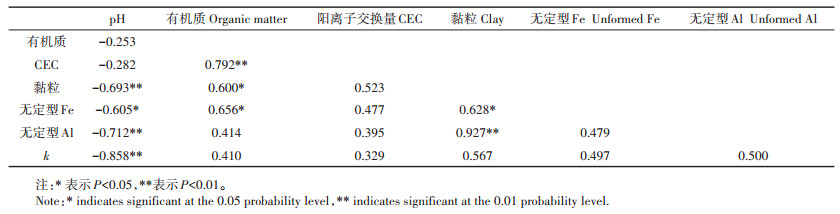
二级动力学模型中速率常数k的绝对值表示Cr(Ⅵ)的老化速率(表 2)。其中,S12中|k|值最小(0.010 1 kg·mg-1·d-1),S2中|k|值最大(0.234 6 kg·mg-1·d-1),说明Cr(Ⅵ)在S2中的老化速率最快,而在S12中最慢。将土壤性质与Cr(Ⅵ)老化速率(k)进行Pearson相关分析(表 3),结果表明pH与Cr(Ⅵ)老化速率常数呈显著负相关(r=-0.858,P < 0.01),而与有机质、CEC、黏粒、无定形Fe和无定形Al呈中等正相关(r=0.329~ 0.567)。为了进一步研究不同土壤性质对Cr(Ⅵ)老化速率的影响,利用SPSS软件对pH、有机质、CEC、黏粒含量、无定形Fe、无定形Al和Cr(Ⅵ)老化速率常数进行逐步回归分析,来确定影响Cr(Ⅵ)老化速率的主控因子并建立回归模型,如公式(7)所示。
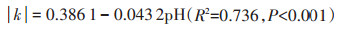
|
(7) |
式中:k为Cr(Ⅵ)老化速率常数,kg·mg-1·d-1;pH为土壤pH值。
|
|
表 3 Cr(Ⅵ)老化速率常数(k)与土壤性质的Pearson相关系数 Table 3 Pearson correlation coefficient between Cr(Ⅵ)aging rate constant and selected soil properties |
由公式(7)可知,土壤pH是土壤中Cr(Ⅵ)老化速率的主控因子。Cr(Ⅵ)的老化速率与pH呈负相关,表明Cr(Ⅵ)的老化速率随土壤pH的升高而降低。土壤pH值是土壤化学性质的综合反映[1],对Cr(Ⅵ)的吸附和氧化还原过程有很大影响[7]。Choppala等[37]通过研究pH对Cr(Ⅵ)吸附的影响发现,pH升高使土壤表面所带的正电荷减少,减弱了Cr(Ⅵ)与土壤表面的静电引力,使Cr(Ⅵ)的吸附量随pH的升高而降低。Ajouyed等[43]也报道了OH-离子可以占据Cr(Ⅵ)的吸附位点,从而增加了Cr(Ⅵ)在碱性土壤中的迁移率。此外,土壤pH值也影响Cr(Ⅵ)向Cr(Ⅲ)的转化[44]。据Yang等[21]报道,在酸性条件下,土壤中有机质和Fe(Ⅱ)等电子供体存在时,Cr(Ⅵ)很容易转化为Cr(Ⅲ)。
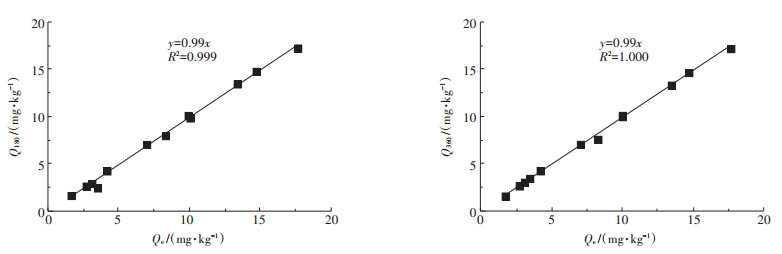
2.2.3 Cr(Ⅵ)近似老化平衡时间平衡浓度(Qe)指老化达到平衡时有效态Cr(Ⅵ)的浓度,如图 3所示,Qe与第180 d和360 d测得的有效态Cr(Ⅵ)浓度呈很好的线性关系(R2=0.999和1.000,P < 0.01),说明所有土壤中Cr(Ⅵ)在第360 d或更早时已达到平衡状态。为了研究不同土壤中Cr(Ⅵ)达到平衡所需的具体时间,假设当土壤中有效态Cr(Ⅵ)浓度为平衡浓度(Qe)的98%时,老化过程达到近似平衡[28]。根据近似平衡浓度,采用二级动力学模型计算不同土壤中Cr(Ⅵ)的近似老化平衡时间T,如表 4所示。不同土壤中Cr(Ⅵ)的近似老化平衡时间有明显差异。Cr(Ⅵ)在S2达到近似老化平衡所需的时间最短,仅为6 d,而在S12中最长,为158 d,这意味着添加到S2土壤中的外源Cr(Ⅵ)可以迅速达到平衡状态,而S12则需要更长的时间。当前结果与文献报道的结果相似。Yang等[21]利用水稻土和潮土进行Cr(Ⅵ)老化实验显示,有效态Cr(Ⅵ)分别在30 d和80 d左右达到平衡。Stewart等[31]研究显示,有效态Cr(Ⅵ)约在100 d左右在土壤中达到平衡。逐步回归分析结果表明,土壤pH值和有机质(OM)含量是影响Cr(Ⅵ)在不同土壤中近似老化平衡时间的主控因子(公式8)。

|
(8) |
式中:T为近似老化平衡时间,d;pH为土壤pH值;OM为土壤有机质含量,mg·kg-1。
|
图 3 老化第180、360 d时有效态Cr(Ⅵ)浓度(Q180、Q360)与平衡时有效态Cr(Ⅵ)浓度(Qe)的比较 Figure 3 Comparison of available Cr (Ⅵ)at 180 d, 360 d (Q180, Q360)with those at equilibrium(Qe) |
|
|
表 4 Cr(Ⅵ)在不同土壤中近似老化平衡时间(d) Table 4 Approximate aging equilibrium time of Cr(Ⅵ)in different soils (d) |
由公式(8)可以看出,Cr(Ⅵ)的近似老化平衡时间与土壤pH值呈正相关,说明酸性土壤中外源Cr(Ⅵ)达到平衡状态所需的时间比碱性土壤短。例如,S2和S11二者有机质含量近似相等(21.88 mg·kg-1和21.63 mg·kg-1),而pH差异显著(5.29和8.39),二者的近似老化平衡时间存在较大差异(6 d和51 d)。土壤有机质含量与土壤中Cr(Ⅵ)的近似老化平衡时间呈负相关,说明土壤有机质可以加速Cr(Ⅵ)的老化。有机质是土壤的重要组成部分,影响着土壤中重金属的有效性[45]。Chiu[24]通过XANES的光谱分析,发现有机质降低Cr(Ⅵ)有效性的主要原因是促进Cr(Ⅵ)还原为Cr(Ⅲ)。土壤有机质通过两种途径影响Cr(Ⅵ)的还原。首先,有机质可以作为电子供体,促进Cr(Ⅵ)还原为Cr(Ⅲ)。其次,有机质可以刺激某些具有Cr(Ⅵ)还原能力的微生物繁殖,从而促进Cr(Ⅵ)的生物还原[46]。因此,与pH值较高、有机质含量较低的土壤(S12,pH=8.89,有机质含量为3.31 mg·kg-1)相比,在S2和S4这两个pH值较低(5.29和6.6)而有机质含量较高(21.88 mg·kg-1和27.61 mg·kg-1)的土壤中,Cr(Ⅵ)更易固定和转化,因而Cr(Ⅵ)在这两个土壤中的近似老化平衡时间较短。
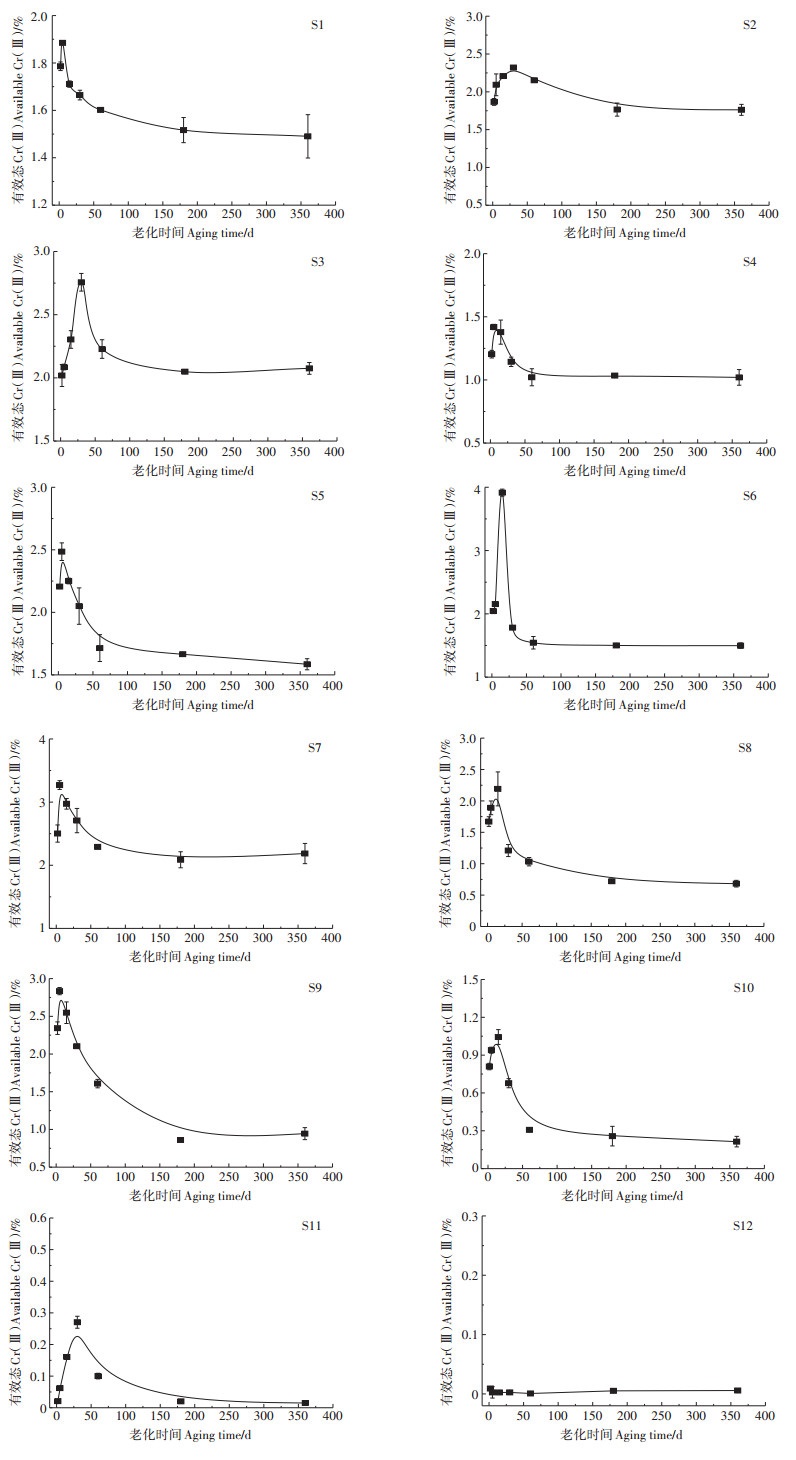
2.3 老化过程中Cr(Ⅲ)的变化与二价阳离子型重金属不同,Cr(Ⅵ)的还原可能对老化过程中有效态Cr(Ⅵ)的降低起着重要作用[23]。为了更好地了解土壤中Cr(Ⅵ)的老化过程,对还原产生的有效态Cr(Ⅲ)做了进一步分析(图 4)。从老化第2 d到老化第30 d,有效态Cr(Ⅲ)从0.02%(S11)~ 2.5%(S7)迅速增加到0.27%(S11)~3.91%(S5),达到峰值后,有效态Cr(Ⅲ)随老化时间的延长而下降,最终在60~180 d到达平衡(平衡浓度范围0.01%~2.19%)。12种土壤在实验过程中没有外源添加Cr(Ⅲ),因此Cr(Ⅵ)的还原是这些土壤中Cr(Ⅲ)增加的唯一原因。土壤中有效态Cr(Ⅲ)的动态过程可能受到Cr(Ⅵ)的还原和Cr(Ⅲ)自身的老化这两个过程的影响[21]。在有效态Cr(Ⅲ)迅速增加阶段,尽管表面沉淀和有机质络合作用可迅速降低有效态Cr(Ⅲ)的含量[47],但是土壤中各种还原性物质如Fe(Ⅱ)和有机质可使还原产生Cr(Ⅲ)的速率大于其老化速率[21],使得有效态Cr(Ⅲ)逐渐增加;随着时间的推移,Cr(Ⅲ)逐渐被自身的老化过程所消耗,还原反应产生Cr(Ⅲ)的速率减慢,而微孔扩散在老化过程中的作用逐步明显[48],从而使土壤中有效态Cr(Ⅲ)逐步降低,最终达到稳定状态。添加Cr(Ⅵ)土壤中,还原产生的Cr(Ⅲ)的老化过程,除了涉及到吸附、沉淀、有机质络合和微孔扩散等过程外,还涉及到氧化还原过程[21],其机理性老化模型的构建,还需要进一步研究。
|
误差线代表平行分析的标准误差 Error bars represent the standard error of duplicate analysis 图 4 老化过程中有效态Cr(Ⅲ)变化趋势 Figure 4 Change of available Cr (Ⅲ)during the aging process |
此外,在360 d的整个老化过程中,S12中只有少部分的有效态Cr(Ⅲ)(0.05%~0.09%)。其原因可能有两个方面。一方面,S12的pH值在12个土壤中最高,高pH值会使吸附到有机质和铁氧化物的Cr(Ⅵ)非常有限,从而不利于Cr(Ⅵ)的还原[38],即使有少量被还原,Cr(Ⅲ)也是以活性较低的Cr(OH)3沉淀形式存在[49]。另一方面,S12中无定形Fe(0.21 g·kg-1)和有机质含量(3.31 mg·kg-1)较低,不利于Cr(Ⅵ)向Cr(Ⅲ)的转化。
3 结论(1)外源Cr(Ⅵ)进入土壤后,有效态Cr(Ⅵ)在60 d之内迅速下降,之后趋势变缓,最终趋于稳定。二级动力学模型可以较好地拟合Cr(Ⅵ)在我国12种典型农田土壤中的老化过程。
(2)土壤性质显著影响Cr(Ⅵ)的老化速率和平衡时间。pH值是控制Cr(Ⅵ)老化速率的主控因子;pH值和有机质含量是控制Cr(Ⅵ)近似老化平衡时间的主控因子。
(3)在Cr(Ⅵ)老化过程中,还原产生的有效态Cr(Ⅲ)在初始阶段迅速增加,然后逐渐减小并趋于稳定,这可能是Cr(Ⅵ)的还原与老化和Cr(Ⅲ)自身老化共同作用的结果。
| [1] |
Xiao W D, Zhang Y B, Li T Q, et al. Reduction kinetics of hexavalent chromium in soils and its correlation with soil properties[J]. Journal of Environmental Quality, 2012, 41(5): 1452-1458. DOI:10.2134/jeq2012.0061 |
| [2] |
Li X Y, Zhang J R, Ma J, et al. Status of chromium accumulation in agricultural soils across China(1989-2016)[J]. Chemosphere, 2020, 256. |
| [3] |
Ashraf A, Bibi I, Niazi N K, et al. Chromium(Ⅵ) sorption efficiency of acid-activated banana peel over organo-montmorillonite in aqueous solutions[J]. International Journal of Phytoremediation, 2017, 13(1): 1-32. |
| [4] |
Zayed A M, Terry N. Chromium in the environment:Factors affecting biological remediation[J]. Plant & Soil, 2003, 249(1): 139-156. |
| [5] |
Papassiopi N, Kontoyianni A, Vaxevanidou K, et al. Assessment of chromium biostabilization in contaminated soils using standard leaching and sequential extraction techniques[J]. Science of the Total Environment, 2009, 407(2): 925-936. DOI:10.1016/j.scitotenv.2008.09.020 |
| [6] |
Bai J, Xun P, Morris S, et al. Chromium exposure and incidence of metabolic syndrome among American young adults over a 23-year followup:The CARDIA trace element study[J]. Scientific Reports, 2015(5): 1560-1566. |
| [7] |
Shahid M, Shamshad S, Rafiq M, et al. Chromium speciation, bioavailability, uptake, toxicity and detoxification in soil-plant system:A review[J]. Chemosphere, 2017, 178: 513-533. DOI:10.1016/j.chemosphere.2017.03.074 |
| [8] |
Antoniadis V, Polyzois T, Golia E E, et al. Hexavalent chromium availability and phytoremediation potential of Cichorium spinosum as affect by manure, zeolite and soil ageing[J]. Chemosphere, 2017, 171: 729-734. DOI:10.1016/j.chemosphere.2016.11.146 |
| [9] |
Zhang X, Tong J, Hu B X, et al. Adsorption and desorption for dynamics transport of hexavalent chromium(Cr(Ⅵ))in soil column[J]. Environmental Science & Pollution Research International, 2018, 25(1): 459-468. |
| [10] |
于修乐, 马义兵, 孙宗全, 等. 土壤中Cr(Ⅵ)和Cr(Ⅲ)生态毒性的差异性研究[J]. 农业环境科学学报, 2018, 37(11): 2522-2531. YU Xiu-yue, MA Yi-bing, SUN Zong-quan, et al. Study on ecotoxicity differences of Cr(Ⅵ)and Cr(Ⅲ)in soils[J]. Journal of Agro-Environmental Science, 2018, 37(11): 2522-2531. DOI:10.11654/jaes.2018-0946 |
| [11] |
Li S W, Li H L, Han X M, et al. Development and validation of a model for whole course aging of nickel added to a wide range of soils using a complementary error function[J]. Geoderma, 2019(348): 54-59. |
| [12] |
Zhang X, Zeng S Q, Chen S B, et al. Change of the extractability of cadmium added to different soils:Aging effect and modeling[J]. Sustainability, 2018, 10(3): 885-899. DOI:10.3390/su10030885 |
| [13] |
郑顺安, 郑向群, 李晓辰, 等. 外源Cr (Ⅲ)在我国22种典型土壤中的老化特征及关键影响因子研究[J]. 环境科学, 2013, 34(2): 698-704. ZHENG Shun-an, ZHENG Xiang-qun, LI Xiao-cheng, et al. Aging process of Cr(Ⅲ) in 22 typical soils of China and influence factors[J]. Environmental Sciences, 2013, 34(2): 698-704. |
| [14] |
Stewart M A, Jardine P M, Brandt C C, et al. Effects of contaminant concentration, aging, and soil properties on the bioaccessibility of Cr(Ⅲ) and Cr (Ⅵ)in soil[J]. Journal of Soil Contamination, 2003, 12(1): 1-21. DOI:10.1080/713610958 |
| [15] |
Perez C, Antelo J, Fiol S, et al. Modeling oxyanion adsorption on ferralic soil, part 2:Chromate, selenate, molybdate, and arsenate adsorption[J]. Environmental Toxicology & Chemistry, 2014, 33(10): 2217-2224. |
| [16] |
Lee D Y, Shih Y N, Zheng H C, et al. Using the selective ion exchange resin extraction and XANES methods to evaluate the effect of compost amendments on soil chromium(Ⅵ)phytotoxicity[J]. Plant and Soil, 2006, 281(1/2): 87-96. |
| [17] |
陈世宝, 陈莉, 马义兵, 等. 同位素技术在测定土壤重金属E、L-值中的应用及研究进展[J]. 农业环境科学学报, 2008, 27(6): 2131-2136. CHEN Shi-bao, CHEN Li, MA Yi-bing, et al. Application of isotopic dilution techniques in E, L-values measurement of heavy metal in soils and its research[J]. Journal of Agro-Environmental Science, 2008, 27(6): 2131-2136. DOI:10.3321/j.issn:1672-2043.2008.06.002 |
| [18] |
Ma Y B, Lombi E, Oliver I, et al. Long-term aging of copper added to soils[J]. Environmental Science & Technology, 2006, 40(20): 6310-6317. |
| [19] |
Zhang X, Jiang B, Ma Y. Aging of zinc added to soils with a wide range of different properties:Factors and modeling[J]. Environmental Toxicology & Chemistry, 2017, 36(11): 2925-2933. |
| [20] |
Jardine P M, Stewart M A, Barnett M O, et al. Influence of soil geochemical and physical properties on chromium(Ⅵ) sorption and bioaccessibility[J]. Environmental Science & Technology, 2013, 47(19): 11241-11248. |
| [21] |
Yang Y, Peng Y, Yang Z, et al. The kinetics of aging and reducing processes of Cr (Ⅵ) in two soils[J]. Bulletin of Environmental Contamination and Toxicology, 2019, 12(6): 45-51. |
| [22] |
Laing G D. Analysis and fractionation of trace elements in soils[M]//Trace Elements in Soils. Hoboken: Wiley, 2010.
|
| [23] |
Pueyo M, López-Sánchez J F, Rauret G. Assessment of CaCl2, NaNO3 and NH4NO3 extraction procedures for the study of Cd, Cu, Pb and Zn extractability in contaminated soils[J]. Analytica Chimica Academic Journal, 2004, 504(2): 217-226. DOI:10.1016/j.aca.2003.10.047 |
| [24] |
Chiu C C, Cheng C J, Lin T H, et al. The effectiveness of four organic matter amendments for decreasing resin-extractable Cr(Ⅵ) in Cr(Ⅵ)-contaminated soils[J]. Journal of Hazardous Materials, 2009, 161(2/3): 1239-1244. |
| [25] |
Zhu G Y, Jiang B, Yang G H, et al. Toxicity thresholds based on EDTA extractable nickel and barley root elongation in Chinese soils[J]. International Journal of Environmental Research & Public Health, 2018, 15(4): 669-675. |
| [26] |
Manouchehri N, Besancon S, Bermond A. Major and trace metal extraction from soil by EDTA:Equilibrium and kinetic studies[J]. Analytica Chimica Academic Journal, 2006, 559(1): 105-112. DOI:10.1016/j.aca.2005.11.050 |
| [27] |
Quevauviller P. Operationally-defined extraction procedures for soil and sediment analysis. Part 3:New CRMs f or trace-element extractable contents[J]. Trace Trends in Analytical Chemistry, 2002, 21(11): 774-785. DOI:10.1016/S0165-9936(02)01105-6 |
| [28] |
Wang Y N, Zeng X B, Liu Y H, et al. Dynamic arsenic aging processes and their mechanisms in nine types of Chinese soils[J]. Chemosphere, 2017, 187(2): 404-412. |
| [29] |
Fabregat-Cabello N, Rodriguez-Gonzalez P, Castillo A, et al. Fast and accurate procedure for the determination of Cr(Ⅵ)in solid samples by isotope dilution mass spectrometry[J]. Environmental Science & Technology, 2012, 46(22): 12542-12549. |
| [30] |
McSheehy S, Nash M. 高效液相色谱与电感耦合等离子体质谱联用测定矿泉水中的三价铬与六价铬[J]. 环境化学, 2009, 28(4): 618-620. McSheehy S, Nash M. Determination of chromium(Ⅲ) and chromium(Ⅵ) in mineral water by high performance liquid chromatography coupled with inductively coupled plasma mass spectrometry[J]. Environmental Chemistry, 2009, 28(4): 618-620. DOI:10.3321/j.issn:0254-6108.2009.04.037 |
| [31] |
Stewart M A, Jardine P M, Brandt C C. Effects of contaminant concentration, aging, and soil properties on the bioaccessibility of Cr(Ⅲ) and Cr (Ⅵ)in soil[J]. Journal of Soil Contamination, 2003, 12(1): 37-41. |
| [32] |
Fendorf S E. Surface reactions of chromium in soils and waters[J]. Geoderma, 1995, 67(1/2): 55-71. |
| [33] |
Choppala G, Burton E D. Chromium(Ⅲ)substitution inhibits the Fe (Ⅱ)-accelerated transformation of schwertmannite[J]. PLoS One, 2018, 13(2): 342-364. |
| [34] |
Shi Z Q, Peng S M, Lin X F, et al. Predicting Cr(Ⅵ)adsorption on soils:The role of the competition of soil organic matter[J]. Environmental Science and Process Impacts, 2019, 22(1): 95-104. |
| [35] |
Zhu L, Fu F, Tang B. Three-dimensional transfer of Cr(Ⅵ)co-precipitated with ferrihydrite containing silicate and its redistribution and retention during aging[J]. Science of the Total Environment, 2019, 696(1): 1339-1366. |
| [36] |
Jardine P M, Fendorf S E, Mayes M A, et al. Fate and transport of hexavalent chromium in undisturbed heterogeneous soil[J]. Environmental Science & Technology, 1999, 33(17): 2939-2944. |
| [37] |
Choppala G, Kunhikrishnan A, Seshadri B, et al. Comparative sorption of chromium species as influenced by pH, surface charge and organic matter content in contaminated soils[J]. Journal of Geochemical Exploration, 2016(1): 255-260. |
| [38] |
Jardine P M, Stewart M A, Barnett M O, et al. Influence of soil geochemical and physical properties on chromium(Ⅵ)sorption and bioaccessibility[J]. Environmental Science & Technology, 2013, 47(19): 11241-11248. |
| [39] |
He T Y, Traina S J. Cr(Ⅵ)reduction and immobilization by magnetite under alkaline pH conditions:The role of passivation[J]. Environmental Science & Technology, 2005, 39(12): 4499-4504. |
| [40] |
Plazinski W, Dziuba J, Rudzinski W. Modeling of sorption kinetics:The pseudo-second order equation and the sorbate intraparticle diffusivity[J]. Adsorption-journal of the International Adsorption Society, 2013, 19(5): 1055-1064. DOI:10.1007/s10450-013-9529-0 |
| [41] |
徐明岗, 王宝奇, 周世伟, 等. 外源铜锌在我国典型土壤中的老化特征[J]. 环境科学, 2008, 29(11): 3213-3218. XU Ming-gang, WANG Bao-qi, ZHOU Shi-wei, et al. Aging characteristics of copper and zinc added to typical soils of China[J]. Environmental Science, 2008, 29(11): 3213-3218. DOI:10.3321/j.issn:0250-3301.2008.11.039 |
| [42] |
Li J, Peng Q, Liang D L, et al. Effects of aging on the fraction distribution and bioavailability of selenium in three different soils[J]. Chemosphere, 2016, 144: 2351-2359. DOI:10.1016/j.chemosphere.2015.11.011 |
| [43] |
Ajouyed O, Hurel C, Ammari M, et al. Sorption of Cr(Ⅵ) onto natural iron and aluminum(oxy) hydroxides:Effects of pH, ionic strength and initial concentration[J]. Journal of Hazardous Materials, 2010, 174(1/2/3): 616-622. |
| [44] |
蔡少华, 和文祥, 梁艳茹, 等. 土壤Cr (Ⅵ)与土壤生化活性关系研究[J]. 农业环境科学学报, 2009, 28(2): 251-255. CAI Shao-hua, HE Wen-xiang, LIANG Yan-ru, et al. The state of chromium(Ⅵ)in polluted soils and effect on soil urease activities[J]. Journal of AgroEnvironmental Science, 2009, 28(2): 251-255. DOI:10.3321/j.issn:1672-2043.2009.02.006 |
| [45] |
Lin X, Sun Z, Zhao L, et al. Toxicity of exogenous hexavalent chromium to soil-dwelling springtail Folsomia candida in relation to soil properties and aging time[J]. Chemosphere, 2019, 224: 734-742. DOI:10.1016/j.chemosphere.2019.02.196 |
| [46] |
Banks M K, Schwab A P, Henderson C. Leaching and reduction of chromium in soil as affected by soil organic content and plants[J]. Chemosphere, 2006, 62(2): 255-264. DOI:10.1016/j.chemosphere.2005.05.020 |
| [47] |
Sparks D L. Environmental soil chemistry: An overview[M]//Environmental Soil Chemistry. 2nd Edition. Salt Lake City: Academic Press, 2003: 1-42.
|
| [48] |
Alexander M. Aging, bioavailability, and overestimation of risk from environmental pollutants[J]. Environmental Science & Technology, 2000, 34(20): 4259-4265. |
| [49] |
Choppala G, Kunhikrishnan A, Seshadri B, et al. Comparative sorption of chromium species as influenced by pH, surface charge and organic matter content in contaminated soils[J]. Journal of Geochemical Exploration, 2016(1): 255-260. |
 2021, Vol. 40
2021, Vol. 40