近年来,抗生素作为一类新兴痕量污染物,在自然水体中的频繁检出引发了广泛关注。四环素作为世界上第二广泛使用的抗生素,因其良好的抗菌作用被广泛用于医疗、养殖[1-2]。与大多数抗生素一样,四环素不能完全被人和动物机体代谢,约有90%通过尿液排入到环境中进而造成耐药基因的出现以及传播等负面影响[3]。
吸附因其易于操作、成本低廉且无有毒副产物产生等优点被广泛用于水中抗生素的去除,常用的吸附剂有金属氧化物、黏土、活性炭、碳纳米管和生物炭等[4-8]。生物炭是利用生物质(秸秆、中药渣、废弃果皮、木屑等)热解而得的一类富碳物质,来源广泛、成本低廉,被认为是活性炭的潜在替代品[9-10]。我国秸秆资源丰富,年产量约在7.6亿t,资源化利用是其处理的发展趋势,但传统秸秆制备的生物炭吸附能力因其有限的孔道和比表面积受到限制[11]。
锰是一种典型的过渡金属,具有多种氧化物晶体形态,其氧化物与生物炭结合的复合材料被广泛应用于吸附。在热解过程中,锰氧化物可作为催化剂促进生物质的热解,改善生物炭的孔隙结构,提高生物炭的比表面积及孔容,增强其物理吸附作用[12]。此外,抗生素含有羟基、酮基、氨基等给电子基团,易与金属离子结合产生配合物,推测四环素中的二甲氨基可与锰氧化物发生络合反应从而达到吸附四环素的目的[13]。因此,使用锰氧化物改性生物炭可能会提高生物炭对四环素的吸附作用,但目前关于锰氧化物改性秸秆生物炭去除水中四环素的研究较少。
本研究以高粱秸秆为原料,通过金属浸渍制备改性生物炭,探讨锰氧化物改性生物炭(MBC)对四环素(TC)的吸附动力学、等温吸附、热力学以及影响因素(溶液pH、离子浓度、腐植酸)。研究结果可评价锰改性生物炭对水中四环素的强化吸附作用,为去除水中四环素以及秸秆的资源化利用提供参考。
1 材料与方法 1.1 试验试剂与仪器试剂:四环素(TC,C22H24N2O8,相对分子量为444.43,纯度大于98%,CAS号为60-54-8)购自上海阿拉丁有限公司,其他化学试剂均为分析纯,试验用水为四川优普UPR-11-10TN所制超纯水。
仪器:恒温振荡箱(THZ-100,上海一恒)、真空气氛马弗炉(KBF13Q,南京南大)、多功能粉碎机(Q-400B,上海冰都)、电热鼓风干燥箱(DHG-9140A,上海浦东)、紫外-可见分光光度计(UV-2600,日本岛津)。
1.2 材料制备及表征将秸秆剥皮、裁块,于烘箱中60 ℃干燥24 h,粉碎后过100目筛备用。取适量秸秆粉末放入坩埚,置于马弗炉中,限氧条件下以10 ℃∙min-1速率升至500 ℃,保持2 h冷却到室温取出,研磨后过100目筛,得到原始生物炭,记为BC。改性生物炭通过浸渍法制备,将2 g秸秆粉末浸渍于100 mL氯化锰溶液(0.5 mol∙L-1),搅拌2 h,抽滤分离,过夜干燥后于马弗炉中高温煅烧(条件与BC相同),记为MBC。
利用N2吸附比表面积法(BET,ASAP2010)测定材料的表面积及孔容。通过X射线衍射分析仪(XRD,ESCALAB250Xi)分析材料的晶体结构。使用傅里叶红外光谱分析仪(FTIR,Nicolet iS50)对比改性前后材料表面的官能团变化。采用扫描电镜(SEM,Sigma 500)和能谱仪(EDS,Xflash6130)扫描改性前后材料的表面形貌和元素成分。
1.3 吸附试验为避免光解对试验的影响,吸附试验于恒温振荡箱以25 ℃、180 r·min-1为条件进行。吸附动力学试验时,将10 mg吸附剂与30 mL TC溶液(C0 =20 mg∙L-1,pH=7)混合,在不同时间下取样过0.45 μm滤膜后,采用紫外分光光度计在λ=360 nm处测定TC的浓度。等温吸附试验中,将10 mg吸附剂置于不同浓度(10、20、35、50、75、100、150、200、300、500 mg∙L-1)TC溶液中,分别在15、25 ℃和35 ℃条件下恒温吸附12 h。pH影响试验中,通过0.1 mol∙L-1HCl或NaOH溶液调节溶液初始pH为3~11,振荡12 h,其余条件与动力学试验相同。离子浓度影响试验中,控制溶液中离子(K+、Na+、Ca2+和Mg2+)浓度分别为0、5、10、20、40、80 mmol·L-1,振荡12 h,其余条件与吸附动力学试验相同。腐植酸(HA)影响试验中,控制HA的浓度分别为0、10、20、30、40、50 mg∙L-1,振荡12 h,其余条件与吸附动力学试验相同。以上试验每组均设置2个平行,取平均值。
1.4 数据处理与分析 1.4.1 去除效能生物炭及改性生物炭对水溶液TC的吸附容量可用下式计算:
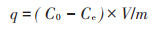
|
(1) |
式中:q为吸附容量,mg·g-1;C0和Ce分别为初始质量浓度和平衡质量浓度,mg·L-1;V为溶液体积,mL;m为吸附剂添加量,mg。
1.4.2 吸附动力学利用准一级动力学、准二级动力学模型和颗粒扩散模型拟合改性前后生物炭对TC的吸附过程,公式分别如下:
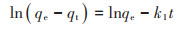
|
(3) |
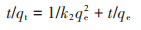
|
(4) |
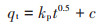
|
(5) |
式中:qe为吸附平衡时的吸附容量,mg·g-1;qt为t(h)时刻的吸附容量,mg·g-1;k1为准一级动力学速率常数,h-1,k2为准二级动力学速率常数,g·mg-1·h-1;kp为颗粒内扩散模型的速率常数,mg·g-1·h 0.5;c为反映边际层效应,mg·g-1。
1.4.3 等温吸附采用Langmuir模型和Freundlich模型拟合改性前后生物炭在四环素溶液中的等温吸附过程。Lang⁃ muir模型和Freundlich模型分别如下:
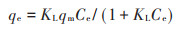
|
(6) |

|
(7) |
式中:qe为吸附平衡时的吸附容量,mg·g-1;qm为吸附剂理论饱和吸附量,mg·g-1;Ce为吸附平衡时的浓度,mg·L-1;KL为Langmuir常数,mg·L-1;Kf为Freundlich常数,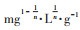
通过计算热力学参数从而确定吸附过程中的能量变化,判断吸附行为是否为自发过程。

|
(8) |
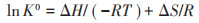
|
(9) |
式中:ΔG为吉布斯自由能变,kJ·mol-1;ΔH为焓变,kJ·mol-1;ΔS为熵变,J·mol-1·K-1;R为气体常数,其值为8.314 J·mol-1·K-1;T为反应体系的热力学温度,K;K0为吸附质在固液两相中的分配系数,通过ln(qe /Ce)对qe作图,求得截距即获得不同温度下的K0值。
1.4.5 差异显著性分析为探讨影响因素(pH、共存离子、HA)对吸附的影响,采用SPSS软件对试验数据进行了单因素差异显著性分析。若二者对应字母相同则说明二者影响无显著差异,字母不同表明二者影响存在显著差异。
2 结果与讨论 2.1 材料表征结果分析 2.1.1 BET表征结果BET结果表明,MBC的比表面积和孔容分别为301.61 m2∙g-1和0.22 cm3∙g-1,与BC(164.78 m2∙g-1和0.11 cm3∙g-1)相比,比表面积和孔容都增大了约1倍。一方面是因为锰氧化物在碳化过程中促进了生物质的热解,致使孔道数量增多,比表面积和孔容增大;另一方面是锰氧化物生成并附着在生物炭表面,使表面更粗糙,增加了外比表面积。比表面积和孔容的增加提供了更多的吸附位点,有利于吸附。
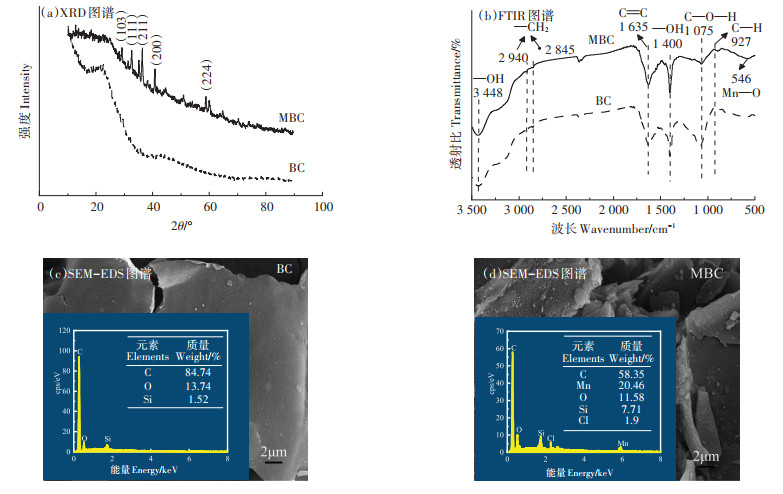
2.1.2 XRD表征结果图 1(a)为MBC和BC的广角XRD谱图。在MBC的谱图中可以清晰地观察到锰氧化物的特征峰,35.2°和40.9°处的衍射峰分别属于MnO(JCPDS. NO.75-0257)的(111)和(200)晶面,而32.4°、36.1°和59.9°对应的是Mn3O4(JCPDS.NO.80-0382)的(103)(211)和(224)晶面衍射峰,表明锰氧化物成功负载到了生物炭上。此外,改性前存在明显石墨的特征峰(2θ =22.5°),改性后有所削弱,说明锰氧化物的引入对石墨晶体的有序性有一定的影响。
|
图 1 MBC与BC的微观表征结果 Figure 1 The character of the MBC and BC |
MBC和BC的红外光谱如图 1(b)所示,3 448 cm-1处较宽的峰和1 400 cm-1处的尖峰对应—OH伸缩振动峰,1 500 cm-1到1 700 cm-1区间的吸收峰则对应C=O和C=C的伸缩振动峰,1 075 cm-1附近为C—O—H的振动吸收峰[14]。与BC相比,经MnCl 2改性的MBC在1 075 cm-1处的特征峰强度变弱,这可能是因为在改性过程中,Mn2+与生物炭表面的C—O—H络合形成络合物,经高温煅烧后变为锰氧化物。在MBC的光谱图中也观察到了Mn—O的特征峰(546 cm-1),证实了锰氧化物的存在。
2.1.4 SEM-EDS表征结果为进一步分析材料的微观形貌和锰氧化物的分布情况,通过SEM-EDS对样品进行观察,结果见图 1(c)和图 1(d)。BC的表面较光滑,而MBC表面粗糙,且存在许多小颗粒,可能是由于锰氧化物覆盖或嵌入生物炭造成的形貌变化。MBC的粗糙表面会增加材料的比表面积及吸附位点,对TC的吸附有利。EDS可描述材料表面元素的含量分布情况,对比可知,改性后的样品中的锰元素含量从0增加到20.46%,进一步证实了锰氧化物的存在。锰氧化物的存在为锰与TC通过配位作用进行吸附提供了可能。
2.2 吸附动力学BC和MBC对TC的吸附量随时间变化以及动力学拟合见图 2(a)。两种生物炭的TC吸附量在前2 h内快速增加,之后增速放缓趋于平稳,在4 h后基本达到平衡。快速吸附阶段是因为吸附剂表面可接触的位点被快速占据,而后吸附位点逐渐减少,表面吸附接近饱和,分子向内部迁移,吸附速率放缓,吸附趋于稳定。从图中可以看出,MBC对TC的平衡吸附量为37 mg∙g-1,远高于BC(8 mg∙g-1),这是因为锰氧化物改性改善了材料的孔道结构和增多了材料表面的吸附位点。

|
图 2 TC在MBC和BC上的吸附动力学 Figure 2 Kinetics of TC adsorption onto MBC and BC |
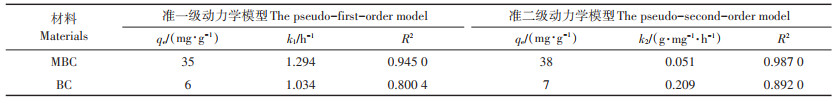
为解释吸附机制,采用准一级动力学和准二级动力学对试验数据进行拟合,参数拟合结果见表 1。准二级动力学模型关于两种生物炭(MBC和BC)对TC吸附行为的拟合度(R2)分别为0.987 0和0.892 0,均高于同等条件下准一级动力学的拟合相关度(0.945 0和0.800 4),故准二级动力学模型更适合描述改性前后的生物炭对TC的吸附行为。通常,准二级动力学可以描述膜扩散、表面吸附等过程中的孔径填充、共价键(配位键)形成,电子交换等物理化学作用,可见生物炭的吸附过程受控于物理化学吸附[15]。
|
|
表 1 MBC和BC吸附TC的吸附动力学参数 Table 1 Kinetics parameters for TC adsorption on MBC and BC |
采用颗粒内扩散模型进一步探讨四环素在BC和MBC上的吸附机理和限速步骤,结果见图 2(b)。吸附过程较为复杂,可分为2到3个阶段,其中第一阶段是膜扩散,描述了吸附质迅速扩散到吸附剂的边界面,而第2、3阶段是颗粒内扩散阶段。此外,第一阶段直线不过原点说明颗粒扩散不是唯一的限速步骤[16]。
2.3 等温吸附吸附等温线被广泛用于描述吸附容量和平衡浓度之间的关系,以及吸附分子在吸附剂上的分布,而且有助于揭示吸附特性。本研究选用Langmuir和Freundlich模型来评价生物炭(BC和MBC)对TC的等温吸附特性,其中Langmuir模型是基于吸附剂表面活性位点均匀分布、吸附质在吸附剂表面形成单层吸附的假设而得到的,而Freundlich模型是一个经验公式,主要用于描述发生在非均相固体表面的吸附过程[17]。
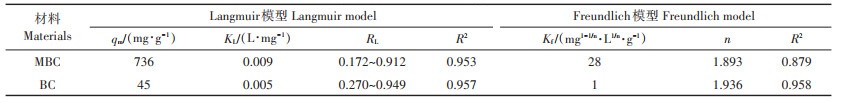
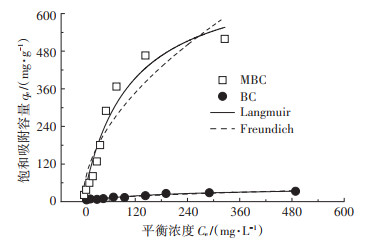
试验拟合结果见图 3和表 2。相较于Freundlich模型,Langmuir模型能更好地拟合等温吸附数据,这说明吸附剂是均质表面,吸附剂表面的吸附位点均匀分布,吸附更接近于单分子层吸附。Langmuir拟合结果显示,MBC的吸附能力和亲和力分别为736 mg-1∙ g-1和0.009 L∙mg-1,远高于原始生物炭45 mg-1∙g-1和0.005 L∙mg-1,锰氧化物改性提高了生物炭对TC的吸附能力和亲和力。这是因为改性增加了比表面积和孔容,提高了孔径填充等物理吸附能力。此外,锰氧化物可以与有机物上的羧基、氨基等官能团相互作用形成配合物,所以可促进MBC对TC的吸附。本研究制备的MBC对水中TC的qm高达736 mg∙g-1,高于TC在NaOH活化的生物炭(456 mg∙g-1)[3]、多壁碳纳米管修饰的金属有机框架(364 mg∙g-1)[18]、活性炭(251 mg∙g-1)[19]。此外,Freundlich模型中1/n值小于1,表明吸附易于发生[20-21]。因此,MBC去除水中TC具有潜在的应用前景。
|
图 3 TC在MBC和BC的等温吸附 Figure 3 Isotherms of TC adsorption on the BC and MBC |
|
|
表 2 MBC和BC吸附TC的吸附等温参数 Table 2 Isotherm parameters for TC adsorption on MBC and BC |
MBC对不同质量浓度TC溶液分别在15、25 ℃和35 ℃条件下的等温吸附数据见图 4。随着温度的升高,MBC对TC的吸附容量也随之增大。为进一步评价温度对MBC吸附TC的影响,利用吉布斯自由能方程计算吸附过程中的标准自由能变(ΔG)、标准焓变(ΔH)以及标准熵变(ΔS),从能量变化的角度解释温度对于吸附过程的影响,计算结果见表 3。ΔG为负表示吸附是一个自发的过程,ΔH为正表明吸附是一个典型的吸热过程,温度的升高有利于吸附的进行,与试验结果相符。而ΔS为正是因为在溶液中吸附剂和吸附质都被水化层包裹,水分子有序排列,而当吸附发生时,吸附剂与吸附质接触,两种水化层之间的水分子被迫打乱,从而造成熵的增加,固液间自由能增加,使吸附过程趋于稳定[19]。

|
图 4 TC在MBC和BC的等温吸附 Figure 4 Isotherms of TC adsorption on the BC and MBC |
|
|
表 3 MBC吸附TC的热力学参数 Table 3 Thermodynamic parameters for TC adsorption on MBC |
通常热力学参数值与吸附作用力相对应(表 4),可通过其大小判断吸附过程中存在的作用力[22]。对比可知,MBC对TC的吸附(ΔH = 34.96kJ∙mol-1)是由氢键作用和配位作用共同驱动的。
|
|
表 4 热力学参数对应的吸附作用力 Table 4 Thermodynamic parameters for adsorption types |
溶液的pH值对吸附过程至关重要,不仅会改变生物炭表面电荷,还会影响TC在水中的存在形态,从而影响生物炭对TC的吸附。TC是典型的两性分子,能以阳离子(pH < 3.3)、两性离子(3.3 < pH < 7.7)以及阴离子(pH>7.7)形态存在于溶液中[23]。
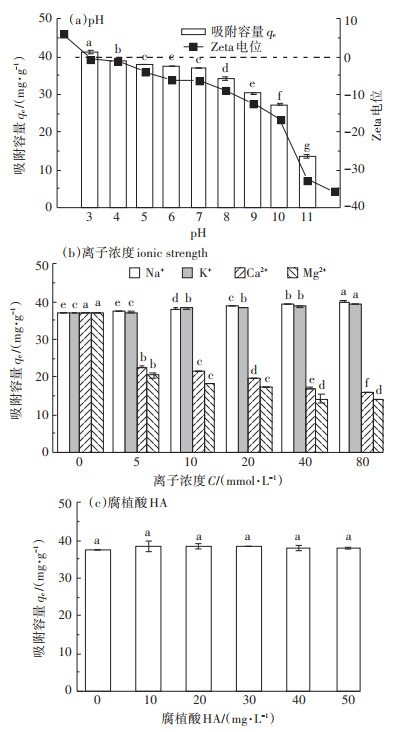
图 5(a)是溶液pH值在3.0 ~ 11.0时,MBC对TC的吸附情况。当pH在3.0~7.0范围内变化时,MBC对TC的吸附情况变化不大,而随着pH进一步增大到11时,吸附容量明显下降。酸性、中性以及弱碱性条件下可以有效去除水中的TC,说明MBC具有较广pH适应范围。Zeta电位结果表明,pH在3 ~ 11范围内,MBC表面带负电,所以MBC对TC的吸附情况主要随TC形态变化而变化。当pH < 3.3时,TC主要以阳离子形态存在,此时污染物与吸附剂之间的静电吸引增强,促进了吸附。当pH从3增大到7时,TC逐渐向两性分子转变,静电吸引作用逐渐减弱。随着溶液pH进一步增大到碱性时,TC主要以阴离子形态存在,MBC表面含氧基团进一步电离,负电荷密度增大,静电排斥作用增强,且阳离子-π和π-π作用减弱,导致MBC吸附TC能力下降[24-25]。MBC对TC的吸附受pH影响表明静电作用是影响吸附的一个重要作用。
|
不同字母代表处理间差异显著 Different letters indicate significant differences among treatments 图 5 水环境对MBC吸附TC的影响 Figure 5 Effects of solution quality on TC adsorption on MBC |
图 5(b)展示了4种常见阳离子(K+、Na+、Ca2+和Mg2+)在不同浓度下对MBC吸附TC的影响。当离子浓度从1 mmol·L-1增大到80 mmol·L-1时,K+和Na+对MBC吸附TC有轻微的促进作用,一方面可归结于盐析作用,当盐离子浓度增大时,导致TC溶解度降低,有利于MBC对TC的吸附;另一方面,根据研究报道,非静电力可以抵消部分静电斥力,从而增加吸附容量[26]。但二价阳离子Ca2+和Mg2+却表现出明显的抑制作用,一方面是因为Ca2+和Mg2+电荷数更高,与带负电的MBC的结合力远大于K+和Na+,而吸附到材料上的Ca2+和Mg2+与水分子结合,产生水化层,抑制MBC与TC间的接触及吸附[15, 27]。另一方面是因为Ca2+和Mg2+可与TC结合,占据TC的可吸附位点。与Ca2+相比,Mg2+的半径更小,对水分子的吸引力更强,产生的水化层更厚,且在中性条件下,Mg2+可与更多的TC结合,占据吸附位点更多,所以对吸附的抑制作用大于Ca2+[28]。共存离子的影响表明吸附位点对于吸附至关重要,吸附位点的竞争与阻隔会严重抑制MBC吸附TC。
2.7 腐植酸对吸附的影响有研究指出,水中70%的天然有机物(NOM)是由腐植酸(HA)构成的[29],因此本研究以HA为代表来考察NOM对MBC吸附TC的影响,结果如图 5(c)所示。当HA浓度从0增大到50 mg∙L-1时,MBC对TC的吸附去除没有明显变化,可能与HA的分子大小有关,HA的分子尺寸较大,而本研究制备的MBC的平均孔径为2.58 nm,HA几乎不能进入到MBC的内部孔道与TC竞争MBC内部的吸附位点。试验结果表明,HA对MBC吸附TC的影响并不显著,说明MBC可通过孔径筛分阻碍HA进入孔道内部,削弱HA对吸附的抑制作用。因此,在实际应用中,MBC可以削弱水中HA对吸附的干扰。
3 结论(1)TC在MBC上的吸附行为符合准二级动力学模型,吸附过程受物理化学过程控制,4 h基本达到吸附平衡。等温吸附符合Langmuir模型,pH=7、T=298 K时,理论吸附容量为736 mg∙g-1,是BC的15倍。热力学分析表明该吸附过程是一个自发、吸热的过程,且由氢键作用及锰与四环素间的配位作用共同驱动。
(2)与BC相比,MBC的吸附容量大幅提升,这是源于二者比表面积、孔隙结构以及组成成分的差异。MBC的比表面积更大、孔隙结构更发达,可以提供更多的吸附位点。此外,MBC上负载的锰氧化物可以通过配位作用与TC结合,有利于吸附。
(3)MBC可适应pH变化,在酸性、中性以及弱碱性条件下对TC均有良好的去除效果,而且具有较强的抗腐植酸能力,是一种去除水中抗生素的潜在的高效吸附剂。
| [1] |
Cao J, Lai L, Lai B, et al. Degradation of tetracycline by peroxymonosulfate activated with zero-valent iron:Performance, intermediates, toxicity and mechanism[J]. Chemical Engineering Journal, 2019, 364: 45-56. DOI:10.1016/j.cej.2019.01.113 |
| [2] |
Zhang P, Li Y, Cao Y, et al. Characteristics of tetracycline adsorption by cow manure biochar prepared at different pyrolysis temperatures[J]. Bioresource Technology, 2019, 285: 121348. DOI:10.1016/j.biortech.2019.121348 |
| [3] |
Martins A C, Pezoti O, Cazetta A L, et al. Removal of tetracycline by NaOH-activated carbon produced from macadamia nut shells:Kinetic and equilibrium studies[J]. Chemical Engineering Journal, 2015, 260: 291-299. DOI:10.1016/j.cej.2014.09.017 |
| [4] |
Ahmed M B, Zhou J L, Ngo H H, et al. Adsorptive removal of antibiotics from water and wastewater:Progress and challenges[J]. Science of the Total Environment, 2015, 532: 112-126. DOI:10.1016/j.scitotenv.2015.05.130 |
| [5] |
Yu F, Li Y, Han S, et al. Adsorptive removal of antibiotics from aqueous solution using carbon materials[J]. Chemosphere, 2016, 153: 365-385. DOI:10.1016/j.chemosphere.2016.03.083 |
| [6] |
Peiris C, Gunatilake S R, Mlsna T E, et al. Biochar based removal of antibiotic sulfonamides and tetracyclines in aquatic environments:A critical review[J]. Bioresource Technology, 2017, 246: 150-159. DOI:10.1016/j.biortech.2017.07.150 |
| [7] |
Zusman O B, Kummel M L, De la Rosa J M, et al. Dissolved organic matter adsorption from surface waters by granular composites versus granular activated carbon columns:An applicable approach[J]. Water Research, 2020, 181: 115920. DOI:10.1016/j.watres.2020.115920 |
| [8] |
Xia L, Lu Y, Meng H, et al. Preparation of C-MOx nanocomposite for efficient adsorption of heavy metal ions via mechanochemical reaction of CaC2 and transitional metal oxidesden[J]. Journal of Hazardous Materials, 2020, 393: 122487. DOI:10.1016/j.jhazmat.2020.122487 |
| [9] |
朱银涛, 李业东, 王明玉, 等. 玉米秸秆碱化处理制备的生物炭吸附锌的特性研究[J]. 农业环境科学学报, 2018, 37(1): 179-185. ZHU Yin-tao, LI Ye-dong, WANG Ming-yu, et al. Adsorption characteristics of biochar prepared by corn stalk alkalization on zinc[J]. Journal of Agro-Environment Science, 2018, 37(1): 179-185. |
| [10] |
Yang H, Ye S, Zeng Z, et al. Utilization of biochar for resource recovery from water:A review[J]. Chemical Engineering Journal, 2020, 397: 125502. DOI:10.1016/j.cej.2020.125502 |
| [11] |
李林璇, 廖云开, 范世锁. 改性秸秆-Fe3O4复合材料对染料废水中亚甲基蓝的去除研究[J]. 农业环境科学学报, 2019, 38(5): 1130-1141. LI Lin-xuan, LIAO Yun-kai, FAN Shi-suo. Removal of methylene blue in aqueous solution by citric acid-modified rice straw loaded with Fe3O4 composite[J]. Journal of Agro-Environment Science, 2019, 38(5): 1130-1141. |
| [12] |
Premarathna K S D, Rajapaksha A U, Sarkar B, et al. Biochar-based engineered composites for sorptive decontamination of water:A review[J]. Chemical Engineering Journal, 2019, 372: 536-550. DOI:10.1016/j.cej.2019.04.097 |
| [13] |
Zhu S, Wu Y, Qu Z, et al. Green synthesis of magnetic sodalite sphere by using groundwater treatment sludge for tetracycline adsorption[J]. Journal of Cleaner Production, 2020, 247: 119140. DOI:10.1016/j.jclepro.2019.119140 |
| [14] |
Ma J, Jiang Z, Cao J, et al. Enhanced adsorption for the removal of antibiotics by carbon nanotubes/graphene oxide/sodium alginate triplenetwork nanocomposite hydrogels in aqueous solutions[J]. Chemosphere, 2020, 242: 125188. DOI:10.1016/j.chemosphere.2019.125188 |
| [15] |
Liu S, Xu W, Liu Y, et al. Facile synthesis of Cu(Ⅱ)impregnated biochar with enhanced adsorption activity for the removal of doxycycline hydrochloride from water[J]. Science of the Total Environment, 2017, 592: 546-553. DOI:10.1016/j.scitotenv.2017.03.087 |
| [16] |
李蕊宁, 王兆炜, 郭家磊, 等. 酸碱改性生物炭对水中磺胺噻唑的吸附性能研究[J]. 环境科学学报, 2017, 37(11): 419-4128. LI Rui-ning, WANG Zhao-wei, GUO Jia-lei, et al. Adsorption characteristics of sulfathiazole in aqueous solution by acid/alkali modified biochars[J]. Acta Scientiae Circumstantiae, 2017, 37(11): 419-4128. |
| [17] |
Ji L L, Wang Y Q, Zheng S R, et al. Adsorption of tetracycline and sulfamethoxazole on crop residue-derived ashes:Implication for the relative importance of black carbon to soil sorption[J]. Environmental Science & Technology, 2011, 45(13): 5580-5586. |
| [18] |
Xiong W P, Guang M Z, Zhao H Y, et al. Adsorption of tetracycline antibiotics from aqueous solutions on nanocomposite multi-walled carbon nanotube functionalized MIL-53(Fe)as new adsorbent[J]. Science of the Total Environment, 2018, 627: 235-244. DOI:10.1016/j.scitotenv.2018.01.249 |
| [19] |
Zhou J, Ma F, Guo H. Adsorption behavior of tetracycline from aqueous solution on ferroferric oxide nanoparticles assisted powdered activated carbon[J]. Chemical Engineering Journal, 2020, 384: 123290. DOI:10.1016/j.cej.2019.123290 |
| [20] |
Eniola J O, Kumar R, Al-Rashdi A A, et al. Hydrothermal synthesis of structurally variable binary CuAl, MnAl and ternary CuMnAl hydroxides for oxytetracycline antibiotic adsorption[J]. Journal of Environmental Chemical Engineering, 2020, 28: 2213-3437. |
| [21] |
Cao D Q, Yang W Y, Wang Z, et al. Role of extracellular polymeric substance in adsorption of quinolone antibiotics by microbial cells in excess sludge[J]. Chemical Engineering Journal, 2019, 370: 684-694. DOI:10.1016/j.cej.2019.03.230 |
| [22] |
Lin R Y, Liang Z J, Yang C. Selective adsorption of organic pigments on inorganically modified mesoporous biochar and its mechanism based on molecular structure[J]. Journal of Colloid and Interface Science, 2020, 573: 21-30. DOI:10.1016/j.jcis.2020.03.112 |
| [23] |
Cao J, Xiong Z, Lai B. Effect of initial pH on the tetracycline(TC)removal by zero-valent iron:Adsorption, oxidation and reduction[J]. Chemical Engineering Journal, 2018, 343: 492-499. DOI:10.1016/j.cej.2018.03.036 |
| [24] |
Hu X, Zhang H, Sun Z. Adsorption of low concentration ceftazidime from aqueous solutions using impregnated activated carbon promoted by iron, copper and aluminum[J]. Applied Surface Science, 2017, 392: 332-341. DOI:10.1016/j.apsusc.2016.09.047 |
| [25] |
Yan L, Liu Y, Zhang Y, et al. ZnCl2 modified biochar derived from aerobic granular sludge for developed microporosity and enhanced adsorption to tetracycline[J]. Bioresource Technology, 2019, 297: 122381. |
| [26] |
Xiang Y, Yang X, Xu Z, et al. Fabrication of sustainable manganese ferrite modified biochar from vinasse for enhanced adsorption of fluoroquinolone antibiotics:Effects and mechanisms[J]. Science of the Total Environment, 2019, 709: 136079. |
| [27] |
Yang K, Chen B, Zhu X, et al. Aggregation, adsorption, and morphological transformation of graphene oxide in aqueous solutions containing different metal cations[J]. Environmental Science & Technology, 2016, 50, 2: 11066-11075. |
| [28] |
Xu Q, Zhou Q, Pan M, et al. Interaction between chlortetracycline and calcium-rich biochar:Enhanced removal by adsorption coupled with flocculation[J]. Chemical Engineering Journal, 2020, 382: 122705. DOI:10.1016/j.cej.2019.122705 |
| [29] |
王懿萱, 张娣, 牛红云, 等. 核壳式磁性碳纳米吸附剂的制备及其对水环境中金霉素的吸附研究[J]. 环境科学, 2012, 33(4): 196-202. WANG Yi-xuan, ZHANG Di, NIU Hong-yun, et al. Synthesis of core/shell structured magneetic carbon nanoparticles and its adsorption ability to chlortetracycline in aquatic environment[J]. Chinese Journal of Environmental Science, 2012, 33(4): 196-202. |
 2021, Vol. 40
2021, Vol. 40