甲酸作为一种小分子有机酸,广泛应用于化工、纺织品、医药、橡胶等领域[1-4]。此外,甲酸可以在Cr、Co、Ni、Cu等催化剂作用下进一步分解为氢气[5],是氢能源的重要载体,最高容量可达53.4 g·L-1[6],达到美国能源部设立的氢载体条件(40 g·L-1)。氢能是除核能之外发热值最高的二次能源,其燃烧的最终产物是水,是一种公认的极具应用前景的绿色清洁能源。因此,催化转化生物质基碳水化合物产甲酸,不仅能够实现可再生农林废弃物资源向高附加值化学品的有效转化,而且对于氢能的生产储存也具有十分重要的意义。
目前,均相类催化剂如FeCl3、VOSO4和金属卟啉等[7-9],常用来催化转化碳水化合物产甲酸。例如,在1.65 MPa O2氛围下,Fe2(SO4)3催化葡萄糖转化为甲酸的产率为39.7%[10]。此外,含V氧化物具有较强的氧化能力,对甲酸具有较高的选择性,能将葡萄糖高效催化转化为甲酸。例如,Wang等[11]制备了NaVO3催化剂,其在较温和的水热条件下催化葡萄糖转化为甲酸产率为42.8%。研究发现,相比于其他金属,V具有更高的催化活性转化葡萄糖。因此,目前的均相催化剂大部分都含有V,如H5PV2Mo10O40和K5V3W3O19等。大部分均相催化剂转化葡萄糖制甲酸的产率为40%~70%。均相催化剂虽能有效转化碳水化合物产甲酸,但存在无法回收利用、与产物难分离等不足。因此,开发能与反应体系实现有效分离并且能够循环使用的固体催化剂对于碳水化合物定向转化具有重要意义。
浸渍法是目前制备金属负载型固体催化剂最常用的方法。例如,众多研究者使用浸渍法制备了CeO2@ZSM-5、SiO2-FeOx/ZSM-5、Cu-Fe/ZSM-5、TiO2/ ZSM-5以及Ga/H-ZSM-5等固体催化剂[12-16]。但是,浸渍法制备过程需要大量溶剂,还需要加热除去溶剂,合成时间相对较长。减少溶剂的使用,是绿色化学十二条原则之一。本工作采用无溶剂机械球磨法合成了V负载型固体催化剂,比较了传统浸渍法和无溶剂球磨法制备的催化剂在物理化学结构以及催化性能上的区别,系统研究了球磨法合成的固体催化剂转化碳水化合物产甲酸情况。
1 材料与方法 1.1 材料偏钒酸铵(NH4VO3),分子筛ZSM-5和木糖(C5H10O5,99%)均购自阿拉丁试剂(上海)有限公司;葡萄糖(C6H12O6)、果糖(C6H12O6,99%)和木聚糖(C5H10O5,95%)均购自上海麦克林生化科技有限公司;纤维二糖(C12H22O11,98%)和麦芽糖(C12H22O11,98%),均购自北京百灵威科技有限公司;微晶纤维素(101QD)购自天津市雅博生物工程技术有限公司;蔗糖(C12H22O11)购自天津市江天化工技术有限公司;可溶性淀粉([C6H10O5)x]购自北京奇特新化工公司。所有试剂均为分析纯,未进行前处理直接使用。
1.2 V-ZSM-5催化剂制备称取1.5 g ZSM-5和0.068 g NH4VO3于球磨罐中(不锈钢,50 mL)。同时放入20颗直径为5 mm的不锈钢球磨珠。将上述球磨罐固定在行星球磨机(Retsch PM100)上,然后在350 r·min-1的转速下球磨1 h。随后,将上述所得的混合物转移至坩埚中,在500 ℃空气氛围下煅烧2 h(升温速率为2 ℃·min-1)。最后用去离子水洗脱3次,80 ℃烘干12 h,所得催化剂命名为V/ZSM-5(B)。
作为对照,同时采用传统浸渍法制备V/ZSM-5催化剂。向盛有5 mL去离子水的烧杯中加入0.068 g固体NH4VO3,然后在搅拌条件下将1.5 g ZSM-5加入到上述溶液中,磁力搅拌4 h。随后在85 ℃下加热搅拌去除溶剂。将所得材料放入坩埚中,在500 ℃空气氛围下煅烧2 h(升温速率为2 ℃·min-1)。最后用去离子水洗脱3次,烘干。所得催化剂命名为V/ZSM-5(P)。
1.3 V-ZSM-5催化剂表征采用美国FEI公司热场发射QUANTA FEG 400超高分辨率场发射扫描电镜(SEM)观察样品形貌;EDS能谱仪(美国EDAX公司GENESIS)对样品进行元素含量测定,样品均匀分散在导电胶上,加速电压20 kV。使用德国布鲁克D8 Advance的X射线粉末衍射仪(XRD)对样品的晶相进行表征,测试条件是铜靶,入射线波长0.154 18 nm,扫描电压40 kV,扫描电流是40 mA,测试速度0.1 s·step-1,扫描范围为5°~ 90°。使用型号为ASAP 2460的表面积和孔隙度测定系统(美国麦克默瑞提克)测定样品的比表面积和孔体积。使用美国赛默飞世尔科技公司ESCALAB 250Xi X射线光电子能谱仪(XPS)表征元素存在形式,测试条件为单色Al Ka(hν=1 486.6 eV),功率150 W,500 μm束斑,结合能以C1s 284.8来校准。电感耦合等离子体质谱(ICP-MS)所用设备为Agilent 7700 ce,粉末样品碱溶后,定容至100 mL后测试。
1.4 催化反应及产物分析以葡萄糖为例,典型的催化反应如下:将0.1 g葡萄糖、5 mL去离子水和0.05 g V/ZSM-5催化剂置于50 mL不锈钢高压釜反应器中。反应釜充满氧气(3 MPa),然后在不同设定温度下(160~180 ℃)反应一定时间(10~50 min)。反应结束后,用冷水快速冷却反应釜,待冷却至室温后取上清液过滤,滤液中的成分用超高效液相色谱(Waters Acquity UPLC H-Class)测定。以流速为0.5 mL·min-1的稀硫酸水溶液(5 mmol· L-1)为流动相,采用示差检测器(RI)和Shodex SH1011糖柱进行分析,柱温为50 ℃,RI检测器温度为35 ℃。葡萄糖转化率、甲酸产率用下列方程式计算:

|
无溶剂球磨法和传统浸渍法制备的V/ZSM-5催化剂物理形貌及表面V元素分布情况如图 1所示。从V元素的面扫描结果来看,两种方法合成的催化剂V元素都均匀分布在载体表面(图 1c和图 1d)。但是球磨法合成的催化剂(图 1b)颗粒尺寸明显小于浸渍法制备的催化剂(图 1a)。这主要是由于球磨提供高能机械作用力,起到粉碎ZSM-5载体的作用。催化剂的颗粒尺寸越小,比表面积越大,暴露的催化位点也会更多。因此,相比于浸渍法,球磨法合成的V负载ZSM-5催化剂的活性可能更高。为进一步探究球磨法合成的催化剂上的V是否存在于孔道内,进行了催化剂孔径测定。结果发现,单独球磨ZSM-5载体1 h并煅烧后的材料,其平均孔径为2.62 nm;而加入V的前驱体同ZSM-5共球磨1 h并煅烧后得到的材料,其平均孔径下降为2.12 nm。因此推测,球磨过程中部分V也进入到了孔道中,造成了孔径的减小[17]。

|
a、b为扫描电镜图,c、d为V元素Mapping图 a, b are SEM images, and c, d are SEM-Mapping images 图 1 浸渍法和球磨法合成的催化剂扫描电镜图及V元素Mapping图 Figure 1 SEM and SEM-Mapping images of catalyst synthesized by impregnation and ball milling method |
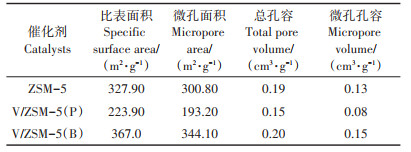
为考察传统浸渍法和本研究提出的球磨法合成的负载V催化剂孔隙结构特征,对制备的样品进行了N2吸附脱附表征。从图 2可以看出,在相对压力0.4 < P/P0 < 0.9时,3个样品都存在回滞环,均为典型的Ⅳ型回滞环吸附等温曲线,表明3个样品中都存在介孔结构。由表 1可知,ZSM-5母体材料本身具有多孔结构,其比表面积和孔容分别为327.90 m2·g-1和0.19 cm3·g-1。其中微孔为主,占比表面积的91.7%。采用浸渍法负载金属V以后,总比表面积和孔容均有所下降,分别为223.90 m2·g-1和0.15 cm3·g-1。这可能是由于浸渍法合成的催化剂,其金属氧化物负载在ZSM-5表面,堵塞了部分孔隙。但是,球磨法合成的催化剂V/ZSM-5(B)比表面积显著上升,由扫描电镜图片可以看出,球磨法合成的催化剂颗粒大小显著降低,这可能是导致其比表面积增大的主要原因。但通过浸渍法和球磨法合成的V负载ZSM-5催化剂主要都是微孔结构。

|
图 2 催化剂的氮气吸附/脱附等温线 Figure 2 Nitrogen adsorption/desorption isotherms |
|
|
表 1 Nitrogen adsorption/desorption isotherms Table 1 Nitrogen adsorption/desorption isotherms |
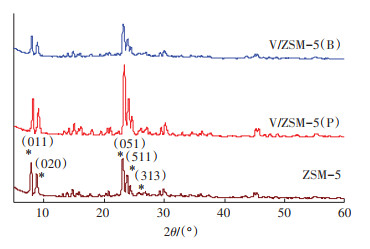
ZSM-5和不同方法合成的V/ZSM-5催化剂的X射线粉末衍射(XRD)结构如图 3所示。未改性的原始ZSM-5在2θ表现为7.86°、8.78°、23.18°、23.90°、24.40°,分别对应于ZSM-5的(011)(020)(051)(511)(313)晶面峰[18]。其晶体结构与文献报道的一致。通过浸渍法和球磨法合成的V改性沸石V/ZSM-5催化剂,其XRD图谱与母体ZSM-5基本一致(图 3),所有样品都具有典型ZSM-5分子筛的MFI结构,表明ZSM-5负载金属V后没有导致ZSM-5的晶格发生变化。与ZSM-5和V/ZSM-5(P)相比,V/ZSM-5(B)的衍射峰强度明显降低,这是由于金属V掺杂到ZSM-5中,ZSM-5的晶胞参数发生改变,有序度下降导致的。此外,XRD图谱中并未出现金属V的特征衍射峰,可能是因为金属V高度分散在ZSM-5表面,难以检测。此外,采用ICP对合成的催化剂V含量进行了测定,结果表明V/ZSM-5(P)和V/ZSM-5(B)中V含量分别为1.63%和1.69%。较低的含量也是其XRD图谱未出现金属V特征衍射峰的可能原因,这在其他文献中也有报道[19]。
|
图 3 ZSM-5及V改性后V/ZSM-5的XRD图谱 Figure 3 XRD spectrum of ZSM-5 before and after modification |
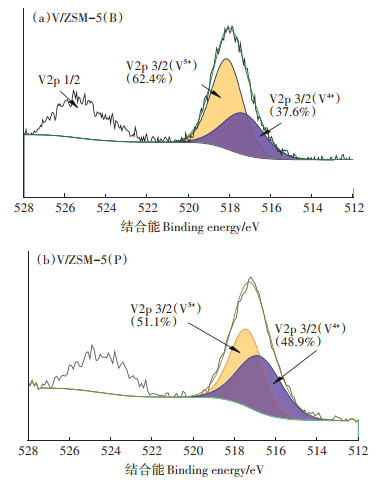
为进一步明确球磨法合成的固体催化剂V/ZSM- 5(B)上金属V的价态存在形式,以及不同合成方法对价态分布的影响,对其进行了X射线光电子能谱分析(XPS)测试表征。由图 4可知,两种方法合成的催化剂V均有两个轨道峰,分别位于~518 eV和~525 eV附近。根据文献报道,电子结合能位于~518.1 eV处的信号峰属于V5+的特征谱带,~517 eV处V的信号峰归属于V4+的特征谱带[20]。通过分析计算得到催化剂样品中均含有V5+和V4+两种价态的V。对XPS进行了分峰拟合,对其面积进行计算得知,V/ZSM-5(B)催化剂中V5+占62.4%,V4+占37.6%,而浸渍法得到的催化剂V/ZSM-5(P)中V5+占51.1%,V4+占48.9%。因此,球磨处理过程中提供的机械能(摩擦力、剪切力等)有助于高价态V的形成。根据葡萄糖氧化机理[21],在反应过程中,V5+将葡萄糖氧化为甲酸,自身被还原为V4+价,然后在氧气的作用下,V4+会被重新氧化为高价态V5+,持续促进葡萄糖催化转化为甲酸。
|
图 4 V/ZSM-5(B)和V/ZSM-5(P)的V2p XPS图谱 Figure 4 V2p XPS of the catalyst V/ZSM-5(B)and V/ZSM-5(P) |
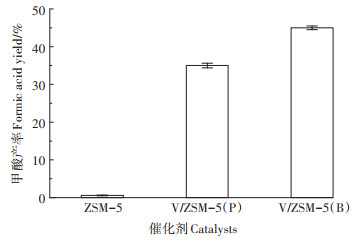
从图 5可以看出,在相同的条件下,不同催化剂转化葡萄糖产甲酸的性能差别较大。在没有金属V负载的情况下,ZSM-5由于没有氧化催化位点,基本上没有催化活性,几乎没有甲酸生成(产率为2%)。而采用传统浸渍法合成的金属V负载催化剂[V/ZSM-5(P)]催化葡萄糖时,甲酸产率达到35%。在同样的催化条件下,机械球磨法合成的金属V负载催化剂[V/ZSM-5(B)]转化葡萄糖产甲酸的产率增加到45%。由于ICP测定结果表明V/ZSM-5(P)和V/ZSM-5(B)金属V含量基本相同,因此,球磨法合成的催化剂性能优于传统浸渍法合成的催化剂主要原因是V/ZSM- 5(B)颗粒尺寸更小,比表面积更大,暴露出的催化位点更多。机械球磨法合成的金属V负载催化剂不仅在催化性能上有优势,其相对于浸渍法在工艺上也更绿色环保(无溶剂)、更快速。
|
反应条件:0.1 g葡萄糖,0.05 g催化剂,5 mL去离子水,180 ℃,3 MPa O2,30 min Condition:0.1 g glucose, 0.05 g catalyst, 5 mL water, 180 ℃, 3 MPa O2, 30 min 图 5 ZSM-5及不同方法合成的V改性催化剂性能比较 Figure 5 Catalytic performance of different catalysts |
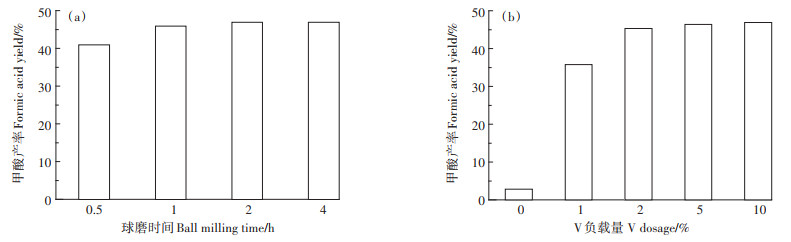
球磨时间(0.5、1、2、4 h)以及不同V负载量(0%、1%、2%、5%、10%)对催化性能的影响如图 6所示。球磨时间较短时(0.5 h),其合成的催化剂性能相对较差,甲酸产率为41.0%。当球磨时间延长至1 h后,甲酸的产率增加到46%,继续延长球磨时间,其合成的催化剂性能并没有随之提升。该结果说明球磨时间太短难以将金属均匀地稳定负载在ZSM-5上,而球磨1 h即能高效负载金属氧化物,且整个过程无需任何溶剂,绿色友好。不同V负载量的催化结果如图 6(b)所示。当V的负载量为0%时,甲酸的产率极低,说明载体本身不具有催化活性。当负载1%的V时,甲酸产率迅速增加。V含量为2%时,甲酸产率可以达到45.3%。继续增加V的负载量,葡萄糖的转化率和甲酸产率没有明显的增加。为了节约成本,故选择V的最佳含量为2%。
|
反应条件:0.1 g葡萄糖,0.05 g催化剂,5 mL去离子水,180 ℃,3 MPa O2,30 min Condition:0.1 g glucose, 0.05 g catalyst, 5 mL water, 180 ℃, 3 MPa O2, 30 min 图 6 球磨时间及V负载量对催化性能的影响 Figure 6 Effect of ball milling time and V dosage on the yield of formic acid |
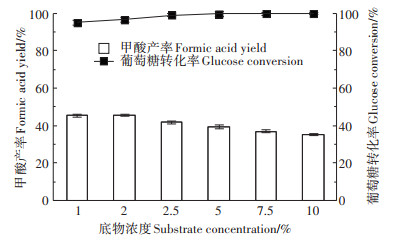
系统研究了催化体系(底物浓度、催化剂用量、气体氛围等)对V/ZSM-5(B)转化葡萄糖的影响。首先研究了葡萄糖初始浓度对V/ZSM-5(B)催化剂在水相中催化葡萄糖转化为甲酸的影响,结果如图 7所示。从图中可知,不同初始浓度下葡萄糖的转化率均较高,几乎转化完全(96%~98%),表明了该水热催化体系下葡萄糖比较容易转化。甲酸的产率随着葡萄糖浓度的增加有逐渐下降的趋势。当底物浓度为1%或2%时,甲酸产率最高,为45%。结果表明,底物浓度较低时,催化剂有足够的催化位点转化葡萄糖。随着底物浓度进一步增加到10%,催化剂能提供的催化位点有限,导致甲酸产率有所下降,但仍能达到35%。这对催化葡萄糖转化为甲酸的实际应用具有重要意义,一次转化的碳水化合物越多,成本越低。此外,从图中可以看出,葡萄糖的转化率远大于甲酸的产率,这主要是由于同时生成了大量的副产物CO2。
|
反应条件:0.05 g V/ZSM-5(B)催化剂,5 mL去离子水,180 ℃,3 MPa O2,30 min Condition:0.05 g catalyst, 5 mL water, 180 ℃, 3 MPa O2, 30 min 图 7 Condition:0.1 g glucose,0.05 g catalyst,5 mL water,180 ℃,3 MPa O2,30 min Figure 7 Effect of glucose concentration on the formic acid yield |
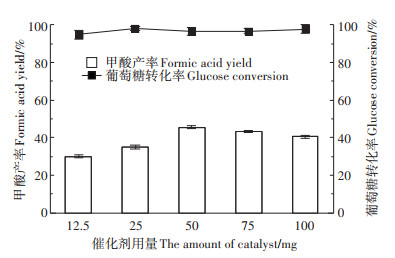
催化剂的用量对催化反应有着重要的影响,需要适量才能发挥最大的催化效率。因此本研究考察不同V/ZSM-5(B)用量对葡萄糖产甲酸的影响,结果如图 8所示。从图中可以看出,葡萄糖的转化率随着催化剂用量的增加逐渐上升,当该体系下V/ZSM-5(B)用量为12.5 mg时,葡萄糖转化率为90%,甲酸产率为30%。随着催化剂用量增加至25 mg,葡萄糖转化率增加到95%,甲酸产率也增至35%。当催化剂用量为50 mg时,甲酸产率达到最大值(45%)。催化剂量继续增加时,甲酸产率有所下降。这可能是由于催化剂用量过多时,催化剂容易发生团聚现象,导致该催化剂的催化活性略有下降[22]。
|
反应条件:0.1 g葡萄糖,5 mL去离子水,180 ℃,3 MPa O2,30 min Condition:0.1 g glucose, 5 mL water, 180 ℃, 3 MPa O2, 30 mi 图 8 催化剂用量对甲酸产率的影响 Figure 8 Effect of catalyst dosage on the formic acid yield |
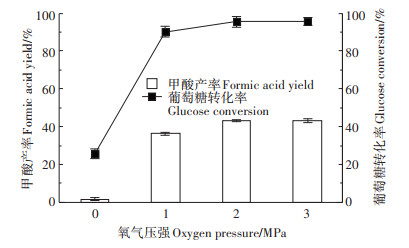
葡萄糖催化转化为甲酸是一个氧化的过程,因此,气体氛围及压强对反应影响较大。研究考察了不同氧气压强下对V/ZSM-5(B)催化葡萄糖转化为甲酸的影响,结果如图 9所示。结果表明,在常压空气氛围下(0 MPa O2)进行催化反应,葡萄糖转化率较低,几乎不产生甲酸(2%)。当反应气氛为1 MPa O2时,葡萄糖转化率增加,甲酸产率也迅速提高。随着反应氧气压强继续增加到2 MPa,葡萄糖转化率和甲酸产率明显增高,达到最大值。当葡萄糖作为底物在适宜的温度下反应生成甲酸时,较高的氧气压强(≥2 MPa)有利于葡萄糖转化率的提高[23]。在3 MPa O2下进行催化反应,葡萄糖转化率和甲酸产率相比于2 MPa条件下几乎无变化,说明2 MPa的氧气已足够该反应的进行。
|
反应条件:0.05 g催化剂,0.1 g葡萄糖,5 mL去离子水,180 ℃,30 min, Condition:0.05 g catalyst, 0.1 g glucose, 5 mL water, 180 ℃, 30 min 图 9 底物浓度Substrate concentration/% Figure 9 Effect of gas atmosphere on formic acid yield |
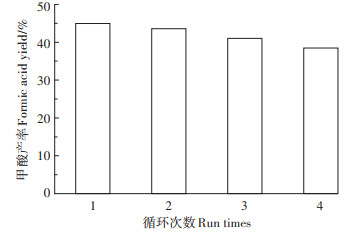
与均相催化剂相比,固体催化剂的优势之一是其可循环使用。本工作中球磨法合成的V/ZSM-5(B)循环使用性能如图 10所示。在180 ℃下,反应30 min,进行了4次循环实验。反应结束后,用过滤法从反应混合物中分离出固体V/ZSM-5催化剂,并用去离子水多次冲洗。在真空烘箱中于80 ℃干燥12 h后,在相同的反应条件下,进行下一次循环实验。V/ ZSM-5(B)催化剂第1次使用时其催化葡萄糖产甲酸的产率为45.0%,第2次使用时甲酸的产率几乎没变(43.6%),经过4次循环使用后,甲酸收率仍能达到38.5%。该实验结果表明,球磨法合成的V/ZSM-5(B)催化剂在葡萄糖制甲酸的催化氧化反应体系中具有较高的活性和稳定性。
|
反应条件:0.1 g葡萄糖,0.05 g催化剂,5 mL去离子水,180 ℃,3 MPa O2,30 min Condition:0.1 g glucose, 0.05 g catalyst, 5 mL water, 180 ℃, 3 MPa O2, 30 min 图 10 V/ZSM-5(B)循环使用性能 Figure 10 Recycling of the V/ZSM-5(B) |
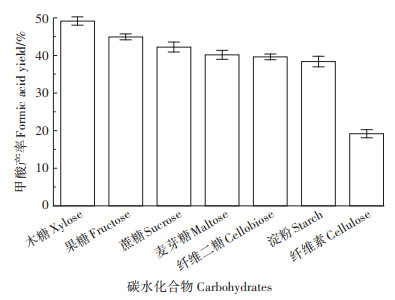
除葡萄糖以外,还使用其他碳水化合物,包括单糖(如木糖、果糖)、二糖(如蔗糖、麦芽糖和纤维二糖)和多糖(如纤维素和淀粉)作为生产甲酸的生物质原料,以考察该催化剂广泛的适用范围,结果如图 11所示。几乎所有单糖(木糖和果糖)都能被V/ZSM-5(B)高效转化,甲酸产率分别为49%和46%。二糖类碳水化合物如蔗糖、麦芽糖和纤维二糖也能高效转化为甲酸,产率分别为42%、40%和39%。淀粉和纤维素属于高分子聚合物,聚合度较高,相对难以转化。在本研究中,将淀粉转化的反应时间从单糖和二糖的30 min延长至60 min,甲酸的产率也能达到38%。而纤维素结构稳定,结晶度更高,在水相中极难转化。本研究首先利用机械球磨法对纤维素进行了预处理,并延长催化反应时间到8 h,甲酸的产率为19%。以上结果表明,甲酸的产量随着底物结构复杂性的增加而降低,单糖和双糖类碳水化合物比较容易转化为甲酸,聚合度和结晶度较高的纤维素则较难转化。但总体而言,本研究合成的V/ZSM-5(B)催化剂适用于多种碳水化合物选择性转化为甲酸。
|
图 11 V/ZSM-5(B)催化转化不同碳水化合物为甲酸 Figure 11 Catalytic conversion of different carbohydrates to formic acid with V/ZSM-5(B) |
(1)采用无溶剂机械球磨法成功将金属V负载在ZSM-5分子筛上,制备出新型固体催化剂V/ZSM-5(B)。相比于传统浸渍法,避免了溶剂的使用,制备方法绿色、高效。球磨法合成的催化剂颗粒尺寸更小,比表面积更大,且金属V的价态更高,使得其催化活性进一步提升。
(2)不同反应条件(底物浓度、催化剂量、气体氛围等)均影响该催化剂转化葡萄糖产甲酸的效率。在底物用量与催化剂用量比为2:1,氧气压强为3 MPa,180 ℃下催化氧化反应30 min时,葡萄糖产甲酸的产率最高(45%),达到目前固体催化剂的较高水平。
(3)同时,V/ZSM-5(B)催化剂还适用于多种生物质基碳水化合物催化转化产甲酸,展现出良好的催化活性。
| [1] |
Bulushev D A, Ross J R H. Towards sustainable production of formic acid[J]. Chem Sus Chem, 2018, 11(5): 821-836. DOI:10.1002/cssc.201702075 |
| [2] |
Valentin F, Kozell V, Petrucci C, et al. Formic acid, a biomass-derived source of energy and hydrogen for biomass upgrading[J]. Energy & Environmental Science, 2019, 12(9): 2646-2664. |
| [3] |
Choi M, Ahn C Y, Lee H, et al. Bi-modified Pt supported on carbon black as electro-oxidation catalyst for 300 W formic acid fuel cell stack[J]. Applied Catalysis B:Environmental, 2019, 253: 187-195. DOI:10.1016/j.apcatb.2019.04.059 |
| [4] |
Jiang M P, Wu H J, Li Z D, et al. Highly selective photoelectrochemical conversion of carbon dioxide to formic acid[J]. ACS Sustainable Chemistry & Engineering, 2018, 6(1): 82-87. |
| [5] |
Doustkhah E, Hasani M, Ide Y, et al. Pd nanoalloys for H2 generation from formic acid[J]. ACS Applied Nano Materials, 2020, 3(1): 22-43. DOI:10.1021/acsanm.9b02004 |
| [6] |
Wang C, Chen X, Qi M, et al. Room temperature, near-quantitative conversion of glucose into formic acid[J]. Green Chemistry, 2019, 21(22): 6089-6096. DOI:10.1039/C9GC02201E |
| [7] |
Zhang H D, Li N, Pan X J, et al. Direct transformation of cellulose to gluconic acid in a concentrated iron(Ⅲ)chloride solution under mild conditions[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(5): 4066-4072. |
| [8] |
李宗祥.金属卟啉催化O2氧化纤维素制备甲酸和乙醇酸反应研究[D].长沙: 湖南大学, 2010. LI Zong-xiang. The research on metalloporphyrins catalyzed O2 oxidation of cellulose to produce formic acid and glycolic acid[D].Changsha: Hunan University, 2010. |
| [9] |
牛牧歌, 侯玉翠, 任树行, 等. 含钒催化剂作用下生物质选择性氧化制备甲酸[J]. 科学通报, 2015, 60(16): 1434-1442. NIU Mu-ge, HOU Yu-cui, REN Shu-hang, et al. Catalytic oxidation of biomass to formic acid in aqueous solutions using vanadium-containing catalysts[J]. Chinese Science Bull, 2015, 60(16): 1434-1442. |
| [10] |
Mcginnis G D, Prince S E, Biermann C J, et al. Wet oxidation of model carbohydrate compounds[J]. Carbohydrate Research, 1984, 128(1): 51-60. DOI:10.1016/0008-6215(84)85083-1 |
| [11] |
Wang W H, Niu M G, Hou Y C, et al. Catalytic conversion of biomass-derived carbohydrates to formic acid using molecular oxygen[J]. Green Chemistry, 2014, 16(5): 2614-2618. DOI:10.1039/c4gc00145a |
| [12] |
Dai Q G, Wang W, Wang X Y, et al. Sandwich-structured CeO2@ZSM-5 hybrid composites for catalytic oxidation of 1, 2-dichloroethane:An integrated solution to coking and chlorine poisoning deactivation[J]. Applied Catalysis B:Environmental, 2017, 203: 31-42. DOI:10.1016/j.apcatb.2016.10.009 |
| [13] |
Hu Q F, Huang X F, Cui Y, et al. High yield production of C2-C3 olefins and para-xylene from methanol using a SiO2-coated FeOx/ZSM-5 catalyst[J]. RSC Advances, 2017, 7(46): 28940-28944. DOI:10.1039/C7RA04111J |
| [14] |
Oliveira T K R D, Rosset M, Perez-Lopez O W. Ethanol dehydration to diethyl ether over Cu-Fe/ZSM-5 catalysts[J]. Catalysis Communications, 2017, 104: 32-36. |
| [15] |
Huang H B, Huang H L, Feng Q Y, et al. Catalytic oxidation of benzene over Mn modified TiO2/ZSM-5 under vacuum UV irradiation[J]. Applied Catalysis B:Environmental, 2017, 203: 870-878. DOI:10.1016/j.apcatb.2016.10.083 |
| [16] |
Schreiber M W, Plaisance C P, Baumgartl M, et al. Lewis-Bronsted acid pairs in Ga/H-ZSM-5 to catalyze dehydrogenation of light alkanes[J]. Journal of the American Chemical Society, 2018, 140(14): 4849-4859. DOI:10.1021/jacs.7b12901 |
| [17] |
Xu Y Y, Wang Q H, Yoza B A, et al. Catalytic ozonation of recalcitrant organic chemicals in water using vanadium oxides loaded ZSM-5 zeolites[J]. Frontiers in Chemistry, 2019, 7: 384-390. DOI:10.3389/fchem.2019.00384 |
| [18] |
Zhao B, Liu X W, Zhou Z J, et al. Effect of molybdenum on mercury oxidized by V2O5-MoO3/TiO2 catalysts[J]. Chemical Engineering Journal, 2014, 253: 508-517. DOI:10.1016/j.cej.2014.05.071 |
| [19] |
Taylor A, Sinclair H. On the determination of lattice parameters by the Debye-Scherrer method[J]. Proceedings of the Physical Society, 1945, 57(2): 126-135. DOI:10.1088/0959-5309/57/2/306 |
| [20] |
祝琳华, 贺召宏, 司甜, 等. 柱撑型钒基催化剂的制备及其丙烷氧化脱氢催化性能[J]. 化工进展, 2019, 38(8): 3711-3719. ZHU Lin-hua, HE Zhao-hong, SI Tian, et al. Preparation of vanadia pillared catalysts and the catalytic performance in the oxidative dehydrogenation of propane to propylene[J]. Chemical Industry and Engineering Progress, 2019, 38(8): 3711-3719. |
| [21] |
Albert J, Luders D, Bosmann A, et al. Spectroscopic and electrochemical characterization of heteropoly acids for their optimized application in selective biomass oxidation to formic acid[J]. Green Chemistry, 2014, 16(1): 226-237. DOI:10.1039/C3GC41320A |
| [22] |
梁文珍, 王慧龙, 姜文凤. 太阳光下TiO2/SiO2气凝胶复合光催化剂光催化降解2, 4-二硝基酚[J]. 环境科学学报, 2011, 31(6): 1162-1167. LIANG Wen-zhen, WANG Hui-long, JIANG Wen-feng. Solar photocatalytic degradation of 24-dinitrophenol DNP using TiO2/SiO2 aerogel composite photocatalysts[J]. Acta Scientia Circumstantiae, 2011, 31(6): 1162-1167. |
| [23] |
Li J, Ding D J, Deng L, et al. Catalytic air oxidation of biomass-derived carbohydrates to formic acid[J]. ChemSusChem, 2012, 5(7): 1313-1318. DOI:10.1002/cssc.201100466 |
 2021, Vol. 40
2021, Vol. 40