2. 吉林农业大学资源与环境学院, 长春 130000;
3. 华标(天津)科技有限责任公司, 天津 300392
2. College of Resources and Environment, Jilin Agricultural University, Changchun 130000, China;
3. Huabiao (Tianjin)Technology Co. Ltd, Tianjin 300392, China
玉米是我国重要的粮食作物。根据世界粮农组织数据,2019年我国玉米总产量和总种植面积分别占世界总量的43%和36%[1]。但在玉米种植过程中会受到病虫害的危害,为了控制病虫害以提高产量[2-3],越来越多的杀虫剂、除草剂和杀菌剂被使用[4],从而造成了玉米中的农药残留问题。为了确保玉米的质量安全,为我们的饮食健康保驾护航,我国食品安全国家标准(GB 2763—2019)中明确规定了玉米中农药最大残留限量标准。
食品中农药残留的分析方法主要分为样品前处理和仪器分析[5]。样品前处理主要有索式提取法、固相萃取法、基质固相分散萃取法、加速溶剂萃取法、液液萃取法、QuEChERS(Quick easy cheap effective rugged safe)法等,其中QuEChERS法在玉米等粮谷类基质农药残留分析中得到越来越广泛的应用。李同宾等[6]基于QuEChERS-液相色谱串联质谱(LC-MS/MS)建立了同时检测玉米粉中41种常见农药残留的分析方法;李菊颖等[7]建立了玉米粉中吡虫啉、三唑酮、乙草胺与异丙甲草胺的QuEChERS结合LC-MS/MS法;叶倩等[8]开发了玉米粉中乙草胺、异丙甲草胺和三唑酮残留检测的气相色谱串联质谱(GC-MS/MS)法;HE等[9]建立了粮谷中200余种农药残留的GC-MS/MS检测方法。但上述这些前处理方法的溶剂消耗量大、操作繁琐[10],例如QuEChERS法提取时需要15~20 mL乙腈,且需经过称量、振摇提取、离心、净化、再离心等多个步骤。相对而言,在线超临界流体萃取具有节省有机溶剂、操作简便等优点,将样品称量至萃取池并添加分散剂混匀后即可上机进行自动化在线萃取,且萃取时通常有机溶剂的消耗量低于5 mL。然而该方法尚未应用于玉米粉中农药多残留分析。
玉米粉中农药残留的仪器分析方法多为LC-MS/MS[6-7]、GC -MS/MS[8-9]等。目前,超临界流体色谱(SFC)与液相色谱(LC)相比,超临界二氧化碳流体作为流动相具有低黏度和高分子扩散性,可以提高分析效率,降低有机溶剂的消耗[11]。此外,搭配串联质谱后,超临界流体色谱串联质谱(SFC-MS/MS)显示出良好的选择性和灵敏度[12]。
目前,尚无研究应用在线超临界流体萃取-超临界流体色谱串联质谱(SFE-SFC-MS/MS)开展食品中农药多残留分析。本研究针对现有玉米粉中农药多残留分析方法存在的不足,结合超临界流体萃取、超临界流体色谱串联质谱的优点,建立了用于分析玉米粉中农药多残留的在线SFE-SFC-MS/MS分析方法。
1 材料与方法 1.1 仪器、试剂与材料Nexera超临界流体萃取仪(日本岛津公司)、Nexera UC超临界流体色谱仪(日本岛津公司);Shimpack UC-X-RP色谱柱(3 μm,2.1 mm×150 mm,日本岛津公司)。涡旋振荡器(Thermo,美国);高速冷冻离心机(Heal Force,中国香港);Milli-Q净水系统(德国MILLIPURE);食品粉碎机(中国奥克斯集团有限公司);万分之一天平(SQP,赛多利斯科学仪器北京有限公司)。
色谱纯甲醇、异丙醇、乙腈购于美国Fisher Scientific公司;无水乙醇购于中国天津市康科德科技有限公司;95%甲酸、LC-MS级甲酸铵(纯度≥99%)、无水硫酸镁(纯度≥99.5%)购于美国Sigma-Aldrich公司;超纯水由实验室Milli-Q制备。71种农药标准品购于美国Chemservice和德国Dr.Ehrenstorfer公司,纯度均大于98%。空白玉米粉购自天津市某超市。此外,另从河南省玉米主产地采集10份玉米粉样品用于残留测定。
1.2 标准溶液配制精确称取71种农药的标准品,用色谱纯乙腈分别配制1 000 mg·L-1标准储备溶液,-20 ℃储存。色谱纯乙腈稀释配制10 mg·L-1混合标准工作溶液。
1.3 超临界流体萃取(SFE)以玉米粉为基质,农药混标添加浓度为50 μg·kg-1对超临界流体萃取条件进行优化。在SFE提取阶段,优化5个变量,具体包括:提取剂的组成、比例、萃取时间、动态萃取流速、分散剂无水硫酸镁和样品的比例。通过单因素变量法,控制其他条件不变,只改变单个因素以摸索最优的萃取条件,基础条件如下:萃取剂组成及比例为95%超临界二氧化碳流体和5%含0.1%甲酸的甲醇溶液,动态萃取流速为5 mL·min-1,静态和动态萃取时间为3 min,分散剂无水硫酸镁和样品比例为1∶1(m/m)。
(1)提取剂的组成:95%超临界二氧化碳流体和5%的甲醇、乙醇、异丙醇、乙腈、含1 mmol·L-1甲酸铵的甲醇溶液、含0.1%甲酸的甲醇溶液、含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液。
(2)乙醇和超临界流体二氧化碳的比例:1∶99、3∶ 97、5∶95、7∶93、9∶91(V/V),即乙醇含量为1%、3%、5%、7%、9%的超临界流体二氧化碳。
(3)动态萃取流速:1、2、3、4、5 mL·min-1。
(4)静态和动态萃取时间:1、2、3、4、5 min。
(5)分散剂无水硫酸镁和样品的比例(m/m):1∶5、1∶2、1∶1、2∶1、5∶1。
每个处理3个平行。通过在线SFE-SFC-MS/MS进行检测,计算回收率。
1.4 超临界流体色谱(SFC)色谱柱为Shim-pack UC-X RP(3 μm,2.1 mm×150 mm),进样量为2 μL,背压调节器B(Back pressure regulator B,BPRB)压力为40 MPa,流动相A为超临界二氧化碳流体,流动相B为改性剂。对改性剂、流速、背压调节器A(BPRA)压力、柱温、柱后补偿溶剂及流速等条件进行优化,基础色谱条件为:改性剂为含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液,流速为1.5 mL ·min-1,BPRA压力为14.8 MPa,柱温为40 ℃,柱后补偿溶剂为含0.1%甲酸的甲醇溶液,柱后补偿溶剂流速为0.1 mL·min-1。采用单因素变量法,保持其他条件不变,分别对以下条件进行优化:
(1)改性剂:甲醇、乙醇、异丙醇、正丁醇、含0.01%甲酸和1 mmol·L-1甲酸铵的甲醇溶液、含0.1%甲酸和2 mmol·L-1甲酸铵的甲醇溶液、含1 mmol·L-1甲酸铵的甲醇溶液、含0.1%甲酸的甲醇溶液、含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液。
(2)流速:1.3、1.5、1.8、2.0、2.2、2.6、3.0 mL·min-1。
(3)BPRA压力:10.0、12.0、14.0、14.8、16.0、18.0MPa。
(4)柱温:30、35、40、45、50 ℃。
(5)柱后补偿溶剂:甲醇、含0.1%甲酸和5 mmol·L-1甲酸铵的甲醇溶液、含0.1%甲酸和1 mmol·L-1甲酸铵的甲醇溶液、含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液、含0.1%甲酸的甲醇溶液。
(6)柱后补偿溶剂流速:0.05、0.10、0.15、0.20、0.25 mL·min-1。
通过对以上条件的优化,考察不同条件对色谱分离效果、目标化合物峰面积的影响。
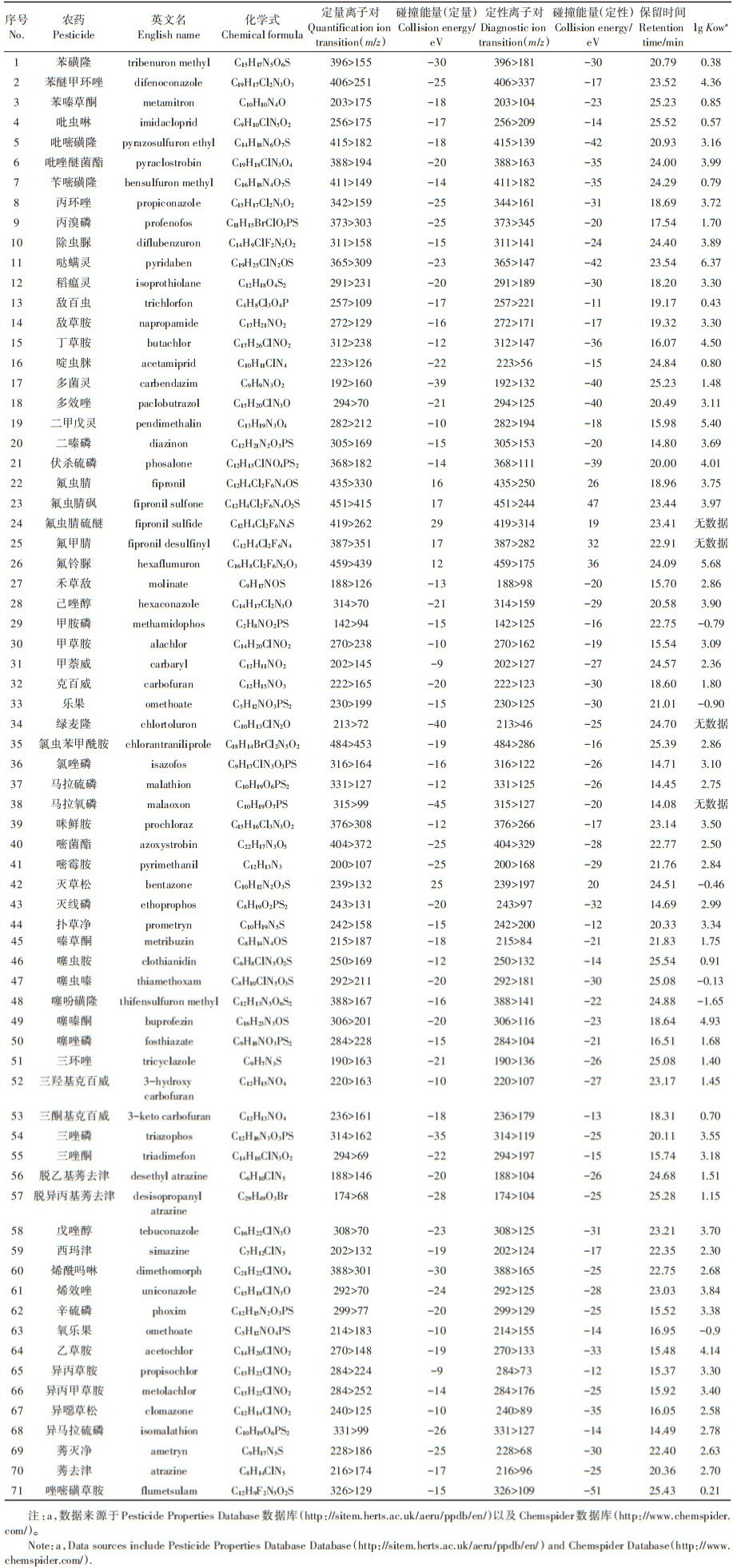
1.5 质谱条件采用MRM模式,71种目标农药的离子对、碰撞能等信息见表 1。雾化气流量3 L·min-1,加热气流量10 L·min-1,干燥气流量10 L·min-1,接口温度300 ℃,DL温度250 ℃,加热块温度400 ℃。
|
|
表 1 71种农药及代谢物的质谱参数 Table 1 Mass spectrometric parameters for 71 pesticides and metabolites |
SFE在线萃取后,作为特殊进样设备,在线将目标物导入SFC系统分离分析。因此,在考察目标物线性范围时,使用玉米粉空白基质配制9个农药混标浓度水平的玉米基质标准添加样品(浓度分别为1、2、5、10、20、50、100、200、500 μg·kg-1),SFE-SFC-MS/MS上机分析。以峰面积为纵坐标,以与峰面积对应的浓度为横坐标,得到玉米粉基质校准曲线。分别以信噪比S/N为3和10时所对应的71种农药的浓度作为检出限(LOD)和定量限(LOQ)。
1.6.2 准确度和精密度在玉米粉中设置1、10、100 μg·kg-1 3个农药混标添加水平,每个添加水平5个平行。按照优化后的在线SFE-SFC-MS/MS条件进行分析,计算回收率。
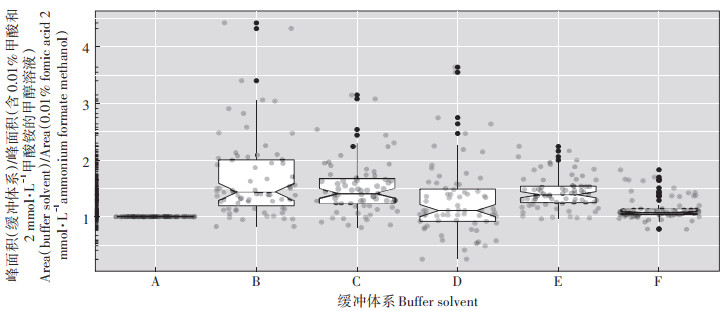
2 结果与讨论 2.1 SFC条件优化 2.1.1 改性剂优化超临界二氧化碳流体属于非极性流动相,因此对一些中等极性的化合物不能很好地分离。添加改性剂可以提高SFC的分离能力,拓宽其分析范围。本研究比较了甲醇、乙醇、异丙醇和正丁醇等不同改性剂对目标化合物分离效果的影响。根据lg Kow大小评估化合物的极性,lg Kow越小,化合物在水相中的溶解度越大,极性越高。在71种化合物中有67种可查询到lg Kow值(表 1),其范围为-1.65~6.37,中位值为2.84,表明本研究中目标化合物的极性范围较宽。乙醇、异丙醇、正丁醇较甲醇的保留时间都有延后,且异丙醇和正丁醇条件下部分化合物未出峰。甲醇在考察的改性剂中极性最大,流动相极性的调节范围也最宽[12],因此选择甲醇作为改性剂。在此基础上,对不同缓冲体系进行优化,考察了不同甲酸、甲酸铵组合及不同浓度对目标化合物响应的影响,如图 1所示,通过比较不同改性剂缓冲体系与初始缓冲体系作为流动相时目标化合物峰面积,可知只有在含0.1%甲酸的甲醇溶液条件下,所有化合物的峰面积才会大于等于初始缓冲体系条件下目标化合物的峰面积,由此确定含0.1%甲酸的甲醇溶液条件为最优条件,以此进行后续优化。
|
A:含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液;B:含0.01%甲酸和1 mmol·L-1甲酸铵的甲醇溶液;C:含0.1%甲酸和2 mmol·L-1甲酸铵的甲醇溶液;D:含1 mmol·L-1甲酸铵的甲醇溶液;E:含0.1%甲酸的甲醇溶液;F:甲醇 A: 0.01% formic acid 2 mmol·L-1 ammonium formate methanol; B: 0.01% formic acid 1 mmol·L-1 ammonium formate methanol; C: 0.1% formic acid 2 mmol·L-1 ammonium formate methanol; D: 1 mmol·L-1 ammonium formate methanol; E: 0.1% formic acid methanol; F: methanol 图 1 不同缓冲体系下峰面积(缓冲体系)/峰面积(含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液) Figure 1 The ratio of area(buffer solvent)/area(0.01% formic acid 2 mmol·L-1 ammonium formate methanol) under different buffer systems |
随着SFC流速增大,目标化合物的保留时间逐渐前移。由于Shim-pack UC-X RP色谱柱(5 μm)最高耐压为30 MPa,为延长色谱柱寿命,工作压力需在20 MPa以下。本研究中上述色谱柱在1.3~3.0 mL·min-1流速下柱压可达17.26~23.47 MPa,因此从延缓色谱柱损耗的角度,选择流速为1.5 mL·min-1,此条件下柱压可控制在17.72 MPa之内。并且在1.5 mL·min-1流速下,每针样品所消耗的改性剂为3.60 mL,对环境更加友好,因此最终选择1.5 mL·min-1的流速进行后续优化。
2.1.3 柱温优化随着柱温的升高,超临界二氧化碳的密度降低[13],进而削弱了其对目标化合物的洗脱能力,原因可能是随着柱温的不断升高,化合物在柱上的保留得到了有效增强,从而使得化合物的出峰时间后移。考虑到超临界二氧化碳的临界温度(31.06 ℃)及分离效果,选择40 ℃作为柱温进行后续优化。
2.1.4 BPRA背压优化随着BPRA压力的增加,保留时间逐渐减小,这是由于随着压力的增加,二氧化碳的密度增加,进而增强了对目标化合物的洗脱能力[14]。在10.0、12.0、18.0 MPa压力下部分化合物未检出,且在10 MPa条件下化合物峰大多展宽。在14.0、14.8、16.0 MPa条件下目标物均可出峰,14.8 MPa时目标物在时间窗内分布较均匀,且14.8 MPa为仪器推荐的BPRA压力,因此,选择14.8 MPa进行后续的条件优化。
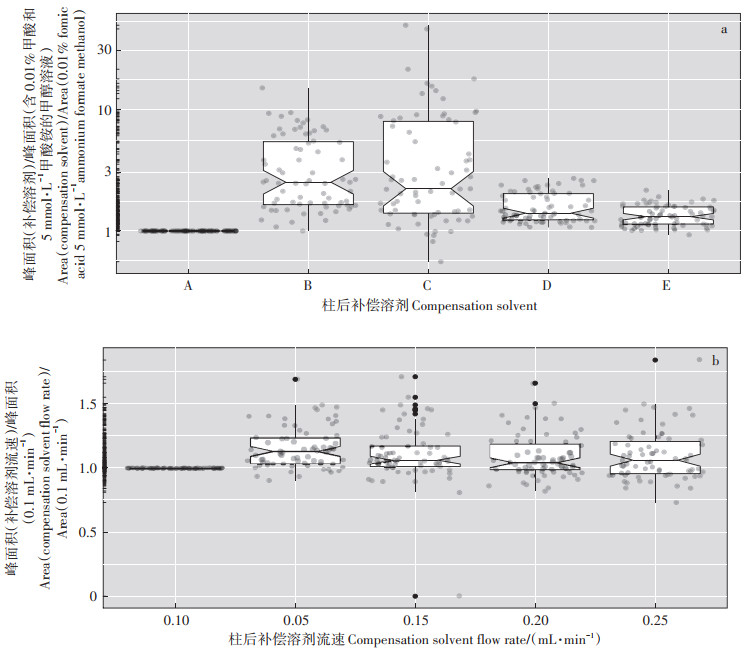
2.1.5 柱后补偿溶剂及流速的优化含0.1%甲酸的甲醇溶液在提高被分析物的电喷雾电离效率上效果最好(图 2a),因此选择其进一步优化流速。当柱后补偿溶剂流速为0.05 mL·min-1时,目标化合物的响应最优(图 2b)。最终选择上述两个条件作为最优条件。
|
A:含0.1%甲酸和5 mmol·L-1甲酸铵的甲醇溶液,B:含0.1%甲酸的甲醇溶液,C:甲醇,D:含0.1%甲酸和1 mmol·L-1甲酸铵的甲醇溶液,E:含0.01%甲酸和2 mmol·L-1甲酸铵的甲醇溶液 A: 0.1% formic acid 5 mmol·L-1 ammonium formate methanol, B: 0.1% formic acid methanol, C: methanol, D: 0.1% formic acid 1 mmol·L-1 ammonium formate methanol, E: 0.1% formic acid 2 mmol·L-1 ammonium formate methanol 图 2 不同柱后补偿溶剂条件下的峰面积(补偿溶剂)/峰面积(含0.1%甲酸和5 mmol·L-1甲酸铵的甲醇溶液)以及优化的补偿溶剂在不同流速条件下的峰面积(补偿溶剂流速)/峰面积(0.1 mL·min-1) Figure 2 The ratio of area(compensation solvent)/area(0.1% formic acid 5 mmol·L-1 ammonium formate methanol)under different postcolumn compensation solvents and the ratio of area(compensation solvent flow rate)/area(0.1 mL·min-1)under different flow rates of the optimized post-column compensation solvent |
通过2.1.1~2.1.5部分的优化,确定最优SFC条件如下:改性剂为含0.1%甲酸的甲醇溶液,流速为1.5 mL·min-1,BPRA为14.8 MPa,柱温为40 ℃,柱后补偿溶剂为含0.1%甲酸的甲醇溶液,柱后补偿溶剂流速为0.05 mL·min-1。梯度程序为:0 min,流动相B为2%;0~1 min,流动相B为3%;1~5 min,流动相B为4%;5~8 min,流动相B为6%;8~10 min,流动相B为10%;10~11 min,流动相B为24%;11~12 min,流动相B为40%;12~14 min,流动相B为50%;14~15 min,流动相B为50%;15~15.1 min,流动相B为2%,保持0.4 min。
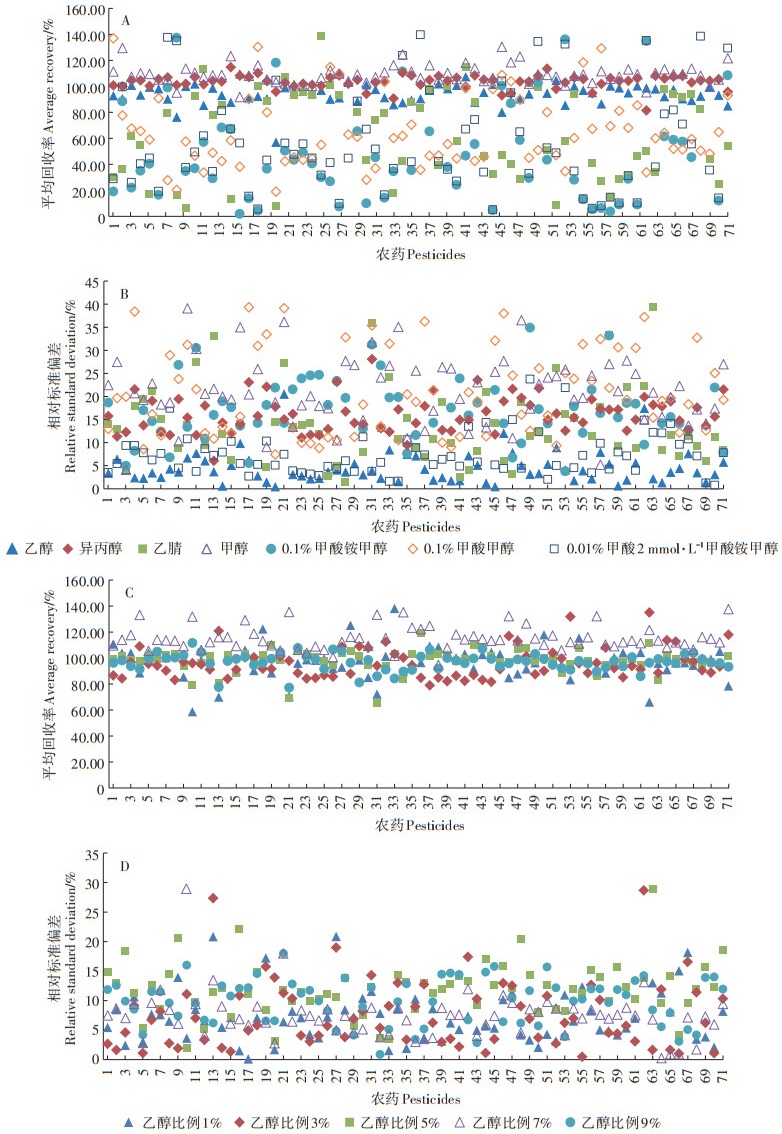
2.2 SFE条件优化 2.2.1 提取溶剂组合和比例的优化超临界二氧化碳流体属于非极性溶剂,用其萃取中等极性或者极性更强的化合物效果不理想,因此须通过添加其他极性萃取剂改变其极性,进而扩展其萃取化合物的范围。乙醇与超临界二氧化碳流体组合的回收率符合要求(图 3A),且其相对标准偏差最低(图 3B)。图 3C和图 3D分别为含1%~9%乙醇的超临界二氧化碳流体萃取下目标化合物的添加回收结果,根据回收率及相对标准偏差最终选择含有9%乙醇的二氧化碳超临界流体进行后续条件的优化。
|
图 3 不同有机溶剂与超临界流体二氧化碳组合以及不同乙醇含量的超临界流体二氧化碳下农药的平均回收率(A、C)和相对标准偏差(B、D) Figure 3 Average recoveries(A and C)and relative standard deviations(B and D)of the selected pesticides at different extract solvent and different ethanol proportions coupled with supercritical CO2 |
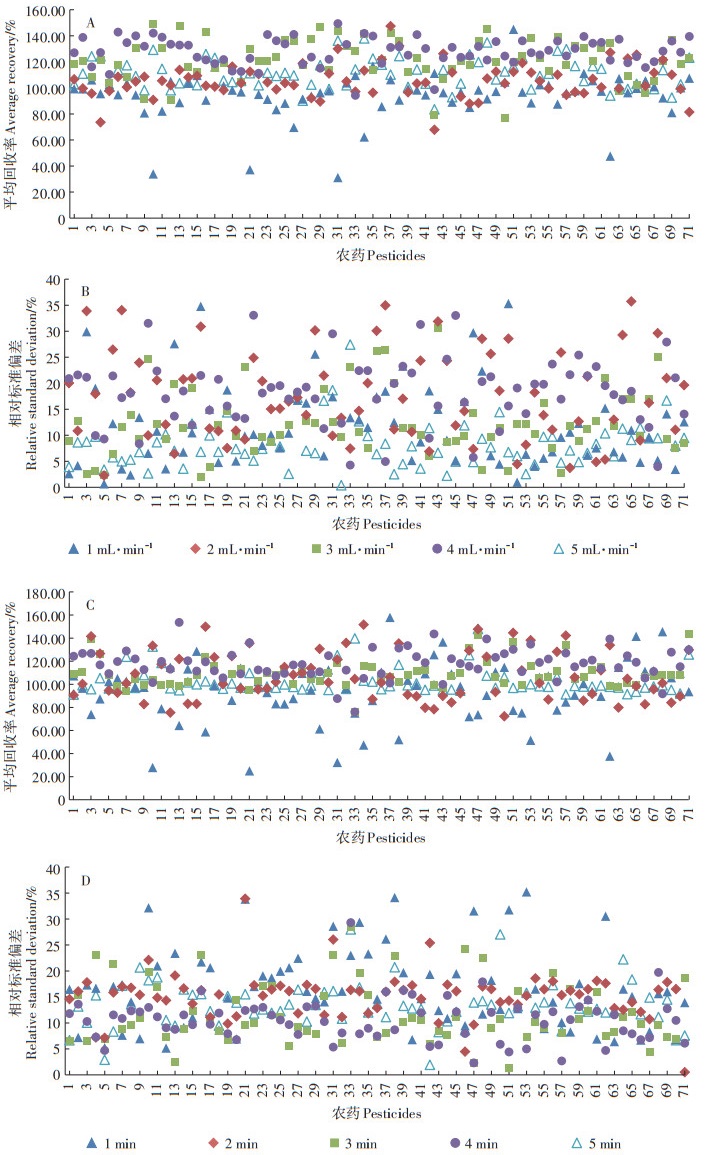
提取溶剂在动态萃取时的流速大小会影响目标物的萃取效率[15]。因此,本研究在保证其他萃取条件不变的情况下,考察了1、2、3、4、5 mL·min-1 5个动态萃取流速下目标物的回收率。结果如图 4A和图 4B所示,在5 mL·min-1动态萃取时目标化合物的回收率在80%~120%之间,且相对标准偏差均在20%以下。因此,选择了5 mL·min-1进行后续条件优化。
|
图 4 不同动态萃取流速及静态/动态萃取时间下玉米粉中农药的平均回收率(A、C)和相对标准偏差(B、D) Figure 4 Average recoveries(A and C)and relative standard deviations(B and D)of the pesticides at different dynamic extraction velocities and static/ dynamic extraction time |
在SFE中萃取剂与样品基质的萃取时间决定了其萃取率,萃取时间越长,萃取率越高。在保持其他条件不变情况下,考察了静态/动态萃取时间(静态萃取和动态萃取时间保持一致,为1、2、3、4、5 min)对目标物提取回收率的影响。图 4C和图 4D表明静态/动态萃取时间为5 min时,目标物的回收率在80%~ 120%范围内,且方法精密度最优。
2.2.4 分散剂无水硫酸镁和样品的比例优化本研究考察了分散剂无水硫酸镁与样品的不同比例(1∶5、1∶2、1∶1、2∶1、5∶1)对目标农药提取率的影响。不同比例下,目标物的回收率均在60%~120%范围内,最终选择5∶1的无水硫酸镁与样品的比例。
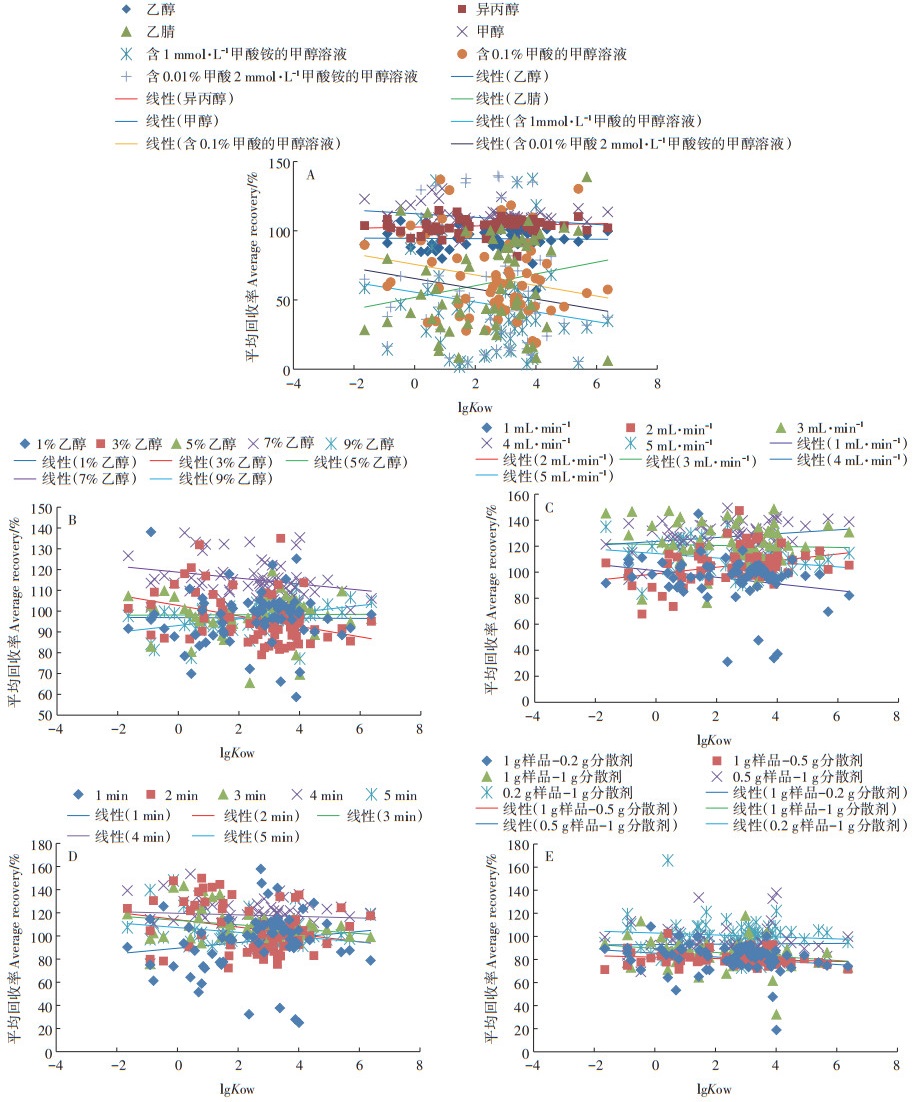
2.2.5 最优的SFE条件通过2.2.1至2.2.4的比较分析,确定最优SFE条件如下:准确称取0.200 0 g玉米粉样品,将其与1 g无水硫酸镁混合,再填入萃取池进行萃取,温度为40 ℃。提取溶剂为超临界二氧化碳∶乙醇(91∶9,V/V),静态萃取和动态萃取时间均为5 min,动态萃取流速为5 mL·min-1。此外,图 5表明,上述筛选出的最优SFE条件可以兼顾较宽的目标物极性范围。
|
图 5 不同有机溶剂与超临界流体二氧化碳组合(A)以及不同乙醇含量的超临界流体二氧化碳(B)、动态萃取流速(C)、静态/动态萃取时间(D)、样品和分散剂比例(E)等条件下目标物平均回收率及其同lg Kow的关系 Figure 5 Average recoveries of the selected pesticides at different extract solvent coupled with supercritical CO2(A), different ethanol proportions coupled with supercritical CO2(B), dynamic extraction velocities(C), static/ dynamic extraction time(D), and weight ratio of sample and dispersant (E)and their relationship with lg Kow |
选择优化好的SFE-SFC-MS/MS条件进行分析,目标化合物的校准曲线呈现良好的线性,相关系数R2均大于0.99。方法的检出限和定量限分别为0.003~ 2.770 μg·kg-1和0.01~8.41 μg·kg-1。
2.3.2 准确度和精密度玉米粉中71种农药在1、10、100 μg·kg-1时的回收率(相对标准偏差)分别为71.2%~123.4%2(.8%~ 30.5%)、94.3%~124.6%(4.9%~29.3%)、75.2%~120.4%(1.9%~28.4%),根据原农业部2386号公告[16],当农药添加浓度为1 μg·kg-1时,回收率须介于50%~120%之间,相对标准偏差≤36%;当添加浓度为10 μg·kg-1时,回收率须介于60%~120%之间,相对标准偏差≤32%;当添加浓度为100 μg·kg-1时,回收率须在70%~120%之间,相对标准偏差≤22%。本研究所建立的SFE SFC-MS/MS方法基本满足上述要求。
2.3.3 玉米粉实际样品测定在玉米样品中共有吡虫啉、三环唑和克百威3种化合物被检出,其中,1号样品检出吡虫啉(1.34 μg·kg-1)和三环唑(1.15 μg·kg-1),9号样品检出三环唑(0.89 μg·kg-1),10号样品检出克百威(1.41 μg·kg-1)。其残留浓度均小于2 μg·kg-1,符合我国农药残留限量标准的规定。
3 结论(1)本研究针对玉米粉中71种农药及代谢物残留,优化超临界流体色谱及超临界流体萃取条件,建立了一种高效、灵敏、绿色环保的在线超临界流体萃取-超临界流体色谱串联质谱分析方法,在最佳分析条件下,32 min内可以实现对71种农药残留的在线提取和精准定性定量分析。
(2)方法验证结果表明,建立的在线SFE-SFCMS/MS方法具有良好的线性、灵敏度及准确度,并具有萃取效率高、操作简便、省时、节省溶剂等优点,可以为玉米粉中农药多残留检测提供可靠的技术支撑。
| [1] |
The United Nations. Food and Agriculture Organization of the United Nations, FAO. (1945-08-09)[2021-05-01]. http://www.fao.org/faostat/en/#home.
|
| [2] |
PIZZUTTI I R, DE KOK A, ZANELLA R, et al. Method validation for the analysis of 169 pesticides in soya grain, without clean up, by liquid chromatography-tandem mass spectrometry using positive and negative electrospray ionization[J]. Journal of chromatography A, 2007, 1142(2): 123-136. DOI:10.1016/j.chroma.2006.12.030 |
| [3] |
ANDREU V, PICÓ Y. Determination of pesticides and their degradation products in soil: Critical review and comparison of methods[J]. Trends in Analytical Chemistry, 2004, 23(10/11): 772-789. |
| [4] |
FERNANDES V C, LEHOTAY S J, GEIS-ASTEGGIANTE L, et al. Analysis of pesticide residues in strawberries and soils by GC-MS/MS, LC-MS/MS and two-dimensional GC-time-of-flight MS comparing organic and integrated pest management farming[J]. Food Additives and Contaminants-Part A Chemistry, Analysis, Control, Exposure and Risk Assessment, 2013, 31(2): 262-270. |
| [5] |
张艳, 王松雪, 孙长坡. 超临界流体萃取技术在粮食农药残留检测中的应用[J]. 食品科学, 2010, 31(1): 274-277. ZHANG Y, WANG S X, SUN C P. Application of supercritical fluid extraction for detection of pesticide residues in cereal grains: A review[J]. Food Science, 2010, 31(1): 274-277. |
| [6] |
李同宾, 李红, 孙丰收, 等. QuEChERS-超高效液相色谱-串联质谱法测定玉米粉中41种农药残留[J]. 农药学学报, 2021, 23(1): 154-161. LI T B, LI H, SUN F S, et al. Determination of 41 pesticides in maize meal by QuEChERS and ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Pesticide Science, 2021, 23(1): 154-161. |
| [7] |
李菊颖, 郭欣妍, 何健, 等. 玉米粉中吡虫啉、三唑酮、乙草胺与异丙甲草胺的QuEChERS/高效液相色谱-串联质谱快速检测[J]. 分析测试学报, 2017, 36(6): 783-787. LI J Y, GUO X Y, HE J, et al. Rapid determination of imidacloprid, triadimefon, acetochlor and metolachlor in corn flour by QuEChERS/ultra-performance liquid chromatography-tandem mass spectrometry[J]. Journal of Instrumental Analysis, 2017, 36(6): 783-787. DOI:10.3969/j.issn.1004-4957.2017.06.014 |
| [8] |
叶倩, 路大海, 邓义才, 等. 气相色谱-串联质谱法快速检测玉米粉中乙草胺、异丙甲草胺和三唑酮残留[J]. 农药学学报, 2016, 18(2): 268-272. YE Q, LU D H, DENG Y C, et al. Simultaneous determination of acetochlor, metolachlor and triadimefon residue in corn flour by gas chromatography -tandem mass spectrometry[J]. Chinese Journal of Pesticide Science, 2016, 18(2): 268-272. |
| [9] |
HE Z, WANG L, PENG Y, et al. Multiresidue analysis of over 200 pesticides in cereals using a QuEChERS and gas chromatography-tandem mass spectrometry-based method[J]. Food Chemistry, 2015, 169: 372-380. DOI:10.1016/j.foodchem.2014.07.102 |
| [10] |
SONG S, ZHANG C, CHEN Z, et al. Simultaneous determination of neonicotinoid insecticides and insect growth regulators residues in honey using LC-MS/MS with anion exchanger-disposable pipette extraction[J]. Journal of Chromatography A, 2018, 1557: 51-61. DOI:10.1016/j.chroma.2018.05.003 |
| [11] |
杨直, 彭彦, 金朦娜, 等. 固相萃取-超临界流体色谱-质谱联用同时快速测定中成药和保健食品中的12种抗过敏化学药物[J]. 色谱, 2018, 36(9): 889-894. YANG Z, PENG Y, JIN M N, et al. Simultaneous rapid determination of 12 anti-allergic chemical drugs in Chinese traditional patent medicine and health food by supercritical fluid chromatography tandem mass spectrometry with solid phase extraction[J]. Chinese Journal of Chromatography, 2018, 36(9): 889-894. |
| [12] |
LIU L X, ZHANG Y, ZHOU Y, et al. The application of supercritical fluid chromatography in food quality and food safety: An overview[J]. Critical Reviews in Analytical Chemistry, 2020, 50(2): 1-25. |
| [13] |
宋镠. 超临界流体色谱-质谱法在食品成分测定中的应用[D]. 广州: 广东药科大学, 2020. SONG L. Application of supercritical fluid chromatography-mass spectrometry in determination of food ingredients[D]. Guangzhou: Guangdong Pharmaceutical University, 2020. |
| [14] |
唐广云. 超临界流体色谱串联质谱技术在食品分析中的应用[D]. 广州: 暨南大学, 2018. TANG G Y. The applications of supercritical fluid chromatography coupled with single quadrupole mass spectrometry technique in food analysis[D]. Guangzhou: Jinan University, 2018. |
| [15] |
贾小辉, 刘刚, 孙亚君, 等. 超临界CO2流体萃取红花籽油研究[J]. 粮食与油脂, 2007(3): 21-22. JIA X H, LIU G, SUN Y J, et al. Study on supercritical CO2 liquid extraction of safflower oil[J]. Cereals & Oils, 2007(3): 21-22. |
| [16] |
中华人民共和国农业农村部. 中华人民共和国农业部公告2386号. (2016-12-31)[2021-05-01]. http://www. moa. gov. cn/govpublic/ZZYGLS/201604/t20160413_5093548. htm. Ministry of Agriculture and Rural Affairs of the People's Republic of China. Announcement No. 2386 of the Ministry of Agriculture of the People's Republic of China. (2016-12-31)[2021-05-01]. http://www.moa.gov.cn/govpublic/ZZYGLS/201604/t20160413_5093548.htm. |
 2021, Vol. 40
2021, Vol. 40