2. 河北工业大学能源与环境工程学院, 天津 300401;
3. 中国科学院沈阳应用生态研究所, 沈阳 110016;
4. 高丽大学环境科学与生态工程学部韩国生物炭研究中心, 韩国 首尔 02841
2. School of Energy and Environmental Engineering, Hebei University of Technology, Tianjin 300401, China;
3. Institute of Applied Ecology, Chinese Academy of Sciences, Shenyang 110016, China;
4. Korea Biochar Research Center Division of Environmental Science and Ecological Engineering, Korea University, Seoul 02841, Korea
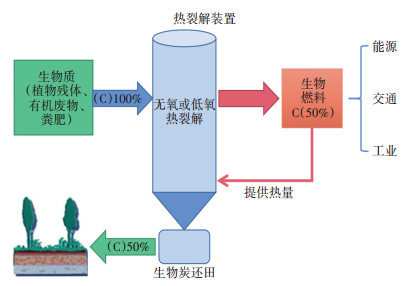
生物炭是生物质原料在完全绝氧或部分缺氧条件下经热裂解产生的一类富碳、高度芳香化且稳定性较高的固体产物[1]。由于生物炭具有丰富的孔隙结构、较大的比表面积、一定的持水性和丰富的官能团等特征,其广泛应用于土壤修复、污水处理、制备能源和功能材料等方面[2]。生物质原料来源广泛,包括农作物秸秆、森林残留物、木屑、活性污泥、动物粪便和有机固体废物等[3]。我国是农业种植大国,随着第一产业林业、牧业和渔业的发展,产生了大量以畜禽粪便、污泥和农作物秸秆为代表的有机生物质,这些生物质可以通过热解制备得到生物炭[4]。由此得到的生物炭,作为土壤改良剂和污染物吸附剂,又对土壤的改良和土壤、水体污染修复至关重要(图 1)。因此,国内外学者对生物炭的研究越来越广泛。
|
图 1 生物质热裂解转化生物炭的基本流程与产物[5] Figure 1 Flow chart and products of biochar production through biomass pyrolysis[5] |
生物质原料、制备方法、热解温度和时间会严重影响生物炭的物理和化学性质[5]。已有较多文献综述了生物炭的制备方法、表征及其在水污染修复中的应用研究进展[6-8]。比如,Meyer等[7]总结了不同制备方法(热解、气化、水热和闪蒸炭化)对生物炭性质的影响;Ahmad等[8]总结了生物炭在水体和土壤修复中的应用研究进展。除了原始的生物炭,目前,很多研究已关注到通过改性技术来提升生物炭对污染物的吸附能力以及其在环境修复应用中的可操作性(比如,通过过渡金属纳米粒子合成磁性生物炭,使生物炭更易从环境介质中分离出来)。改性技术(物理、化学和生物)对生物炭的理化性质和去除污染物的效能影响较大,然而,目前针对改性生物炭在环境修复,特别是土壤和水体污染修复中应用的综述较少。因此,本文首先综述了改性生物炭的制备方法、不同改性生物炭对污染物的吸附原理,以及改性生物炭的优缺点、使用场景等,为改性生物炭实验及改性方法提供理论依据。其次,阐述改性生物炭对土壤的修复、改良作用,以及改性生物炭对土壤中重金属和有机污染物的去除作用。特别针对研究较为广泛的磁性生物炭,重点讨论其对水中重金属和有机物的去除作用及原理,为改性生物炭在环境治理方面的推广应用提供理论依据。
1 改性生物炭的制备对生物炭的改性方法可以分为物理法、化学法和生物法,常见的主要包括球磨、酸碱/有机溶剂浸渍法、金属负载法、紫外辐射法和生物方法等,改性后生物炭对污染物具有更好的去除效果。表 1总结了不同改性方法的原理和优缺点。
|
|
表 1 常见生物炭的改性方法 Table 1 Conventional modification methods of biochar |
近年来,球磨技术应用于生物炭改性的研究已经引起广泛的重视[9-12]。球磨主要是利用小球的运动产生动能来达到破坏化学键、改变颗粒形状并产生纳米级颗粒的目的[13]。球磨后,生物炭的理化性质得到增强,比如更大的比表面积和孔容积、更负的Zeta电位、更丰富的含氧官能团和更强的污染物吸附能力。Lyu等[14-15]研究发现球磨甘蔗渣生物炭对镍和亚甲基蓝的去除率分别是原始生物炭的8倍和20倍。这主要是因为球磨可以增加生物炭的内外表面积,并暴露其石墨结构和含氧官能团。通过球磨技术还能将氮原子[16]、巯基基团[17]掺杂在生物炭表面,氮基团的掺杂提升了生物炭对二氧化碳和阴离子对活性汞的吸附性能,而巯基基团的负载使得改性生物炭对汞和甲基汞的吸附能力明显提升。综上,球磨技术是制备改性生物炭的有效方法,其通过提升生物炭的物理化学性质和吸附性能,可拓展改性生物炭在环境修复中的应用。
通过酸碱/有机溶剂浸渍法化学改性生物炭,能够使生物炭比表面积和官能团等性质发生变化,提高吸附性能。例如,通过盐酸处理生物炭能够显著增加生物炭的孔体积和官能团的数量[18]。用盐酸进行改性时,大量的氢离子会导致生物炭表面负电荷基团减少,正电荷基团增多,从而有利于生物炭吸附带负电荷的物质。王博等[19]以芦苇和香蒲为原料合成生物炭并使用浓盐酸进行改性,研究表明改性后的生物炭比表面积扩大,表面正电荷提高,为带负电荷的硝酸根提供更多吸附位点,增加了改性水生植物生物炭对硝酸盐的吸附量。而有机改性剂对生物炭改性的主要作用是增加生物炭表面的特定官能团,从而提升改性生物炭对特定污染物的吸附效果。例如,巯基(-SH)的增加能够显著增加材料对甲基汞的吸附能力。通过液相反应或者球磨法将3-巯基丙基三甲氧基硅烷与生物炭进行复合,得到巯基化改性生物炭[17],其对甲基汞和无机汞的吸附能力比原始生物炭分别提升大约10倍和3倍。Liatsou等[20]使用2-硫脲嘧啶对丝瓜生物炭纤维进行改性,结果表明改性生物炭纤维对Cu2+离子具有非常显著的亲和力和吸附性(486.9 mg·g-1),并能够对现实酸性矿山废水样品中的Cu2+离子进行选择性分离。
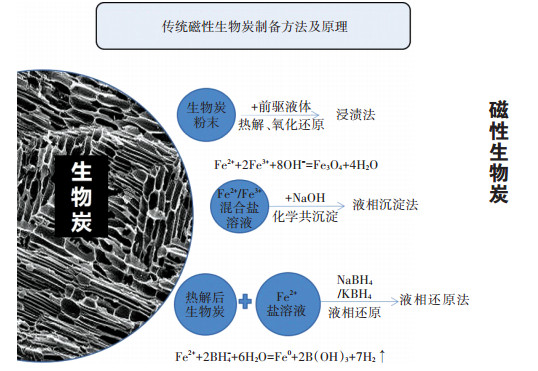
除了酸碱或有机溶剂改性,金属负载法也是一种常见的化学改性生物炭方法。它主要是指通过金属盐溶液与生物炭反应或直接将金属氧化物负载在生物炭上,将金属/金属氧化物的性质与生物炭的性质结合,从而提高改性生物炭的理化性质。例如,使用铁、钴、锰等金属或纳米粒子对生物炭进行改性合成磁性生物炭,能够有效解决生物炭颗粒易分散在水中且很难进行分离的缺点[21-22]。常见的磁改性生物炭是采用铁盐/铁的氧化物作为前驱体,包括FeCl3、FeSO4等,合成方法主要有浸渍法、液相沉淀法和液相还原法(图 2)。浸渍裂解法是将过渡金属盐溶液与生物质粉末混合,在一定时间搅拌处理后过滤干燥,然后在厌氧或惰性气体下进行热解得到磁性生物炭。Liu等[23]采用简单的浸渍裂解法将FeCl3溶液和花生壳生物质在650 ℃到800 ℃的交替热解温度下制备磁性生物炭。800 ℃下制备的磁性生物炭比表面积和孔容大,还原性铁的负荷高,对Cr(Ⅵ)和三氯乙烯(TCE)的去除率较高。共沉淀法是指生物炭与Fe2+/Fe3+的混合盐溶液充分混合,在惰性气体条件下进行不断搅拌,在一定温度下加入氢氧化钠或氢氧化铵溶液使其产生沉淀,然后经过搅拌、洗涤、干燥获得磁性生物炭[24]。还原沉淀法与共沉淀法相似,但区别之处在于生物炭与过渡金属盐溶液混合时还要加入硼氢化钠或硼氢化钾来进行还原。例如,Zhu等[25]以芦苇为原料,利用还原共沉淀的方法合成纳米级零价铁生物炭复合材料(nZVI-BC),研究表明当Fe/BC质量比为2∶1时,可以完全去除水中Cr(Ⅵ),将其还原为Cr(Ⅲ)。由于该制备方法使用的还原剂有毒且还原过程中会释放氢气,使得该方法存在一定的安全隐患。综合以上合成方法,在制备磁性生物炭用于去除污染物之前,应考虑目标污染物的特征及各个方法的优缺点,选择合适的合成方法。
以上化学改性均需要引入化学药剂,可能带来二次污染。还有一种常见的化学改性生物炭方法是紫外辐射法,其本质也是通过热改性,利用辐射的方法使生物炭表面发生化学反应,产生利于与污染物发生反应的官能团[26]。紫外辐射的优点是可防止其他改性试剂的引入而带来的二次污染问题。紫外辐射改性生物炭主要是提高生物炭表面的官能团,主要为羧基(-COOH)、内酯(C=O)和羟基(-OH)。在这些性质的促进下,改性生物炭对污染物,比如Cd(Ⅱ)、Cr(Ⅵ)和苯的去除能力均能显著提升[27]。但需要注意的是,紫外辐射改性存在耗能较大的问题,不利于大规模推广应用。
生物法改性生物炭是一个相对较新的概念,它是将某些具有特定功能的微生物与生物炭结合进而改善其表面特征的一种方法。对生物质原料或者生物炭进行细菌处理,尤其是厌氧消化或生物燃料工艺[28],均被证明能有效生产具备生物活化性能的生物炭。Luo等[29]首次提出通过培养富铁金孢菌将铁离子嵌入到微生物细胞中,从而得到富含铁的生物质原材料。经过700 ℃氩气环境下裂解得到磁性生物炭材料。研究表明,该改性生物炭具备较大的比表面积(1 986 m2·g-1)和较高的双氯芬酸去除能力(361.25 mg·g-1);同时因具备磁性而易于固液分离。利用生物法改性生物炭的优势是节能环保,生物炭为微生物提供栖息场所,得到的改性生物炭能够有效降解有机污染物,值得深入研究并推广。
综上所述,改性生物炭技术代表了一个新的研究领域。改性技术通过增加生物炭的比表面积、孔体积、含氧官能团、Zeta电位以及吸附能力来提升原始生物炭的性能。获得的改性生物炭具有高效、成本低、环境友好的优势,在许多领域,尤其是环境修复领域中具有巨大的应用潜力。
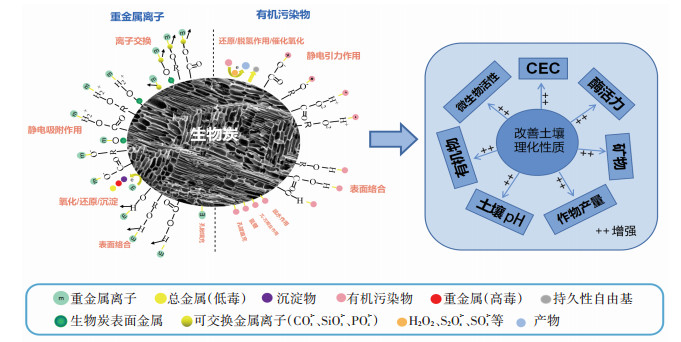
2 生物炭及改性生物炭在土壤改良和污染修复中的应用 2.1 土壤理化性质的改良生物炭已被广泛应用于土壤改良和污染修复。如图 3所示,生物炭不仅能够有效修复土壤有机和重金属污染,还能够改良土壤性质。本章节将主要论述生物炭对土壤理化性质的影响,这些影响主要表现在土壤容重、微生物活性、持水能力、pH、阳离子交换量、农作物产量等方面。
不同类型的土壤容重差异较大。通常来说,向土壤中加入生物炭会降低其容重,从而影响微生物的活性。对82篇相关文献的荟萃分析表明,对所有类型的土壤来说,生物炭的添加将土壤容重平均降低了9%[30],这些结果可归因于生物炭的容重(< 0.6 g·cm-3)普遍比土壤的容重(1.25 g·cm-3)更低。土壤容重降低后,微生物的活性和群落组成会在一定程度上增加。Zheng等[31]研究发现添加生物炭(40 t·hm-2)可显著改变酸性稻田土壤的细菌和真菌群落结构;生物炭增加了细菌的α多样性,但降低了真菌的多样性;与未经处理的土壤相比,经生物炭处理的土壤中变形菌门和担子菌门的相对丰度分别降低了11%和66%,而接合菌门的相对丰度提高了147%。根据实验结果可知,施加生物炭后酸性稻田土壤细菌和真菌群落结构得到改善,处理后的土壤更适合水稻生长,增加稻田产量。
土壤持水能力对作物生长至关重要,其主要受土壤的质地和有机质含量的影响。添加生物炭能有效提高土壤的持水能力。例如,以2%和10%的比例施用生物炭可使稻田土壤的持水能力平均提高9%。研究发现,添加生物炭增加了53~250 mm大小的土壤团聚体的数量,这表明生物炭主要是通过改变土壤孔径分布来提高土壤的持水能力[32]。此外,生物炭添加也能够改变土壤pH值。通常,气候越潮湿,土壤的pH值越低。因此,在干旱或半干旱地区,土壤多数为碱性,而在潮湿地区则多数为酸性。由于大多数生物炭是碱性或弱碱性,在碱性土壤上施用时,土壤的pH值受到的影响很小。例如,当将pH为10.4的生物炭添加到pH为8.38的灰壤土中时,土壤的酸度没有变化[33];但将pH为7.25的生物炭添加到pH为8.34的碱性砂壤土中时,土壤碱度降低了5%[34]。这可能有3个方面的原因:一是低pH生物炭对土壤的稀释作用;二是热解不完全的生物炭表面上的酸性物质对土壤碱度的中和;三是生物炭的添加增加了土壤阳离子交换量,高阳离子交换量可以提高土壤pH缓冲能力。对于酸性土壤来说,添加生物炭会增加土壤pH值。Gul等[35]研究发现生物炭中大量的碳酸盐、碳酸氢盐和硅酸盐能够提高土壤的pH值,从而利于酸性土壤改良。
可见,生物炭较高的孔隙率、较大的比表面积、丰富的有机碳和官能团,可以降低土壤的容重,促进微生物生长,为土壤提供大量的有机物[23],增加土壤的持水保肥能力[21]。然而,目前针对改性生物炭在土壤性质改良中的应用研究较少,需要进一步的研究。
2.2 土壤污染修复除了用于改良土壤性质,生物炭及改性生物炭对土壤中有机和无机污染物的修复也引起了学界的广泛兴趣。土壤理化性质(比如pH值、温度、有机物和氧化还原电位)可能会对生物炭与污染物的反应产生干扰,因此,改性生物炭能够在一定程度上提高其对土壤污染物的修复效果。本章节将从土壤有机污染物和无机污染物两部分进行讨论。
2.2.1 土壤有机污染物修复土壤中有机污染物主要来源于抗生素、农药残留物、石油化工行业废渣废水等[36-37]。这些有机污染物存在于土壤中,其中的有害成分如抗生素罗沙胂(ROX)等对土壤生物的生长造成了一定的影响,长期存在可能会造成作物减产危害。研究表明,生物炭及改性生物炭能够有效去除土壤中有机污染物。You等[38]利用添加生物炭的土壤培养韭黄,并观察韭黄中噻虫嗪(THI)的含量,结果发现韭黄对噻虫嗪及其代谢产物(CLO)的吸收量减少,这说明生物炭对噻虫嗪这类新型碱烟类农药具有较高的吸附性,能够降低其在土壤中的生物有效性。Zheng等[39]研究了芦苇生物炭固有矿物质和低分子量有机酸(LMWOA)对生物炭吸附毒死蜱和甲基毒死蜱的影响,研究表明,脱灰处理和LMWOA老化处理可以使生物炭暴露出更多的碳表面积和孔隙,能够增加毒死蜱和甲基毒死蜱的吸附量。改性生物炭在土壤修复中的优势主要体现在提升修复效果和利于回收两方面。Zhu等[40]通过共沉淀方法制备了具备磁性的针铁矿改性生物炭(GMB),用于去除土壤中抗生素罗沙胂(ROX)等污染物,研究发现GMB-600-1(600 ℃,1 h)表现出良好的理化特性,能使土壤中ROX的有效性降低70.8%,是一种可回收的多功能土壤修复材料。
氯代有机物作为一种重要的有机溶剂和产品中间体,在很多工业中得以广泛使用,但却是“三致”(致癌、致畸、致突变)物质。生物炭及改性生物炭在土壤氯代有机物污染修复方面具有广泛的应用前景。目前研究较多的主要是通过铁改性生物炭,提高改性生物炭对氯代有机物的降解能力,从而实现氯代有机物的无害化。常用的是零价铁改性生物炭,Devi等[41]通过NaBH4还原Fe2+的方法制备了零价铁负载生物炭复合材料(ZVI-MBC),并研究了其对五氯苯酚脱氯的有效性的影响。研究发现水溶液中氯离子的浓度随反应时间的增加而增加,表明ZVI-MBC复合材料对五氯苯酚具有脱氯作用;该生物炭材料在促进五氯苯酚吸附的同时也进行了脱氯反应,从而降低了五氯苯酚的毒性。Liu等[42]使用在650~800 ℃下热解FeCl3溶液处理过的生物质炭来制备磁性FeBCs复合材料。在不同的生物炭热解温度下,所有磁性FeBCs复合材料都能有效去除三氯乙烯(TCE)。另外,用2 g·L-1的FeBC800可以完全去除0.07 mmol·L-1的三氯乙酸。与BC800相比,FeBC800的TCE去除速率更快,这表明铁在磁性生物炭去除TCE中的重要作用。
生物炭及改性生物炭对土壤中有机污染物的修复原理主要包括静电吸附、表面络合和还原。因此,将生物炭/改性生物炭应用于土壤有机污染修复时,应针对污染物的性质来选择合适的生物炭。另外,土壤中的土著微生物会在一定程度上影响生物炭对污染物的去除效果,而目前的研究还较少关注这一方面。因此,在研究土壤有机污染修复时,应更多关注生物炭及改性生物炭与微生物协同降解污染物的效果和机理,提高材料的实际应用前景。
2.2.2 土壤重金属修复土壤中的重金属主要来自采矿业、工业固体废弃物和废水。重金属污染的土壤不仅影响农作物生长,更令人担忧的是食用受污染土壤上种植的农作物会严重危害人体健康。土壤中常见的重金属污染物包括镉(Cd)、铅(Pb)、砷(As)、铜(Cu)、铬(Cr)和锌(Zn)等。生物炭及改性生物炭对重金属的去除机理主要包括离子交换、共沉淀、表面络合和静电吸附等[43]。
镉和锌是同族元素,在自然界中镉常与锌、铅共生。当环境受到镉污染后,镉可在生物体内富集,通过食物链进入人体引起慢性中毒。研究表明,生物炭表面负电荷含量越少越有利于其对土壤中镉的吸附。因此,在800 ℃热解温度下制备的低表面电荷生物炭对土壤中镉的固定效果明显优于低裂解温度制备的生物炭[44]。Nigam等[45]研究发现与其他有机肥相比,生物炭是降低土壤中生物可利用铅和镉的有效途径,并且能够提高农作物产量。与原始生物炭相比,改性生物炭能够针对性地提高对镉的固定效果。有研究表明,硫改性的生物炭和硫铁改性的生物炭可以增加土壤中有机质含量,降低镉的生物有效性,同时还提高了土壤中微生物的丰富度和均匀度[46]。Irshad等[47]利用针铁矿改性生物炭(GB),并探讨了不同生物炭和改性生物炭对土壤-水稻体系中镉迁移和转移的影响。结果表明,GB可以通过提高pH值和改变镉比例来减少根际孔隙水中的镉,增强水稻植物抗镉氧化损伤的能力,并且可以增强铁斑的形成并抑制水稻中镉的积累。
砷和某些砷化合物是致癌物质,过量摄入会引发皮肤、心血管、呼吸系统和神经系统癌变,因此土壤中砷的去除也是研究的重点问题。Lin等[48]成功制备出铁锰改性生物炭复合物,并将其应用到砷污染土壤中。结果发现,改性生物炭能够显著提高土壤氧化还原电位,降低砷的生物有效性,促进原本呈现出非特异性吸收和特异性结合的砷转化为残留无定形的水合氧化物和结晶水合氧化物形式,更有利于土壤微生物成长。Lin等[49]通过分析砷的分馏、酶活性和细菌丰度,研究铁锰改性生物炭复合物(FMBCs)在淹水稻田中对毒性砷挥发的潜在作用。结果表明,FMBCs减少了毒性砷从污染土壤中的挥发,并且在较高剂量下作用更为明显。Zhang等[50]以磷酸钾(K3PO4)为原料,对木材、竹子、玉米秸秆、稻壳等生物质原料进行热解,制备了新型磷改性生物炭,并研究改性生物炭对土壤重金属固定性能及机理。结果表明,磷改性的稻壳和玉米秸秆生物炭对Cd(Ⅱ)和Cu(Ⅱ)的固定化效率分别比另外两种改性生物炭高14%~24% 和19%~33%;而无论采用何种原料,添加磷都能提高As(Ⅴ)的提取率和迁移率。
改性生物炭能够吸附土壤重金属,减少重金属在土壤和作物中的累积,提高农作物的产量。目前,在土壤重金属污染修复的问题上更倾向于多种重金属共同研究,利用生物炭及改性生物炭对重金属污染的土壤进行一体化修复具有重要的现实意义。然而,改性后的生物炭在土壤中的矿化行为尚未见系统的研究,其在土壤中的迁移行为对土壤微生物的长期效应也亟须深入研究。
3 生物炭及改性生物炭在废水处理中的应用已有较多的文献综述了生物炭及改性生物炭在废水处理中的应用。例如,Inyang等[51]讨论了生物炭对水中重金属的去除研究进展;Wang等[52]重点研究了零价铁改性生物炭在环境修复中的应用。然而,由于生物炭颗粒较小,易分散在水中,在处理污水后很难将其分离。并且生物炭中可能存在一定污染物,如不及时分离会造成二次污染,也不利于生物炭回收利用。传统的分离方法包括过滤和离心等,操作复杂且成本高,为了解决这一难题,利用铁、镍、钴等过渡金属及其氧化物颗粒磁化生物炭,使其在外界磁场的作用下分离出来,避免产生二次污染,实现多次回收利用[53]。目前常用的磁改性生物炭的方法是采用铁及其氧化物(例如Fe3O4、FeCl3、FeSO4等),也有部分研究选择镍、钴、稀土元素La(OH)3等[53]。铁在环境中储量丰富,因此应用最为广泛。而贵金属和稀土元素存在价格昂贵、来源有限等缺点,目前在磁性生物炭的研究中应用较少。接下来将重点总结磁性生物炭在废水处理中的应用,其机理方面可分为吸附和催化,目标污染物包括重金属、无机阴离子、有机污染物。
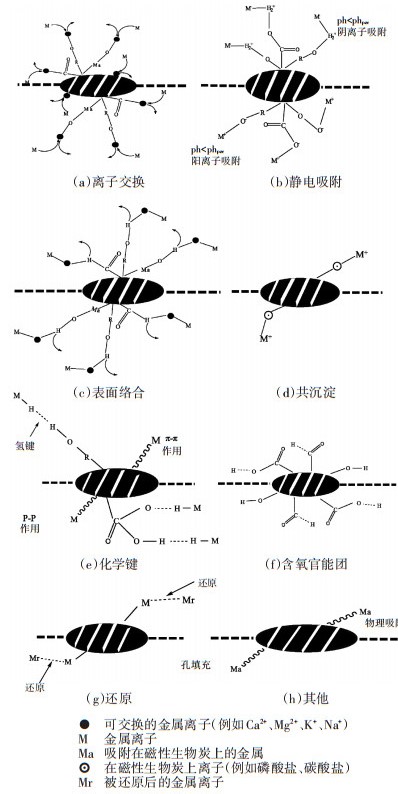
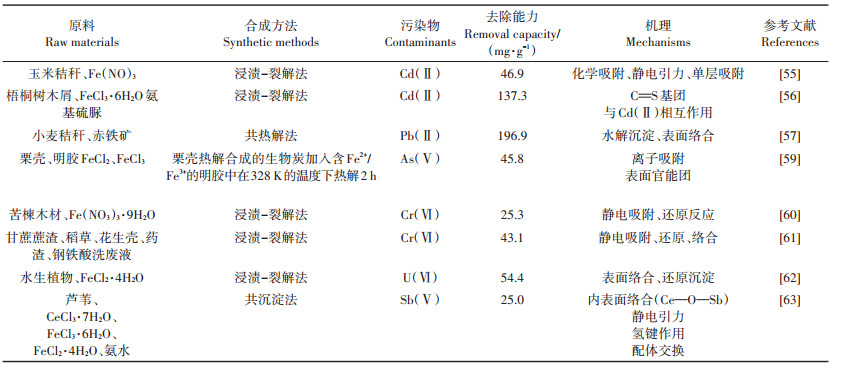
3.1 吸附废水中的重金属与生物炭相比,磁性生物炭对重金属的去除机理类似,主要有离子交换、静电吸附、表面络合、沉淀作用、化学键、官能团和还原作用(图 4)[53]。由于磁性生物炭具有更多的官能团、更强的静电吸附能力和还原能力(负载还原性铁的生物炭),因此磁性生物炭对重金属的去除能力更强。镉、铅、砷、铬等是工业废水中常见的有毒重金属离子,若不经处理直接将废水排放到环境中,将对人体健康产生严重威胁[54-56]。即利用磁性生物炭吸附是一种可以去除水中污染物的新型方法。因此,人们开发出既实用又有效的方法,利用磁性生物炭的吸附性能在去除废水中重金属的同时将其从水溶液中分离出来循环利用。表 2总结了磁性生物炭对重金属的吸附性能和机理。
|
|
表 2 磁性生物炭吸附重金属的应用 Table 2 Application of magnetic biological carbon in adsorbing heavy metals |
对于镉来说,无论是磁性生物炭[54]还是氨基硫脲改性的磁性生物炭[56],均对其具有很好的去除效果。其机理主要是通过化学吸附、静电引力、单层吸附以及C=S基团对Cd(Ⅱ)的去除。此外,磁性生物炭在外加磁力的作用下能够很容易地被收集起来重复利用。研究表明热解温度和时间能够影响磁性生物炭的孔结构、表面积、铁价态和磁化率,比如在800 ℃下热解2 h得到的磁性生物炭对Pb(Ⅱ)的吸附能力最佳,且PbOHCl的水解沉淀和表面络合是Pb(Ⅱ)的主要去除机制[57]。除了外加过渡金属之外,在制备生物炭时采用富含金属的生物质原材料也是制备磁性生物炭的一种有效方法。Cho等[58]以CO2为反应介质,热解造纸污泥使铁转化为氧化铁,同时生成合成气和磁性生物炭,作为As(Ⅴ)的吸附剂。研究表明含铁、钙固体矿物的磁性生物炭对As(Ⅴ)有较强的吸附力,最大吸附量达到34.1 mg·g-1。除了粉末状的材料,磁性生物炭还可制备成明胶微球,这样可以扩大生物炭的比表面积,增加对重金属的吸附位点,是处理含As(Ⅴ)废水的有效材料[59]。针对Cr(Ⅵ)和U(Ⅵ),磁性生物炭的去除机理除了传统的吸附,还能通过还原作用将高价态的金属还原为低价态的金属,降低其毒性。例如,对于Cr(Ⅵ),磁性生物炭对Cr(Ⅵ)吸附能力明显增强,且吸附后MMABC仍保持饱和磁化强度(16.1 emu·g-1)[60]。生物质原材料也会对磁性生物炭去除重金属的性能产生影响,Yi等[61]首次利用钢铁酸洗废液(作为铁盐)和甘蔗渣、稻草、花生壳、草本残渣制备了4种类型的磁性生物炭,考察生物质原料对磁性生物炭结构反应活性的影响。其中,磁性甘蔗渣生物炭对Cr(Ⅵ)的吸附性最高,且磁性生物炭中的总铁,尤其是Fe(Ⅱ),对Cr(Ⅵ)的去除和还原起主导作用。除了以上几种重金属离子外,U(Ⅵ)等具有放射性和毒性的离子越来越受人们的关注。磁性氧化铁/生物炭在pH为3.0和293 K条件下,对U(Ⅵ)具有较大的去除能力。磁性生物炭首先通过内球表面络合作用吸附U(Ⅵ),然后磁性生物炭上Fe(Ⅱ)将U(Ⅵ)部分还原为U(Ⅳ),从而实现对U(Ⅵ)的有效去除[62]。
3.2 吸附废水中无机阴离子在许多水源中已经发现存在大量的无机化合物,包括阴离子如硝酸盐、磷酸盐、碳酸盐、氯酸盐、溴酸盐、砷酸盐和氟化物以及某些条件下的金属型阴离子。生物炭及改性生物炭对无机阴离子具有较好的去除效果。有些研究表明,磁改性之后,生物炭的比表面积减小,但是磁性生物炭对PO43-的去除能力却明显提升近一倍,这是由于磁改性生物炭更高的等电位点利于其通过静电吸附去除阴离子,并且其高重复利用的潜力可高效经济地回收磷酸盐[64]。通过改变溶液条件,发现磷的吸附不仅受pH的影响,且砷酸盐和碳酸盐的存在也会抑制磷的吸附[65]。也有研究表明,在pH=2~10的范围内,磁性生物炭对硝酸盐和氟化物的吸附能力均保持较高水平,且最高吸附容量分别为15 mg·g-1和9 mg·g-1,高于其他生物炭和氧化铁吸附剂的吸附容量[66]。当无机阴离子与有机物共存时,磁性生物炭表现出比非磁性生物炭更高的去除性能,且表现出了在水溶液中较好的稳定性,有机污染物和磷酸盐之间没有明显的竞争效应[67]。这表明磁性生物炭可以同时去除废水中的有机污染物和磷酸盐。综上,在无机阴离子污染的水体(比如富营养化的湖水)中,磁性生物炭具有优越的、稳定的除磷能力,且利于回收,具有较大应用前景。
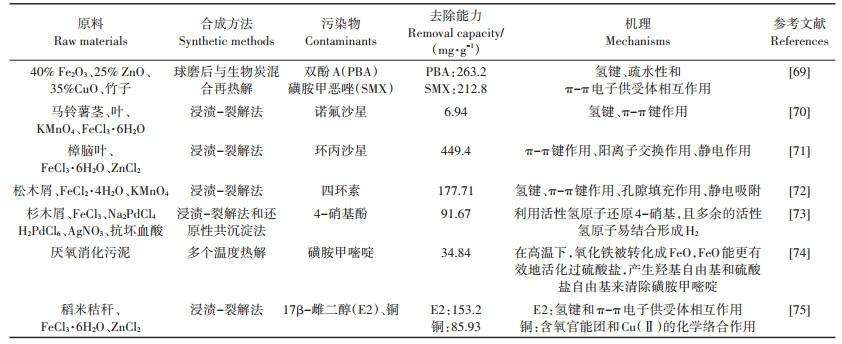
3.3 吸附废水中有机污染物磁性生物炭对水中有机污染物也表现出较高的吸附性,其有效性与芳香性指数、极性指数、比表面积和含氧官能团的数量密切相关。例如,大的比表面积利于Fe3O4纳米颗粒合成的磁性生物炭对呋喃唑酮类(FZD)抗生素的吸附效果,其中,氢键作用也对FZD的去除起到重要作用[68]。当双酚A和磺胺甲恶唑共存时,CuZnFe2O4-生物炭可以对两种污染物均保持较高的去除效率(> 90%),且具有易分离、可多次重复利用等优点[69]。表面活性剂的存在能够促进磁性生物炭对有机物的去除,比如Li等[70]研究阴离子表面活性剂(SDS或SDBS)对含铁糠醛渣磁性生物炭吸附诺氟沙星(NOR)的影响,研究发现有SDS和SDBS存在时,NOR的最大吸附量分别为无表面活性剂时的2.33倍和1.97倍,表明表面活性剂与磁性生物炭去除NOR之间存在协同增强作用。表 3总结了磁性生物炭吸附有机污染物的研究和相应的机理,可以看出磁性生物炭对水中的有机污染物去除效率有着良好的表现,改性后具有易分离、可重复利用、与活性剂协同作用等性能。
|
|
表 3 磁性生物炭吸附/催化降解有机污染物 Table 3 Adsorption/catalytic degradation of organic contaminant s by magnetic biological carbon |
生物炭及改性生物炭用于污染物催化可以通过以下3种方式进行:一是生物炭及改性生物炭的环境持久性自由基与O2反应以产生羟基自由基(·OH);二是生物炭及改性生物炭活化过氧化氢或过硫酸盐分别产生羟基自由基(·OH)或硫酸根自由基(SO4-·);三是生物炭及改性生物炭用作电子受体和吸附剂以提高光降解能力[76]。MnFe2O4改性得到的磁性生物炭活化过氧单硫酸盐(PMS)降解橙Ⅱ、亚甲基蓝、双酚A、磺胺嘧啶和环丙沙星的效率明显高于原始生物炭[77]。Zhang等[78]将印染废水处理过程中产生的过量生物污泥和含铁污泥在最佳水热炭化条件下制成纳米级磁性生物炭复合物,该复合物易于回收,且在Fenton反应中具备稳定且高效的亚甲基蓝降解性能,是一种可循环利用的优良催化剂。研究结果表明该方法可用于实际印染废水处理过程中污泥减量及内部循环。Yang等[79]采用CO2作为钴前体物和木质素热解的反应介质,合成磁性生物炭(CoBC)。研究表明由于CoBC具有高孔隙率、大表面积和磁性等优点,是活化水中过氧单磺酸钾(Oxone)良好的催化剂,产生的硫酸根离子能够使苋菜红(AMR)在60 min内完全脱色。Chen等[74]利用一种过氧化二硫酸盐/零价铁体系(PDS-ZVI)来破坏厌氧消化污泥中的可溶性胞外聚合物和松散结合胞外聚合物中的蛋白质,进而提升污泥的脱水性能;在此基础上,通过一步热解法合成磁性生物炭(Fe-ADSBC),研究表明ADSBC不仅作为碳载体,而且也作为碳催化剂激活PDS,促进磺胺甲嘧啶(SMT)等有机污染物的去除。Huang等[80]通过锰掺杂的磁性生物炭(MMBC)激活过硫酸盐(PS)来降解四环素(TC)。其中,MMBC-900-2h(900 ℃,2 h)的吸附和催化性能最好。电子自旋共振结果表明MMBC-PS体系生成的具有强氧化性的SO4-·和OH-·是降解TC的主要机理。
3.5 磁性生物炭的回收磁性生物炭与污染物反应后,通过外加磁场进行固液分离,材料的再生成为其能否广泛应用的重要因素之一。吸附材料再生主要是依靠脱附液与表面吸附质的离子交换作用,经脱附后仍会保留一定的吸附性能[75, 81]。磁性生物炭常见的脱附剂主要包括盐酸、氢氧化钠和甲醇等有机溶剂。Liang等[72]利用氢氧化钠对磁性生物炭进行再生,研究表明磁性生物炭对盐酸四环素的吸附能力随循环次数的增加而逐渐下降,在3个循环后吸附容量为初始值的80.6%,说明该材料具有良好的吸附性、重现性和潜在的实际应用价值。Wang等[82]研究发现甲醇溶液对磁性生物炭解吸土霉素效果最好,且经过5次循环后磁性生物炭的吸附能力稳定(约3.90 mg·g-1),约比第一次降低20%。由此可知,磁性生物炭在回收利用几次后吸附性能有所降低,其原因可能有以下几点:一是金属元素和生物炭表面的基团发生反应,形成晶体沉淀,改变了生物炭表面的化学基团、孔隙结构等,多次吸附后孔隙变少,影响吸附效果;二是磁性生物炭的电磁性作用使吸附的一些金属覆盖生物炭表面,影响继续吸附的效果。因此如何确保磁性生物炭再生后的吸附活性是今后的研究重点。
4 结论与展望本文主要综述了生物炭的改性方法以及其在环境修复中的应用,重点介绍了磁性生物炭的制备、作为吸附剂或催化剂在土壤和水污染处理中的应用以及磁性生物炭的再生与循环利用。通过对生物炭改性,可以优化生物炭理化性质和功能,但在应用过程中也存在一定不足。因此,在今后改性生物炭的研究过程中,应综合分析目标污染物及制备条件,并注意以下一些问题:一是特异性吸附有待提高。土壤和污水中通常多种重金属和有机污染物同时存在,而不同改性方法得到的生物炭复合物存在一定缺陷,对某种污染物的去除作用易受共存物的影响。因此,研究针对污染物性质而进行的特定的改性生物炭技术,并通过放大优势作用机制,从而提升改性生物炭对特定污染物的去除效果,需要进一步的探索。二是潜在的环境风险。在改性生物炭的制备过程中会产生一些有毒的副产物,在应用过程中会出现吸附污染物释放现象,易造成二次污染,且吸附后的重金属和有机污染物的处置问题也亟待解决。三是再生循环利用的吸附活性需要改善。磁性生物炭可在外界磁场作用下回收利用,但几次循环利用后吸附性能会有明显降低,研究最佳的再生方法,以及探索如何在吸附污染物的同时使得改性生物炭表面活性基团再生以保证稳定的吸附效率,还有待进一步探究。四是实际应用效果有待评价。目前对改性生物炭的研究还是仅限于单一污染物的实验模拟阶段,而应用于实际环境污染修复的可行性需要进一步验证。
| [1] |
Lehmann J, Rillig M C, Thies J, et al. Biochar effects on soil biota: A review[J]. Soil Biology and Biochemistry, 2011, 43(9): 1812-1836. DOI:10.1016/j.soilbio.2011.04.022 |
| [2] |
何选明, 冯东征, 敖福禄, 等. 生物炭的特性及其应用研究进展[J]. 燃料与化工, 2015, 46(4): 1-4. HE Xuan-ming, FENG Dong-zheng, AO Fu-lu, et al. The characteristics of biochar and its application research progress[J]. Fuel and Chemical Industry, 2015, 46(4): 1-4. DOI:10.3969/j.issn.1001-3709.2015.04.001 |
| [3] |
吕宏虹, 宫艳艳, 唐景春, 等. 生物炭及其复合材料的制备与应用研究进展[J]. 农业环境科学学报, 2015, 34(8): 1429-1440. LÜ Hong-hong, GONG Yan-yan, TANG Jing-chun, et al. Advances in preparation and applications of biochar and its composites[J]. Journal of Agro-Environment Science, 2015, 34(8): 1429-1440. |
| [4] |
王申宛, 郑晓燕, 校导, 等. 生物炭的制备、改性及其在环境修复中应用的研究进展[J]. 化工进展, 2020, 39(增刊2): 352-361. WANG Shen-wan, ZHENG Xiao-yan, XIAO Dao, et al. Research progress of production, modification and application in environment remediation of biochar[J]. Chemical Industry and Engineering Progress, 2020, 39(Suppl 2): 352-361. |
| [5] |
Premarathna K S D, Rajapaksha A U, Sarkar B, et al. Biochar-based engineered composites for sorptive decontamination of water: A review[J]. Chemical Engineering Journal, 2019, 372: 536-550. DOI:10.1016/j.cej.2019.04.097 |
| [6] |
Wang S, Zhao M, Zhou M, et al. Biochar-supported nZVI(nZVI/BC) for contaminant removal from soil and water: A critical review[J]. Journal of Hazardous Materials, 2019, 373: 820-834. DOI:10.1016/j.jhazmat.2019.03.080 |
| [7] |
Meyer S, Glaser B, Quicker P. Technical, economical, and climate-related aspects of biochar production technologies: A literature review[J]. Environmental Science & Technology, 2011, 45(22): 9473-9483. |
| [8] |
Ahmad M, Rajapaksha A U, Lim J E, et al. Biochar as a sorbent for contaminant management in soil and water: A review[J]. Chemosphere, 2014, 99: 19-33. DOI:10.1016/j.chemosphere.2013.10.071 |
| [9] |
Xiao Y, Lyu H H, Yang C L, et al. Graphitic carbon nitride/biochar composite synthesized by a facile ball-milling method for the adsorption and photocatalytic degradation of enrofloxacin[J]. Journal of Environmental Sciences, 2021, 103: 93-107. DOI:10.1016/j.jes.2020.10.006 |
| [10] |
Xiao Y, Lyu H H, Tang J C, et al. Effects of ball milling on the photochemistry of biochar: Enrofloxacin degradation and possible mechanisms[J]. Chemical Engineering Journal, 2020, 384: 123311. DOI:10.1016/j.cej.2019.123311 |
| [11] |
Zhang Q R, Wang J M, Lyu H H, et al. Ball-milled biochar for galaxolide removal: Sorption performance and governing mechanisms[J]. Science of the Total Environment, 2019, 659: 1537-1545. DOI:10.1016/j.scitotenv.2019.01.005 |
| [12] |
Lyu H H, Yu Z B, Gao B, et al. Ball-milled biochar for alternative carbon electrode[J]. Environ Sci Pollut Res Int, 2019, 26(14): 14693-14702. DOI:10.1007/s11356-019-04899-4 |
| [13] |
Lyu H H, Gao B, He F, et al. Ball-milled carbon nanomaterials for energy and environmental applications[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(11): 9568-9585. |
| [14] |
Lyu H H, Gao B, He F, et al. Experimental and modeling investigations of ball-milled biochar for the removal of aqueous methylene blue[J]. Chemical Engineering Journal, 2018, 335: 110-119. DOI:10.1016/j.cej.2017.10.130 |
| [15] |
Lyu H H, Gao B, He F, et al. Effects of ball milling on the physicochemical and sorptive properties of biochar: Experimental observations and governing mechanisms[J]. Environmental Pollution, 2018, 233: 54-63. DOI:10.1016/j.envpol.2017.10.037 |
| [16] |
Xu X Y, Zheng Y L, Gao B, et al. N-doped biochar synthesized by a facile ball-milling method for enhanced sorption of CO2 and reactive red[J]. Chemical Engineering Journal, 2019, 368: 564-572. DOI:10.1016/j.cej.2019.02.165 |
| [17] |
Lyu H H, Xia S Y, Tang J C, et al. Thiol-modified biochar synthesized by a facile ball-milling method for enhanced sorption of inorganic Hg2+ and organic CH3Hg+[J]. Journal of Hazardous Materials, 2020, 384: 121357. DOI:10.1016/j.jhazmat.2019.121357 |
| [18] |
Liu H K, Xu F, Xie Y L, et al. Effect of modified coconut shell biochar on availability of heavy metals and biochemical characteristics of soil in multiple heavy metals contaminated soil[J]. Science of the Total Environment, 2018, 645: 702-709. DOI:10.1016/j.scitotenv.2018.07.115 |
| [19] |
王博, 叶春, 李法云, 等. 水生植物制生物炭对硝态氮的吸附规律研究[J]. 中国环境科学, 2017, 37(1): 116-122. WANG Bo, YE Chun, LI Fa-yun, et al. Study on the adsorption law of nitrate nitrogen on biochar from aquatic plants[J]. China Environmental Science, 2017, 37(1): 116-122. |
| [20] |
Liatsou I, Pashalidis I, Dosche C. Cu(Ⅱ) adsorption on 2-thiouracil-modified Luffa cylindrica biochar fibres from artificial and real samples, and competition reactions with U(Ⅵ)[J]. Journal of Hazardous Materials, 2020, 383: 120950. DOI:10.1016/j.jhazmat.2019.120950 |
| [21] |
Fang L, Li J S, Donatello S, et al. Use of Mg/Ca modified biochars to take up phosphorus from acid-extract of incinerated sewage sludge ash(ISSA) for fertilizer application[J]. Journal of Cleaner Production, 2020, 244: 118853. DOI:10.1016/j.jclepro.2019.118853 |
| [22] |
Xu K N, Zhang C K, Dou X M, et al. Optimizing the modification of wood waste biochar via metal oxides to remove and recover phosphate from human urine[J]. Environmental Geochemistry and Health, 2019, 41: 1767-1776. DOI:10.1007/s10653-017-9986-6 |
| [23] |
Liu Y Y, Sohi S P, Liu S Y, et al. Adsorption and reductive degradation of Cr(Ⅵ) and TCE by a simply synthesized zero valent iron magnetic biochar[J]. Journal of Environmental Management, 2019, 235: 276-281. |
| [24] |
Zhou J Y, Liu Y Y, Han Y T, et al. Bone-derived biochar and magnetic biochar for effective removal of fluoride in groundwater: Effects of synthesis method and coexisting chromium[J]. Water Environment Research, 2019, 91(7): 588-597. DOI:10.1002/wer.1068 |
| [25] |
Zhu S S, Huang X C, Wang D W, et al. Enhanced hexavalent chromium removal performance and stabilization by magnetic iron nanoparticles assisted biochar in aqueous solution: Mechanisms and application potential[J]. Chemosphere, 2018, 207: 50-59. DOI:10.1016/j.chemosphere.2018.05.046 |
| [26] |
李桥, 高屿涛, 姜蔚, 等. 紫外辐照改性生物炭对土壤中Cd的稳定化效果[J]. 环境工程学报, 2017, 11(10): 5708-5714. LI Qiao, GAO Yu-tao, JIANG Wei, et al. Stabilization of Cd contaminated soil by ultraviolet irradiation modified biochar[J]. Chinese Journal of Environmental Engineering, 2017, 11(10): 5708-5714. DOI:10.12030/j.cjee.201611090 |
| [27] |
Peng Z Y, Zhao H, Lyu H H, et al. UV modification of biochar for enhanced hexavalent chromium removal from aqueous solution[J]. Environmental Science and Pollution Research, 2018, 25(11): 10808-10819. DOI:10.1007/s11356-018-1353-3 |
| [28] |
Yao Y, Gao B, Wu F, et al. Engineered biochar from biofuel residue: Characterization and its silver removal potential[J]. ACS Applied Materials Interfaces, 2015, 7(19): 10634-10640. DOI:10.1021/acsami.5b03131 |
| [29] |
Luo H Q, Zhang Y K, Xie Y, et al. Iron-rich microorganism-enabled synthesis of magnetic biocarbon for efficient adsorption of diclofenac from aqueous solution[J]. Bioresource Technology, 2019, 282: 310-317. DOI:10.1016/j.biortech.2019.03.028 |
| [30] |
Razzaghi F, Obour P B, Arthur E. Does biochar improve soil water retention? A systematic review and meta-analysis[J]. Geoderma, 2020, 361: 114055. DOI:10.1016/j.geoderma.2019.114055 |
| [31] |
Zheng J F, Chen J H, Pan G X, et al. Biochar decreased microbial metabolic quotient and shifted community composition four years after a single incorporation in a slightly acid rice paddy from southwest China[J]. Science of the Total Environment, 2016, 571: 206-217. DOI:10.1016/j.scitotenv.2016.07.135 |
| [32] |
Yoo G Y, Kim H J, Chen J J, et al. Effects of biochar addition on nitrogen leaching and soil structure following fertilizer application to rice paddy soil[J]. Soil Science Society of America Journal, 2014, 78(3): 852-860. DOI:10.2136/sssaj2013.05.0160 |
| [33] |
Zhang A F, Liu Y M, Pan G X, et al. Effect of biochar amendment on maize yield and greenhouse gas emissions from a soil organic carbon poor calcareous loamy soil from Central China Plain[J]. Plant and Soil, 2012, 351: 263-275. DOI:10.1007/s11104-011-0957-x |
| [34] |
Zhang X, Qu J S, Li H, et al. Biochar addition combined with daily fertigation improves overall soil quality and enhances water-fertilizer productivity of cucumber in alkaline soils of a semi-arid region[J]. Geoderma, 2020, 363: 114170. DOI:10.1016/j.geoderma.2019.114170 |
| [35] |
Gul S, Whalen J K, Thomas B W, et al. Physico-chemical properties and microbial responses in biochar-amended soils: Mechanisms and future directions[J]. Agriculture, Ecosystems & Environment, 2015, 206: 46-59. |
| [36] |
王雪玉, 刘金泉, 胡云, 等. 生物炭对黄瓜根际土壤细菌丰度、速效养分含量及酶活性的影响[J]. 核农学报, 2018, 32(2): 370-376. WANG Xue-yu, LIU Jin-quan, HU Yun, et al. Effect of biochar on microorganism, nutrient content and enzyme activity of cucumber rhizosphere soil[J]. Journal of Nuclear Agricultural Sciences, 2018, 32(2): 370-376. |
| [37] |
Gundale M J, Deluca T H. Charcoal effects on soil solution chemistry and growth of Koeleria macrantha in the ponderosa pine/Douglas-fir ecosystem[J]. Biology and Fertility of Soils, 2007, 43(3): 303-311. |
| [38] |
You X W, Jiang H T, Zhao M, et al. Biochar reduced Chinese chive (Allium tuberosum) uptake and dissipation of thiamethoxam in an agricultural soil[J]. Journal of Hazardous Materials, 2020, 390: 121749. DOI:10.1016/j.jhazmat.2019.121749 |
| [39] |
Zheng H, Zhang Q, Liu G C, et al. Characteristics and mechanisms of chlorpyrifos and chlorpyrifos-methyl adsorption onto biochars: Influence of deashing and low molecular weight organic acid(LMWOA) aging and co-existence[J]. Science of the Total Environment, 2019, 657: 953-962. DOI:10.1016/j.scitotenv.2018.12.018 |
| [40] |
Zhu S H, Zhao J J, Zhao N, et al. Goethite modified biochar as a multifunctional amendment for cationic Cd(Ⅱ), anionic As(Ⅲ), roxarsone, and phosphorus in soil and water[J]. Journal of Cleaner Production, 2020, 247: 119579. DOI:10.1016/j.jclepro.2019.119579 |
| [41] |
Devi P, Saroha A K. Synthesis of the magnetic biochar composites for use as an adsorbent for the removal of pentachlorophenol from the effluent[J]. Bioresource Technology, 2014, 169: 525-531. DOI:10.1016/j.biortech.2014.07.062 |
| [42] |
Liu Y Y, Sohi S P, Liu S Y, et al. Adsorption and reductive degradation of Cr(Ⅵ) and TCE by a simply synthesized zero valent iron magnetic biochar[J]. Journal of Environmental Management, 2019, 235: 276-281. |
| [43] |
Wang L, Wang Y J, Ma F, et al. Mechanisms and reutilization of modified biochar used for removal of heavy metals from wastewater: A review[J]. Science of the Total Environment, 2019, 668: 1298-1309. DOI:10.1016/j.scitotenv.2019.03.011 |
| [44] |
Tan Z X, Yuan S N, Hong M F, et al. Mechanism of negative surface charge formation on biochar and its effect on the fixation of soil Cd[J]. Journal of Hazardous Materials, 2020, 384: 121370. DOI:10.1016/j.jhazmat.2019.121370 |
| [45] |
Nigam N, Yadav V, Khare P, et al. Exploring the benefits of biochar over other organic amendments for reducing of metal toxicity in Withania somnifera[J]. Biochar, 2019, 1: 293-307. DOI:10.1007/s42773-019-00023-4 |
| [46] |
Wu L P, Wei C B, Zhang S R, et al. MgO-modified biochar increases phosphate retention and rice yields in saline-alkaline soil[J]. Journal of Cleaner Production, 2019, 235: 901-909. DOI:10.1016/j.jclepro.2019.07.043 |
| [47] |
Irshad M K, Chen C, Noman A, et al. Goethite-modified biochar restricts the mobility and transfer of cadmium in soil-rice system[J]. Chemosphere, 2020, 242: 125152. DOI:10.1016/j.chemosphere.2019.125152 |
| [48] |
Lin L, Li Z Y, Liu X W, et al. Effects of Fe-Mn modified biochar composite treatment on the properties of As-polluted paddy soil[J]. Environmental Pollution, 2019, 244: 600-607. DOI:10.1016/j.envpol.2018.10.011 |
| [49] |
Lin L, Song Z G, Liu X W, et al. Arsenic volatilization in flooded paddy soil by the addition of Fe-Mn-modified biochar composites[J]. Science of the Total Environment, 2019, 674: 327-335. DOI:10.1016/j.scitotenv.2019.04.144 |
| [50] |
Zhang H, Shao J A, Zhang S H, et al. Effect of phosphorus-modified biochars on immobilization of Cu(Ⅱ), Cd(Ⅱ), and As(Ⅴ) in paddy soil[J]. Journal of Hazardous Materials, 2020, 390: 121349. DOI:10.1016/j.jhazmat.2019.121349 |
| [51] |
Inyang M I, Gao B, Yao Y, et al. A review of biochar as a low-cost adsorbent for aqueous heavy metal removal[J]. Critical Reviews in Environmental Science and Technology, 2016, 46(4): 406-433. DOI:10.1080/10643389.2015.1096880 |
| [52] |
Wang S S, Zhao M Y, Zhou M, et al. Biochar-supported nZVI(nZVI/BC) for contaminant removal from soil and water: A critical review[J]. Journal of Hazardous Materials, 2019, 373: 820-834. DOI:10.1016/j.jhazmat.2019.03.080 |
| [53] |
Zhang Y, Akindolie M S, Tian X, et al. Enhanced phosphate scavenging with effective recovery by magnetic porous biochar supported La(OH) 3:Kinetics, isotherms, mechanisms and applications for water and real wastewater[J]. Bioresource Technology, 2021, 319: 124232. DOI:10.1016/j.biortech.2020.124232 |
| [54] |
吴明山, 马建锋, 杨淑敏, 等. 磁性生物炭复合材料研究进展[J]. 功能材料, 2016, 7(7): 7028-7033. WU Ming-shan, MA Jian-feng, YANG Shu-min, et al. Progress of the magnetic biochar composite materials[J]. Journal of Functional Materials, 2016, 7(47): 7028-7033. |
| [55] |
Khan Z H, Gao M L, Qiu W W, et al. Mechanisms for cadmium adsorption by magnetic biochar composites in an aqueous solution[J]. Chemosphere, 2020, 246: 125701. DOI:10.1016/j.chemosphere.2019.125701 |
| [56] |
Li R H, Liang W, Huang H, et al. Removal of cadmium(Ⅱ) cations from an aqueous solution with aminothiourea chitosan strengthened magnetic biochar[J]. Journal of Applied Polymer Science, 2018, 135(19): 46239. DOI:10.1002/app.46239 |
| [57] |
Zhao Y L, Zhang R Y, Liu H B, et al. Green preparation of magnetic biochar for the effective accumulation of Pb(Ⅱ): Performance and mechanism[J]. Chemical Engineering Journal, 2019, 375: 122011. DOI:10.1016/j.cej.2019.122011 |
| [58] |
Cho D W, Kwon G, Yoon K, et al. Simultaneous production of syngas and magnetic biochar via pyrolysis of paper mill sludge using CO2 as reaction medium[J]. Energy Conversion and Management, 2017, 145: 1-9. DOI:10.1016/j.enconman.2017.04.095 |
| [59] |
Zhou Z, Liu Y G, Liu S B, et al. Sorption performance and mechanisms of arsenic(Ⅴ) removal by magnetic gelatin-modified biochar[J]. Chemical Engineering Journal, 2017, 314: 223-231. DOI:10.1016/j.cej.2016.12.113 |
| [60] |
Zhang X, Lv L, Qin Y Z, et al. Removal of aqueous Cr(Ⅵ) by a magnetic biochar derived from Melia azedarach wood[J]. Bioresource Technology, 2018, 256: 1-10. DOI:10.1016/j.biortech.2018.01.145 |
| [61] |
Yi Y Q, Tu G Q, Zhao D Y, et al. Biomass waste components significantly influence the removal of Cr(Ⅵ) using magnetic biochar derived from four types of feedstocks and steel pickling waste liquor[J]. Chemical Engineering Journal, 2019, 360: 212-220. DOI:10.1016/j.cej.2018.11.205 |
| [62] |
Hu Q Y, Zhu Y L, Hu B W, et al. Mechanistic insights into sequestration of U(Ⅵ) toward magnetic biochar: Batch, XPS and EXAFS techniques[J]. Journal of Environmental Sciences, 2018, 70: 217-225. DOI:10.1016/j.jes.2018.01.013 |
| [63] |
Wang L, Wang J Y, Wang Z X, et al. Synthesis of Ce-doped magnetic biochar for effective Sb(Ⅴ) removal: Performance and mechanism[J]. Powder Technology, 2019, 345: 501-508. DOI:10.1016/j.powtec.2019.01.022 |
| [64] |
Ajmal Z, Muhmood A, Dong R J, et al. Probing the efficiency of magnetically modified biomass-derived biochar for effective phosphate removal[J]. Journal of Environmental Management, 2020, 253: 109730. DOI:10.1016/j.jenvman.2019.109730 |
| [65] |
Cai R, Wang X, Ji X H, et al. Phosphate reclaim from simulated and real eutrophic water by magnetic biochar derived from water hyacinth[J]. Journal of Environmental Management, 2017, 187: 212-219. |
| [66] |
Dewage N B, Liyanage A S, Pittman C U, et al. Fast nitrate and fluoride adsorption and magnetic separation from water on α-Fe2O3 and Fe3O4 dispersed on Douglas fir biochar[J]. Bioresource Technology, 2018, 263: 258-265. DOI:10.1016/j.biortech.2018.05.001 |
| [67] |
Chen B L, Chen Z M, Lv S F. A novel magnetic biochar efficiently sorbs organic pollutants and phosphate[J]. Bioresource Technology, 2011, 102(2): 716-723. DOI:10.1016/j.biortech.2010.08.067 |
| [68] |
Gurav R, Bhatia S K, Choi T R, et al. Treatment of furazolidone contaminated water using banana pseudostem biochar engineered with facile synthesized magnetic nanocomposites[J]. Bioresource Technology, 2020, 297: 122472. DOI:10.1016/j.biortech.2019.122472 |
| [69] |
Heo J Y, Yoon Y M, Lee G Y, et al. Enhanced adsorption of bisphenol A and sulfamethoxazole by a novel magnetic CuZnFe2O4-biochar composite[J]. Bioresource Technology, 2019, 281: 179-187. DOI:10.1016/j.biortech.2019.02.091 |
| [70] |
Li C J, Gao Y, Li A M, et al. Synergistic effects of anionic surfactants on adsorption of norfloxacin by magnetic biochar derived from furfural residue[J]. Environmental Pollution, 2019, 254(Part B): 113005. |
| [71] |
Hu Y, Zhu Y, Zhang Y, et al. An efficient adsorbent: Simultaneous activated and magnetic ZnO doped biochar derived from camphor leaves for ciprofloxacin adsorption[J]. Bioresource Technology, 2019, 288: 121511. DOI:10.1016/j.biortech.2019.121511 |
| [72] |
Liang J, Fang Y L, Luo Y, et al. Magnetic nanoferromanganese oxides modified biochar derived from pine sawdust for adsorption of tetracycline hydrochloride[J]. Environmental Science and Pollution Research, 2019, 26(6): 5892-5903. DOI:10.1007/s11356-018-4033-4 |
| [73] |
Jiang S F, Xi K F, Yang J, et al. Biochar-supported magnetic noble metallic nanoparticles for the fast recovery of excessive reductant during pollutant reduction[J]. Chemosphere, 2019, 227: 63-71. DOI:10.1016/j.chemosphere.2019.04.044 |
| [74] |
Chen Y D, Bai S W, Li R X, et al. Magnetic biochar catalysts from anaerobic digested sludge: Production, application and environment impact[J]. Environment International, 2019, 126: 302-308. DOI:10.1016/j.envint.2019.02.032 |
| [75] |
Yin Z H, Liu Y G, Liu S B, et al. Activated magnetic biochar by onestep synthesis: Enhanced adsorption and coadsorption for 17β-estradiol and copper[J]. Science of the Total Environment, 2018, 639: 1530-1542. DOI:10.1016/j.scitotenv.2018.05.130 |
| [76] |
Lyu H H, Zhang Q R, Shen B X. Application of biochar and its composites in catalysis[J]. Chemosphere, 2020, 240: 124842. DOI:10.1016/j.chemosphere.2019.124842 |
| [77] |
Fu H C, Ma S L, Zhao P, et al. Activation of peroxymonosulfate by graphitized hierarchical porous biochar and MnFe2O4 magnetic nanoarchitecture for organic pollutants degradation: Structure dependence and mechanism[J]. Chemical Engineering Journal, 2019, 360: 157-170. DOI:10.1016/j.cej.2018.11.207 |
| [78] |
Zhang H, Xue G, Chen H, et al. Magnetic biochar catalyst derived from biological sludge and ferric sludge using hydrothermal carbonization: Preparation, characterization and its circulation in Fenton process for dyeing wastewater treatment[J]. Chemosphere, 2018, 191: 64-71. DOI:10.1016/j.chemosphere.2017.10.026 |
| [79] |
Yang M T, Tong W C, Lee J C, et al. CO2 as a reaction medium for pyrolysis of lignin leading to magnetic cobalt-embedded biochar as an enhanced catalyst for oxone activation[J]. Journal of Colloid and Interface Science, 2019, 545: 16-24. DOI:10.1016/j.jcis.2019.02.090 |
| [80] |
Huang D L, Zhang Q, Zhang C, et al. Mn doped magnetic biochar as persulfate activator for the degradation of tetracycline[J]. Chemical Engineering Journal, 2020, 391: 123532. DOI:10.1016/j.cej.2019.123532 |
| [81] |
王靖宜, 王丽, 张文龙, 等. 生物炭基复合材料制备及其对水体特征污染物的吸附性能[J]. 化工进展, 2019, 38(8): 3838-3851. WANG Jing-yi, WANG Li, ZHANG Wen-long, et al. Preparation of biochar-based composites and their adsorption performances for characteristic contaminants in wastewater[J]. Chemical Industry and Engineering Progress, 2019, 38(8): 3838-3851. |
| [82] |
Wang Z W, Yang X, Qin T T, et al. Efficient removal of oxytetracycline from aqueous solution by a novel magnetic clay-biochar composite using natural attapulgite and cauliflower leaves[J]. Environmental Science and Pollution Research, 2019, 26: 7463-7475. DOI:10.1007/s11356-019-04172-8 |
 2021, Vol. 40
2021, Vol. 40