2. 南京农业大学资源与环境科学学院,南京 210095
2. College of Resources and Environmental Sciences, Nanjing Agricultural University, Nanjing 210095, China
随着工业的飞速发展和农药、化肥的滥用,我国耕地重金属污染程度日益加深,我国农田生态系统和农产品质量安全受到威胁[1]。陈玉鹏等[2]发现国内多个省市地区设施蔬菜集散地Cd、Pb污染严重,近30年来有大量蔬菜产品受重金属污染情况的报道[3]。在重金属污染的土壤中施加具有离子吸附特性的钝化剂可实现重金属钝化解毒修复功效,其中石灰、黏土矿物、生物炭等材料因具有调节土壤pH、吸附钝化重金属等特性而成为重金属污染农田修复的主要材料,但其使用量通常较大,潜在二次污染风险也不容乐观[4-5]。
一些植物促生细菌被用于生物钝化修复的研究和实践。XU等[6]发现菌株Raoultella sp. X13显著促进了白菜的生长,提高其生物量,并显著降低了白菜地上部Cd含量。葛占标等[7]应用Bacillus velezensis B9使小白菜地上部Cd和Pb含量比不接菌对照分别显著降低了24%和33%,B. velezensis B25使长叶莴苣地上部Cd和Pb含量比不接菌对照分别显著降低了33% 和35%。为了提高微生物在土壤中的存活率和修复效果,可将钝化剂与微生物联合使用。XIONG等[8]利用恶臭假单胞菌X4/pIME与生物炭、稻草灰、石灰等复合处理Cd污染土壤,发现最佳处理组合能使生菜地上部Cd含量降低到0.14 mg·kg-1。贺卓等[9]在田间小区试验中发现细菌联合海泡石能够显著降低辣椒和茄子果实中Pb含量,提高蔬菜品质。上述研究中采用的制剂多为实验室丰富培养基制备的菌悬液,缺乏菌悬液的发酵培养基和培养条件优化技术;且与固体菌剂相比,菌悬液在实际使用中运输和保藏不方便。多数研究中菌悬液与固体钝化剂联合使用时,并没有制备固体菌剂的过程,符合《农用微生物菌剂》(GB 20287—2006)的产品还很少见。
本实验室前期研究发现Cd耐性细菌Bacillus megaterium H3菌株显著降低了蔬菜地上部Cd、Pb含量和根际土壤有效态Cd含量,并增加了蔬菜地上部生物量[10]。因此开展菌株H3产孢培养基优化,并配合常用重金属钝化剂研发重金属阻控菌剂,通过田间小区试验考察重金属阻控菌剂减少蔬菜吸收Cd和Pb的效果和初步机制,为防控蔬菜积累重金属、改善土壤生态环境提供科学理论基础和技术支持。
1 材料与方法 1.1 材料与试剂试验菌种:以本实验室保藏的具有Pb、Cd抗性的芽孢杆菌B. megaterium H3(登录号KP159386)为供试菌株。
培养基:LB培养基,包含酵母膏5.0 g、蛋白胨10.0 g、NaCl 10.0 g、蒸馏水1 000 mL,pH 7.0。发酵培养基,包含蔗糖2.5 g、蛋白胨5.0 g、MgSO4 5.0 g、蒸馏水1 000 mL,pH 7.5。
试剂:蔗糖、玉米粉(购于安徽燕之坊食品有限公司)、糖蜜(购于广西省柳州市金黔湾糖蜜有限公司)、酵母粉、硫酸铵、大豆粉(购于安徽燕之坊食品有限公司)、CaCO3、MgSO4∙7H2O、NaCl。
供试载体:生物炭(购于寿光禾能生物科技有限公司)为限氧裂解法制备的稻壳生物炭,颗粒直径为0.5~1.0 mm,pH为(7.8±0.1),有机质含量(9.5±1.2)g∙kg-1,C含量≥46.4%,N含量≥1.3%,O含量≥21.6%,表面积15.4 m2∙g-1,未检测到Cd、Pb;海泡石(购于湘潭建联丰禾生物科技有限责任公司)为天然海泡石,化学成分为Si和Mg,未检测到Cd、Pb。供试载体均用80目试验筛过筛备用。
供试蔬菜:意大利生菜(Lactuca sativa L. var. ramosa Hort.)购于江苏农科院种子站。
1.2 试验方法 1.2.1 种子培养用接种环从斜面上挑取3环菌苔,接到装有40 mL新鲜LB液体培养基的250 mL三角瓶中,30 ℃、160 r∙min-1振荡培养20 h。
1.2.2 芽孢计数法将发酵液在80 ℃水浴槽中热处理20 min,然后采用十倍梯度稀释、涂布培养、计数,测定芽孢数量。
1.2.3 菌株H3产孢培养基优化采用单因子试验、Plackett-Burman优化试验、最陡爬坡试验和中心组合试验对菌株H3产孢培养基进行优化[11-12]。单因子试验:分别以玉米粉和糖蜜替代发酵培养基中的蔗糖,其他成分同初始发酵培养基,筛选最佳碳源;分别以硫酸铵和大豆粉替代培养基中的蛋白胨,其他成分不变,配制培养基,筛选最佳氮源;分别以硫酸镁和碳酸钙替代发酵培养基的氯化钠,其他成分不变,配制培养基,筛选最佳无机盐。将种子液接入上述培养基中,接种量为2%,30 ℃、160 r∙min-1振荡培养,于24、36、48、60、72 h取样,测定发酵液中芽孢数量,以发酵液中芽孢数量作为筛选指标。
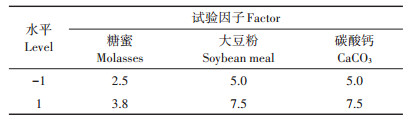
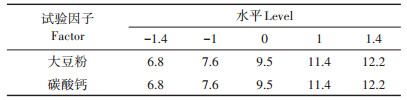
根据单因子试验结果,考察糖蜜、大豆粉和碳酸钙的添加量对芽孢数量的影响。利用Minitab 17软件进行Plackett-Burman试验设计及数据处理,每个因子取高、低两个水平,以发酵培养基的初始含量为低水平,初始含量的1.5倍作为高水平,试验设计因素水平见表 1。根据试验结果,确定添加量影响显著。以最陡爬坡试验逼近最优点的一组数据为中心点,设计2因素5水平中心组合试验,具体设计见表 2。按试验所得数据进行二次多项回归,拟合预测发酵芽孢数量最大值所对应的关键因子范围。用所得到的最佳培养基进行3次平行试验,取平均值,以验证模型是否可靠,进而得出最终优化结果。
|
|
表 1 培养基成分Plackett-Burman设计因素水平(g∙L-1) Table 1 Plackett-Burman design factor level of strain H3 medium composition (g∙L-1) |
|
|
表 2 中心组合设计各因素水平(g∙L-1) Table 2 Factor level of central composite design(g∙L-1) |
选用海泡石和生物炭作为载体,设置C1(海泡石)、C2(生物炭)、C3(生物炭50%+海泡石50%)3种处理。分别称取载体10 g装于摇瓶中,混合均匀后121 ℃间歇灭菌两次。将种子液按2%接种量接种于上述优化后发酵培养基中,30 ℃、160 r∙min-1,振荡培养48 h,获得菌株H3发酵菌液。将发酵菌液按载体与发酵菌液比例1∶2(m∶V)加入载体中,160 r∙min-1、30 ℃振荡混合均匀,放入30 ℃恒温培养箱中发酵48 h,再在50 ℃下恒温干燥,制得固体菌剂,常温保存6个月。参照《农用微生物菌剂》(GB 20287—2006)中测定方法检测菌剂中有效活菌数、杂菌数、水分、细度和pH。
1.2.5 固体菌剂阻控生菜吸收Pb、Cd试验在江苏省南京市栖霞区某农田进行田间小区试验,评价固体菌剂减少生菜Pb、Cd含量的作用。土壤基本理化性质如下:pH(6.92 ± 0.03),有机质含量(22.50±1.20)g∙kg-1,总Cd含量(1.83±0.10)mg∙kg-1,总Pb含量(256.12±12.30)mg∙kg-1。经过人工除草、翻地、晾干、碎土和平整土地等处理后,用卷尺将区域分成12个试验小区,每个小区面积为4 m2(2 m×2 m),小区之间间隔20 cm。试验设对照CK、H3发酵菌液(用量15 mL∙m-2)、生物炭(用量15 g∙m-2)、生物炭+菌株H3发酵菌液制成的固体菌剂C2(用量15 g∙m-2)4个处理,每个处理重复3次,小区随机排列。提前15 d将不同处理的材料均匀撒在小区土地上,与耕作层的土壤混匀。生菜种子经75% 酒精表面消毒5 min后,播种至装有营养土的穴盘,置于光照温室培养,定期间苗补水。15 d后移栽至各小区,常规田间管理。
收集长至成熟期的生菜植株,将植株连根带土放入灭菌袋中,带回实验室。收集附着在根系表面的土壤,即根际土壤。土壤样品放于室外自然风干,过80目试验筛,筛出细度为20 mm的土壤样品。按照WANG等[13]的方法,用DTPA提取剂提取土壤样品中有效态重金属,并用电感耦合等离子体发射光谱仪(ICP-OES)测定。土壤脲酶和蔗糖酶活性的测定参考关松荫[14]的方法。植物样品经0.01 mol∙L-1 EDTA- 2Na溶液浸泡10 min和去离子水清洗后,分为地上部与根部,测定鲜质量,烘干、粉碎,用5% HNO3消煮定容,用ICP-OES测定Cd、Pb含量。将新鲜生菜地上部研磨成匀浆,稀释后离心并去除沉淀,上清液中Vc浓度用钼蓝比色法测定。
1.2.6 数据处理方法试验中图表绘制采用Excel和Graphpad Prism。利用SPSS 20.0软件对数据进行统计分析,差异显著性分析利用单因素ANOVA,P<0.05表示差异显著。Plackett-Burman优化试验和中心组合试验设计与结果分析采用Minitab 17软件。
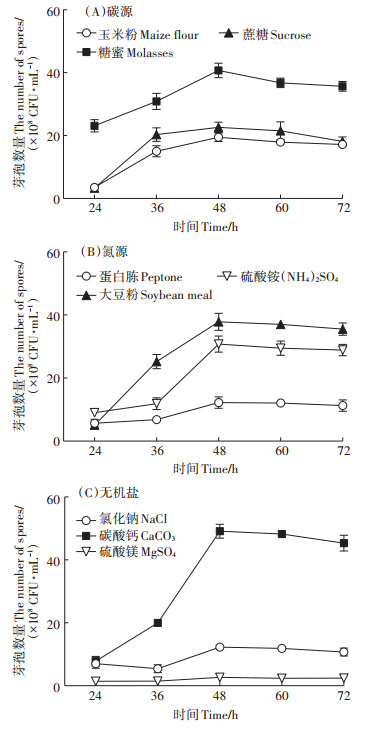
2 结果与分析 2.1 菌株H3产孢培养基优化 2.1.1 影响发酵液中芽孢数量的单因子试验碳源是细胞生长和新陈代谢必需的营养物质,其种类和浓度直接影响芽孢的形成速率和产量。选择玉米粉和糖蜜作为蔗糖的替代碳源,其他成分保持不变,通过H3菌株在发酵培养基中的芽孢数量曲线,筛选出发酵培养基最佳碳源,结果见图 1(A)。3种碳源下H3芽孢产量的大小顺序为:糖蜜>蔗糖>玉米粉,糖蜜明显优于其他碳源。以糖蜜为碳源的培养基中菌株H3在48 h达到最大芽孢数4.0×109 CFU∙mL-1。
|
图 1 不同碳源、氮源和无机盐对菌株H3芽孢数量的影响 Figure 1 Effects of different carbon sources, nitrogen sources and inorganic ions on the spores number of strain H3 |
氮源主要作用是构成菌体细胞物质和合成含氮代谢物,在形成芽孢上也发挥着重要的作用。选择大豆粉、硫酸铵作为蛋白胨的替代氮源,其他成分保持不变,结果见图 1(B)。3种氮源下H3芽孢产量的大小顺序为:大豆粉>硫酸铵>蛋白胨,以大豆粉为氮源的培养基中菌株H3最大芽孢数达到3.8×109 CFU∙mL-1。
无机盐是菌体细胞中组成酶的激活剂或抑制剂的成分之一,可以用来调节培养基的渗透压、pH等。选择碳酸钙、硫酸镁作为氯化钠的替代无机盐,其他成分保持不变。由图 1(C)可知,碳酸钙作为无机盐时,发酵液中H3芽孢数量远大于硫酸镁和氯化钠培养基,且在48 h达到最大芽孢数4.9×109 CFU∙mL-1。
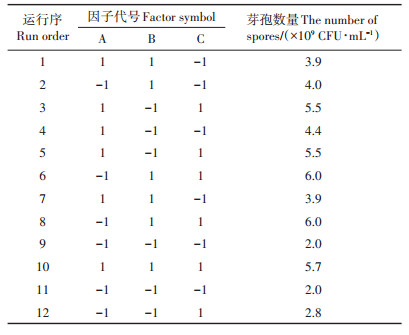
2.1.2 Plackett-Burman优化试验分析单因子试验筛选出发酵培养基中的最佳碳源为糖蜜,氮源为大豆粉,无机盐为碳酸钙。通过Minitab 17软件设计Plackett-Burman试验,初步优化菌株H3发酵培养基的3种成分,不同组合的发酵液中芽孢数量结果见表 3,各因素水平及效应评价见表 4。根据试验数据回归分析可以得到拟合回归方程:Y=4.308+ 0.508 A+0.608 B+0.942 C(Y为芽孢数量,A为糖蜜,B为大豆粉,C为碳酸钙)。回归模型的P<0.01,说明模型所建立的回归方程能很好地表达糖蜜、大豆粉及碳酸钙3个因素之间的关系。回归方程中效应值的绝对值大小决定各因素对H3芽孢数量影响程度,即碳酸钙>大豆粉>糖蜜,而且各因素对H3芽孢数量的影响均为正效应,因此糖蜜应取高水平值(3.80 g∙L-1)。大豆粉和碳酸钙P值均小于0.05,即大豆粉和碳酸钙对H3芽孢数量具有显著影响。选定对响应值具有显著效应且为正效应的大豆粉和碳酸钙进行下一阶段最陡爬坡试验,调整水平范围。
|
|
表 3 Plackett-Burman试验设计与结果 Table 3 Design matrix and experimental results of PlackettBurman design |
|
|
表 4 Plackett-Burman试验设计回归分析结果 Table 4 Regression analysis by Plackett-Burman test design |
根据Plackett-Burman优化试验结果可知,大豆粉及碳酸钙是影响发酵液芽孢数量的关键因素,且是正效应,应依次增大,进行爬坡试验,结果见表 5。随着爬坡试验步长增加,芽孢数量呈现先增加后降低的趋势,当培养基中大豆粉为9.5 g∙L-1、碳酸钙为9.5 g∙L-1时,对应的发酵液芽孢数量达到最大值,将其作为中心组合试验的响应面区域中心点。
|
|
表 5 最陡爬坡试验设计和结果 Table 5 Test design and results of steepest ascent path |
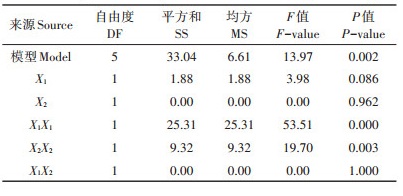
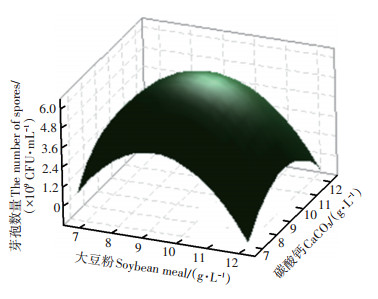
根据最陡爬坡试验结果,采用Minitab 17软件进行二次回归的中心组合设计,进一步优化显著因素的含量。回归分析结果见表 6。依据中心组合试验结果,得到二次拟合回归方程为:Y=6.140 - 0.485X1 - 0.012X2-1.907X12-1.157X22-0.000X1X2(Y为芽孢数量,X1为大豆粉,X2为碳酸钙)。对二次模型进行方差分析,结果见表 6。模型的F值为13.97,多元决定系数R2=0.908 9,模型拟合度较高。回归模型的P=0.002,模型的拟合极显著,所建立的回归方程能很好地表达大豆粉和碳酸钙2个因素之间的关系。采用Minitab 17软件对中心组合试验配方优化(图 2),结果显示大豆粉9.25 g∙L-1、碳酸钙9.50 g∙L-1时,响应值达到最大值。
|
|
表 6 中心组合试验设计回归分析结果 Table 6 Regression analysis based on central composite design |
|
图 2 中心组合试验响应面优化图 Figure 2 Response surface optimization diagram of central composite design |
经过5次验证试验,H3在最优发酵培养基中形成芽孢数平均值为5.9×109 CFU∙mL-1,与预测值较为吻合,表明芽孢形成数目模型的准确性较高。较优化前(2.3×109 CFU∙mL-1)提高156%,相应的H3最优发酵培养基为糖蜜3.80 g∙L-1,大豆粉9.25 g∙L-1,碳酸钙9.50 g∙L-1。
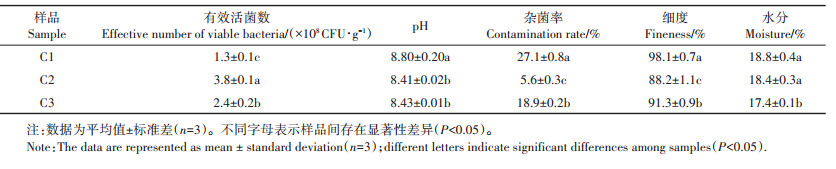
2.2 固体菌剂指标测定结果《农用微生物菌剂》(GB 20287—2006)产品技术指标中指出,粉剂微生物菌剂在保藏第6个月后,有效活菌数要求达到2.0×108 CFU∙g-1,杂菌率≤20%,水分≤35%,细度高于80%,pH控制在5.5~8.5范围内。考虑到有机钝化剂类的有机肥可能存在的重金属、抗生素等二次污染风险,颗粒状有机肥与菌悬液不容易混匀,以及本试验场地的土壤有机质含量较高([22.50±1.20)g∙kg-1]等原因,本研究选取海泡石和生物炭两种无机钝化剂作为载体,与菌悬液制备固体菌剂。表 7为两种无机载体与菌株H3发酵液复配制成的固体菌剂C1(海泡石)、C2(生物炭)、C3(生物炭50%+海泡石50%)在保藏6个月后相关指标检测结果。供试菌剂C1、C2和C3的细度都符合要求,C2和C3的有效活菌数、pH、杂菌率和水分均达到标准,且C2有效活菌数高于C3,杂菌率显著低于C3。有效活菌数为微生物菌剂检测的重要指标,根据农用微生物菌剂的相关指标,选择C2作为后续田间试验施用的固体菌剂。
|
|
表 7 微生物菌剂指标测定 Table 7 Determination of microbial agent index |
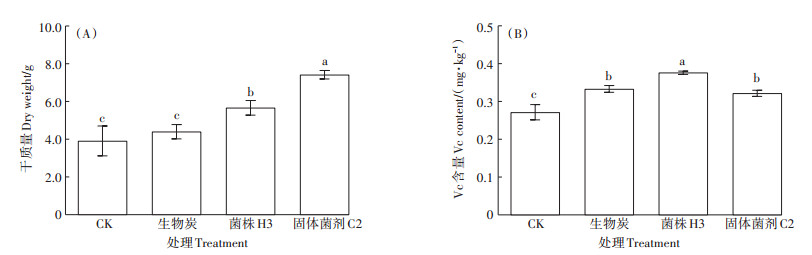
在田间小区试验中,与对照相比,3种处理均能促进生菜可食用部分干质量和Vc含量增加,其中固体菌剂C2和H3菌液分别显著增加了生菜可食用部分干质量89.9%和44.9%[图 3(A)],菌株H3与生物炭协同促生作用明显。3种处理的生菜Vc含量比对照显著增加19.1%~39.5%,H3菌液对生菜Vc含量增加效果好于生物炭和固体菌剂C2[图 3(B)](P<0.05)。
|
不同小写字母表示处理间在0.05水平差异显著。下同 Different lowercase letters indicate significant differences among treatments at 0.05 level. The same below 图 3 H3发酵菌液、生物炭、固体菌剂C2处理对生菜可食用部分干质量和Vc含量的影响 Figure 3 Effects of H3 fermentation broth, biochar, solid bacteria agent C2 treatment on the biomass and Vc content in fresh edible tissue of lettuce |
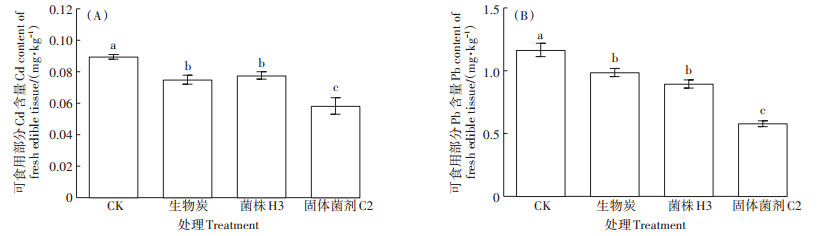
从图 4看出,不同处理均能降低生菜可食用部分Cd、Pb含量。4种处理的生菜可食用部分Cd含量表现为C2<生物炭<H3<CK,Pb含量表现为C2<H3<生物炭<CK。其中,固体菌剂C2减少生菜Cd和Pb含量的效果最好,与对照相比,生菜可食用部分Cd和Pb含量分别显著降低35.2%和50.1%(P<0.05)。
|
图 4 H3发酵菌液、生物炭、固体菌剂C2处理对生菜可食用部分Cd和Pb含量的影响 Figure 4 Effects of H3 fermentation broth, biochar, solid bacteria agent C2 treatment on Cd and Pb content in fresh edible tissue of lettuce |
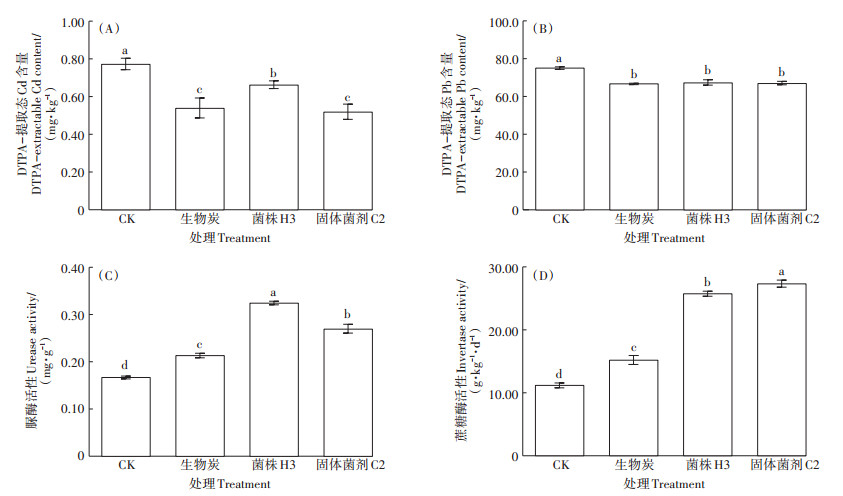
从图 5(A)、图 5(B)看出,与对照相比,3种处理均能显著降低生菜根际土壤有效态Cd和Pb含量,分别降低了14.2%~32.7% 和10.4%~11.1%。其中,固体菌剂C2降低根际土重金属生物有效性的效果较好,与对照相比,根际土有效态Cd和Pb含量分别显著降低32.7% 和11.1%。与对照相比,生物炭、菌株H3以及固体菌剂C2均能显著增加生菜根际土壤脲酶和蔗糖酶活性[图 5(C)、图 5(D)],其中固体菌剂C2处理的生菜根际土壤脲酶和蔗糖酶活性比对照显著增加60.8%和143.7%。
|
图 5 H3发酵菌液、生物炭、固体菌剂C2处理对生菜根际土壤DTPA提取态Cd和Pb含量、脲酶和蔗糖酶活性的影响 Figure 5 Effects of H3 fermentation broth, biochar, solid bacteria agent C2 treatment on the DTPA extractable of Cd and Pb, urease activity and invertase activity in lettuce rhizosphere soils |
芽孢的形成与菌种有关,同时还受到营养物质及环境因素的影响。因此,培养基成分、含量以及发酵条件的选择对促进芽孢的生成至关重要。响应面分析法以回归方法作为函数估算的工具,将多因子与试验结果(响应值)的关系函数化,研究因子与响应值、因子与因子之间的相互关系,并进行优化[15]。近年来运用响应面分析法来优化芽孢杆菌产胞培养基的报道较多,均取得了比较好的结果。刘清术等[11]对巨大芽孢杆菌1013培养基进行摇瓶发酵,优化后发酵产芽孢数为(89.34±3.87)×108 CFU∙mL-1,比基础培养基提高了3.35倍。本研究采用响应面法优化菌株H3产芽孢培养基,将发酵芽孢数提高到5.9 × 109 CFU∙mL-1,较初始培养基芽胞数提高了156%。优化后培养基采用糖蜜、大豆粉作为碳、氮源,原材料廉价易得,生产成本降低,为工业化生产奠定了基础。
3.2 土壤修复菌剂降低蔬菜重金属含量、修复污染农田效果近年来,受污染农田的安全利用得到多方重视,重金属污染农田修复材料和蔬菜安全生产技术成为研究热点之一[16-17]。以微生物菌剂为核心的农田土壤调理剂、修复剂等产品的研发和应用报道较多,但以在实验室水平上开展为主[18-20]。能够分泌IAA、铁载体和精氨酸脱羧酶的Cd抗性细菌Bacillus megaterium H3在盆栽试验中能够促进小白菜生长,且定殖在小白菜根际土壤后能显著降低根际土壤有效态Cd/ Pb含量,提高土壤蔗糖酶活性,从而显著降低小白菜地上部Cd、Pb含量[21]。本研究田间试验中,菌株H3和固体菌剂C2均能增强土壤脲酶和蔗糖酶活性,显著降低根际土壤DTPA提取态Cd和Pb含量,减少生菜吸收重金属,说明菌株H3具有稳定的修复作用。固体菌剂C2的有效活菌数、pH、杂菌率和水分均达到农用微生物菌剂产品技术指标标准,后续研究中需扩大应用范围和使用面积,开展生态风险和安全使用管理研究,以适应修复菌剂产品大幅增长需求。
本研究中各处理均减少了蔬菜中Cd、Pb含量,效果表现为固体菌剂C2>H3菌液>生物炭,可见固体菌剂C2协同了H3菌液和生物炭的作用,可能与土壤脲酶活性增强、有效态Pb、Cd含量降低有关。土壤脲酶对土壤和肥料的氮素转化起着重要作用,能够使尿素转化为氨态氮,从而使土壤氨含量增加[22]。FISHER等[23]的研究表明,脲酶产生菌和脲酶基因丰度的提高可以提高土壤pH值,YANG等[24]的研究表明,具有脲酶活性的细菌与土壤氮代谢密切相关,能够提高土壤铵离子含量和pH值。此外,HAN等[25]发现菌株Serratia liquefaciens CL-1能够提高根际土壤中精氨酸脱羧酶产生菌相对丰度和多胺含量,从而提高土壤pH、降低土壤有效态Cd含量。因此,固体菌剂C2和H3菌液降低土壤有效态Cd、Pb含量还可能与其分泌精氨酸脱羧酶有关。
生物炭作为土壤改良剂被广泛应用[26-27],其不仅能够通过提高土壤的pH值来降低重金属的生物有效性,还可以通过阳离子吸附作用降低其在土壤中的迁移,同时生物炭能够通过改善和提高土壤肥力降低重金属对植物的毒害[28]。考虑到生物炭多孔性和营养作用,可以将其作为载体材料制备固体菌剂。王潇敏等[29]通过室内培养试验发现中性小麦秸秆炭可作为胶冻样芽孢杆菌较理想的载体。CHEN等[30]利用热重分析、XRD、SEM和XPS等物理化学手段研究发现,碱性富磷生物炭可以保护细菌Enterobacter sp.免受高Cd危害,生物炭多孔性能够保护细胞,同时碱性有利于碳酸镉和磷酸镉矿物形成,降低Cd毒害。本研究制备的固体菌剂C2中,菌株H3在生物炭中存活率高于海泡石中,且生物炭杂菌率低于海泡石,可见生物炭可以起到保护细胞的作用。在田间试验中,固体菌剂C2也表现出良好的降低土壤Cd、Pb生物有效性效果,并增强根际土壤脲酶和蔗糖酶活性。多位研究者也发现此效应,TU等[31]发现生物炭负载Pseudomonas sp. NT-2比单一生物炭使用更能提高土壤pH值,降低交换态和碳酸盐结合态Cd、Cu含量,提高土壤脲酶和蔗糖酶活性,提升土壤微生物多样性指数,且多糖能强化Pseudomonas sp. NT-2与玉米秸秆生物炭的黏附。CHENG等[32]在田间试验中发现Serratia liquefaciens CL-1和生物炭复合处理可以降低小麦籽粒Cd和Pb含量,主要原因是单菌处理、生物炭与菌株复合处理可以增加小麦根际腐胺含量和基因aguA拷贝数,提高土壤pH值,降低小麦根际土壤Cd生物有效性以及根-籽粒转移系数。今后应深入研究生物炭-微生物-重金属的相互作用,长期定位监测和评估生物修复效果,以期为揭示生物炭负载细菌修复剂钝化重金属的机理提供更多依据。
4 结论(1)菌株H3产胞培养基优化后,菌株B. megaterium H3在产胞培养基中发酵48 h后,芽孢数量可达5.9×109 CFU∙mL-1,芽孢数较原始培养基显著提高了156%,生产成本降低,原材料廉价易得,配合常用重金属钝化剂研发重金属阻控菌剂,能够适于大规模应用。
(2)生物炭与H3菌液制成的固体菌剂C2保藏6个月后,有效活菌数仍能保持在2×108 CFU∙g-1以上,杂菌率低于20%,各项指标均达到国家农用微生物菌剂要求,为以微生物菌剂为核心的农田土壤调理剂、修复剂等产品的研发和应用提供技术支持。
(3)固体菌剂C2处理后生菜根际土有效态Cd和Pb含量分别显著降低32.7%和11.1%,生菜可食用部分Cd和Pb含量分别显著降低35.2% 和50.1%,且根际土壤脲酶和蔗糖酶活性比对照显著增加60.8% 和143.7%,菌剂在保障蔬菜安全生产方面具有广阔的应用前景,为防控蔬菜积累重金属、改善土壤生态环境提供技术支持。
| [1] |
陈世宝, 王萌, 李杉杉, 等. 中国农田土壤重金属污染防治现状与问题思考[J]. 地学前缘, 2019, 26(6): 35-41. CHEN S B, WANG M, LI S S, et al. Current status and discussion on farm land heavy metal pollution prevention in China[J]. Earth Science Frontiers, 2019, 26(6): 35-41. |
| [2] |
陈玉鹏, 梁东丽, 刘中华, 等. 大棚蔬菜土壤重金属污染及其控制的研究进展与展望[J]. 农业环境科学学报, 2018, 37(1): 9-17. CHEN Y P, LIANG D L, LIU Z H, et al. Analysis of present situation and control of heavy metal pollution in vegetable greenhouse soils[J]. Journal of Agro-Environment Science, 2018, 37(1): 9-17. |
| [3] |
冯英, 马璐瑶, 王琼, 等. 我国土壤-蔬菜作物系统重金属污染及其安全生产综合农艺调控技术[J]. 农业环境科学学报, 2018, 37(11): 2359-2370. FENG Y, MA L Y, WANG Q, et al. Heavy-metal pollution and safety production technologies of soil - vegetable crop systems in China[J]. Journal of Agro - Environment Science, 2018, 37(11): 2359-2370. DOI:10.11654/jaes.2018-0787 |
| [4] |
苏诗博, 徐慧婷, 贾飞, 等. 矿物固化剂添加对蔬菜重金属吸收富集和污染风险的影响[J]. 湖北农业科学, 2020, 59(7): 136-141. SU S B, XU H T, JIA F, et al. Effects of mineral curing agents on absorption and enrichment of heavy metals in vegetables and pollution risk[J]. Hubei Agricultural Sciences, 2020, 59(7): 136-141. |
| [5] |
LIU Q Q, SHENG Y Q, WANG W J, et al. Remediation and its biological responses of Cd contaminated sediments using biochar and minerals with nanoscale zero-valent iron loading[J]. Science of the Total Environment, 2020, 713: 136-150. |
| [6] |
XU S, XING Y, LIU S, et al. Role of novel bacterial Raoultella sp. strain X13 in plant growth promotion and cadmium bioremediation in soil[J]. Applied Microbiology and Biotechnology, 2019, 103(9): 3887-3897. DOI:10.1007/s00253-019-09700-7 |
| [7] |
葛占标, 殷涂童, 周倩倩, 等. 产生物膜芽胞杆菌阻控叶菜吸收镉、铅及其修复菜地土壤的作用[J]. 南京农业大学学报, 2020, 43(1): 80-88. GE Z B, YIN T T, ZHOU Q Q, et al. Reduced cadmium and lead uptake by leafy vegetables and soil remediation in the presence of the biofilm -producing Bacillus strains[J]. Journal of Nanjing Agricultural University, 2020, 43(1): 80-88. |
| [8] |
XIONG Z Q, ZHANG J Q, CAI P, et al. Bio-organic stabilizing agent shows promising prospect for the stabilization of cadmium in contaminated farmland soil[J]. Environmental Science and Pollution Research, 2019, 26(23): 23399-23406. DOI:10.1007/s11356-019-05619-8 |
| [9] |
贺卓, 殷涂童, 葛占标, 等. Bacillus thuringiensis P34与海泡石联合阻控蔬菜积累铅和改良土壤的作用[J]. 农业环境科学学报, 2019, 38(6): 1240-1247. HE Z, YIN T T, GE Z B, et al. Synergistic effect of Bacillus thuringiensis P34 and sepiolite on lead uptake of vegetables and remediation in Pb-contaminated soils[J]. Journal of Agro-Environment Science, 2019, 38(6): 1240-1247. |
| [10] |
WANG Q, ZHANG W J, HE L Y, et al. Increased biomass and quality and reduced heavy metal accumulation of edible tissues of vegetables in the presence of Cd-tolerant and immobilizing Bacillus megaterium H3[J]. Ecotoxicology and Environmental Safety, 2018, 148: 269-274. DOI:10.1016/j.ecoenv.2017.10.036 |
| [11] |
刘清术, 郭照辉, 刘前刚, 等. 响应面法优化巨大芽孢杆菌发酵培养基[J]. 中国农学通报, 2013, 29(18): 142-146. LIU Q S, GUO Z H, LIU Q G, et al. Optimization of medium for Bacillus megaterium fermentation by response-surface methodology[J]. Chinese Agricultural Science Bulletin, 2013, 29(18): 142-146. DOI:10.11924/j.issn.1000-6850.2012-2611 |
| [12] |
胡瑞萍, 丁贤, 李来好, 等. 响应面法优化枯草芽孢杆菌NHS1产芽孢发酵培养[J]. 生态学杂志, 2018, 37(2): 605-612. HU R P, DING X, LI L H, et al. Optimization of fermentation medium composition by response surface methodology for the spore production of Bacillus subtilis[J]. Chinese Journal of Ecology, 2018, 37(2): 605-612. |
| [13] |
WANG Q, CHEN L, HE L Y, et al. Increased biomass and reduced heavy metal accumulation of edible tissues of vegetable crops in the presence of plant growth-promoting Neorhizobium huautlense T1-17 and biochar[J]. Agriculture, Ecosystems & Environment, 2016, 228: 9-18. |
| [14] |
关松荫. 土壤酶及其研究法[M]. 北京: 农业出版社, 1986: 233-236. GUAN S Y. Soil enzyme and its research methods[M]. Beijing: Agriculture Press, 1986: 233-236. |
| [15] |
SONG D Y, REDDY L V, CHARALAMPOPOULOS D, et al. Produc tion and optimization from agro-industrial bioresources as renewable substrates by Bacillus sp. Fbl-2 through response surface methodology[J]. Biomolecules, 2019, 9(12): 754-764. DOI:10.3390/biom9120754 |
| [16] |
刘杏梅, 赵健, 徐建明. 污染农田土壤的重金属钝化技术研究——基于Web of Science数据库的计量分析[J]. 土壤学报, 2021, 58(2): 445-455. LIU X M, ZHAO J, XU J M. Research on immobilization of heavy metals in contaminated agricultural soils: Bibliometric analysis based on Web of Science database[J]. Acta Pedologica Sinica, 2021, 58(2): 445-455. |
| [17] |
吴霄霄, 曹榕彬, 米长虹, 等. 重金属污染农田原位钝化修复材料研究进展[J]. 农业资源与环境学报, 2019, 36(3): 253-263. WU X X, CAO R B, MI C H, et al. Research progress of in-situ passivated remedial materials for heavy metal contaminated soil[J]. Journal of Agricultural Resources and Environment, 2019, 36(3): 253-263. |
| [18] |
HAN H, CAI H, WANG X Y, et al. Heavy metal-immobilizing bacteria increase the biomass and reduce the Cd and Pb uptake by pakchoi (Brassica chinensis L.)in heavy metal-contaminated soil[J]. Ecotoxicology and Environmental Safety, 2020, 195: 110375. DOI:10.1016/j.ecoenv.2020.110375 |
| [19] |
Ravindran A, Sajayan A, Priyadharshini G B, et al. Revealing the efficacy of thermostable biosurfactant in heavy metal bioremediation and surface treatment in vegetables[J]. Frontiers in Microbiology, 2020, 11: 222. DOI:10.3389/fmicb.2020.00222 |
| [20] |
段桂兰, 崔慧灵, 杨雨萍, 等. 重金属污染土壤中生物间相互作用及其协同修复应用[J]. 生物工程学报, 2020, 36(3): 455-470. DUAN G L, CUI H L, YANG Y P, et al. Interactions among soil biota and their applications in synergistic bioremediation of heavy-metal contaminated soils[J]. Chinese Journal of Biotechnology, 2020, 36(3): 455-470. |
| [21] |
LI Y, PANG H D, HE L Y, et al. Cd immobilization and reduced tissue Cd accumulation of rice(Oryza sativa wuyun-23)in the presence of heavy metal-resistant bacteria[J]. Ecotoxicology and Environmental Safety, 2017, 138: 56-63. DOI:10.1016/j.ecoenv.2016.12.024 |
| [22] |
WANG T J, WANG S L, TANG X C, et al. Isolation of urease-producing bacteria and their effects on reducing Cd and Pb accumulation in lettuce(Lactuca sativa L.)[J]. Environmental Science and Pollution Research, 2020, 27(8): 8707-8718. DOI:10.1007/s11356-019-06957-3 |
| [23] |
FISHER K A, YARWOOD S A, JAMES B R. Soil urease activity and bacterial ureC gene copy numbers: Effect of pH[J]. Geoderma, 2017, 285(4): 1-8. |
| [24] |
YANG Y F, GAO Y, WANG S P, et al. The microbial gene diversity along an elevation gradient of the Tibetan grassland[J]. ISME Journal, 2014, 8(2): 430-440. DOI:10.1038/ismej.2013.146 |
| [25] |
HAN H, WANG Q, HE L Y, et al. Increased biomass and reduced rapeseed Cd accumulation of oilseed rape in the presence of Cd-immobilizing and polyamine-producing bacteria[J]. Journal of Hazardous Materials, 2018, 353(14): 280-289. |
| [26] |
陈温福, 张伟明, 孟军. 农用生物炭研究进展与前景[J]. 中国农业科学, 2013, 46(16): 3324-3333. CHEN W F, ZHANG W M, MENG J. Advances and prospects in research of biochar utilization in agriculture[J]. Scientia Agricultura Sinica, 2013, 46(16): 3324-3333. DOI:10.3864/j.issn.0578-1752.2013.16.003 |
| [27] |
AHMAD M, RAJAPAKSHA A U, LIM J E, et al. Biochar as a sorbent for contaminant management in soil and water: A review[J]. Chemosphere, 2014, 99(45): 19-33. |
| [28] |
李鸿博, 钟怡, 张昊楠, 等. 生物炭修复重金属污染农田土壤的机制及应用研究进展[J]. 农业工程学报, 2020, 36(13): 173-185. LI H B, ZHONG Y, ZHANG H N, et al. Mechanism for the application of biochar in remediation of heavy metal contaminated farmland and its research advances[J]. Transactions of the Chinese Society of Agricultural Engineering, 2020, 36(13): 173-185. DOI:10.11975/j.issn.1002-6819.2020.13.021 |
| [29] |
王潇敏, 李恋卿, 潘根兴, 等. 胶冻样芽孢杆菌与生物质炭复配及对番茄产量和品质的影响[J]. 土壤, 2016, 48(3): 479-485. WANG X M, LI L Q, PAN G X, et al. Compound of Bacillus mucilaginosus and biochar and its effects on tomato yield and quality[J]. Soils, 2016, 48(3): 479-485. |
| [30] |
CHEN H M, TANG L Y, WANG Z J, et al. Evaluating the protection of bacteria from extreme Cd(Ⅱ)stress by P-enriched biochar[J]. Environmental Pollution, 2020, 263: 114483. DOI:10.1016/j.envpol.2020.114483 |
| [31] |
TU C, WEI J, GUAN F, et al. Biochar and bacteria inoculated biochar enhanced Cd and Cu immobilization and enzymatic activity in a polluted soil[J]. Environment International, 2020, 137: 105576. DOI:10.1016/j.envint.2020.105576 |
| [32] |
CHENG C, HAN H, WANG Y P, et al. Biochar and metal-immobilizing Serratia liquefaciens CL-1 synergistically reduced metal accumulation in wheat grains in a metal-contaminated soil[J]. Science of the Total Environment, 2020, 740: 139972. DOI:10.1016/j.scitotenv.2020.139972 |
 2022, Vol. 41
2022, Vol. 41