2. 中国科学院地理科学与资源研究所,陆地水循环及地表过程院重点实验室,北京 100101
2. Key Laboratory of Water Cycle and Related Land Surface Processes, Institute of Geographic Sciences and Natural Resources Research, Chinese Academy of Sciences, Beijing 100101, China
近年来城市化进程加剧导致水资源短缺,再生水逐渐成为城市景观河流的主要补给来源[1]。与天然水相比,再生水含有氮、磷、重金属及有机污染物等,大量排进城市河流后,易引起河道污染[2-3]。北京市潮白河-顺义段为再生水回补的天然河道,由城北减河入口的污水处理厂排入经过二级生化处理的再生水,其出水水质指标中总氮质量浓度高于地表水Ⅲ类水质标准,并主要以NO3--N形式存在。NO3--N是植物生长所需氮的主要来源,是水生植物生命活动的基础[4-5]。而较高的NO3--N会导致水体溶解氧降低,引起水中生物和植物的异常生长,造成水体富营养化,危害水体环境及水生态系统。同时,河水中污染物经过河床底泥进入地下水,对地下水水质有直接影响,进而对人体健康造成威胁[6-7]。
河床底泥可视作一个渗滤系统,通过物理、化学和生物反应对再生水中污染物起到去除作用[8]。潘维艳[9]通过室内土柱实验得出NO3--N质量浓度随水流方向逐渐下降,定流速补水下NO3--N平均去除率高于90%。吴振斌等[10]的研究表明,复合垂直流人工湿地系统对NO3--N的去除率为56.96%。ASANO等[11]发现NO3--N在河床沉积物中可发生异化还原及反硝化作用,使河岸渗滤系统对NO3--N的去除率几乎达到100%。闫雅妮等[12]在室内设置地表水地下水交替实验装置,得出NO3--N的衰减是同化合成有机氮、反硝化作用及异化还原作用的共同结果,NO3--N在底泥潜流带介质中通过吸附和微生物合成有机氮的方式被截留;随后其又以河岸带沉积物为实验对象,验证了上述的第一个理论[13]。众多研究表明,污染物质量浓度、水力条件、温度、pH、溶解氧等对反硝化等作用均有影响[14-16]。目前,有关不同NO3--N质量浓度水平的研究相对较少。景观河道中污染程度和NO3--N质量浓度不同,对环境影响也不同。本实验主要探究不同NO3--N质量浓度条件下,河道底泥对再生水中NO3--N的净化能力,并简析NO3--N的去除机制。
实验采用潮白河再生水补给河道河岸带土壤进行河槽实验,在改变外源输入NO3--N质量浓度的情况下,分析温度、pH和溶解氧等因素的变化,探究河槽中NO3--N、NO2--N、NH4+-N的质量浓度变化规律,讨论河道底泥沉积物对NO3--N的去除效果及机制,为再生水安全利用提供数据支撑和理论支持。
1 材料与方法 1.1 实验材料实验用土取自潮白河向阳闸附近河岸带的非表层土壤,取土深度为10~100 cm,土样采集后剔除杂物,过10 mm筛,搅拌均匀后填入河槽,土壤中砂粒含量为97.1%,粉粒和黏粒含量不足3%。根据《土壤农化分析》[17]测定土壤理化性质:pH 7.32,NO3--N 4.58 mg·kg-1,NH4+-N 2.66 mg·kg-1,有机质5.32 g·kg-1。实验用NO3--N溶液用自来水配制,室内实验用水采用超纯水。
1.2 实验方法 1.2.1 实验设计采用河槽模拟装置进行实验,示意图与实物图见图 1。河槽装置长6 m、宽0.8 m、高1.2 m,以直径约为10 mm和2.5 mm的粗细石粒各铺底5 cm,上方填装实验用土,厚度为90 cm,模拟河流底泥构造。实验设置3个NO3--N质量浓度水平,分别为5、10、20 mg·L-1。供试水样采用人工配制,在自来水中加入一定量的硝酸钾和醋酸钠配制NO3--N溶液,C∶N为2∶1[12]。用水泵将NO3--N溶液通入河槽,调整河槽底部排水阀门,使流入与流出速率均为150 mL·min-1,控制定水头在底泥表层以上5~10 cm。在10、20、30、50 cm和70 cm深度处放置由聚乙烯管和多孔陶瓷管组成的土壤溶液提取器[18],采样时将聚乙烯管与密封瓶连接,用脚踏吸引器抽取瓶中空气,利用负压取水。5个深度各设置3组平行,从进水与闸门排出的底层水取样,共17个采样点。
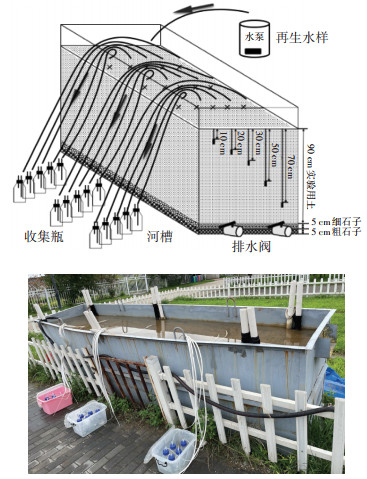
|
图 1 河槽实验装置示意图和实物图 Figure 1 Schematic diagram and physical diagram of channel experimental device |
3个NO3--N质量浓度水平下,每个浓度20 d为一周期,前10 d每日取样,后10 d每2 d取一次样。第一周期(N1,NO3--N质量浓度为5 mg·L-1)为2019年8月23日至9月11日,第二周期(N2,NO3--N质量浓度为NO3--N质量浓度为10 mg·L-1)为2019年9月16日至10月5日,第三周期(N3,NO3--N质量浓度为20 mg·L-1)为2019年10月8日至10月27日。测定指标为温度、pH、DO(溶解氧)、NO3--N、NO2--N和NH4+-N。河槽露天放置在室外草坪中,水样在室内进行测试分析。
1.2.2 分析方法实验水体的水质指标检测参考国家环境保护局《水和废水监测分析方法》[19],NO3--N、NO2--N和NH4+-N分别采用紫外分光光度法、重氮偶合分光光度法和纳氏试剂比色法测定,温度、pH和DO采用HQ11d便携式分析仪(美国哈希HACH)测定。
1.2.3 数据处理采用Excel 2015进行数据统计,SPSS 17.0软件进行相关性分析,Origin 2018b进行图表制作。NO3--N去除率由进水NO3--N质量浓度与河槽系统中NO3--N质量浓度计算得出。
NO3--N去除率计算公式为:
Re=(Cj-Cd)/Cj×100%
式中:Re为NO3--N去除率,%;Cj为进水NO3--N质量浓度,mg·L-1;Cd为河槽系统中NO3--N质量浓度,mg·L-1。
2 结果与分析 2.1 底泥中温度、pH及DO变化河槽系统中水体温度受室外天气影响较大。N1温度为25~30 ℃,N2温度在23 ℃上下波动,N3水温逐渐下降,由23 ℃降至13 ℃。
由图 2可知,N1底泥中各深度pH在前7 d呈下降趋势,在第12 d达到一个小峰值后逐渐稳定在7.4左右。N2各深度pH在7.4~7.8间波动。N3时各深度pH在前10 d较稳定,后10 d 10 cm和20 cm处pH升至7.7。各周期底层水pH远高于河槽中各深度pH,N1、N2和N3分别为8.48~9.11、9.01~9.21、8.85~9.25。
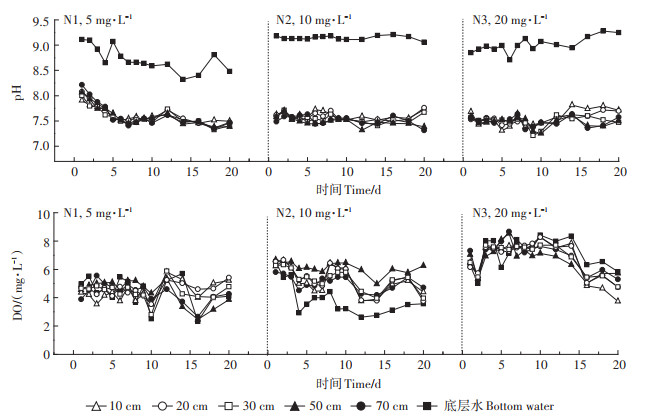
|
图 2 3种NO3--N质量浓度下各深度pH、DO随时间的变化 Figure 2 Temporal variation of pH, DO concentrations at different depths under three NO3--N concentrations |
N1底泥中各深度DO水平为2~6 mg·L-1,第9 d开始波动较大,表明底泥微生物反应活动较为剧烈。N2底泥各深度DO水平为4~7 mg·L-1,在8~10 d达到高峰。N3底泥各深度DO水平为5~9 mg·L-1,整体呈现先上升后下降的趋势。3个周期下温度整体降低,DO质量浓度整体升高。
2.2 底泥中NO3--N、NO2--N和NH4+-N质量浓度变化3种NO3--N质量浓度下NO3--N、NO2--N和NH4+-N质量浓度随时间变化关系见图 3。实验中N1时NO3--N质量浓度较为平稳,N2和N3波动较大,各周期10、20、30 cm处变化趋势相似,统称浅层底泥;50、70 cm处变化趋势相似,统称深层底泥。N1河槽中NO3--N质量浓度为3~6 mg·L-1,整体呈下降趋势。N2与N3分别在前5 d和前7 d浅层底泥NO3--N质量浓度降低,深层底泥质量浓度升高。N2第9、10 d时NO3--N质量浓度波动较大,因这两日出现的降雨对河槽中各反应有一定影响。N3在12~20 d时浅层底泥质量浓度增加,深层底泥质量浓度减少。最终河槽中N1、N2和N3的NO3--N质量浓度分别稳定在2~4、3~6、5~8 mg·L-1。底层水NO3--N质量浓度在N1时由4.84 mg·L-1降至1.93 mg·L-1,在N2时由1.6 mg·L-1升至3.3 mg·L-1,在N3第5~7 d由0.91 mg·L-1骤增至9.2 mg·L-1后在8~10 mg·L-1小幅波动。

|
图 3 3种NO3--N质量浓度下各深度NO3--N、NO2--N和NH4+-N质量浓度的变化 Figure 3 Temporal variation of NO3--N, NO2--N and NH4+-N concentrations at different depths under three NO3--N concentrations |
NO2--N在N1和N2时底泥各深度中质量浓度较低,为0~0.1 mg·L-1;N3时NO2--N质量浓度在前9 d较为稳定,第9 d开始于10、20、30、50 cm和70 cm处质量浓度依次骤增,最后稳定在0.4~0.5 mg·L-1。对于底层排出水,N1和N2时NO2--N质量浓度明显高于河槽中质量浓度,分别于第14 d和第10 d升至最大值0.33 mg·L-1和0.27 mg·L-1,而后逐渐下降,N3则在前10 d于0~0.3 mg·L-1波动强烈,后期稳定在0.1 mg·L-1左右。整体来看,各周期底层水中,N1和N2的中期NO2--N质量浓度最高,N3前期NO2--N波动较大,质量浓度较高,后期质量浓度降低并趋于稳定。最终底层水NO2--N质量浓度为N1 > N2 > N3。
NH4+-N质量浓度随时间无明显变化规律,3个周期各深度分别在0.040~0.134、0.031~0.151 mg·L-1和0.051~0.139 mg·L-1范围内波动。N1、N2和N3浅层底泥NH4+-N平均质量浓度均高于深层底泥平均质量浓度。底层水NH4+-N质量浓度基本高于底泥中各深度质量浓度,3个周期分别为0.098~0.278、0.068~0.141、0.057~0.253 mg·L-1,各周期结束时底层水NH4+-N质量浓度为N1 > N2 > N3。
2.3 NO3--N去除率 2.3.1 底层水NO3--N去除率3种NO3--N质量浓度水平下,河槽系统底层出水中NO3--N质量浓度及系统对NO3--N去除率随时间的变化见图 4。由图 4a可知,实验期间,各NO3--N质量浓度水平下底层水中NO3--N质量浓度随时间呈现不同的变化趋势。N1时NO3--N质量浓度整体呈降低趋势,第14 d起趋于平稳,质量浓度变化范围为1.77~5.59 mg·L-1,去除率整体升高,周期结束时稳定在67.8%(图 4b)。N2时底层水NO3--N质量浓度范围为1.67~6.38 mg·L-1,其出水NO3--N质量浓度在第5 d大幅升高,在第9、10 d降雨时较低,最终稳定在3 mg·L-1左右。N2时NO3--N去除率为29%~81%,前12 d去除率高于N1,14~20 d低于N1。N3时底层水NO3--N质量浓度变化较大,前5 d低于2.2 mg·L-1,第6、7 d骤增至9 mg·L-1以上,远高于N1、N2;去除率也由90%左右降至50%左右。各周期结束时N1、N2和N3的去除率分别为67.8%、63.0% 和55.0%,去除率随NO3--N质量浓度增大而减小。
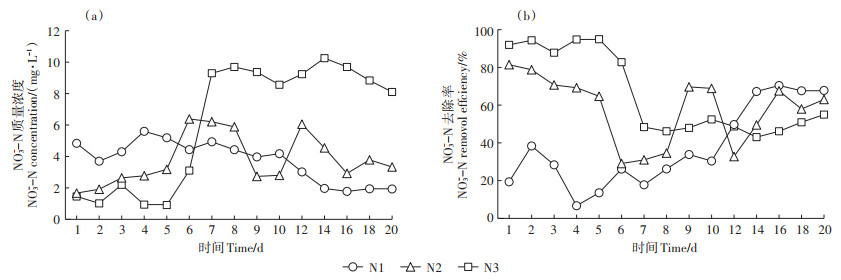
|
图 4 3种NO3--N质量浓度下底层出水NO3--N质量浓度以及NO3--N去除率随时间的变化 Figure 4 Temporal variation of NO3--N concentration in effluents and NO3--N removal efficiency under three NO3--N concentrations |
图 5为3种NO3--N质量浓度下不同深度NO3--N质量浓度和相应土层的去除率。由图 5a可知,3种NO3--N质量浓度水平下底泥中NO3--N质量浓度也随进水质量浓度由低到高,分别为2.74~3.69、3.85~5.69、6.05~7.57 mg·L-1,浅层底泥(10、20、30 cm)中NO3--N质量浓度随深度增加而增加,深层底泥(50、70 cm)中NO3--N质量浓度随深度增加而降低。由图 5b可知,底泥中3种NO3--N质量浓度下,除20 cm处外,NO3--N进水质量浓度越高,各深度去除率越高。N1中10 cm和70 cm处去除率较高,分别为48.0%和54.3%,N2中10、50 cm和70 cm处去除率较高,分别为51.5%、54.7%和57.2%,N3各深度去除率都大于50%,最高是10 cm和70 cm处,分别为63.8%和66.4%。说明河槽表层和下部对NO3--N去除效果较好。
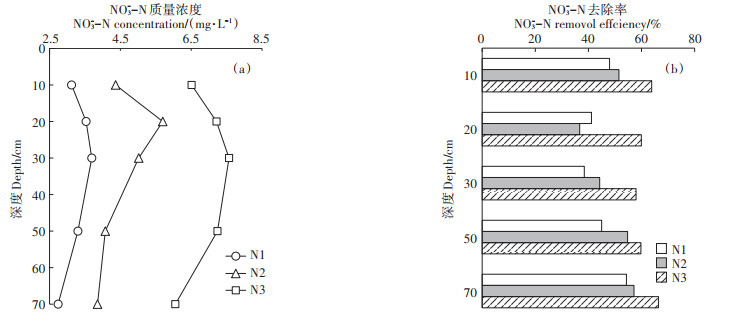
|
图 5 3种NO3--N质量浓度下不同深度处NO3--N质量浓度以及去除率的变化 Figure 5 Temporal variation of NO3--N concentration and NO3--N removal efficiency at different depths under three NO3--N concentrations |
3种NO3--N质量浓度水平下(N1、N2、N3)底泥水中pH为7~8,硝化与反硝化等细菌活性较高,适宜在底泥中发生硝化与反硝化等反应[20]。N1时前7 d pH下降明显,因实验用底泥取自自然土体,含有较丰富的钙、镁、钾、钠等碱性盐基物质,实验进行中其随水流向下积累,使pH随底泥深度增加而增大,直至第7 d各深度pH相近,底泥本体包含的盐类物质接近淋溶完毕。由图 6可知,3个周期底层水中NO3--N质量浓度与pH的相关性分析结果表明,N1和N3时二者呈正相关性(P < 0.05),N2时呈负相关性(P < 0.05)。硝化作用产酸,反硝化和异化还原反应耗酸[21],说明河槽系统中pH变化与NO3--N参与的各反应有关。
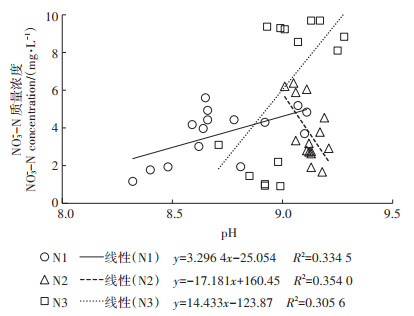
|
图 6 底层水中pH与NO3--N质量浓度的关系 Figure 6 The relationship between pH and NO3--N concentration in bottom water |
底泥中DO主要通过影响微生物硝化和反硝化反应,间接影响氮的形态转化[22]。由表 1可知,N1、N2和N3下50 cm和70 cm处DO质量浓度与NO2--N质量浓度均呈显著负相关(P < 0.05),说明DO质量浓度越低,NO2--N质量浓度越高,即深层底泥中主要发生反硝化反应。低DO条件不利于硝化反应的发生,因此河槽系统深层底泥中反硝化反应强度与DO质量浓度紧密相关。SHAO等[23]同样发现,DO大于4.2 mg·L-1时,反硝化速率降低,因为DO质量浓度越高,反硝化反应越弱,NO2--N质量浓度越低。
|
|
表 1 底泥中DO与NO2--N的相关关系 Table 1 The correlation between DO and NO2--N in sediment |
温度变化会影响细菌活性,温度下降会使反硝化速率和DO的消耗速率降低[24]。3个周期的温度逐期降低,DO平均值逐期升高,NO3--N去除率逐期降低。王子珏[25]利用模型分析湿地系统脱氮过程,得到随水温升高,脱氮过程中各反应速率与总氮去除率升高的规律,这与本研究一致。
3.2 NO3--N去除机理3种NO3--N质量浓度下各深度底泥中第1 d与最后1 d相比,浅层底泥(10、20、30 cm)NO3--N质量浓度平均降低1.29、3.85、6.60 mg·L-1,深层底泥(50、70 cm)质量浓度平均升高1.06、3.33、6.48 mg·L-1,最后1 d时底层水中NO3--N质量浓度分别为1.93、3.32、8.10 mg·L-1。NO3--N在底泥中会经历淋溶、吸附等物理作用和硝化、反硝化、同化、异化还原等复杂的生物化学反应,其质量浓度和形态可能发生改变,此处主要讨论NO3--N的去除机理:
(1)土壤淋溶作用。NO3--N带负电,不易被土壤胶体吸附,在土壤中移动性较强,易淋滤[26]。3个周期的前期浅层底泥NO3--N质量浓度明显降低,深层底泥质量浓度明显升高,表明NO3--N随水流向下迁移。N1、N2和N3在50 cm处NO3--N质量浓度分别于第3、5、12 d升至最高点,70 cm处于之后1 d达到最大值。说明3个周期以来,NO3--N淋溶时间增长。杨岚鹏等[27]也认为随着时间的增加,土壤逐渐紧实,滤液在河槽系统中停留时间增加,淋溶速度也随之减慢。
(2)同化作用。微生物在生长繁殖过程中可将NO3--N合成为自身所需的有机氮而发生同化作用[28],反应式为:0.142 9 NO3--N+C+0.285 7 H2O→0.142 9 C5H7NO2+0.142 9 OH-+0.285 8 CO2[29]。本实验中3种NO3--N质量浓度水平下0~10 cm处NO3--N去除率均较高,因为在底泥-水界面上,碳源最充足,细菌大量繁殖,大量的NO3--N被细菌利用并合成有机氮[30],这与潘维艳等[31]在定水头淹水条件下土柱系统对NO3--N的去除效果类似。
(3)反硝化作用。NO2--N作为反硝化作用的中间产物,反映了反硝化作用的强弱。本实验3个NO3--N质量浓度水平下底层水NO2--N质量浓度为N1 > N2 > N3,同时3个周期温度逐渐降低,细菌活性减弱,DO质量浓度升高,反硝化作用减弱,NO3--N去除率降低。不同深度下,3个周期中深层底泥NO3--N去除率均较高,因为深层底泥中DO质量浓度较低,有利于反硝化作用的发生。这与潘维艳等[31]得出的限定流速补水条件下,土柱下部对NO3--N也有一定去除作用的结论相似。
(4)异化还原作用。底泥环境中厌氧菌和兼性厌氧菌同样会将NO3--N异化还原成易被土壤吸附的NH4+-N,并留存于底泥中[32],反应式为:NO -3+10H++ 8e-→NH4++3H2O[12]。本实验各周期之间底泥中NH4+-N质量浓度相差较小,因为河槽中土壤较多,吸附NH4+-N能力较强。李薇[22]同样发现在NO3--N进水质量浓度为2~40 mg·L-1时,排出水中NH4+-N质量浓度差别较小。不同深度下,浅层底泥中NH4+-N质量浓度高于深层底泥,因为在底泥-水界面处氮循环较强烈,NH4+-N质量浓度显著上升[8],且NH4+-N淋溶性较小,故多被吸附于浅层底泥。胡喆[33]同样提出氮质量浓度较高的河流中,浅层底泥的NH4+-N不会向深层底泥扩散,深层底泥中NO3--N会转化生成NH4+-N,故浅层底泥NH4+-N质量浓度较高,深层底泥NH4+-N质量浓度较低。
本实验中,土壤淋溶作用造成了河槽中NO3--N的物理迁移;生物化学作用下,有机氮同化、反硝化与异化还原作用共同造成NO3--N质量浓度的衰减,因为底泥-水界面氧气充足,且有外界碳源添加,氮循环中各反应强烈[34],有机氮同化作用较强。NO3--N是反硝化作用与异化还原作用的共同基质,两种作用存在竞争关系。从能量角度看,微生物反硝化作用得到的能量为2 333.84 kJ·mol-1,而异化还原作用得到的能量为679.60 kJ·mol-1 [13],故微生物优先发生能够得到更多能量的反硝化作用。王飞[35]提出对于潜流带中NO3--N的减少,反硝化作用占85%,异化还原作用占14%。闫雅妮等[13]估算出沉积物中有机氮同化、反硝化作用以及异化还原作用对NO3--N衰减的贡献率分别为56.6%、26.6%和13.1%。本实验中,对于NO3--N的去除,有机氮同化与反硝化作用较强,异化还原作用较弱,各反应对NO3--N衰减的具体贡献率还有待进一步研究。本研究结果表明,模拟自然河道环境下,河道水体中不同NO3--N质量浓度会影响河槽系统中各形态氮的质量浓度,从而影响各反应的发生强度,造成不同的NO3--N去除效果。
4 结论(1)河床底泥对水体中NO3--N有显著去除作用。水中NO3--N质量浓度为5、10、20 mg·L-1时去除率分别为67.8%、63.0%和55.0%。
(2)河槽表层10 cm处和下部70 cm处对NO3--N去除效果最好,分别主要通过有机氮合成和反硝化作用去除NO3--N。
(3)底层排出水中pH与NO3--N质量浓度相关性较强;底泥中50 cm与70 cm处反硝化作用强度与溶解氧质量浓度紧密相关;随着温度降低,溶解氧质量浓度升高,反硝化作用减弱,NO3--N去除效果变差。
(4)底泥中NO3--N衰减主要为土壤淋溶作用、同化作用、反硝化作用与异化还原作用等共同作用;部分氮素以同化作用形成的有机氮和异化还原作用形成的NH4+-N形式留存于底泥中。
| [1] |
霍健. 北京市中心城再生水发展历程及"十二五" 发展规划[J]. 水利发展研究, 2011, 11(7): 57-60, 92. HUO J. Development process of reclaimed water in the central city of Beijing and development plan of the "12th Five Year Plan"[J]. Water Conservancy Development Research, 2011, 11(7): 57-60, 92. DOI:10.3969/j.issn.1671-1408.2011.07.015 |
| [2] |
陈卫平, 吕斯丹, 王美娥, 等. 再生水回灌对地下水水质影响研究进展[J]. 应用生态学报, 2013, 24(5): 1253-1262. CHEN W P, LÜ S D, WANG M E, et al. Effects of reclaimed water recharge on groundwater quality: A review[J]. Chinese Journal of Applied Ecology, 2013, 24(5): 1253-1262. |
| [3] |
李小牛, 周长松, 周孝德, 等. 污灌区浅层地下水污染风险评价研究[J]. 水利学报, 2014, 45(3): 326-334. LI X N, ZHOU C S, ZHOU X D, et al. Study on risk assessment of groundwater pollution in sewage irrigation area[J]. Journal of Hydraulic Engineering, 2014, 45(3): 326-334. |
| [4] |
路璐, 杨培岭, 李云开, 等. 水生植物对河湖中回用的再生水富营养化的控制效应[J]. 农业工程学报, 2011, 27(增刊2): 196-203. LU L, YANG P L, LI Y K, et al. Control effects of aquatic plants on eutrophication in reclaimed water rivers-lake[J]. Transactions of the Chinese Society of Agricultural Engineering, 2011, 27: 196-203. |
| [5] |
HU B, TENG Y G, ZHAI Y Z, et al. Riverbank filtration in China: A review and perspective[J]. Journal of Hydrology, 2016, 541: 914-927. DOI:10.1016/j.jhydrol.2016.08.004 |
| [6] |
王庆锁, 顾颖, 孙东宝. 巢湖流域地下水硝态氮含量空间分布和季节变化格局[J]. 生态学报, 2014, 34(15): 4372-4379. WANG Q S, GU Y, SUN D B. Spatial and seasonal variations of nitrate-N concentration in groundwater within Chao Lake watershed[J]. Acta Ecologica Sinica, 2014, 34(15): 4372-4379. |
| [7] |
赵越, 陈建平, 吴丽. 农业地下水中氮素面源污染研究进展[J]. 环境污染与防治, 2016, 38(5): 111. ZHAO Y, CHEN J P, WU L. Progress in the study of nitrogen non-point source pollution in agricultural groundwater[J]. Environmental Pollution and Control, 2016, 38(5): 111. |
| [8] |
陈平, 倪龙琦. 河湖底泥中氮磷迁移转化的研究进展[J]. 徐州工程学院学报(自然科学版), 2020, 35(2): 60-66. CHEN P, NI L Q. Research progress on nitrogen and phosphorus migration and transformation in river and lake sediment[J]. Journal of Xuzhou Institute of Technology(Natural Science Edition), 2020, 35(2): 60-66. |
| [9] |
潘维艳. 再生水回补河湖条件下污染物的迁移转化机制研究[D]. 北京: 中国农业大学, 2017: 10-12. PAN W Y. Removal and transformation of pollutant during refilling rivers and lakes process[D]. Beijing: China Agricultural University, 2017: 10-12. |
| [10] |
吴振斌, 徐光来, 周培疆, 等. 复合垂直流人工湿地污水氮的去除效果研究[J]. 农业环境科学学报, 2004, 23(4): 757-760. WU Z B, XU G L, ZHOU P J, et al. Removal effects of nitrogen in integrated vertical flow constructed wetland sewang treating systtem[J]. Journal of Agro-Environmental Science, 2004, 23(4): 757-760. DOI:10.3321/j.issn:1672-2043.2004.04.031 |
| [11] |
ASANO T, COTRUVO J A. Groundwater recharge with reclaimed municipal wastewater: Health and regulatory considerations[J]. Water Research, 2004, 38(8): 1941-1951. DOI:10.1016/j.watres.2004.01.023 |
| [12] |
闫雅妮, 马腾, 张俊文, 等. 地下水与地表水相互作用下硝态氮的迁移转化实验[J]. 地球科学, 2017, 42(5): 783-792. YAN Y N, MA T, ZHANG J W, et al. Experiment onmigration and transformation of nitrate under interaction of groundwater and surface water[J]. Earth Science, 2017, 42(5): 783-792. |
| [13] |
闫雅妮, 廖曼, 王智真, 等. 河岸带介质中硝态氮衰减机制的实验研究[J]. 桂林理工大学学报, 2020, 40(1): 218-223. YAN Y N, LIAO M, WANG Z Z, et al. Experimental study on the attenuation mechanism of nitrate in riparian zone medium[J]. Journal of Guilin University of Technology, 2020, 40(1): 218-223. |
| [14] |
许宽, 刘波, 王国祥, 等. 曝气和pH对城市污染河道底泥氮形态的影响[J]. 环境工程学报, 2012, 6(10): 3553-3558. XU K, LIU B, WANG G X, et al. Influence of aeration and pH on nitrogen in urban heavily polluted river sediment[J]. Chinese Journal of Environmental Engineering, 2012, 6(10): 3553-3558. |
| [15] |
李金荣, 王莉, 陈停, 等. 溶解氧影响河流底泥中氮释放的实验研究[J]. 中国农村水利水电, 2012(5): 32-34, 38. LI J R, WANG L, CHEN T, et al. A study of DO on nitrogen releasing in the sediment of river[J]. China Rural Water and Hydropower, 2012(5): 32-34, 38. |
| [16] |
REGNERY J, BARRINGER J, WING A D, et al. Start-up performance of a full-scale riverbank filtration site regarding removal of DOC, nutrients, and trace organic chemicals[J]. Chemosphere, 2015, 127: 136-142. DOI:10.1016/j.chemosphere.2014.12.076 |
| [17] |
鲍士旦. 土壤农化分析[M]. 三版. 北京: 中国农业出版社, 2000: 204-208. BAO S D. Soil agrochemical analysis[M]. 3rd Edition. Beijing: China Agriculture Press, 2000: 204-208. |
| [18] |
刘彩堂, 宋献方, 于静洁. 一种土壤水分采集装置: 200520110649. 5[P]. 2006-08-23. LIU C T, SONG X F, YU J J. A device for suction of soil water: 200520110649. 5[P]. 2006-08-23. |
| [19] |
国家环境保护总局. 水和废水监测分析方法[M]. 四版. 北京: 中国环境科学出版社, 2002: 701-705. State Environmental Protection Administration. Methods for monitoring and analysis of water and wastewater[M]. 4th Edition. Beijing: China Environmental Science Press, 2002: 701-705. |
| [20] |
李一平, 逄勇, 向军. 太湖水质时空分布特征及内源释放规律研究[J]. 环境科学学报, 2005, 25(3): 300-306. LI Y P, PANG Y, XIANG J. Analysis to the characteristics of temporal and spatial distribution of the pollutant and the law of release from sedment in Taihu Lake[J]. Acta Scientiae Circumstantiae, 2005, 25(3): 300-306. DOI:10.3321/j.issn:0253-2468.2005.03.004 |
| [21] |
黄瑞华, 吴耀国, 李云峰, 等. 硝态氮在河床垂向渗滤系统中环境行为的模拟实验[J]. 地球科学与环境学报, 2006, 28(3): 92-96. HUANG R H, WU Y G, LI Y F, et al. Simulating experiment of NO3--N in vertical system of riverbank filtration[J]. Journal of Earth Sciences and Environment, 2006, 28(3): 92-96. DOI:10.3969/j.issn.1672-6561.2006.03.020 |
| [22] |
李薇. 溶解氧水平对富营养化水体底泥氮磷转化影响的研究[D]. 南京: 南京理工大学, 2014: 12-14. LI W. Study on the impact of DO on the release of nitrogen and phosphorus from sediment in eutrophic water[D]. Nanjing: Nanjing University of Technology, 2014: 12-14. |
| [23] |
SHAO L, XU Z X, YIN H L, et al. Rice husk as carbon source and biofilm carrier for water denitrification[J]. Journal of Biotechnology, 2008, 136(Suppl): 662. |
| [24] |
杨磊, 林逢凯, 胥峥, 等. 底泥修复中温度对微生物活性和污染物释放的影响[J]. 环境污染与防治, 2007, 29(1): 22-25, 29. YANG L, LIN F K, XU Z, et al. Effect of temperature on the activities of microorganism and the pollutants release in the bioremediation of the sediment[J]. Environmental Pollution and Control, 2007, 29(1): 22-25, 29. DOI:10.3969/j.issn.1001-3865.2007.01.006 |
| [25] |
王子珏. 处理低污染河水湿地内氮迁移转化过程模拟分析[D]. 上海: 上海交通大学, 2014: 22-24. WANG Z J. Simulation of nitrogen transfer processes in a constructed wetland for a lightly contaminated river[D]. Shanghai: Shanghai Jiao Tong University, 2014: 22-24. |
| [26] |
高太忠, 付海燕. 氮在河北平原包气带中的迁移转化机制[J]. 安全与环境学报, 2015, 15(1): 217-221. GAO T Z, FU H Y. Migration and transformation regularity of nitrogen in vadose zone in Hebei plain[J]. Journal of Safety and Environment, 2015, 15(1): 217-221. |
| [27] |
杨岚鹏, 李娜, 张军. pH对浅层地下水中"三氮" 迁移转化的影响[J]. 中国农学通报, 2017, 33(30): 56-60. YANG L P, LI N, ZHANG J. Effect of pH value on migration and transformation of "three nitrogen" in shallow groundwater[J]. Chinese Agricultural Science Bulletin, 2017, 33(30): 56-60. |
| [28] |
程谊, 黄蓉, 余云飞, 等. 应重视硝态氮同化过程在降低土壤硝态氮质量浓度中的作用[J]. 土壤学报, 2017, 54(6): 1326-1331. CHENG Y, HUANG R, YU Y F, et al. Role of microbial assimilation of soil NO3- in reducing soil NO3- concentration[J]. Acta Pedologica Sinica, 2017, 54(6): 1326-1331. |
| [29] |
郭瑜, 彭党聪, 张新艳, 等. 硝态氮为唯一氮源时异养微生物增长特性[J]. 环境工程学报, 2014, 8(3): 882-886. GUO Y, PENG D C, ZHANG X Y, et al. Growth characteristics of heterotrophic bacteria with nitrate as a sole nitrogen source[J]. Chinese Journal of Environmental Engineering, 2014, 8(3): 882-886. |
| [30] |
夏绮文, 李炳华, 何江涛, 等. 潮白河再生水生态补给河道区浅层地下水氮转化[J]. 环境科学研究, 2021, 34(3): 618-628. XIA Q W, LI B H, HE J T, et al. Nitrogen transformation of shallow groundwater in the river area of ecological recharge of reclaimed water in Chaobai River[J]. Research of Environmental Sciences, 2021, 34(3): 618-628. |
| [31] |
潘维艳, 黄权中, 张子元, 等. 不同补水方式下砂壤土渗滤系统对硝态氮去除效果[J]. 农业工程学报, 2017, 33(8): 197-203. PAN W Y, HUANG Q Z, ZHANG Z Y, et al. Removal effect of nitrate nitrogen for sandy loam filtration system under different water supply conditions[J]. Transactions of the Chinese Society of Agricultural Engineering, 2017, 33(8): 197-203. |
| [32] |
杨杉, 吴胜军, 蔡延江, 等. 硝态氮异化还原机制及其主导因素研究进展[J]. 生态学报, 2016, 36(5): 1224-1232. YANG S, WU S J, CAI Y J, et al. The synergetic and competitive mechanism and the dominant factors of dissimilatory nitrate reduction progress: A review[J]. Acta Ecologica Sinica, 2016, 36(5): 1224-1232. |
| [33] |
胡喆. 南四湖沉积物-水体界面氮磷迁移转化规律研究[D]. 济南: 山东建筑大学, 2015. HU Z. Study on migration and transformation of nitrogen and phosphorus in the sediment-water interface of Nansi Lake[D]. Jinan: Shandong Jianzhu University, 2015. |
| [34] |
RÜTTING T, BOECKX P, MÜLLER C, et al. Assessment of the importance of dissimilatory nitrate reduction to ammonium for the terrestrial nitrogen cycle[J]. Biogeosciences, 2011, 8(7): 1779-1791. DOI:10.5194/bg-8-1779-2011 |
| [35] |
王飞. 潜流带氮素迁移转化过程的影响因素研究[D]. 长春: 吉林大学, 2013. WANG F. Study on the influencing factors of transformation-transportation processes for nitrogen in hyporheic zone[D]. Changchun: Jilin University, 2013. |
 2022, Vol. 41
2022, Vol. 41



