2. 浙江省土壤污染生物修复重点实验室,杭州 311300
2. Key Laboratory of Soil Contamination Bioremediation of Zhejiang Province, Zhejiang A & F University, Hangzhou 311300, China
汞(Hg)是一种生物非必需重金属元素,具有极强的生物毒性和生物富集效应。自1956年日本发生“水俣病”事件以来,Hg及其化合物受到社会的广泛关注。水、土壤等环境的Hg污染已成为全球性问题[1]。我国是全球最大的Hg生产、使用和排放国,以2017年为例:世界汞矿开采量约为3 790 t,其中我国占近90%[2]。有学者预计2050年的全球Hg排放量将在2 390~4 860 t[3]。环境中的Hg主要以元素汞(Hg0)、无机汞(Hg+、Hg2+)和有机汞3种形式存在,其中以有机汞中的甲基汞(MeHg)毒性最强,其对人类及食鱼生物有极强的毒性效应[4]。研究表明,自然环境中的厌氧微生物可将无机汞转化为MeHg[5],人类MeHg暴露的主要途径为食用大米或鱼类等水产品[6]。
生物炭、底泥、有机黏土、藻类等均可有效吸附水溶液中的MeHg[1, 7-9],但其对MeHg的去除能力不尽相同。生物炭是一种富含碳的新型环境多功能材料,具有比表面积大、表面含氧官能团丰富和吸附位点多等特点[10],在温室气体减排、农业土壤改良、农作物增产以及土壤污染修复等方面有着巨大的应用潜力,是近年来的研究热点之一[11-13]。但在实际应用中,生物炭存在吸附选择性差、易吸附饱和、结合能力弱、易解析和长效性不足等缺点[14]。为提高生物炭对不同污染物的吸附容量和去除能力,广大研究人员通过多种物理化学以及生物等方法对其进行表面修饰,以提高其吸附能力,从而达到修复目标[15-16]。如杨雪玲等[10]成功制备的壳聚糖改性生物炭能明显降低土壤及间歇水中总汞和MeHg的含量;彭阳[17]通过有机酸对微藻进行改性,增加了其表面孔隙结构和酸性位点的数量,从而显著提高其对Hg(Ⅱ)的去除性能。也有研究表明,通过对芦苇和松树锯末生物炭进行化学活化不仅没有增强其对MeHg的吸附,反而降低了其对MeHg的吸附[18]。研究表明,木材生物炭在去除Hg时不仅有Hg—C π键的形成,还有羧基和羟基与Hg的络合作用,经硫化后还增加了C—Sox—C键与Hg的相互作用[19]。刘俊[20]制备的Cl2等离子体改性生物炭增加了活性位点C—Cl基团的数量,从而提高了Hg0的去除效率。
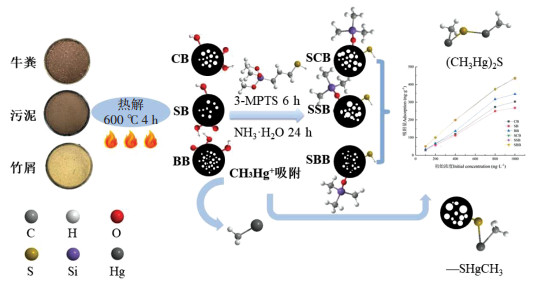
在吸附材料上嫁接对Hg具有高亲和力的功能基团——巯基(—SH)能够明显提高其对Hg的吸附能力,具有很好的土壤Hg污染稳定化修复效果[14]。目前,有关生物炭对Hg2+的络合机理已有研究报道,但是关于其对MeHg的络合机理特征尚不清楚。且—SH的改性技术多针对于镉、铅、铜、锌等重金属[21-24],而对MeHg的吸附特征还鲜有报道。3-巯丙基三甲氧基硅烷是一种常用的硫醇改性化学物质,带有—SH官能团,重金属亲和力强,广泛应用于水溶液中重金属的吸附研究[25]。近年来,有关生物炭的研究多针对单一类型原料制备的生物炭,不同类型原料制备的生物炭对MeHg的吸附特征鲜有报道。因此,本文采用3-巯丙基三甲氧基硅烷对牛粪、污泥、竹屑3种生物炭进行改性,引入—SH官能团,并对改性前后的生物炭与MeHg的络合特征及机理进行探索分析,为理解不同来源的巯基改性生物炭对水中MeHg的去除机制提供依据。
1 材料与方法 1.1 生物炭的处理及改性供试生物炭原料牛粪、污泥和竹屑分别来自于临安某农家肥、临安市生活污水处理厂和竹材料加工厂。将3种原料自然风干、去除杂物、破碎、过10目筛,105 ℃下烘干2 h后分别放于自封袋中备用。
将经上述处理的原材料置于箱式气氛炉(上海一恒,中国)中以10 ℃·min-1的升温速率在600 ℃下热解2 h,全程充氮气作为保护气。待其冷却后将所得牛粪炭(CB)、污泥炭(SB)、竹屑炭(BB)样品经研磨过60目筛保存备用。
分别称取6.0 g不同类别生物炭于250 mL的锥形瓶中,依次加入7.2 mL水、228 mL乙醇及4.8 mL 3-巯丙基三甲氧基硅烷,搅拌6 h后,滴加NH3·H2O调节pH为9.5,继续反应24 h[15]。随后用去离子水和无水乙醇洗涤至中性,于70 ℃烘干,将所得巯基改性牛粪炭(SCB)、巯基改性污泥炭(SSB)、巯基改性竹屑炭(SBB)保存备用。
1.2 实验设计 1.2.1 吸附动力学实验准确称取各生物炭0.050 0 g于50 mL离心管中,加入25 mL浓度为1 000 ng·L-1的MeHg标准溶液,在25 ℃、180 r·min-1条件下振荡,分别于0.5、1、2、4、8、16、24 h取样,置于高速冷冻离心机(Hitachi,日本)下12 000 r·min-1高速离心20 min后,取5 mL上清液用MERX型形态汞/总汞分析仪测定其MeHg浓度。每种处理设置3个重复。
1.2.2 等温吸附实验准确称取各生物炭0.050 0 g于50 mL离心管中,加入25 mL浓度分别为100、200、400、800、1 000 ng·L-1的MeHg标准溶液,在25 ℃、180 r·min-1条件下振荡8 h,置于高速冷冻离心机下12 000 r·min-1高速离心20 min后,取5 mL上清液用MERX型形态汞/总汞分析仪测定其MeHg浓度。每种处理设置3个重复。
1.3 样品分析比表面积和孔径分布(BET):以氮气为吸附质气体,采用全自动比表面积及孔隙度分析仪(麦克2460,美国)测定3种生物炭改性前后比表面积的变化。
扫描电镜(SEM):采用SEM扫描电镜(Phenom ProX,荷兰)观察5 000倍下牛粪、污泥、竹屑3种生物炭改性前后的形貌特征变化。
傅里叶变换红外光谱(FTIR):将制备的生物炭与溴化钾按1∶200质量比混合压片制样后采用傅里叶变换红外光谱仪(Thermo Scientific Nicolet iS 50,美国)分析3种生物炭改性前后以及吸附前后官能团的变化。
元素组成:通过元素分析仪(Vario EL Cube,德国)分析测定3种生物炭改性前后C、H、N、O、S元素的含量。
MeHg的测定:采用蒋红梅等[26]的蒸馏-乙基化结合气相色谱-冷原子荧光法(CVAFS法,最低检出限0.009 ng·L-1)在MERX型形态汞/总汞分析仪(Brooks Rand Lab,美国)上测定溶液中MeHg的质量浓度。测定步骤主要分为蒸馏、乙基化、预富集和上机测定4部分。其中蒸馏是为了消除基体的干扰,在135 ℃下加热二连通的Teflon蒸馏瓶,使气相中的MeHg随氮气进入接收瓶。乙基化过程是为了将溶液中的MeHg在pH为4.9和NaBEt4存在的条件下,转化为挥发性更强的甲基乙基汞。预富集过程旨在速率40~45 mL· min-1下通入氮气17 min,使甲基乙基汞富集到Tenax管上。
1.4 质量控制所有实验及样品测定均设定3个平行样,每批次样品均设定3个空白样品,控制其相对标准偏差小于20%,加标回收率介于80.5%~95.2%之间。实验使用的所有玻璃仪器均用10% 的硝酸浸泡24 h以上,并经电阻炉500 ℃灼烧2 h,再置于洁净无汞的环境中待自然冷却后使用。实验过程中佩戴一次性手套防止交叉污染。实验分析过程中,严格按照US EPA Method 1630所要求的质量控制过程进行操作,以确保实验质量。
2 结果与分析 2.1 理化性质采用元素分析仪测定各生物炭中C、H、O、N和S元素的质量组成和原子比,结果见表 1。通常用H/C和(N+O)/C原子比表征材料的芳香性和极性指数的大小,H/C比值越小,芳香性越强,而(N+O)/C比值越大,则极性越大。由表 1可知,不同原料热解所得生物炭的H/C比值小,炭化程度高,芳香性强,极性大,其中以BB的热解效果最好。在改性后,3种生物炭的S含量显著增加,说明本实验成功将含硫官能团引入生物炭中。
|
|
表 1 不同生物炭改性前后的元素组成 Table 1 Elementary composition of raw and thiol-modified biochar |
扫面电镜照片能够直观地展示不同生物炭的表面结构,了解其孔隙结构。牛粪、污泥、竹屑3种原料热解所得生物炭改性前后的5 000倍电镜照片见图 1。

|
图 1 生物炭改性前、后电镜扫描图(×5 000倍) Figure 1 SEM images of raw and thiol-modified biochar(×5 000 times) |
由图 1可知,3种生物炭改性前表面粗糙,零星分布着一些碎屑状物质;改性后,表面均增加了很多颗粒物。表明改性材料负载到生物炭表面后,提供了大量络合位点,使改性后的生物炭拥有良好的物理和化学吸附能力,有利于对MeHg络合能力的提高。CB在改性后,生物炭内部孔隙增加,从而增大了其比表面积。SB在改性后,表面形貌变化明显,团状结构被破坏,表面碎裂,孔隙变大,颗粒变小,更有利于其对MeHg的吸附。BB较CB和SB而言,束管状结构明显,孔隙结构均匀致密,为多孔的网状结构,孔壁较为光滑,能够明显观察到孔壁内的微孔小而密集。改性后其表面变得粗糙,颗粒增加,同时孔隙有一定程度上的堵塞,这可能是由于改性后,其表面负载上了丰富的表面基团。
2.2 等温吸附模型分别采用Langmuir线性方程(1)和Freundlich线性方程(2)拟合生物炭对MeHg的等温吸附过程,结果见表 2。

|
(1) |

|
(2) |
|
|
表 2 不同生物炭对MeHg的等温吸附拟合相关参数 Table 2 Isothermal adsorption parameters of MeHg by raw and thiol-modified biochar |
式中:qe为MeHg的平衡吸附量,ng·g-1;qm为MeHg的最大吸附量,ng·g-1;Ce为MeHg的平衡浓度,pg·mL-1;b为Langmuir方程的吸附常数,mL·pg-1;Kf和n为Freundlich方程关于吸附容量和吸附强度且只与温度有关的吸附常数。通常,Freundlich方程中1/n在0~1范围内表示吸附容易进行,大于2则表示吸附难以进行;Langmuir方程中b大于0说明吸附过程为自发进行。
Langmuir模型适于描述均相表面的单分子层吸附,而Freundlich模型适用于非均相体系的多分子层吸附过程。由表 2可知,两种吸附模型均能很好地拟合6种生物炭对MeHg的等温吸附过程,但更偏向于Langmuir模型,说明生物炭对MeHg的吸附以单分子层吸附为主,其表面的吸附位点分布均匀,以化学吸附为主。Langmuir模型的拟合曲线见图 2。

|
图 2 不同生物炭对MeHg的Langmuir等温吸附曲线 Figure 2 Langmuir isotherm of MeHg by raw and thiol-modified biochar |
比较生物炭改性前后qm值可知,3种改性生物炭对MeHg的吸附容量均有不同程度的增大,其中SCB对MeHg的吸附效果提升最为明显,其理论吸附量提高了3倍以上。BB孔隙丰富,有利于MeHg的吸附,但其孔隙在改性后有一定程度的堵塞,故SBB对MeHg的吸附效果提升不明显。而SCB、SSB由于表面基团的作用,对MeHg的络合能力有所提高。比较Langmuir方程中不同生物炭b值(SBB > SCB > SSB > 0)发现,改性后的不同原料生物炭对MeHg的吸附能力均显著大于改性前,且吸附过程为自发进行。
2.3 动力学吸附模型分别采用准一级反应动力学方程(3)和准二级反应动力学方程(4)对生物炭吸附MeHg的动力学进行拟合:

|
(3) |

|
(4) |
式中:qe为MeHg的平衡吸附量,ng·g-1;qt为t时刻MeHg的吸附量,ng·g-1;k1为准一级动力学常数,min-1;k2为准二级动力学常数,g·ng-1·min-1。
由图 3可知,相比于改性前,经过巯基改性后的3种生物炭对MeHg的吸附能力显著增强,吸附平衡时间明显缩短,对MeHg的吸附主要集中在前30 min。随着吸附时间的延长,生物炭对MeHg的吸附量缓慢增大到一定量后基本保持不变,说明达到吸附平衡,24 h的吸附量均在390 ng·g-1左右。这可能是因为生物炭对MeHg的吸附主要是通过离子交换和表面配合进行,当吸附时间足够长时,孔道堵塞,有效吸附位点减少,造成吸附速度减慢,直至吸附平衡。

|
图 3 不同生物炭对MeHg的动力学吸附曲线 Figure 3 Kinetics adsorption curves of MeHg by raw and thiol-modified biochar |
由表 3可知,6种生物炭对MeHg的吸附均符合准一级、准二级动力学方程(R2 > 0.9),但更偏向于准二级动力学方程,其理论吸附量与实验结果更为接近。比较生物炭对MeHg的吸附速率常数k2(SCB > CB;SSB > SB;SBB > BB)可知,改性后的生物炭对MeHg的络合是一个更为快速的吸附过程。
|
|
表 3 不同生物炭对MeHg的吸附动力学拟合相关参数 Table 3 Fitted kinetics parameters of MeHg adsorption by raw and thiol-modified biochar |
傅里叶变换红外光谱图可反映出物质所含的官能团种类及其所处的化学环境,从而推断出物质结构。牛粪、污泥、竹屑3种原料热解生物炭改性前后的傅里叶变换红外光谱图如图 4所示。

|
图 4 生物炭巯基改性前、后红外光谱图 Figure 4 FTIR of raw and thiol-modified biochar |
除BB外,CB和SB的含氧官能团(—OH、C=O、C—O)吸收特征峰的位置基本相同,但不同特征峰的峰强存在差异(图 4)。这表明在热解温度为600 ℃的条件下,BB的饱和烃或纤维素等基团已被裂解完全,表面官能团减少;而CB和SB的基团种类基本相同,但官能团的丰富程度不同。这是因为当热解温度逐渐升高至600 ℃时,竹屑所含主要成分纤维素和木质素已分解完全,而牛粪的脂肪族烷基烃逐渐消失,芳香性增强[27-28]。分析谱图可知,3种原料热解所得的生物炭经过改性后,吸收特征峰强度增加且出峰位置增多。这表明改性后的生物炭表面官能团种类更加丰富,官能团数量明显增多,从而增加了表面活性位点,有利于提高其吸附能力[28]。
—SH的伸缩振动峰在2 400~2 580 cm-1范围内[29]。由于—SH伸缩振动的固有弱偶极子,基团灵敏度低,因此不易检出[30]。3-巯丙基三甲氧基硅烷中含有硅氧键(Si—O),其伸缩振动峰在1 020~1 090 cm-1范围内。由图 4可知,SCB、SSB、SBB分别在1 034、1 033、1 040 cm-1位置出现特征吸收峰,间接证明了巯基引入成功[29],且在1 245、1 247、1 247 cm-1位置出现C=S双键的伸缩峰,也进一步验证了生物炭改性成功。与CB、SB、BB相比,SCB、SSB、SBB在3 430 cm-1处的醇羟基(—OH)伸缩振动均有不同程度的增强,表面羟基的增多一定程度上可以促进重金属离子沉淀反应的发生。在1 600 cm-1和1 500 cm-1处的振动带属于C=O键(酮、醛、酸)以及芳环上C=C基团的伸缩骨架振动峰,并且3种改性生物炭在690~900 cm-1之间出现了芳香C—H平面外弯曲振动峰[31],在1 100 cm-1处有C—O键拉伸和—OH键变形的峰值重合,说明酮类、酯类、羰基等芳香结构形成,芳香性增强,有利于提高生物炭的络合能力。
经过热解,3种生物炭表面变得粗糙,这可能是由于生物炭热解温度较高,原料受热释放热量,使内部孔道冲开,因而孔道分布变得无序,使生物炭表面变得粗糙[32]。改性过后,3种生物炭比表面积均有不同程度增加,孔径变大,表面基团增多,这有利于其对MeHg的吸附[33]。在Langmuir模型的吸附研究中常使用分离常数RL[RL=1/(1+b×C0)]来衡量吸附过程是否良性,是否有利于吸附进行[34]。当RL处于0~1之间时,表明该吸附过程是良性的。由表 2可知,6种生物炭对MeHg的吸附过程均为良性。且BHATT等[35]关于硫代壳聚糖聚合物对Hg的吸附研究结果表明,Kf值的大小与吸附质是否易于吸附在吸附剂表面有关。通过比较表 2中的Kf值(SCB > CB;SSB > SB;SBB > BB)可以发现,改性后的生物炭对MeHg的吸附更容易发生。因此,生物炭对MeHg的吸附反应机制可能是生物炭表面官能团与MeHg之间电子对公用或转移从而产生价电子力的络合作用[21, 35]。本实验中所选用的MeHg浓度较低,颗粒内扩散速率可能较小,吸附速率受到化学吸附机理的控制,其吸附过程主要以表面吸附为主[29]。
吸附材料所含成分、内部结构以及表面基团是影响其吸附重金属行为的重要因素[8],其表面功能基团种类和数量也会影响材料的吸附效果。功能化吸附材料具有吸附效率高、二次污染小等特点,对重金属的去除发挥着重要作用。研究—SH功能化生物炭对MeHg吸附机制,推进其市场应用,具有一定的现实意义。
SCB、SSB和SBB对MeHg吸附前后的傅里叶红外光谱图(FTIR)如图 5所示。

|
图 5 巯基改性生物炭对MeHg吸附前后的红外谱图 Figure 5 FTIR of thiol-modified before and after the MeHg adsorption |
经图谱分析可知,3种改性生物炭在吸附MeHg后,部分吸收特征峰发生了位置移动和强度变化。与吸附前相比,SCB、SSB和SBB表面的—OH伸缩峰有轻微减弱,且其位置发生了偏移,这是因为在MeHg的吸附过程中,—OH同样起到了络合作用。SCB、SSB和SBB分别在580、570、575 cm-1处出现了C—S吸收峰的减弱和偏移,这表明C—S键在参与MeHg的络合过程中形成了—SHgCH3和(CH3Hg)2S[15]。吸附MeHg后,SCB在1 426 cm-1处的C=O、C=C的基团出现了峰的位移,并且1 095 cm-1处的C—O特征峰增强,这表明C=O、C=C是反应活位,参与MeHg的吸附过程。SSB在吸附MeHg后,1 650~1 960 cm-1处的C=O伸缩振动吸收峰和1 120 cm-1处的C—O伸缩振动峰减弱,可能是由于形成了O—Hg(Ⅱ)基团,伴随着生物炭表面结构中O、S原子附近的电荷重分布改变而导致正振动峰的强度和频率发生变化,这表明SSB表面的C—O基团也参与了MeHg的络合过程。比较改性前后生物炭的吸附容量,未改性的3种生物炭对MeHg的吸附能力较弱,其吸附过程更符合拟二级动力学模型,由化学吸附控制,涉及生物炭与MeHg之间的电子对共享和转移。经过巯基改性的3种生物炭对MeHg的吸附能力均明显提高,这与生物炭表面引入的—SH有关。对于MeHg,—SH与MeHg络合形成配合物的稳定常数要大于羟基、羧基和氨基[15],所以SCB、SSB、SBB对MeHg的吸附主要依赖于其表面嫁接的—SH与MeHg的络合,这与其他巯基改性吸附材料的结果一致[24, 36-38]。MeHg与炭表面基团稳定络合后,在吸附30 min后趋于吸附平衡,表明生物炭对MeHg的去除主要是通过其表面官能团与MeHg的稳定络合实现的。
4 结论(1)3种生物炭改性前后对MeHg的吸附均符合准一级、准二级动力学方程,但更偏向于准二级动力学方程。
(2)巯基改性后的生物炭对MeHg的吸附以单分子层吸附为主,其表面的吸附位点分布均匀,通过化学键的作用吸附MeHg。
(3)巯基改性的作用主要是增加生物炭表面—SH和C—S等官能团。吸附反应后,C—S吸收峰出现了减弱和偏移,这主要是因为其与MeHg进一步形成—SHgCH3和(CH3Hg)2S等络合物。
(4)生物炭对MeHg的吸附反应机制主要是生物炭表面官能团与MeHg之间公用或交换电子从而产生价电子力的络合作用。
| [1] |
MULLER K A, BRANDT C C, MATHEWS T J, et al. Methylmercury sorption onto engineered materials[J]. Journal of Environmental Management, 2019, 245: 481-488. |
| [2] |
冯新斌, 史建波, 李平, 等. 我国汞污染研究与履约进展[J]. 中国科学院院刊, 2020, 35(11): 1344-1350. FENG X B, SHI J B, LI P, et al. Progress of mercury pollution research and implementation of minamata convention in China[J]. Bulletin of Chinese Academy of Sciences, 2020, 35(11): 1344-1350. |
| [3] |
STREETS D, ZHANG Q, WU Y. Projections of global mercury emissions in 2050[J]. Environmental Science & Technology, 2009, 43(8): 2983-2988. |
| [4] |
冯新斌, 仇广乐, 付学吾, 等. 环境汞污染[J]. 化学进展, 2009, 21(2/3): 436-457. FENG X B, QIU G L, FU X W, et al. Mercury pollution in the environment[J]. Progress in Chemistry, 2009, 21(2/3): 436-457. |
| [5] |
GILMOUR C C, RIEDEL G S, RIEDEL G, et al. Activated carbon mitigates mercury and methylmercury bioavailability in contaminated sediments[J]. Environmental Science & Technology, 2013, 47(22): 13001-13010. |
| [6] |
李平, 冯新斌, 仇广乐. 贵州汞矿区居民食用大米的甲基汞暴露及健康风险评价[J]. 生态学杂志, 2011, 30(5): 914-921. LI P, FENG X B, QIU G L. Methylmercury exposure through rice consumption and its health risk assessment for the residents in Guizhou mercury mining areas[J]. Chinese Journal of Ecology, 2011, 30(5): 914-921. |
| [7] |
邵长来, 麻冰涓, 毛宇翔, 等. 活性污泥对水中低浓度无机汞和甲基汞的吸附特性[J]. 环境化学, 2016, 35(6): 1261-1268. SHAO C L, MA B J, MAO Y X, et al. Study on the adsorption characteristics of low-level inorganic mercury and methylmercury in aqueous solution by activated sludge[J]. Environmental Chemistry, 2016, 35(6): 1261-1268. |
| [8] |
刘朝淑, 莫雅斐, 孙荣国, 等. 水华束丝藻和铜绿微囊藻对水中甲基汞的吸附特征及动力学研究[J]. 地球与环境, 2020, 48(4): 518-524. LIU C S, MO Y F, SUN R G, et al. Study on adsorption characteristics and kinetics of methylmercury in water by aphanizomenon flosaquae and microcystis aeruginosa[J]. Earth and Environment, 2020, 48(4): 518-524. |
| [9] |
刘军晖, 麻冰涓, 毛宇翔, 等. 微藻对无机汞和甲基汞的吸附和吸收特性[J]. 环境化学, 2017, 36(7): 1602-1613. LIU J H, MA B J, MAO Y X, et al. Adsorption and absorption characteristics of inorganic mercury and methylmercury by microalgae[J]. Environmental Chemistry, 2017, 36(7): 1602-1613. |
| [10] |
杨雪玲, 王明星, 徐国敏, 等. 壳聚糖改性生物炭对水稻土甲基汞生成及其稻米积累的影响[J]. 环境科学, 2021, 42(3): 1191-1196. YANG X L, WANG M X, XU G M, et al. Effects of chitosan-modified biochar on formation of methylmercury in paddy soils and its accumulation in rice[J]. Environmental Science, 2021, 42(3): 1191-1196. |
| [11] |
SHU R, WANG Y, ZHONG H. Biochar amendment reduced methylmercury accumulation in rice plants[J]. Journal of Hazardous Materials, 2016, 313: 1-8. DOI:10.1016/j.jhazmat.2016.03.080 |
| [12] |
陈志良, 袁志辉, 黄玲, 等. 生物炭来源、性质及其在重金属污染土壤修复中的研究进展[J]. 生态环境学报, 2016, 25(11): 1879-1884. CHEN Z L, YUAN Z H, HUANG L, et al. Pyrolysis materials, characteristics of biochar and its application on remediation of heavy metal contaminated soil: A review[J]. Ecology and Environmental Sciences, 2016, 25(11): 1879-1884. |
| [13] |
ROMERO C M, LI C, OWENS J, et al. Nutrient cycling and greenhouse gas emissions from soil amended with biochar-manure mixtures[J]. Pedosphere, 2021, 31(2): 289-302. DOI:10.1016/S1002-0160(20)60071-6 |
| [14] |
李述贤, 龚建军, 陈刚, 等. 氧化活性炭负载巯基修复汞污染土壤[J]. 环境保护科学, 2020, 46(5): 133-137. LI S X, GONG J J, CHEN G, et al. Remediation of mercury contaminated soil with sulfhydryl groups loaded on oxidized activated carbon[J]. Environmental Protection Science, 2020, 46(5): 133-137. |
| [15] |
HUANG Y, XIA S, LYU J, et al. Highly efficient removal of aqueous Hg2+ and CH3Hg+ by selective modification of biochar with 3-mercaptopropyltrimethoxysilane[J]. Chemical Engineering Journal, 2019, 360: 1646-1655. DOI:10.1016/j.cej.2018.10.231 |
| [16] |
韩怡新, 何天容, 王祖波. 改性蒙脱土对稻田土壤甲基汞的阻控修复[J]. 环境科学, 2019, 40(11): 5107-5113. HAN Y X, HE T R, WANG Z B. Inhibition and remediation of methylmercury contaminated soil by use of modified montmorillonite[J]. Environmental Science, 2019, 40(11): 5107-5113. |
| [17] |
彭阳. 微藻生物材料对工业污水二价汞的脱除性能及机理研究[D]. 武汉: 华中科技大学, 2018: 43-45. PENG Y. The efficiency and mechanism study on Hg(Ⅱ)removal in industrial wastewater by microalgae biomaterials[D]. Wuhan: Huazhong University of Science and Technology, 2018: 43-45. |
| [18] |
GOMEZ-EYLES J L, YUPANQUI C, BECKINGHAM B, et al. Evaluation of biochars and activated carbons for in situ remediation of sediments impacted with organics, mercury, and methylmercury[J]. Environmental Science & Technology, 2013, 47(23): 13721-13729. |
| [19] |
PARK J H, WANG J J, ZHOU B, et al. Removing mercury from aqueous solution using sulfurized biochar and associated mechanisms[J]. Environmental Pollution, 2019, 244: 627-635. DOI:10.1016/j.envpol.2018.10.069 |
| [20] |
刘俊. 等离子体改性生物炭对汞吸附性能和机理研究[D]. 北京: 华北电力大学(北京), 2018: 22-24. LIU J. Mechanism of elemental mercury adsorption by non-thermal plasma modified biochar[D]. Beijing: North China Electric Power University, 2018: 22-24. |
| [21] |
邓华, 严发, 陆志诚, 等. 巯基改性木薯秸秆对Cd(Ⅱ)吸附性能的研究[J]. 水处理技术, 2018, 44(6): 57-61. DENG H, YAN F, LU Z C, et al. Study on the adsorption of Cd(Ⅱ)by sulfydryl modified cassava straw[J]. Technology of Water Treatment, 2018, 44(6): 57-61. |
| [22] |
邓华, 李雅芬, 康彩艳, 等. 巯基改性木薯秸秆吸附水体Cu(Ⅱ)和Zn(Ⅱ)特性[J]. 水处理技术, 2021, 47(3): 22-27. DENG H, LI Y F, KANG C Y, et al. Adsorption characteristics of sulfhydryl modified cassava straw on Cu(Ⅱ)and Zn(Ⅱ)in water[J]. Technology of Water Treatment, 2021, 47(3): 22-27. |
| [23] |
FAN J, CAI C, CHI H, et al. Remediation of cadmium and lead polluted soil using thiol-modified biochar[J]. Journal of Hazardous Materials, 2020, 388: 122037. DOI:10.1016/j.jhazmat.2020.122037 |
| [24] |
李青竹, 覃文庆, 柴立元, 等. 巯基化改性麦糟对Zn(Ⅱ)的吸附特性[J]. 中国有色金属学报, 2014, 24(4): 1076-1083. LI Q Z, QIN W Q, CHAI L Y, et al. Adsorption characteristics of Zn(Ⅱ)on thiolfunctionalized spent grain[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(4): 1076-1083. |
| [25] |
DE MELLO FERREIRA GUIMARAES A, CIMINELLI V, VASCONCELOS W. Smectite organofunctionalized with thiol groups for adsorption of heavy metal ions[J]. Applied Clay Science, 2009, 42(3/4): 410-414. |
| [26] |
蒋红梅, 冯新斌, 梁琏, 等. 蒸馏-乙基化GC-CVAFS法测定天然水体中的甲基汞[J]. 中国环境科学, 2004, 24(5): 568-571. JIANG H M, FENG X B, LIANG L, et al. Determination of methyl mercury in waters by distillation-GC-CVAFS technique[J]. China Environmental Science, 2004, 24(5): 568-571. DOI:10.3321/j.issn:1000-6923.2004.05.014 |
| [27] |
沈王庆, 王淼, 杨婷. 柠檬渣吸附污水中Hg2+的动力学研究[J]. 光谱学与光谱分析, 2016, 36(3): 788-794. SHEN W Q, WANG M, YANG T. Study on kinetic of Hg2+ form wastewater absorbed by lemon residues[J]. Spectroscopy and Spectral Analysis, 2016, 36(3): 788-794. |
| [28] |
桂向阳, 刘晨, 许吉宏, 等. 畜禽粪便生物炭的二维红外光谱分析[J]. 光谱学与光谱分析, 2020, 40(11): 3606-3612. GUI X Y, LIU C, XU J H, et al. Two-dimensional perturbation correlation infrared spectroscopy analysis of animal manure biochar[J]. Spectroscopy and Spectral Analysis, 2020, 40(11): 3606-3612. |
| [29] |
姚璁, 何天容, 冉澍, 等. 巯基改性泥炭对水体中Hg2+的吸附解吸研究[J]. 工业水处理, 2020, 40(10): 67-71. YAO C, HE T R, RAN S, et al. Adsorption and desorption of Hg2+ in water by thiol group modified peat[J]. Industrial Water Treatment, 2020, 40(10): 67-71. |
| [30] |
RYU J, LEE M Y, SONG M G, et al. Highly selective removal of Hg(Ⅱ)ions from aqueous solution using thiol-modified porous polyaminal-networked polymer[J]. Separation and Purification Technology, 2020, 250: 117120. DOI:10.1016/j.seppur.2020.117120 |
| [31] |
FUERTES A B, CAMPS ARBESTAIN M, SEVILLA M, et al. Chemical and structural properties of carbonaceous products obtained by pyrolysis and hydrothermal carbonisation of corn stover[J]. Australian Journal of Soil Research, 2010, 48: 618. DOI:10.1071/SR10010 |
| [32] |
索桂芳, 吕豪豪, 汪玉瑛, 等. 不同生物炭对氮的吸附性能[J]. 农业环境科学学报, 2018, 37(6): 1193-1202. SUO G F, LÜ H H, WANG Y Y, et al. Study on the adsorption properties of nitrogen by different biochars[J]. Journal of Agro-Environment Science, 2018, 37(6): 1193-1202. |
| [33] |
吴继阳, 郑凯琪, 杨婷婷, 等. 污泥生物炭对土壤中Pb和Cd的生物有效性的影响[J]. 环境工程学报, 2017, 11(10): 5757-5763. WU J Y, ZHENG K Q, YANG T T, et al. Remediation of Pb and Cd contaminated soil by sludge biochar[J]. Chinese Journal of Environmental Engineering, 2017, 11(10): 5757-5763. DOI:10.12030/j.cjee.201612044 |
| [34] |
冯彦房, 薛利红, 杨梖, 等. 载镧生物质炭吸附水体中As(Ⅴ)的过程与机制[J]. 农业环境科学学报, 2015, 34(11): 2190-2197. FENG Y F, XUE L H, YANG B, et al. Adsorption of As(Ⅴ)from aqueous solution by lanthanum oxide-loaded biochar: Process and mechanisms[J]. Journal of Agro-Environment Science, 2015, 34(11): 2190-2197. |
| [35] |
BHATT R, P P. A chitosan-thiomer polymer for highly efficacious adsorption of mercury[J]. Carbohydrate Polymers, 2019, 207: 663-674. DOI:10.1016/j.carbpol.2018.12.018 |
| [36] |
邵爱云, 程德义, 代静玉, 等. 巯基改性稻壳炭对水中Cd2+的吸附特性[J]. 生态与农村环境学报, 2019, 35(8): 1071-1079. SHAO A Y, CHENG D Y, DAI J Y, et al. Characteristice of Cd2+ adsorption from water by sulfhydryl group modified rice hull biochar[J]. Journal of Ecology and Rural Environment, 2019, 35(8): 1071-1079. |
| [37] |
LYU H, XIA S, TANG J, et al. Thiol-modified biochar synthesized by a facile ball-milling method for enhanced sorption of inorganic Hg2+ and organic CH3Hg+[J]. Journal of Hazardous Materials, 2020, 384: 121357. DOI:10.1016/j.jhazmat.2019.121357 |
| [38] |
WU Z, CHENG Z, MA W. Adsorption of Pb(Ⅱ)from glucose solution on thiol-functionalized cellulosic biomass[J]. Bioresource Technology, 2012, 104: 807-809. DOI:10.1016/j.biortech.2011.10.100 |
 2022, Vol. 41
2022, Vol. 41





