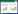文章信息
- 吕宏虹, 宫艳艳, 唐景春, 黄耀, 高凯
- LÜ Hong-hong, GONG Yan-yan, TANG Jing-chun, HUANG Yao, GAO Kai
- 生物炭及其复合材料的制备与应用研究进展
- Advances in Preparation and Applications of Biochar and Its Composites
- 农业环境科学学报, 2015, 34(8): 1429-1440
- Journal of Agro-Environment Science, 2015, 34(8): 1429-1440
- http://dx.doi.org/10.11654/jaes.2015.08.001
-
文章历史
- 收稿日期:2015-03-14
2. 天津市城市环境污染诊断与修复技术工程中心, 天津 300071;
3. 环境污染过程与基准教育部重点实验室, 天津 300071;
4. 天津市环境保护科学研究院, 天津 300191
2. Tianjin Engineering Center of Environmental Diagnosis and Contamination Remediation, Tianjin 300071, China;
3. Key Laboratory of Pollution Processes and Environmental Criteria(Ministry of Education), Tianjin 300071, China;
4. Tianjin Academy of Environmental Science, Tianjin 300191, China
生物炭(Biochar)一般是指生物质原材料在厌氧或缺氧的条件下,经一定的温度(<700℃)热解产生的含碳量高、具有较大比表面积的固体生物燃料,也称为生物质炭[1]。常见的生物炭包括木炭、稻壳炭、秸秆炭和竹炭等[2]。它们主要由芳香烃和单质碳或具有石墨结构的碳组成,除了C元素,还包括H、O、N、S以及少量的微量元素[3]。虽然生物炭的性质受制备条件的影响较大,但总体来说,生物炭比表面积大、容重小、稳定性高、吸附能力强[4],被广泛应用于生态修复、农业和环保领域[5]。将生物炭添加到土壤中,不仅可以增加土壤肥力,提高农作物产量,还能够有效吸附土壤或沉积物中的重金属(如Pb2+、Cd2+、Hg2+等)和有机污染物(如农药、PAHs等)[6]。同时,生物炭具有很高的化学稳定性、难以被微生物降解,可以起到固定大气碳素、增汇减排、缓解气候变化的作用。生物炭来源广泛,是一种更环保、更具成本效益的材料,因而有利于其在环境修复中推广应用[7]。
生物炭吸附污染物的能力取决于其物理、化学性质,不同的原料和裂解条件下制备的生物炭性质有很大的差别。Jeffery等[8]对比了不同裂解温度(250~700℃)制备的生物炭的物理和化学性质,发现随着裂解温度升高,生物炭的产率变低、灰分含量增大,比表面积增大、pH升高、表面电荷减少;高温裂解过程中,挥发性有机物的去除使得生物炭中C含量升高,H、O含量降低,生物炭表面离子官能团减少。离子官能团的减少在一定程度上降低了生物炭与金属离子的结合能力[9, 10]。另外,生物炭施加到环境中具有固液分离难的缺点。研究表明,一般复合材料对污染物的吸附效果优于单一材料[11]。因此,目前已经有部分学者关注生物炭与其他材料的组合使用,利用物理、化学方法将生物炭与其他材料组合制备成具有新性能、新结构的材料,其综合性能优于原组成材料,可满足各种不同的要求。
本文综述了生物炭及其复合材料的制备方法及在环境污染修复的应用。针对不同类别的生物炭复合材料,总结了制备的基本方法和对污染物的作用机理,为生物炭复合材料的研究和应用提供借鉴。 1 生物炭及其复合材料的制备与表征 1.1 生物炭及其复合材料的制备 1.1.1 生物炭
在传统农业阶段,农作物的废弃物一般是以焚烧还田的方式进行处理,人们通常采用将土覆盖在点燃的生物质上的方法实现在缺氧条件下的无烟燃烧,燃烧后的生物炭留在土壤中,可改良土壤并提高土壤肥力。随着技术的发展,目前生物炭的制备多在窑炉中进行,提高了效率,但基本原理与传统农业手段是相同的[12]。
目前制备生物炭常用的方法是热裂解法,即限氧升温炭化法。根据不同的反应条件可以将热裂解法分为两种:一是快速裂解法,反应温度一般在700℃以上,生物燃料的制备通常采用这种方法;另一种是常规裂解法,温度一般在700℃以下,生物炭主要用这种方法制备而成[13]。研究表明,生物质原材料的种类会对生物炭的性质(空间结构和性状)产生影响。在相同裂解条件下,不同生物质材料来源的生物炭不仅稳定性不同,对污染物的吸附能力、对土壤理化性质的影响亦不同[14, 15]。Ameloot等[16]报道了不同生物质来源对生物炭性能的影响,原材料中木质素含量越高,制备的生物炭材料中芳香C的含量和C:N比例越高,与此同时生物炭的矿化度越低。除了生物质原材料种类,裂解温度也是生物炭制备过程中一个非常关键的因素,它不仅能够影响生物炭的产率,还可以控制生物炭的表面结构和吸附性质。Chun等[17]报道了不同温度下(300~700℃)制备的生物炭的区别,发现随着温度升高(300~600℃),生物炭的比表面积增加(116~438 m2·g-1),而当裂解温度升高到700℃时,生物炭比表面积有所降低(363 m2·g-1),说明700℃时生物炭表面的一些细孔隙结构被破坏,可见温度是决定生物炭表面结构的重要因素。陈宝梁等[18]研究了300℃和700℃下裂解制得的生物炭与有机污染物(萘、苯酚、甲萘酚、间二硝基苯)相互作用机制,发现300℃下制备的生物炭对有机物的吸附由分配作用和表面吸附共同作用,700℃下制备的生物炭对有机物的吸附以表面吸附为主导。在利用凋落松针制备生物炭的研究中还发现,在100℃下制备的生物炭呈高极性和脂肪性,随着温度的升高(100~700℃),生物炭的芳香性剧增,但极性迅速降低,生物炭逐渐从"软碳质"过渡到"硬碳质",且比表面积迅速增加(0.65 m2·g-1增加到490.8 m2·g-1)[19]。Lu等[20]研究了不同裂解温度、不同保留时间对生物炭稳定性的影响,发现随着裂解温度的升高和保留时间的延长,生物炭中甲基(-CH3)和亚甲基(-CH2)逐渐消失,芳环结构增加,生物炭芳香化程度增强,H/C下降,可见裂解温度和裂解时间都会对生物炭性质产生影响。
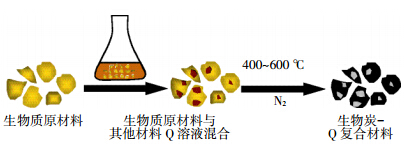
生物炭在环保领域的应用已经引起了国内外学者的普遍关注,然而因其具有高温裂解过程中损失部分离子官能团、吸附后固液分离难的不足,已经有学者开始研究将生物炭与其他材料复合,改善生物炭的物理和化学性质,加强其吸附能力。生物炭复合材料的制备通常是在生物质原材料中添加其他材料(磁性材料、纳米材料、无机盐等),再通过高温裂解制备成复合材料(流程如图 1所示)。以下介绍常见的几种生物炭复合材料。
|
| 图 1 生物炭复合材料制备流程 Figure 1 Procedure for preparing biochar-based composites |
利用生物炭自身具有的吸附性能,将其与其他材料复合制成新的材料,可以赋予生物炭新的性能。将吸附剂磁化是一种新兴的水治理技术,吸附后可以通过外加磁场将吸附材料回收,克服了非磁性吸附剂固液分离难的问题,从而为生物炭的应用提供了新的优势。根据目前的研究,大多学者选择通过将制备好的生物炭水悬浮液与Fe3+/Fe2+溶液混合,利用Fe3+/Fe2+将生物炭磁化,制备过程较简便、易操作。对比磁化后的生物炭性状(比表面积、孔径、表面元素组成、磁化强度等)和对污染物的吸附能力即可说明生物炭-磁性复合材料的优势。另外,从应用的角度看,生物炭价格低廉、来源广泛,与其他的磁性吸附剂(如磁性纳米氧化铁、零价铁等)相比具有较大的应用空间[21, 22, 23, 24, 25]。
Mohan等[25]首先将橡胶树木和橡胶树皮在400、450℃下快速裂解制成生物炭,将制得的生物炭悬浮液与Fe3+/Fe2+溶液混合,向其中加入NaOH调节反应体系的pH为10,经过陈化、清洗、烘干制得磁性橡木生物炭(MOWBC)和磁性橡树皮生物炭(MOBBC),详细流程如图 2所示。通过表征发现两种复合材料的含铁量增加,分别为1.40%~80.6%(MOWBC)、0.21%~51.3%(MOBBC),说明所采用的制备方法有效地将生物炭磁化。铁氧化物与生物炭复合的过程中降低了材料中有机物含量,使得复合材料的孔容增大(MOWBC 0.01~0.69 cm3·g-1;MOBBC 5.4×10-4~0.48 cm3·g-1),然而两种复合材料的比表面积出现了相反的变化,MOWBC的比表面积从2.04 m2·g-1增加到6.1 m2·g-1,而MOBBC的比表面积从25.4 m2·g-1下降到8.8 m2·g-1。这主要取决于NaOH溶液对生物炭表面柏油的去除,因为二者反应可生成可溶性盐,而对MOBBC来说,大量的Ca与NaOH溶液形成了不溶性盐,所以比表面积出现不同的变化趋势;另外,Fe3+的引入导致生物炭从单一颗粒转变为混合颗粒,复合材料的总体密度较难建立。这说明复合材料的比表面积变化趋势有所不同[26, 27]。将制得的复合材料用于处理水中的Pb2+、Cd2+,发现磁性生物炭的饱和吸附量(QMOWBC:Pb2+ 30.2 mg·g-1,Cd2+ 7.4 mg·g-1;QMOBBC:Pb2+ 10.13 mg·g-1,Cd2+ 2.87 mg·g-1)显著大于未经磁化的生物炭(QOWBC:Pb2+ 2.62 mg·g-1,Cd2+ 0.37 mg·g-1;QMOBBC:Pb2+13.10 mg·g-1,Cd2+ 5.40 mg·g-1)[28]。Devi等[29]合成了零价铁磁性生物炭(ZVI-MBC),首先将造纸污泥在700℃下裂解制成生物炭,然后将生物炭与十六烷基三甲基溴化铵(CTMB)混合,在95℃下烘干后,再加入到FeSO4·7H2O与NaBH4混合溶液中,充分搅拌30 min后过滤,将混合物烘干制得ZVI-MBC混合材料;复合之后ZVI-MBC的比表面积(BC 67 m2·g-1,ZVI-MBC 101.23 m2·g-1)和孔径(BC 3.17 nm,ZVI-MBC4.78 nm)都有所增加。通过傅里叶红外线光谱(FTIR)对比复合前后材料表面官能团变化,发现复合材料ZVI-MBC表面的官能团数量增加(羧基、醇羟基等);将复合材料ZVI-MBC用于实际废水中五氯苯酚(PCP)的去除,发现其对PCP的去除率显著提高(BC:~80%;ZVI-MBC:100%)。
综上所述,生物炭磁化之后比表面积和孔径增大,表面官能团增加,这些都是吸附污染物过程中的主要机制,因此磁性复合材料对污染物的去除能力显著提高,且吸附之后易于固液分离,只需外加磁场即可。1.1.3 生物炭-纳米复合材料
生物炭结合纳米材料制备新型复合材料,可以显著提高生物炭的性能,包括增强土壤肥力、碳的封存和污水处理。目前研究较多的生物炭-纳米复合材料主要是石墨烯、碳纳米管、纳米氧化物,此外还有纳米零价铁(后者赋予复合材料磁性,在磁性复合材料中已说明)。生物炭-纳米复合材料的制备多通过浸蘸法,即将生物质原材料直接与纳米材料的悬浮液混合,搅拌均匀后烘干,再在高温下限氧/绝氧裂解。制得的复合材料不仅比表面积大、表面电荷多、酸性官能团数量增加,且具有较好的热稳定性,利于应用。
Inyang等[30]采用浸涂法制备了碳纳米管/生物炭(Carbon nanotube-biochar),分别将生物质原材料山核桃木碎片和甘蔗渣浸泡在碳纳米管悬浮液中,充分搅拌1 h后在烘箱中烘干,然后将混合物置管式炉中600℃绝氧裂解1 h,制得碳纳米管-山核桃木生物炭复合材料(HC-CNT)和碳纳米管-甘蔗渣生物炭复合材料(BC-CNT)。与未经加工的山核桃木生物炭(HC)和甘蔗渣生物炭(BC)相比,碳纳米管的添加增大了生物炭的热稳定性、比表面积(HC:289 m2·g-1,HC-CNT:352 m2·g-1;BC:9 m2·g-1,BC-CNT:390 m2·g-1)、孔隙体积(HC:0.001 mL·g-1,HC-CNT:0.138 mL·g-1;BC:0.000 mL·g-1,BC-CNT:0.220 mL·g-1)、表面电荷(Zeta电位HC:-28.8 mV,HC-CNT:-41.4 mV;BC:-32.7 mV BC-CNT:-44.6 mV),这些性状的优化使得复合材料对亚甲基蓝的去除能力显著提高(HC:9%,HC-CNT:47%;BC:25%,BC-CNT:64%)。Zhang等[31]采用同样的方法制备了石墨烯包覆生物炭(Graphene-coated biochar)复合材料,将制成的复合材料应用于去除水中的亚甲基蓝,其对亚甲基蓝的饱和吸附量达到174 mg·g-1,远大于生物炭对亚甲基蓝的饱和吸附量8 mg·g-1。Zhang等[32]在600℃下制备了生物炭/纳米氧化铝复合材料用于去除水中的亚甲基蓝,其饱和吸附量由8 mg·g-1提高到85 mg·g-1,纳米氧化铝的添加显著提高了生物炭对亚甲基蓝的去除效果。
综上所述,纳米材料不仅具有大的比表面积可有效吸附各类污染物,而且其表面的化学官能团(羧基、羟基、胺基等)提供的高亲和性的吸附位点,能够增加纳米材料对污染物的结合能力。但纳米材料溶解性差,且在环境中容易团聚,这些缺点限制了纳米材料的推广应用[33],因此将其与成本低廉来源广泛的生物炭复合,提高复合材料的性能,具有实际的环境意义。 1.1.4 生物炭-无机复合材料
用化学修饰的方法将无机材料与生物炭复合,在生物炭表面添加一些能够与污染物相互作用的基团,从而提高吸附效果。学者们纷纷将研究目光投向了锰氧化物与生物炭的复合,主要是由于锰的氧化物在陆地环境中储量丰富(30%以上),为复合材料的推广应用提供了便利[34, 35, 36, 37]。
Song等[9]在600℃下将玉米秸秆裂解3 h制成生物炭,将生物炭与KMnO4溶液混合超声2 h,经80℃烘干,置于马弗炉中600℃焙烧0.5 h,最后制成MnOx-生物炭复合材料(MBC)。与原始生物炭(BC)相比,其灰分含量从5.02%升至23.4%,且孔径有所增加(BC:23.7 nm;MBC:92.2 nm),MBC的O/C从0.04升高到0.53,X射线光电子能谱(XPS)分析显示,这些增加的氧主要以Mn-O和Mn-OH形式存在,这是复合材料对Cu2+的最大吸附量显著提高(BC:19.6 mg·g-1;MBC:160.3 mg·g-1)的主要原因。Zhang等[35]分别将甜菜渣(SBTs)、甘蔗渣(SB)、棉花秆(CWs)、松木(PWs)、花生壳(PSs)这五种生物质原材料与MgCl2-6H2O溶液混合,在600℃下绝氧裂解1 h,制成MgO-生物炭复合材料,扫描电子显微镜(SEM)显示MgO颗粒均匀分布在生物炭表面,提高了生物炭的比表面积。按照上述提到的五种生物质原材料顺序,合成的复合材料比表面积分别为253.7、338.0、270.7、432.6、346.5 m2·g-1。将制得的MgO-生物炭用于污水脱氮除磷,复合材料对磷和氮的饱和吸附量分别达到835、95 mg·g-1。Agrafioti等[36]分别将CaO溶液、FeO粉末、FeCl3-6H2O溶液与稻壳(RH)、有机固体废弃物(SW)原材料混合,制备成复合生物炭材料RH-Ca2+、RH-FeO、RH-Fe3+、SW-FeO、SW-Fe3+,将制备好的复合材料应用于As (Ⅴ)的去除,发现复合后的材料对As的去除率(50%~95%)都高于未经复合的原始生物炭(25%~55%)。Zhang等[37]将棉花秆在600℃下绝氧裂解1 h制备成生物炭,再将其与MgCl2-6H2O和AlCl3-6H2O溶液混合,于80℃下烘干制得镁铝水滑石生物炭复合材料(Biochar/MgAl-LDH),复合材料对磷的最大吸附量提高了5~50倍。可见,生物炭与无机材料复合后,一方面为生物炭表面增加了与污染物作用的基团,另一方面,生物炭为无机基团提供了附着点位,利于增大与污染物的作用能力。 1.1.5 改性生物炭
利用KOH、H2O2、O3、H2SO4/HNO3等改性生物炭[38, 39],能够提高生物炭的比表面积,增加生物炭表面的官能团(如羧基),提高生物炭对污染物的固定能力。Regmi等[40]在300℃下通过水热反应制备了Alamo柳枝生物炭,并使用KOH改性生物炭增加其比表面积提高吸附能力,并将改性后的生物炭(HTBC)和未改性的生物炭(HTB)用于吸附水中的重金属Cd2+,研究发现改性后的生物炭(HTBC)比表面积为5.01 m2·g-1,是未改性生物炭(HTB)比表面积的2.4倍;HTBC对Cd2+吸附能力(34 mg·g-1)高于未改性生物炭HTB (31 mg·g-1)。Klasson等[41]研究了磷酸浸泡改性的山核桃壳生物炭对重金属Cd2+的吸附能力,结果表明当Cd2+的初始浓度为10 mmol·L-1和20 mmol·L-1时,经改性的生物炭对Cd2+的吸附量分别为0.97 mmol·g-1和1.3 mmol·g-1。还有研究表明,将生物质原材料先进行厌氧消化后再高温裂解制备而成的生物炭对污染物的去除效果更好。Inyang等[42]对比了未经加工的甘蔗渣生物炭(BC)与经过厌氧消化的甘蔗渣制备而成的生物炭(DBC)对水中Pb2+的去除效果,发现DBC对Pb2+的最大吸附量(653.9 mmol·kg-1)是BC (31.3 mmol·kg-1)的20倍。可见提前对生物质原材料进行厌氧处理,能够提高生物炭对污染物的去除能力。
以上列出的生物炭复合材料在对污染物的去除方面各有优势,文献显示近几年越来越多的学者开始研究生物炭的复合材料[21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43],然而这些研究多将重点放在复合材料的表征和对水体中污染物的去除方面,在现有成果的基础上,将复合材料应用于土壤修复具有广阔的空间,土壤中微生物、溶解性有机物与复合材料之间的作用值得深入探讨(比如纳米材料石墨烯对微生物具有毒性作用,因此生物炭-纳米复合材料的投加对土著微生物的影响是否将导致修复效果降低)。另外,目前针对生物炭复合材料的研究范围比较局限,大多集中于无机材料、碳纳米材料、纳米氧化物,关于生物炭与其他种类材料的复合,比如有机高分子材料、纳米硫化物等其他类型的纳米材料以及复合材料的应用研究鲜见报道。有机高分子材料具有良好的生物相容性,与生物炭复合后对环境更加友好。可见拓宽生物炭复合材料的选材范围,进而将其应用于环境保护领域是十分必要的。 1.2 生物炭及其复合材料的表征
生物炭的物理、化学和机械性能随着制备条件、生物质原材料以及负载材料的不同而改变,对生物炭材料进行表征,了解其特征,有利于生物炭作用机理的研究和推广应用。目前所做的研究中,常用的生物炭及其复合材料的表征手段主要包括元素组成(C、H、O、N)、比表面积、Zeta电位、X射线衍射(XRD)、傅里叶红外线光谱分析(FTIR)、拉曼光谱(Raman spectra)、热重分析(TGA)、X射线光电子能谱(XPS)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)等。
元素组成、比表面积和Zeta电位常作为生物炭及其复合材料的基本理化性质被列出,便于分析材料的性能变化。通过分析生物炭及其复合材料中各元素所占比例,可推断在裂解过程中各类物质的损失情况,如用H/C和O/C分别表示材料的亲水性和芳香性[44],一般情况下随着裂解温度的升高,H/C和O/C下降,表示材料的亲水性下降,芳香性增强[45]。生物炭与其他材料(如无机材料)复合后,复合材料中该元素的含量也可用于验证所采用的复合方法是否有效地将两种材料复合[34]。通常大的比表面积利于材料对污染物的吸附,将生物炭与其他材料(如纳米材料)复合后,因纳米材料自身较大的比表面积而使复合材料的比表面积大于原生物炭(9~390 m2·g-1)[30],然而生物炭复合材料的比表面积有时会低于原生物炭,于志红等[11]发现将生物炭与锰氧化物复合后所得到的复合材料比表面积(3.18 m2·g-1)远低于生物炭(60.97 m2·g-1)。这是由于锰氧化物将生物炭大部分中孔和微孔填充,这一点可以从SEM图中观察到(图 3a)。从SEM图中可以看到,锰氧化物比较均匀的附在生物炭表面,因此生物炭保持了原形态,而因中孔和微孔被锰氧化物填充,使复合材料的比表面积下降。虽然锰氧化物的引入降低了复合材料的比表面积,然而复合材料对As (Ⅲ)的最大吸附量提高(生物炭:11.41 mg·g-1;炭-锰复合材料:20.08 mg·g-1),这是由于锰氧化物增加了复合材料表面的吸附位点。Song等[9]的研究也得到了相同的结论,通过XPS (图 3b)可知生物炭-锰氧化物复合材料中形成较多的Mn-O键(63.9%)和Mn-OH (26.3%)键,可见虽然复合后生物炭的比表面积降低(61.0~2.28 m2·g-1),但是平均孔径增大(23.7~92.2 nm),增强了锰氧化物的负载,使得复合材料含氧官能团含量增加,为重金属的吸附提供了有利条件。
XRD常用于对材料进行物相分析,将所测材料的点阵平面间距及衍射强度与标准物相的衍射数据相比较,确定材料中存在的物相。Wang等[46]采用桉树叶与FeCl3·6H2O制备桉树叶磁性生物炭(MELRC),通过XRD、FTIR和SEM对复合材料MELRC进行表征。从XRD图中(图 4a)明显观察到Fe3O4的特征峰(2θ依次为30.1°、35.4°、43.0°、53.9°、57.0°、62.6°),说明磁铁矿是复合材料MELRC中的主要晶相结构。FTIR光谱(图 4b)用于表征材料的磁化过程和表面官能团变化[47],在587 cm-1处观察到Fe-O伸缩振动,说明材料表面形成了铁氧化合物[48]。通过扫描电镜(SEM)观察到Fe3O4分散在生物炭表面的特定部位,而不是覆盖整个表面,因而MELRC保持了较大的比表面积[49]。将复合材料MELRC与去离子水混合在200 r·min-1下振荡600 min,扫描电镜下观察到MELRC表面没有明显变化,说明Fe-OH与C-OH结合十分紧密,利于吸附之后的固液分离和循环使用。Sun等[50]对不同温度下制备的秸秆生物炭和果木生物炭进行了表征,分别采用核磁共振、X射线光电子能谱仪(XPS)、扫描电子显微镜(SEM)、比表面积法(BET)研究了粒径、热解升温速率和热解时间对生物炭的化学成分、芳香度及孔隙结构的影响,结果表明慢速裂解过程中,提高裂解温度或者延长裂解时间使生物炭中碳含量升高,氧含量和表面亲水性降低。Inyang等[30]对生物炭/碳纳米管复合材料(HC-CNT、BC-CNT)和生物炭(HC、BC)的拉曼强度、热稳定性等特征进行了分析,拉曼光谱图中包括由sp3杂化诱导产生的缺陷峰D峰(~1350 cm-1)和代表石墨结构的G峰(1500~1600 cm-1),两峰的积分强度比率ID/IG与网平面上微晶的平均尺寸或无缺陷区域成反比关系,该比值可用来评价材料的石墨化程度[51]。与生物炭相比,生物炭/碳纳米管复合材料的拉曼强度ID/IG增大,说明添加碳纳米管后生物炭表面的缺陷度升高,官能团(-OH、-C=O、-COOH、-F)增加,正是由于表面官能团的增加,使得生物炭/碳纳米管复合材料对亚甲基蓝的吸附能力提升(HC:9%,HC-CNT:47%;BC:25%,BC-CNT:64%)
生物炭具有较大的比表面积和孔隙度,可溶性低,具有高度羧酸酯化和芳香化结构,是天然的吸附材料。生物炭复合材料具有更大的比表面积、更多的表面活性官能团数量和种类,与污染物的络合能力增强,因此生物炭及其复合材料在环境修复中的应用引起了普遍关注。目前,生物炭及其复合材料被广泛应用于吸附环境中无机污染物(如重金属、氟等)和有机污染物(如染料、石油烃、农药、抗生素等)[52]。 2.1 在无机物污染环境修复中的应用 2.1.1 重金属离子的去除
重金属在生物体和环境中累积和富集会严重威胁生物体健康和生态环境。生物炭具有比表面积大、吸附性能高和成本低的优点,因此作为吸附剂被应用于环境中重金属(Cr3+、Cr6+、Cu2+、Pb2+、Hg2+、As3+、As5+等)的修复[53]。生物炭对重金属的吸附机理主要有静电吸附作用、离子交换作用、表面矿物组分的吸附作用、阳离子-π作用、表面官能团的作用和沉淀作用[54]。
由于生物炭表面一般带负电荷且具有很高的阳离子交换量(CEC),当阳离子污染物重金属接触到生物炭时,静电吸附就起主导作用。静电吸附作用的强度取决于生物炭表面负电基团产生的可变表面电荷,受pH的影响较大[55]。在土壤中施加生物炭,能够增加土壤的阳离子交换作用,从而增强土壤对重金属的吸附能力[56]。Wang等[57]在600℃下制备了赤铁矿复合生物炭材料(HPB),HPB对As5+的最大吸附量达到429 mg·kg-1,是原始生物炭(PB)最大吸附量(265 mg·kg-1)的近两倍,复合材料对As5+的吸附过程中,静电吸附和表面官能团起主导作用。Yakkala等[58]在不同温度下(300、500、700℃)绝氧慢速裂解制备了水牛杂草生物炭,应用于Cd2+和Pb2+的去除,发现700℃下制备的生物炭比表面积远大于300℃和500℃下制备的生物炭(700℃BET 279.8 m2·g-1;300℃BET 1.35 m2·g-1;500℃BET 4.83 m2·g-1),700℃生物炭对Cd2+和Pb2+的吸附量最高,分别达到11.63、333 mg·g-1,因为700℃生物炭具有更高的离子交换能力和络合作用。
生物质原材料中含有多种矿物组分,如Si、Ca、Mg、Fe、Mn等,生物炭裂解的过程中,这些组分以灰分的形式富集在生物炭中[59]。在与污染物作用过程中,生物炭中的矿物组分对重金属的吸附能力和亲和力往往高于有机碳组分。陈再明等[60]对比了生物炭RC350、RC700与酸化去表面矿物生物炭RC350-DA、RC700-DA对Pb2+的吸附能力,与未经酸化的生物炭相比[RC350:(65±6.9) mg·g-1;RC700:(76.3±3.6) mg·g-1],酸化后的生物炭对重金属Pb2+的吸附能力明显降低[RC350-DA:(29.6±1.0) mg·g-1,RC700-DA:(38.2±1.4) mg·g-1]。研究发现酸化后生物炭上有机官能团并无明显减少,而无机矿物(如SiO2)减少,因此无机矿物组分对重金属的吸附起到了关键作用。而在对有机物的吸附过程中,生物质原材料裂解后吸附性能增大的因素主要来源于裂解过程中有机碳组分的变化,而不是矿物组分[61]。
阳离子-π作用(Cπ)大小取决于生物炭表面的芳香度,π共轭芳香结构越多,给电子能力越强[62]。李力等[63]分别在350℃和700℃下制备了玉米秸秆生物炭BC350和BC700,将其应用于重金属Cd2+的吸附,通过Two-site langmuir方程计算发现,在吸附Cd2+的过程中离子交换吸附容量分别为5.4、0.6 mg·g-1,阳离子-π作用吸附容量分别为33.8、52.3 mg·g-1,计算可知阳离子-π作用的吸附容量占总吸附容量的86%~98%,说明该过程阳离子-π吸附占主导作用。Cd2+在生物炭表面的吸附通式可以表述为:
Cπ+2H2O→Cπ-H3O++OH-
Cπ-H3O++Cd2+→Cπ-Cd2++H3O+
或Cπ+Cd2+→Cπ-Cd2+
(π电子与Cd2+的轨道发生配位作用)
生物炭自身表面含有丰富的羧基和酚羟基等含氧官能团,重金属可以和这些官能团发生金属-配体的络合作用[64, 65]。生物炭与其他材料复合之后在表面形成配合物以及含氧基团,在与重金属结合过程中发挥主要作用。于志红等[66]研究了生物炭-锰氧化物复合材料对土壤中Cu2+的吸附效果,发现复合材料明显提高了红壤对Cu2+的吸附能力,与未复合的生物炭相比,吸附量增加了509%;复合材料提高红壤对Cu2+吸附能力的机制是通过改变红壤表面官能团组成,增加红壤表面-OH、Mg-O、Si-O等官能团数量。Wang等[67]研究了MnCl2-4H2O复合松木生物炭(MPB)、水钠锰矿复合松木生物炭(BPB)对水中Pb2+和As5+的吸附效果,发现MPB (分别为4.91、0.59 g·kg-1)和BPB (分别为47.05、0.91 g·kg-1)对Pb2+和As5+的吸附量远大于未经复合的生物炭(BC,分别为2.35、0.20 g·kg-1),复合材料对重金属吸附能力的提高主要取决于表面氧化物与重金属的络合作用。Xue等[68]对比了H2O2改性前后的花生壳生物炭对重金属Pb2+的去除效果,结果表明改性后的生物炭对Pb2+的最大吸附量达到22.82 mg·g-1,是未改性生物炭的20倍。这是由于H2O2改性后,生物炭表面的含氧官能团(尤其是羧基)显著增加,增强了材料对重金属的络合能力。Song等[9]将生物炭与MnOx复合制备MnOx-生物炭复合材料(MBC)用于去除水中的Cu2+,发现复合材料对Cu2+的吸附能力显著提高(MBC:160.3 mg·g-1;BC:19.6 mg·g-1),起主导作用的是MnOx与生物炭表面形成的配合物及含氧基团。
生物炭及其复合材料对金属离子的沉淀作用主要体现在两方面:一方面,生物炭添加到溶液中能够提高溶液的pH值,从而促使重金属(Cu2+、Zn2+、Cd2+、Pb2+等)形成氢氧化物沉淀[69]。另一方面,Xu等[70]通过研究牛粪炭对重金属Cu2+、Zn2+、Cd2+的吸附发现沉淀作用对重金属去除的贡献率达到75%以上。这是因为采用动物粪便为原材料制备的生物炭中通常含有较多可溶性的磷酸盐和/或碳酸盐,可以和重金属离子结合形成磷酸盐、碳酸盐沉淀。 2.1.2 氟离子的去除
生物炭及其复合材料常被应用于吸附水中氟污染,吸附效果受外界环境条件的影响,比如pH、温度等。Mohan等[71]对比研究了磁性生物炭(MCSBC)和非磁性生物炭(CSBC)对地下水中氟的吸附效果。首先将制备好的玉米秸秆生物炭与Fe2+/Fe3+溶液混合制成磁性生物炭(MCSBC),磁化后的生物炭表面形成氧化铁增大了MCSBC的比表面积。通过研究不同温度(25、35、45℃)对吸附效果的影响,发现随着吸附温度升高,吸附剂对氟的吸附性能降低(CSBC:Q250=6.42 mg·g-1,Q350=5.17 mg·g-1,Q450=4.99 mg·g-1,MCSBC:Q250=4.11 mg·g-1,Q350=3.45 mg·g-1,Q450=3.41 mg·g-1),吸附过程符合假一级动力学方程。Oh等[72]研究了不同温度(400、600、700℃)制备的桔皮炭和水处理污泥炭对含氟废水的修复效果。活性污泥炭灰分含量高(76%~90%)、碳含量低(6%~8%),随着裂解温度的升高,其H/C和O/C比例降低。在pH 2.0~3.3范围内,高温制备的桔皮炭(600℃和700℃)能够吸附更多的氟,而活性污泥炭吸附的最佳pH为5.0,这是因为氟离子与活性污泥炭表面氧化铝、氧化铁形成复杂配合物,pH降低导致氟铝酸盐释放,降低活性污泥炭对氟的吸附效率。Mohan等[73]在400℃和450℃下制备了松木炭和松树皮炭,应用于修复地下水氟污染。松木炭在pH为2.0时对氟的吸附效果最好,实验中观察到生物炭在水中膨胀。这是由于生物炭含氧量丰富(8%~11%),添加到水中后增大了内部孔隙度,氟离子容易进入到生物炭内部孔隙中进一步提高吸附效果,离子交换和生物炭中灰分与氟离子的沉淀对吸附起主要贡献作用。研究还发现,虽然松木和松树皮生物炭比表面积(SBET:1~3 m2·g-1)远低于活性炭(SBET:~1000 m2·g-1),但其对氟的吸附量与活性炭相当甚至更多,可能是因为生物炭加入到水中后孔隙度增大。经过测定,松木炭和松树皮炭干燥后失重约0.37~0.38、0.26~0.57 g·g-1,因此水在生物炭中占据了0.37~0.38、0.26~0.57 mL·g-1,这些水分增大生物炭内部孔隙,扩散到生物炭孔壁。 2.2 在有机物污染环境修复中的应用 2.2.1 染料的去除
染料工业废水具有肉眼易识别、有机物含量高、碱性大和具有毒性等特点,由于其性质稳定,难以好氧消化,常规水处理技术难以将其降解。生物炭及其复合材料对染料的吸附研究相当广泛[74],此类研究常用亚甲基蓝作为模型染料。Zhang等[31]对比研究了石墨烯/生物炭(GCBC)与生物炭(BC)对水中亚甲基蓝的去除效果。研究表明GCBC对亚甲基蓝的饱和吸附量达到174 mg·g-1,远大于BC对亚甲基蓝的饱和吸附量8 mg·g-1。这是因为生物炭表面的石墨烯与甲基蓝分子之间产生强大的π-π作用,提高对亚甲基蓝的吸附能力。有研究表明亚甲基蓝和其他芳香族有机化合物能够与石墨烯或石墨形成π-π电子作用,因此GCBC也能够应用于其他有机污染物的去除[75]。用Langmuir吸附等温线对吸附过程进行拟合,发现生物炭对亚甲基蓝的吸附过程更符合Langmuir方程,说明添加石墨烯后吸附剂对污染的吸附机制由分配作用为主逐渐变为表面吸附为主。Xu等[76]在350℃下分别制备了油菜秸秆(CS)、花生秸秆(PS)、大豆秸秆(SS)和稻壳(RH)生物炭,并用于去除水中的甲基紫,四种生物炭对甲基紫的去除能力从高到低为CS>PS>SS>RH,这是由各自的阳离子交换能力决定的。Zhang等[32]在600℃下制备了生物炭/纳米氧化铝复合材料用于去除水中的亚甲基蓝,其饱和吸附量由8 mg·g-1提高到85 mg·g-1,纳米氧化铝的添加显著提高了生物炭对亚甲基蓝的吸附能力。这是由于独特的碳纳米结构增加了生物炭表面的反应点位,更有效地吸附污染物。在预处理时添加的Al3+不仅是为了提供AlOOH纳米颗粒,它还充当活化剂,在热解过程中增加生物炭/纳米氧化铝的官能团作用,因此复合材料对亚甲基蓝的吸附能力增强。 2.2.2 石油烃和农药的去除
生物炭对环境中疏水性有机物石油烃和农药污染的修复是研究的热点,然而目前生物炭复合材料在石油烃和农药修复方面的应用研究鲜见报道,研究较多的仍是生物炭单一材料的应用。Chen等[77]研究了不同温度(100、300、400℃和700℃)下制备的松叶生物炭(分别命名为P100~P700)对多环芳烃(萘、菲、芘)的吸附机理,结果显示P100中无定型有机质含量高,对多环芳烃的等温吸附曲线线性相关性高,分配作用起主导作用,呈非竞争吸附;随着裂解温度升高,P300~P700中芳香碳含量较多,对有机物的吸附规律为非线性吸附,表面吸附起主导作用,呈竞争吸附。除了分配作用和表面吸附,还存在一些微观吸附机制影响生物炭对有机物的吸附[78]。Hale等[79]通过研究生物炭和活性炭对芘的吸附能力来评价其对土壤的修复效果,研究发现在陈化温度为110℃时最大程度地改变了材料的理化性质(如pH升高,生物炭阳离子交换量高达50%),吸附实验表明生物炭和活性炭均适合于污染土壤中石油烃的修复。研究表明,裂解温度对生物炭的吸附机制起主要作用。低裂解温度下制备的生物炭有机物含量高,分配作用起主导作用。随着裂解温度的升高,生物炭中有机物含量降低,表面积和孔隙度增大,表面吸附作用逐渐起主导作用[80]。
生物炭对农药的治理研究主要包括有机氯、氨基甲酸酯、氯苯氧基酸化合物等。Klasson等[81]在650℃下将杏仁壳绝氧裂解1 h制备成杏仁壳炭,然后在800℃下蒸汽活化45 min,使得吸附剂具有更大的比表面积344 m2·g-1,其对二溴氯丙烷的吸附量达到102 m2·g-1,并成功进行了野外实验。 2.2.3 抗生素的去除
抗生素作为一种新型污染物,已经受到国内外学者的普遍关注,其主要来源于农业生产和生活污水,抗生素进入环境中给水生生态系统带来不良影响,导致多种耐药性细菌的产生,也使水生动物生命活动受到影响,同时通过饮水、食物链等方式对人体健康构成潜在威胁[82]。生物炭及其复合材料对抗生素的吸附性能具有广泛的研究前景。景向荣等[83]制备了甲醇改性生物炭材料用于吸附废水中的四环素(CTs)。首先将生物炭放于3 mol·L-1的NaOH溶液中搅拌1 h,分离后使用蒸馏水反复清洗生物炭直至pH中性,然后将处理后的生物炭与甲醇混合,发生酯化反应以及甲醇羰基化反应,制备得到改性生物炭(MeOH-char),将其用于CTs的吸附,MeOH-char对CTs的最大吸附量为95.63 mg·g-1,大于原始生物炭(Ori-char)的最大吸附量81.00 mg·g-1。这是由于经甲醇改性后,MeOH-char表面的羰基吸电子能力提高,有利于吸引CTs结构上的羟基以及相关的基团,因此增强其去除效果。生物炭与其他材料复合后吸附性能的提高,为环境中抗生素的治理提供了另一种选择。
目前,生物炭复合材料在环境修复方面,尤其是有机污染物治理的应用研究较少,生物炭复合材料对有机污染物的吸附机理建立在生物炭自身结构的基础上,由分配作用、表面吸附和微观吸附机制共同作用[84]。当生物炭表面负载其他材料时,其对有机物的吸附机理也受负载材料的影响。
总的来说,生物炭复合材料在结构(比表面积、孔隙度等)和性能上优于生物炭本身,对污染物的修复效果更好,具有广阔的研究和应用前景。 3 总结与展望
生物炭具有比较面积大、来源广泛、价格低廉等优点,在农业和环保领域有广阔的应用前景。为了促进今后的研究和实际应用,应将更多的研究力量放到以下几个方面。
(1)制备更高效的生物炭复合材料。目前对生物炭复合材料的研究主要集中于无机材料和碳纳米材料,关于生物炭与其他种类材料的复合,比如与有机高分子材料复合、纳米硫化物等其他类型的纳米材料复合的研究鲜见报道,而且复合材料的应用研究多局限于实验室对污染物去除效果的对比。对生物炭进行修饰,增加表面官能团作用,提高吸附性能是今后研究的重点。在此基础上,应研究复合材料作用于污染物时动力学、热力学过程,阐明作用机理,为实际应用提供科学依据。
(2)目前针对生物炭复合材料的研究多集中于水体污染,鲜见其在土壤中的应用研究。事实上,土壤环境较水体更为复杂,其中的微生物、可溶性有机物等与生物炭复合材料之间的作用关系值得深入研究。比如,纳米材料(如石墨烯)对微生物具有毒性作用,高效的生物炭-纳米复合材料应用到土壤中是否会导致土著微生物种类和数量下降,从而影响土壤环境,这些问题需要在今后的研究中引起重视。
(3)生物炭复合材料对污染物的去除往往受多种机制控制,所添加的磁性材料、纳米材料或无机材料自身与生物炭之间也会产生相互作用,目前的研究多从定性的角度分析各种机制的作用,鲜见定量化研究复合材料对污染物的作用机理。今后可以将重点放在定量研究方面,为其中优势机制的放大提供科学依据。
| [1] | Wardle D A,Nilsson M C,Zackrisson O.Fire-derived charcoal causes loss of forest Humus[J].Science,2008,320(5876):629-629. |
| [2] | 张峥嵘.生物炭改良土壤物理性质的初步研究[D].杭州:浙江大学,2014.ZHANG Zheng-rong.A preliminary study on the effect of biochar on soil physical properties[D].Hangzhou:Zhejiang University,2014. |
| [3] | 陈温福,张伟明,孟军.农用生物炭研究进展与前景[J].中国农业科学,2013,46(16):3324-3333.CHEN Wen-fu,ZHANG Wei-ming,MENG Jun.Advances and prospects in research of biochar utilization in agriculture[J].Scientia Agricultura Sinica,2013,46(16):3324-3333. |
| [4] | 武玉,徐刚,吕迎春,等.生物炭对土壤理化性质影响的研究进展[J].地球科学进展,2014,29(1):68-79.WU Yu,XU Gang,LÜYing-chun,et al.Effects of biochar amendment on soil physical and chemical properties:Current status and knowledge gaps[J].Advance in Earth Science,2014,29(1):68-79. |
| [5] | Kramer R W,Kujawinski E B,Hatcher P G.Identification of black carbon derived structures in a volcanic ash soil humic acid by Fourier transform ion cyclotron resonance mass spectrometry[J].Environmental Science and Technology,2004,38(12):3387-3395. |
| [6] | Laird D A,Fleming P,Davis D D,et al.Impact of biochar amendments on the quality of a typical Midwestern agricultural soil[J].Geoderma,2010,158(3/4):443-449. |
| [7] | Denyes M J,Langlois V S,Rutter A,et al.The use of biochar to reduce soil PCB bioavailability to Cucurbita pepo and Eisenia fetida[J].Science of the Total Environment,2012,437:76-82. |
| [8] | Jeffrey M N,Isabel L,Xing B S,et al.Characterization of designer biochar produced at different temperatures and their effects on a loamy sand[J].Annals of Environmental Science,2009,3:195-206. |
| [9] | Song Z G,Lian F,Yu Z H,et al.Synthesis and characterization of a novel MnOx-loaded biochar and its adsorption properties for Cu2+ in aqueous solution[J].Chemical Engineering Journal,2014,242:36-42. |
| [10] | Sun K,Ro K,Guo M,et al.Sorption of bisphenol A,17alpha-ethinyl estradiol and phenanthrene on thermally and hydrothermally produced biochars[J].Bioresource Technology,2011,102(10):5757-5763. |
| [11] | 于志红,黄一帆,廉菲.生物炭-锰氧化物复合材料吸附砷(Ⅲ)的性能研究[J].农业环境科学学报,2015,34(1):155-161.YU Zhi-hong,HUANG Yi-fan,LIAN Fei,et al.Adsorption of arsenic (Ⅲ) on biochar-manganese oxid composites[J].Journal of Agro-Environment Science,2015,34(1):155-161. |
| [12] | 安增莉.生物炭的制备及其对Pb (Ⅱ)的吸附特性研究[D].福建:华侨大学,2011.AN Zeng-li.Preparation and lead (Ⅱ) adsorption characteristics of biochar[D].Fujian:Huaqiao University,2011. |
| [13] | Dinesh M,Charles U,Pittman J,et al.Pyrolysis of wood/biomass for bio-oil:A critical review[J].Energy and Fuels,2006,20(3):848-889. |
| [14] | Bridgwater A V.Renewable fuels and chemicals by thermal processing of biomass[J].ChemicalEngineering Journal,2003,91(2/3):87-102. |
| [15] | Scheer C,Grace P R,Rowlings D W,et al.Effect of biochar amendment on the soil-atmosphere exchange of greenhouse gases from an intensive subtropical pasture in northern New South Wales[J].Australia Plant and Soil,2011,345(1/2):47-58. |
| [16] | Ameloot N,Graber E R,Verheijenf G A,et al.Interactions between biochar stability and soil organisms:Review and research needs[J].European Journal of Soil Science,2013,64(4):379-390. |
| [17] | Chun Y,Sheng G G,Chiou C T,et al.Compositions and sorptive properties of crop residue-derived chars[J].Environmental Science and Technology,2004,38(17):4649-4655. |
| [18] | 陈宝梁,陈再明,陈文远,等.有机污染物与生物炭的相互作用:吸附模型、机理和热力学[C]//第六届全国环境化学大会暨环境科学仪器与分析仪器展览会摘要集.2011:1.CHEN Bao-liang,CHEN Zai-ming,CHEN Wen-yuan,et al.Interactions of organic pollutants and biochar:Adsorption model,mechanism and thermodynamics[C]//Sixth national conference of environmental chemistry cum environmental science instruments and analysis equipment exhibition Abstracts.2011:1. |
| [19] | 陈宝梁,周丹丹,朱利中,等.生物碳质吸附剂对水中有机污染物的吸附作用及机理[J].中国科学B辑:化学,2008,38(6):530-537.CHEN Bao-liang,ZHOU Dan-dan,ZHU Li-zhong,et al.Sorption of organic pollutants by biochars and its sorption mechanisms[J].Science China:B:Chemical,2008,38(6):530-537. |
| [20] | Lu H N,Hu X Y,Liu H W.Influence of pyrolysis conditions on stability of biochar[J].Environmental Science and Technology,2013,36(8):11-14. |
| [21] | Mohan D,Singh P,Sarswa,A,et al.Lead sorptive removal using magnetic and nonmagnetic fast pyrolysis energy cane biochars[J].Journal of Colloid and Interface Science,2015,448:238-250. |
| [22] | Zhang M,Gao B,Varnoosfaderani S,et al.Preparation and characterization of a novel magnetic biochar for arsenic removal[J].Bioresource Technology,2013,130:457-462. |
| [23] | Chen B,Chen Z,Lv S.A novel magnetic biochar efficiently sorbs organic pollutants and phosphate[J].Bioresource Technology,2011,102(2):716-723. |
| [24] | Mubarak N M,Alicia R F,Abdullah E C,et al.Statistical optimization and kinetic studies on removal of Zn2+ using functionalized carbon nanotubes and magnetic biochar[J].Journal of Environmental Chemical Engineering,2013,1(3):486-495. |
| [25] | Mohan D,Kumar H,Sarswat A,et al.Cadmium and lead remediation using magnetic oak wood and oak bark fast pyrolysis bio-chars[J].Chemical Engineering Journal,2014,236:513-528. |
| [26] | Oliveira L,Rios R,J D Fabris,et al.Activated carbon/iron oxide magnetic composites for the adsorption of contaminants in water[J].Carbon,2002,40(12):2177-2183. |
| [27] | Nguyen T D,Phan N H,Do M H,et al.Magnetic Fe2MO4(M:Fe,Mn) activated carbons:Fabrication,characterization and heterogeneous Fenton oxidation of methyl orange[J].Journal of Hazardous Materials,2011,185(2/3):653-661. |
| [28] | Mohan D,Pittman J,Bricka M,et al.Sorption of arsenic,cadmium,and lead by chars produced from fast pyrolysis of wood and bark during bio-oil production[J].Journal of Colloid Interface Science,2007,310(1):57-73. |
| [29] | Devi P,Saroha A K.Synthesis of the magnetic biochar composites for use as an adsorbent for the removal of pentachlorophenol from the effluent[J].Bioresource Technology,2014,169:525-531. |
| [30] | Inyang M,Gao B,Zimmerman A,et al.Synthesis,characterization,and dye sorption ability of carbon nanotube biochar nanocomposites[J].Chemical Engineering Journal,2014,236:39-46. |
| [31] | Zhang M,Gao B,Yao Y,et al.Synthesis,characterization,and environmental implications of graphene-coated biochar[J].The Science of the total Environment,2012,435/436:567-572. |
| [32] | Zhang M,Gao B.Removal of arsenic,methylene blue,and phosphate by biochar/AlOOHNanocomposite[J].Chemical Engineering Journal,2013,226:286-292. |
| [33] | Lee G W,Kim J,Yoon J,et al.Structural characterization of carboxylated multi-walled carbon nanotubes[J].Thin Solid Films,2008,516(17):5781-5784. |
| [34] | Wang S,Gao B,Li Y,et al.Manganese oxide-modified biochars:Preparation,characterization,and sorption of arsenate and lead[J].Bioresource technology,2015,181:13-17. |
| [35] | Zhang M,Gao B,Yao Y,et al.Synthesis of porous MgO-biochar nano-composites for removal of phosphate and nitrate from aqueous solutions[J].Chemical Engineering Journal,2012,210:26-32. |
| [36] | Agrafioti E,Kalderis D,Diamadopoulos E.Ca and Fe modified biochars as adsorbents of arsenic and chromium in aqueous solutions[J].Journal of Environmental Management,2014,146:444-50. |
| [37] | Zhang M,Gao B,Yao Y,et al.Phosphate removal ability of biochar/MgAl-LDH ultra-fine composites prepared by liquid-phase deposition[J].Chemosphere,2013,92(8):1042-1047. |
| [38] | Sanchez M P,Utrilla J R.Adsorbent-adsorbate interactions in the adsorption of Cd (Ⅱ) and Hg (Ⅱ) on ozonized activated carbons[J].Environmental Science and Technology,2002,36(17):3850-3854. |
| [39] | Uchimiya M,Bannon D I,Wartelle L H.Retention of heavy metals by carboxyl functional groups of biochars in small arms range soil[J].Journal of Agricultural and Food Chemistry,2012,60(7):1798-1809. |
| [40] | Regmi P,Moscoso J L G,Kumar S,et al.Removal of copper and cadmium from aqueous solution using switchgrass biochar produced via hydrothermal carbonization process[J].Journal of Environmental Management,2012,109:61-69. |
| [41] | Klasson K T,Wartelle L H,Rodgers J E,et al.Copper (Ⅱ) adsorption by activated carbons from pecan shells:Effect of oxygen level during activation[J].Industrial Crops and Products,2009,30(1):72-77. |
| [42] | Inyang M,Gao B,Ding W C,et al.Enhanced lead sorption by biochar derived from anaerobically digested sugarcane bagasse[J].Separation Science and Technology,2011,46:1950-1956. |
| [43] | Hu X,Ding Z,Zimmerman A R,et al.Batch and column sorption of arsenic onto iron-impregnated biochar synthesized through hydrolysis[J].Water Research,2015,68:206-226. |
| [44] | 孙克静,张海荣,唐景春.不同生物质原料水热生物炭特性的研究[J].农业环境科学学报,2014,33(11):2260-2265.SUN Ke-jing,ZHANG Hai-rong,TANG Jing-chun.Properties of hydrochars from different sources of biomass feedstock[J].Journal of Agro-Environment Science,2014,33(11):2260-2265. |
| [45] | Li H,Qu R,Li C,et al.Selective removal of polycyclic aromatic hydrocarbons (PAHs) from soil washing effluents using biochars produced at different pyrolytic temperatures[J].Bioresource Technology,2014,163:193-198. |
| [46] | Wang S Y,Tang Y K,Li K,et al.Combined performance of biochar sorption and magnetic separation processes for treatment of chromium-contained electroplating wastewater[J].Bioresource Technology,2014,174:67-73. |
| [47] | Wahab M A,Jellali S,Jedidi N.Ammonium biosorption onto sawdust:FTIR analysis,kinetics and adsorption isotherms modeling[J].Bioresource Technology,2010,101(14):5070-5075. |
| [48] | Li G Y,Jiang Y R,Huang K L,et al.Preparation and properties of magnetic Fe3O4-chitosan Nanoparticles[J].Journal of Alloys and Compounds,2008,466(1/2):451-456. |
| [49] | Zhang G,Qu J,Liu H,et al.Cu-Fe2O4/activated carbon composite:A novel magnetic adsorbent for the removal of acid orange Ⅱ and catalytic regeneration[J].Chemosphere,2007,68(6):1058-1066. |
| [50] | Sun H,Hockaday W C,Masiello C A,et al.Multiple controls on the chemical and physical structure ofbiochars[J].Industrial and Engineering Chemistry Research,2012,51(9):3587-3597. |
| [51] | 张福勤,黄伯云,黄启忠,等.炭/炭复合材料石墨化度的研究进展[J].矿冶工程,2000,20(4):10-13.ZHANG Fu-qin,HUANG Bo-yun,HUANG Qi-zhong,et al.The study of graphitization degree of C/C composites-recent advances[J].Mining and Metallurgical Engineering,2000,20(4):10-13. |
| [52] | Tang J,Zhu W,Kookana R,et al.Characteristics of biochar and its application in remediation of contaminated soil[J].Journal of Bioscience and Bioengineering,2013,116(6):653-659. |
| [53] | 张振宇.生物炭对稻田土壤镉生物有效性的影响研究[D].沈阳:沈阳农业大学,2013.ZHANG Zhen-yu.Effect of biochar on cadmium bio-availability in paddy soil[D].Shenyang:Shenyang Agricultural University,2013. |
| [54] | Inyang M,Gao B,Yao Y,et al.Removal of heavy metals from aqueous solution by biochars derived fromanaerobically digested biomass[J].Bioresource Technology,2012,110:50-56. |
| [55] | Yang Y,Zhang Y.The characteristics of Cu2+ and Pb2+ electrostatic and specific adsorptions of constant charge soil colloids[J].Acta Pedologica Sinica,2003,40(1):102-109. |
| [56] | Uchimiya M,Klasson K T,Wartelle L H,et al.Influence of soil properties on heavy metal sequestration by biochar amendment:1.Copper sorption isotherms and the release of cations[J].Chemosphere,2011,82(10):1431-1437. |
| [57] | Wang S,Gao B,Zimmerman A R,et al.Removal of arsenic by magnetic biochar prepared from pinewood and natural hematite[J].Bioresource Technology,2014,175:391-395. |
| [58] | Yakkala K,Yu M R,Roh H,et al.Buffalo weed (Ambrosia trifida L.var.trifida) biochar for cadmium (Ⅱ) and lead (Ⅱ) adsorption in single and mixed system[J].Desalination Water Treat,2013,51(40-42):7732-7745. |
| [59] | Gaskin J,Steiner C,Harris K,et al.Effect of low-temperature pyrolysis conditions on biochar for agricultural use[J].Transactions of the Asabe,2008,51(6):2061-2069. |
| [60] | 陈再明,方远,徐义亮,等.水稻秸秆生物碳对重金属Pb2+的吸附作用及影响因素[J].环境科学学报,2012,32(4):769-776.CHEN Zai-ming,FANG Yuan,XU Yi-liang,et al.Adsorption of Pb2+ by rice straw derived-biochar and its influential factors[J].Acta Scientiae Circumstantiae,2012,32(4):769-776. |
| [61] | Chen Z M,Chen B L,Zhou D D.Composition and sorption properties of rice-straw derived biochars[J].Acta Scientiae Circumstantiae,2013,33(1):9-19. |
| [62] | Ma J C,Dougherty D A.The cation-π interaction[J].Chemical Reviews,1997,97(5):1303-1324. |
| [63] | 李力,陆宇超,刘娅,等.玉米秸秆生物炭对Cd (Ⅱ)的吸附机理研究[J].农业环境科学学报,2012,31(11):2277-2283.LI Li,LU Yu-chao,LIU Ya,et al.Adsorption mechanisms of cadmium (Ⅱ) on biochars derived from corn straw[J].Journal of Agro-Environment Science,2012,31(11):2277-2283. |
| [64] | Park J H,Choppala G K,Bolan N S,et al.Biochar reduces the bioavailability and phytotoxicity of heavymetals[J].Plant and Soil,2011,348(1/2):439-451. |
| [65] | 佟雪娇,李九玉,姜军,等.添加农作物秸秆炭对红壤吸附Cu (Ⅱ)的影响[J].生态与农村环境学报,2011,27(5):37-41.TONG Xue-jiao,LI Jiu-yu,JIANG Jun,et al.Effect of biochars derived from crop straws on Cu (Ⅱ) adsorption by red soils[J].Journal of Ecology and Rural Environment,2011,27(5):37-41. |
| [66] | 于志红,谢丽坤,刘爽,等.生物炭-锰氧化物复合材料对红壤吸附铜特性的影响[J].生态环境学报,2014,23(5):897-903.YU Zhi-hong,XIE Li-kun,LIU Shuang,et al.Effects of biochar-manganese oxides composite on adsorption characteristics of Cu in red soil[J].Ecology and Environmental Sciences,2014,23(5):897-903. |
| [67] | Wang S,Gao B,Li Y,et al.Manganese oxide-modified biochars:Preparation,characterization,and sorption of arsenate and lead[J].Bioresource Technology,2015,181:13-17. |
| [68] | Xue Y,Gao B,Yao Y,et al.Hydrogen peroxide modification enhances the ability of biochar (hydrochar) produced from hydrothermal carbonization of peanut hull to remove aqueous heavy metals:Batch and column tests[J].Chemical Engineering Journal,2012,200/202:673-680. |
| [69] | 石红蕾,周启星.生物炭对污染物的土壤环境行为影响研究进展[J].生态学杂志,2014,33(2):486-494.SHI Hong-lei,ZHOU Qi-xing.Research progresses in the effect of biochar on soil-environmental behaviors of pollutants[J].Chinese Journal of Ecology,2014,33(2):486-494. |
| [70] | Xu X,Cao X,Zhao L,et al.Removal of Cu,Zn,and Cd from aqueous solutions by the dairy manure-derived biochar[J].Environmental Science and Pollution Research,2013,20(1):358-368. |
| [71] | Mohan D,Kumar S,Srivastava A.Fluoride removal from ground water using magnetic and nonmagnetic corn stover biochars[J].Ecological Engineering,2014,73:798-808. |
| [72] | Oh T K,Choi B,Shinogi Y,et al.Effect of pH conditions on actual and apparent fluoride adsorption by biochar in aqueous phase[J].Water Air Soil Pollution,2012,223(7):3729-3738. |
| [73] | Mohan D,Sharma R,Singh V K,et al.Fluoride removal from water using biochar,a green waste low cost adsorbent:Equilibrium uptake and sorption dynamics modeling[J].Industrial and Engineering Chemistry Research,2012,51(2):900-914. |
| [74] | Yang Y,Lin X,We B,et al.Evaluation of adsorption potential of bamboo biochar for metal-complex dye:Equilibrium,kinetics and artificial neural network modeling[J].International Journal of Environmental Science and Technology,2014,11(4):1093-1100. |
| [75] | Rochefort A,Wuest J D.Interaction of substituted aromatic compounds with graphene[J].Langmuir,2009,25(1):210-215. |
| [76] | Xu R K,Xia S C,Yuan J H,et al.Adsorption of methyl violet from aqueous solutions by the biochars derived from crop residues[J].Bioresource Technology,2011,102(22):10293-10298. |
| [77] | Chen B,Yuan M.Enhanced sorption of polycyclic aromatic hydrocarbons by soil amended with biochar[J].Journal of Soils and Sediments,2010,11(1):62-71. |
| [78] | 王萌萌,周启星.生物炭的土壤环境效应及其机制研究[J].环境化学,2013,32(5):768-780.WANG Meng-meng,ZHOU Qi-xing.Environmental effects and their mechanisms of biochar applied to soils[J].Environmental Chemistry,2013,32(5):768-780. |
| [79] | Hale S E,Hanley K,Lehmann J,et al.Effects of chemical,biological,and physical aging as well as soil addition on the sorption of pyrene to activated carbon and biochar[J].Environmental Science and Technology,2011,45(24):10445-10453. |
| [80] | Yao Y,Gao B,Fang J,et al.Characterization and environmental applications of clay-biochar composites[J].Chemical Engineering Journal,2014,242:136-143. |
| [81] | Klasson K T,Ledbetter C A,Uchimiya M,et al.Activated biochar removes 100% dibromochloropropane from field well water[J].Environmental Chemistry Letter,2013,11(3):271-275. |
| [82] | 邓玉,倪福全.水环境中抗生素残留及其危害[J].南水北调与水利科技,2011,9(3):96-100.DENG Yu,NI Fu-quan.Research on antibiotics residues and hazardous in aquatic environment[J].South-to North Water Diversion and Water Science and Technology,2011,9(3):96-100. |
| [83] | 景向荣.生物炭材料的修饰应用与毒性评价[D].合肥:中国科学技术大学,2014.JING Xiang-rong.Modification of pyrolytic biochar and toxicity evaluation[D].Hefei:University of Science and Technology of China,2014. |
| [84] | Keiluweit M,Kleber M.Molecular-level interactions in soils and sediments:The role of aromatic systems[J].Environmental Science and Technology,2009,43(10):3421-3429. |
 2015, Vol. 34
2015, Vol. 34