文章信息
- 许彩云, 靳红梅, 杜静, 常志州, 黄红英, 周立祥
- XU Cai-yun, JIN Hong-mei, DU Jing, CHANG Zhi-zhou, HUANG Hong-ying, ZHOU Li-xiang
- 水力停留时间对猪粪厌氧发酵残留物中磺胺类抗生素分布的影响
- Effects of hydraulic retention time on sulfonamides distributions in anaerobic digestates of swine manure
- 农业环境科学学报, 2016, 35(11): 2187-2194
- Journal of Agro-Environment Science, 2016, 35(11): 2187-2194
- http://dx.doi.org/10.11654/jaes.2016-0488
文章历史
- 收稿日期: 2016-04-11
2. 江苏省农业科学院农业资源与环境研究所, 江苏省农业废弃物资源化工程技术研究中心, 南京 210014 ;
3. 农业部农村可再生能源开发利用华东科学观测实验站, 农业部长江中下游平原农业环境重点实验室, 南京 210014
2. Institute of Agricultural Resources and Environment, Jiangsu Academy of Agricultural Sciences;Jiangsu Agricultural Waste Treatment and Recycle Engineering Research Center, Nanjing 210014, China ;
3. East China Scientific Observing and Experimental Station of Development and Utilization of Rural Renewable Energy, Ministry of Agriculture; Key Laboratory of Agro-Environment in Downstream of Yangtze Plain, Ministry of Agriculture, Nanjing 210014, China
我国畜禽养殖年消耗各类抗生素9.68 万t,居世界首位[1]。畜禽摄入的抗生素有30%~90%以母体代谢物的形式排出体外[2-4],导致畜禽粪尿和冲洗水中抗生素含量过高,通过农田施用或随意排放进入环境[5],不仅对动、植物有直接的生物毒性,而且给环境中的细菌带来选择压力,造成抗性细菌的累积和抗性基因(ARGs)的传播,被认为是生态安全风险极高的新型污染物[6]。我国是生猪养殖大国,截至2013 年生猪年饲养总量(出栏+存栏)已超过11亿头[7]。随着养殖规模不断扩大,猪场产生的粪尿及污水也相对集中,猪粪水的处理已成为畜禽污染处理和防治重点[8]。磺胺类药物(Sulfonamides,SAs)是规模猪场最为广泛使用的兽用抗生素之一[9],在猪粪水中的残留量和检出率均较高。以江苏为例[10],在13 个市内选取的80 份猪场粪便样品中,以磺胺二甲嘧啶(SM)检出率最高,达到50%以上,磺胺氯哒嗪(SCP)、磺胺嘧啶(SD)检出率也均高于30.0%,三者的平均残留量分别为34.0、49.0、69.0 μg·kg-1。猪场粪污中SAs及其携带的大量ARGs 在周边土壤和水体中的检出率、含量和危害远高于其他兽用抗生素[11-12]。
沼气工程是我国规模猪场粪污处理的重要环节[8, 13]。截至2012年末全国大中型猪场沼气工程的覆盖率已达52.6%(约为1.28 万处),发酵残留物(即沼液和沼渣)总量超过1.30伊109 t,大部分未经处理就直接还田或排放[8]。由于抗生素对大多数细菌具有抑制和杀灭作用,采用厌氧消化等生物处理技术并不能将其完全去除[14]。Mitchell 等[15]通过序批式试验发现,中温厌氧发酵对牛粪中SM 未有降解。Mohring 等[16]以猪粪为原料,经34 d 中温厌氧消化后发现,SD、SMR(磺胺甲嘧啶)、SMX(磺胺甲恶唑)、SMDP(磺胺地索辛)、TMP(甲氧苄胺嘧啶)几乎全部被去除,而SM 和SCP未观察到有降解。处理工艺和反应条件是影响厌氧发酵中SAs降解的关键因子[17]。田世烜等[18]利用UASBSBR工艺去除生活污水中SM 的研究结果发现,厌氧处理对SM 的平均去除率仅为35.0%。Chen等[19]对猪场厌氧消化处理、兼氧-好氧生物处理出水中兽用抗生素的消减规律研究表明,生物处理技术对SD 的去除率不足10.0%。尽管Sponza 等[20]研究认为升流式厌氧污泥床(UASB)和完全混合式反应器(CSTR)厌氧发酵工艺对药厂废水中SMR 的去除率可达90.0%,但由于药厂废水中SAs 含量(10-6 级)远高于养殖粪污和污水中SAs 含量(10-9级),发酵残留物中SAs 浓度仍然过高。可见,厌氧发酵残留物中仍可能含有高浓度的SAs,但对残留的SAs 在沼液和沼渣中如何分布尚不清楚。这将影响畜禽粪污发酵残留物后续无害化处理工艺选择和农田利用环境安全性评价。
目前,国内外大型沼气工程以中温CSTR 厌氧发酵工艺应用最为广泛,也是我国高浓度畜禽粪污处理沼气工程主导工艺之一[13]。在此工艺条件下,水力停留时间(HRT)是影响厌氧反应体系缓冲能力和稳定性、物料降解程度及微生物活性的重要指标[17, 21]。根据前期的调查结果分析[13],江苏省畜禽养殖场大中型沼气工程的HRT普遍为15~20 d。基于此,本研究以猪粪为发酵原料,采用CSTR 工艺在中温(37±1℃)条件下进行室内模拟实验,探讨HRT=20 d和HRT=15 d条件下,SD、SM 和SCP 的残留水平及其在固/液相中的分配特征,以期为厌氧发酵条件下规模猪场粪污中抗生素的有效去除提供理论支撑,为沼液和沼渣农田安全利用的环境影响评价提供科学依据。
1 材料与方法 1.1 试验材料与装置猪粪取自江苏省金坛市某规模养猪场,一次性取样,0~4℃冷藏备用。猪粪总固体(TS)、挥发性固体(VS)、总有机碳(TOC)、总氮(TN)和总磷(TP)含量分别为24.3%、79.9%、34.6%、2.01%和1.97%,仅检测出金霉素(37.3 μg·kg-1干重),未检出磺胺类抗生素。厌氧发酵接种物为本实验室污泥罐排出液(发酵底物为新鲜猪粪),经纱布过滤后于(37±1)℃下保存待用。接种物的TS 为3.28%,VS为65.28%,pH为7.78。
厌氧发酵装置采用自行设计的CSTR(图 1),材质为有机玻璃,总容积为12.5 L(内径20 cm、高40 cm),有效容积10.0 L。反应器采用双层夹套,用恒温水浴锅为反应器保温。反应器内设有搅拌器,机械密封,搅拌器电机和定时开关相连接,采用上方进料、下方出料的形式,各由一个阀门进行控制。

|
| 图 1 完全混合式反应器(CSTR)示意图 Figure 1 Schematic diagram of the CSTR in this study 1.水浴进口Inlet of water bath;2.水浴出口Outlet of water bath;3.进料口Feed inlet;4.出料口Discharge hole;5.搅拌电机Stirring motor;6.搅拌叶片Stirring blades;7.出气口Gas outlet;8.气体流量计Gas flowmeter |
试验采用半连续发酵方式,HRT 分别为20 d和15 d。整个试验持续时间为91 d,分为启动期和稳定运行期。启动阶段(S0)自2015 年8 月20 日开始,向上述CSTR 中一次性进料800 g(干物质),同时加入接种污泥调节各处理的TS 负荷均为8.0%,通入氮气15 min 以除去反应器内的空气,密封。反应器通过水浴夹套进行加温,水浴温度保持在(37±1)℃。采用间歇搅拌,每2 h 搅拌一次,每次持续时间为5 min,搅拌频率为20 r·min-1。运行21 d后,系统达到稳定状态,进行半连续进料试验。
稳定运行阶段:(1)HRT=20 d时(S1),每日一次性进料500 mL,TS=8.0%。在进料中加入SD、SM 和SCP 的混合液(纯度>98%,购自百灵威科技有限公司,用超纯水配制成10 mg·L-1 的抗生素混合标准溶液),使其在进料中的浓度为10 μg·L-1(根据前期猪场沼气工程进料中抗生素的调查结果)。每日定时进料,同时出料500 mL,每4 d将出料经离心后固液分离,液体为沼液,固体为沼渣,均在-18℃条件下保存。(2)HRT=15 d时(S2),各处理每日进料667 mL,TS=8.0%,同时出料667 mL。抗生素添加浓度及运行方法同S1,每3 d将出料经固液分离后在-18℃条件下保存。每个HRT各运行2 个周期,取数据平均值用于分析。整个试验共有样本20个(n=20),分析其中的各项指标。每日监测产气量及甲烷含量,确保反应正常进行。
1.2.2 分析方法基本理化指标:(1 )TS 采用105℃烘24 h,差重法测定[17];(2)VS 采用550℃马弗炉灼烧4 h,差重法测定[17];(3)日产气量采用排水法测定[17];(4)产气中的甲烷含量采用GC9890A/T 气相色谱仪分析(TCD 检测器),检测器温度120℃,进样器为平面流通阀,分析柱为TDC-01椎4伊1 m,柱温100℃,载气为氢气,流速50 mL·min-1,定量管1 mL,标准气体为氮气(含42.4%甲烷+28.4%二氧化碳),分析方法为外标法;(5)消化液的pH 采用玻璃电极法(GB 6920—1986),化学需氧量(COD)采用重铬酸钾氧化法(GB 11914—1989),氨氮(NH3-N)采用纳氏试剂分光光度法(HJ535—2009),挥发性有机酸(VFA)采用气相色谱仪(GC—2014,日本岛津)。
磺胺类抗生素:采用超高效液相色谱/串联质谱法测定[22]。出料首先固液分离,提取和净化方法为:沼液经0.45 μm玻璃纤维滤膜过滤,取500 mL 加入10μL内标(磺胺二甲嘧啶,98.0%,购自加拿大多伦多研究化学品公司)以及0.4 g EDTA,立即储存在4℃条件下。用甲酸调节提取液至pH 2.0~3.0,过经活化的HLB 固相萃取柱,控制流速为3~5 mL·min-1。之后用超纯水冲洗HLB 柱,抽真空以去除柱中残留水分,然后将HLB 柱在氮气保护下干燥10 min。最后以2 mL甲醇洗脱3 次,收集洗脱液,并在室温下用氮气吹至近干,用乙腈/0.2%甲酸(1:9,V/V)混合液定容至1mL,涡旋振荡2~3 min,18 000 r·min-1 离心10 min,取上清液待分析。
沼渣置于-40℃冷冻一周后,使用冷冻干燥仪进行干燥。研磨干燥沼渣,过250 μm 孔径尼龙筛,置于-40℃存放。准确称取(5±0.01)g研磨样品于50 mL离心管中,加入10 μL 内标物质,并加入0.4 g EDTA以及混合提取液[磷酸盐缓冲液(pH3)/乙腈,1:1,V/V]30 mL,涡旋2 min,超声提取20 min,4℃下8000 r·min-1离心8 min,收集上层提取液。反复提取2 次后,合并提取液并混匀。用旋转蒸发仪旋蒸(220 Pa,50℃)提取液,直至剩余30 mL 以下,用蒸馏水稀释到200 mL,用甲酸调至pH 2.8~3.0,将稀释液用100 mL正己烷萃取2 次,脱去粪便中的脂肪,之后过0.45μm 玻璃纤维微孔滤膜。提取液用SAX-HLB 串联固相萃取柱净化与富集,过柱完成后去除SAX 柱,其余处理过程与液体方法相同。详细步骤参照郭欣妍等[22]。
利用ACQUITYTM 超高效液相色谱仪-QuattroPremier XE 质谱仪(美国Waters 公司),配MassLynxV.4.1 软件Waters Acquity 和UPLC BEH C18 色谱柱(100 mm×2.1 mm,1.7 μm),测定上清液中抗生素的含量。MS 检测条件:电喷雾离子源(ESI),离子源温度120℃,脱溶剂温度380℃,脱溶剂气和锥孔气为氮气,脱溶剂气流速500 L·h-1,锥孔气流速50 L·h-1,碰撞气为高纯氩气,采用多反应监测模式(MRM)检测。ESI-MS/MS 选择性反应正离子源检测,进样量5 μL。HPLC 测定时柱温35℃,流动相为乙腈(A)和0.2%(V/V)甲酸(B),流速0.3 mL·min-1,测定时采用的流动相梯度为:0~7 min,10%~40%A;7~9 min,40%~60%A;9~9.01 min,60%~10% A;9.01~12 min,10%A。
1.3 数据分析相同HRT条件下各指标在不同处理间的差异采用单因素方差分析(ANOVA),均值比较采用最小显著差法(LSD),显著性水平α=0.05;同一处理组不同HRT间的差异采用独立样本t 检验。统计分析软件为SPSS 21.0。
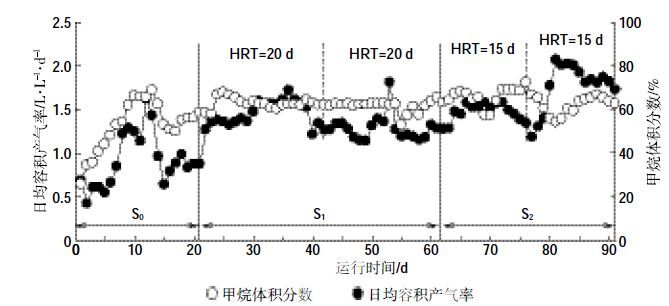
2 结果与讨论 2.1 产气特性各处理厌氧消化容积产气率和甲烷体积分数如图 2所示。可以看出,经过3 周的启动阶段(S0),系统逐步稳定。至启动期结束时,系统累积产气率达286mL·g-1 VS。半连续发酵S1阶段,添加物料后系统在第21 d产气达到正常水平,之后日产气量稳定在1.40L·L-1·d-1左右,累积VS 产气率为428 mL·g-1;S2阶段日均容积产气率略高于S1阶段,约为1.70 L·L-1·d-1,累计VS 产气率为380 mL·g-1。厌氧发酵产气中甲烷体积分数在第7 d即达到60.0%以上,半连续进料阶段由于新物料的加入对原发酵系统有机负荷的冲击,系统的甲烷含量均有不同程度的下降,但总体维持在65.0%左右。S1阶段产甲烷总量为340 L,S2阶段总量为308 L。从整个运行阶段的产气率和甲烷含量来看,各处理的厌氧消化过程均正常,并没有因为抗生素的添加而影响厌氧微生物基本活性;但HRT=20 d(S1)时,发酵体系的累计VS 产气率和产甲烷量均高于HRT=15 d的处理,分别提高12.4%和10.4%。
|
| 图 2 各处理日均容积产气率和甲烷体积分数 Figure 2 Daily volume biogas yield and volume fraction of CH4 in biogas during anaerobic digestion of three treatments |
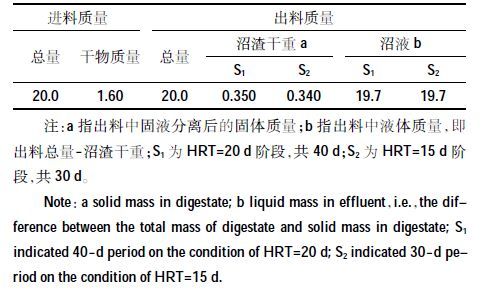
半连续发酵阶段进料及沼液、沼渣的总质量详见表 1。不同HRT 条件下,出料中固相和液相的质量无明显差异。但在厌氧消化过程中,微生物及其驱动的理化性状变化是影响抗生素降解最主要的因子,其中pH、COD、NH3-N、总VFA 及其组分等表征厌氧消化的重要指标[21, 23-25],均可间接反映发酵过程对SAs 的降解作用。例如,pH可影响不同酸度系数的抗生素的吸附和疏水分配;COD 易于与抗生素络合或配合,直接影响SD、SM 和SCP 在固相中分配,并间接影响抗生素结构及其生物降解[25]。
 |
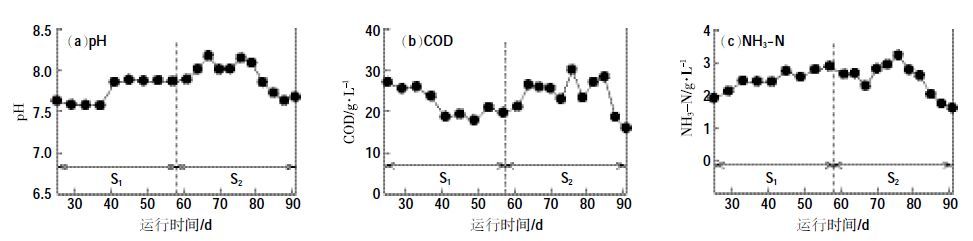
半连续发酵阶段发酵液pH、COD 和NH3-N 浓度如图 3 所示。S1阶段发酵液pH 维持在7.50~7.90 范围内,随着水力停留时间的缩短,单位体积内的有机负荷增加;S2阶段发酵液pH 有小幅提高(图 3a),但均在正常厌氧发酵所要求的pH 条件下(即6.50~8.00)[17]。进料中平均COD 为86.2 g·L-1,S1阶段发酵液平均COD 浓度为21.9 g·L-1,COD 平均去除率为74.6%;随着有机负荷的增加,S2阶段COD 去除率降低,消化液中平均COD 浓度为24.3 g·L-1,COD 平均去除率为71.8%(图 3b)。整个发酵过程中,发酵液中NH3-N 维持在1.60~3.30 g·L-1 之间(图 3c),此水平NH3-N 浓度不会对厌氧消化产生氨抑制作用。
|
| 图 3 厌氧发酵过程中消化液pH、COD 和NH3-N 的变化 Figure 3 The pH,concentration of COD and NH3-N in digestates during the anaerobic digestion |
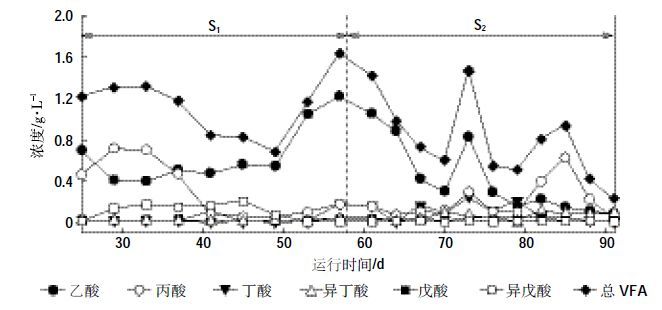
VFA 是厌氧发酵过程中关键的中间产物,主要成分为乙醇、乙酸、丙酸、丁酸、乳酸等,是反映消化效果的重要调控指标[24-25]。半连续发酵阶段发酵液中有机酸组分和总VFA 浓度如图 4 所示。产气量和产甲烷量的变化可从发酵液中VFA 浓度变化得到验证。总体上看,消化液中以乙酸为主,其他酸含量较少,后期丙酸有所增加,说明反应底物的乙酸大量被厌氧微生物利用;而丙酸不易被微生物利用,因此在消化体系中积累。
|
| 图 4 各处理消化液中有机酸组分及总VFA浓度 Figure 4 The concentrations of organic acids in three treatments |
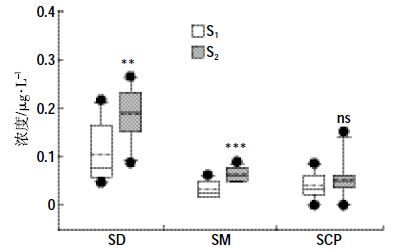
各处理沼液中SAs浓度水平如图 5所示。整个反应过程中,发酵液中磺胺类抗生素的浓度变化较大。HRT=20 d和15 d时,SD 的平均浓度分别为0.106 0、0.191 0 μg·L-1,SM 分别为0.033 0、0.066 0 μg·L-1,SCP分别为0.040 0、0.055 0 μg·L-1。总体来讲,除了SCP 之外,水力停留时间较短时(S2)沼液中SD 和SM含量显著(P<0.01 和0.001)高于水力停留时间较长的处理(S1)。这可能与较长水力停留时间下微生物有更长的时间降解抗生素有关。
|
| 图 5 不同HRT条件下沼液中SD、SM和SCP的浓度水平 Figure 5 The concentrations of SD,SMand SCP indigestates at two HRTs 箱体上线、中线和下线分别表示第三四分位、中值和第一四分位值;虚线表示平均值;最上方和最下方的线段表示最大值和最小值;黑点表示异常值;ns、**和*** 分别表示两个HRT之间无显著性差异、差异显著(P<0.01)和差异极显著(P<0.001) The upper,middle and lower edges of the box indicated the 75th,50th and25th percentiles of the data set,respectively. The broken lines indicated themean values. The vertical lines indicated the minimumand maximumdatavalues. The black dots outside the ends of the vertical lines were outlier orsuspected outlier. ns,** and *** indicated that the differences between thetwo HRTs were not significant,significant at levels of 0.01 and 0.001,respectively |
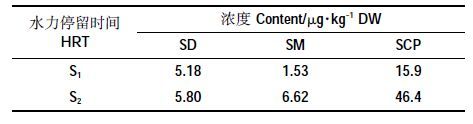
各处理沼渣中SAs浓度水平如表 2所示。总体来看,沼渣中SD、SM 和SCP 的浓度均显著高于其在沼液中的浓度,分别为沼液中的几倍甚至百倍。这说明厌氧消化过程中进料中未被分解的抗生素在沼渣中有浓缩作用。对于不同的HRT 条件,S2阶段沼渣中SD、SM 和SCP 的浓度明显高于S1阶段,最主要的原因是HRT 较短的条件下微生物无法对SAs 充分降解。对于3 种抗生素,SCP在沼渣中的浓度明显高于SD 和SM。这可能是由于SCP 酸度系数较低(pKa5.50),在厌氧消化过程中主要以阴离子形式存在,与沼渣的吸附较疏水分配更强;而SD(pKa 6.40)和SM(pKa 7.50)主要以中性分子存在,以疏水分配为主[26]。
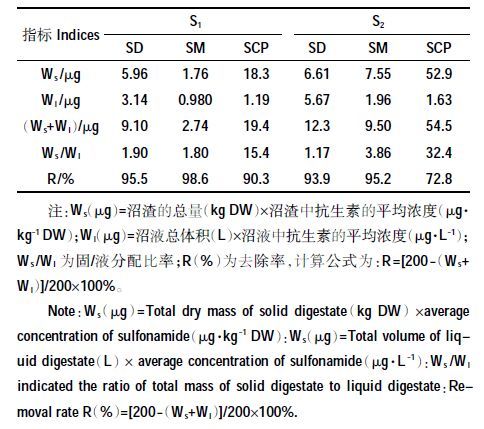
经中温厌氧消化后,SD、SM 和SCP 的去除率及其残留在固相和液相中的分配特征详见表 3。整个运行过程中,各处理组中SD 和SM 的去除率均大于90%,而SCP的降解率略低于二者。就不同HRT 而言,HRT 较短的处理磺胺类抗生素的降解率均低于HRT较长的处理,特别是对于SCP降幅更为明显。这与总VFA 及乙酸的变化一致,说明厌氧消化系统中抗生素的去除与厌氧微生物的活动密切相关。此外,磺胺类抗生素的乙酰化代谢物占总量的20%~40%,会与母体化合物一同随猪粪尿排泄到体外,在清扫、收集和进料过程中可进一步生成乙酰化代谢物[27]。这些代谢物在厌氧条件下易通过生物转化重新形成药物原型[28],以此为原料进行厌氧发酵,极大地增加了磺胺类代谢产物转化为原型的风险[29]。因此,如何有效降解SAs及其代谢物是未来研究的重点。
 |
对于未降解的SAs而言,猪粪沼渣中的3 种抗生素残留量显著高于沼液(即固液比>1),其中SCP 在沼渣中的分配比率最高,主要与其酸度系数较低、与沼渣的吸附分配更强有关[26];同时发现,发酵时间较短的猪粪沼渣中抗生素残留量大(即S2>S1)。这说明,与猪粪沼液相比,沼渣还田利用过程中的环境风险更大。因此,在发酵过程中应使物料充分降解,同时在后续处理环节应进一步对沼液和沼渣中的抗生素进行消减[30-31],降低其环境危害。
3 结论(1)中温厌氧消化可大幅降低猪粪中SD、SM 和SCP 的含量,去除率为72.8%~98.6%。提高反应体系的HRT对SAs 和COD 的去除率、累积产气率及产甲烷总量均有积极的作用。特别是对于SCP,HRT=20 d时其去除率达到90.3%,远远高于HRT=15 d时的72.8%。
(2)猪粪沼渣中抗生素的浓度是沼液的几倍至百倍,且沼渣中抗生素的残留量显著高于沼液,在后续处理中应重点对其进行消减,降低其还田利用的环境危害。
(3)对于3 种磺胺类抗生素而言,SD 更多地分布在液相中,而SCP则在沼渣中占有绝对优势。增强底物可利用性、提高微生物活性、抑制磺胺类抗生素乙酰化代谢产物在厌氧条件下的生物转化,是提高厌氧消化过程中SAs有效去除的关键。
| [1] | Zhang Q Q, Ying G G, Pan C G, et al. A comprehensive evaluation of antibiotics emission and fate in the river basins of China:Source analysis, multimedia modelling and linkage to bacterial resistance[J]. Environmental Science and Technology , 2015, 49 (11) : 6772–6782. DOI:10.1021/acs.est.5b00729 |
| [2] | Fang H, Han Y L, Yin Y M, et al. Variations in dissipation rate, microbial function and antibiotic resistance due to repeated introductions of manure containing sulfadiazine and chlortetracycline to soil[J]. Chemosphere , 2014, 96 : 51–56. DOI:10.1016/j.chemosphere.2013.07.016 |
| [3] | 王瑞, 魏源送. 畜禽粪便中残留四环素类抗生素和重金属的污染特征及其控制[J]. 农业环境科学学报 , 2013, 32 (9) : 1705–1719. WANG Rui, WEI Yuan-song. Pollution and control of tetracyclines and heavy metals residues in animal manure[J]. Journal of Agro-Environment Science , 2013, 32 (9) : 1705–1719. |
| [4] | Zhang Y P, Zhang C Q, Parker D B, et al. Occurrence of antimicrobials and antimicrobial resistance genes in beef cattle storage ponds and swine treatment lagoons[J]. Science of the Total Environment , 2013, 463 . |
| [5] | Luo Y, Xu L, Rysz M, et al. Occurrence and transport of tetracycline, sulfonamide, quinolone, and macrolide antibiotics in the Haihe River basin, China[J]. Environmental Science and Technology , 2011, 45 (5) : 1827–1833. DOI:10.1021/es104009s |
| [6] | 王健, 贲伟伟, 强志民, 等. 我国养猪业废弃物中四环素类、磺胺类抗生素及相关抗性基因污染研究进展[J]. 生态毒理学报 , 2015, 10 (5) : 2–10. WANG Jian, BEN Wei-wei, QIANG Zhi-min, et al. Contamination of tetracyclines, sulfonamides and corresponding resistance genes in the waste from Chinese pig industry[J]. Asian Journal of Ecotoxicology , 2015, 10 (5) : 2–10. |
| [7] | . 2014年中国统计年鉴[M]. 中华人民共和国国家统计局: 2014 . . China statistical yearbook 2014[M]. National Bureau of Statistics of the People's Republic of China: 2014 . |
| [8] | 武深树, 谭美英, 刘伟. 沼气工程对畜禽粪便污染环境成本的控制效果[J]. 中国生态农业学报 , 2012, 20 (2) : 247–252. WU Shen-shu, TAN Mei-ying, LIU Wei. Environmental cost control of livestock and poultry fecal pollution via biogas project[J]. Chinese Journal of Eco-Agriculture , 2012, 20 (2) : 247–252. DOI:10.3724/SP.J.1011.2012.00247 |
| [9] | Lon A U, Michele A D. Subtherapeutic use of antibiotics in food producing animals[J]. Clinical Research and Regulatory Affairs , 2008, 9 (3) : 187–195. |
| [10] | 陈昦, 董元华, 王辉, 等. 江苏省畜禽粪便中磺胺类药物残留特征[J]. 农业环境科学学报 , 2008, 27 (1) : 385–389. CHEN Hao, DONG Yuan-hua, WANG Hui, et al. Residual characteristic of sulfonamides in animal feces in Jiangsu Province[J]. Journal of Agro-Environment Science , 2008, 27 (1) : 385–389. |
| [11] | Zhu Y G, Johnson T A, Su J Q, et al. Diverse and abundant antibiotic resistance genes in Chinese swine farms[J]. Proceedings of the National Academy of Sciences of the United States of America , 2013, 110 (9) : 3435–3440. DOI:10.1073/pnas.1222743110 |
| [12] | Wang N, Guo X Y, Xu J, et al. Pollution characteristics and environmental risk assessment of typical veterinary antibiotics in livestock farms in Southeastern China[J]. Journal of Environmental Science and Health, Part B , 2014, 49 : 1–12. |
| [13] | 叶小梅, 常志州, 钱玉婷, 等. 江苏省大中型沼气工程调查及沼液生物学特性研究[J]. 农业工程学报 , 2012, 28 (6) : 222–227. YE Xiao-mei, CHANG Zhi-zhou, QIAN Yu-ting, et al. Investigation on large and medium scale biogas plants and biological properties of digestate in Jiangsu Province[J]. Transactions of the Chinese Society of Agricultural Engineering , 2012, 28 (6) : 222–227. |
| [14] | 常红, 胡建英, 王乐征, 等. 城市污水处理厂中磺胺类抗生素的调查研究[J]. 科学通报 , 2008, 53 (2) : 159–164. CHANG Hong, HU Jian-ying, WANG Le-zheng, et al. Survey on sulfonamides in municipal wastewater treatment plant[J]. Chinese Science Bulletin , 2008, 53 (2) : 159–164. |
| [15] | Mitchell S M, Ullman J L, Teel A L, et al. The effects of antibiotics ampicillin, florfenicol, sulfamethazine, and tylosin on biogas production and their degradation efficiency during anaerobic digestion[J]. Bioresource Technology , 2013, 149 (10) : 244–252. |
| [16] | Mohring S A I, Strzysch I, Fernandes M R, et al. Degradation and elimination of various sulfonamides during anaerobic fermentation:A promising step on the way to sustainable pharmacy?[J]. Environmental Science and Technology , 2009, 43 (7) : 2569–2574. DOI:10.1021/es802042d |
| [17] | 贺延龄. 废水的厌氧生物处理[M]. 北京: 中国轻工业出版社, 1999 : 536 . HE Yan-ling. Anaerobic biological treatment of waste water[M]. Beijing: China Light Industry Press, 1999 : 536 . |
| [18] | 田世烜, 张萌, 陈亮, 等. UASB-SBR工艺去除生活污水中磺胺二甲基嘧啶的试验研究[J]. 水处理技术 , 2011, 37 (4) : 84–87. TIAN Shi-xuan, ZHANG Meng, CHEN Liang, et al. Lab-scale study on removal of sulfamethazine from sewage by UASB-SBR process[J]. Technology of Water Treatment , 2011, 37 (4) : 84–87. |
| [19] | Chen Y S, Zhang H B, Luo Y M, et al. Occurrence and dissipation of veterinary antibiotics in two typical swine wastewater treatment systems in east China[J]. Environmental Monitoring and Assessment , 2012, 184 : 2205–2217. DOI:10.1007/s10661-011-2110-y |
| [20] | Sponza D T, Demirden P. Treatability of sulfamerazine in sequential upflow anaerobic sludge blanket reactor(UASB)/completely stirred tank reactor(CSTR) processes[J]. Separation Purification Technology , 2007, 56 (1) : 108–117. DOI:10.1016/j.seppur.2006.07.013 |
| [21] | 冯孝善, 方士. 厌氧消化技术[M]. 杭州: 浙江科学技术出版社, 1989 . FENG Xiao-shan, FANG Shi. Anaerobic digestion technology[M]. Hangzhou: Zhejiang Science and Technology Publishing Press, 1989 . |
| [22] | 郭欣妍, 王娜, 郝利君, 等. 超高效液相色谱法/串联质谱法同时测定水、土壤及粪便中25种抗生素[J]. 分析化学 , 2015, 43 (1) : 13–20. GUO Xin-yan, WANG Na, HAO Li-jun, et al. Simultaneous detection of 25 kinds of veterinary antibiotics in soil, manure and water samples using liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry , 2015, 43 (1) : 13–20. |
| [23] | Starkenburg W V. Anaerobic treatment of wastewater:State of the art[J]. Microbiology , 1997, 66 : 705–715. |
| [24] | Wang J Q, Shen D S, Xu Y H. Effect of acidification percentage and volatile organic acids on the anaerobic biological process in simulated landfill bioreactors[J]. Process Biochemistry , 2006, 41 (7) : 1677–1681. DOI:10.1016/j.procbio.2006.02.005 |
| [25] | Lim S J, Kim B J, Jeong C M, et al. Anaerobic organic acid production of food waste in once-a-day feeding and drawing-off bioreactor[J]. Bioresource Technology , 2008, 99 (16) : 7866–7874. DOI:10.1016/j.biortech.2007.06.028 |
| [26] | Gevao B, Semple K T, Jones K C. Bound pesticide residues in soils:A review[J]. Environmental Pollution , 2000, 108 (1) : 3–14. DOI:10.1016/S0269-7491(99)00197-9 |
| [27] | Radke M, Lauwigi C, Heinkele G, et al. Fate of the antibiotic sulfamethoxazole and its two major human metabolites in a water sediment test[J]. Environmental Science & Technology , 2009, 43 (9) : 3135–3141. |
| [28] | 王娜. 环境中磺胺类抗生素及其抗性基因的污染特征及风险研究[D]. 南京:南京大学, 2014. WANG Na. Pollution characteristics and risk of sulfonamides antibiotics and their resistance genes in the environment[D]. Nanjing:Nanjing University, 2014. http://cdmd.cnki.com.cn/Article/CDMD-10284-1015506560.htm |
| [29] | Qin M N, Lin Z F, Wang D L, et al. What are the differences between aerobic and anaerobic toxic effects of sulfonamides on Escherichia coli?[J]. Environmental Toxicology and Pharmacology , 2015, 41 : 251–258. |
| [30] | Ben W W, Qiang Z M, Pan X, et al. Removal of veterinary antibiotics from sequencing batch reactor(SBR) pretreated swine wastewater by Fenton's reagent[J]. Water Research , 2009, 43 (17) : 4392–4402. DOI:10.1016/j.watres.2009.06.057 |
| [31] | Garoma T, Umamaheshwar S K, Mumper A. Removal of sulfadiazine, sulfamethizole, sulfamethoxazole, and sulfathiazole from aqueous solution by ozonation[J]. Chemosphere , 2010, 79 (8) : 814–820. DOI:10.1016/j.chemosphere.2010.02.060 |
 2016, Vol. 35
2016, Vol. 35