2. 吉林大学地下水环境与资源教育部重点实验室, 长春 130021;
3. 黑龙江省水文地质工程地质勘察院, 哈尔滨 150030
2. Key Laboratory of Groundwater Environment and Resources, Ministry of Education, Jilin University, Changchun 130021, China;
3. Hydrogeology and Engineering Geology Exploration Institute of Heilongjiang Province, Haerbin 150030, China
蒙脱石和高岭石是土壤中分布最广泛的黏土胶粒[1],它们在地下水中具有一定的迁移能力。由于胶粒粒径小,比表面积大,且具有一定的吸附能力,能够通过携带迁移机制促进地下水污染物的迁移[2]。近年来,学者们研究了黏土胶粒对环境污染物迁移的影响,以及物理化学参数对于胶粒迁移的控制作用。孙慧敏等[3-4]探讨了离子强度和pH对黏土矿物胶体在饱和多孔介质中运移的影响,发现高岭石胶粒表面Zeta电位受pH控制,低pH条件有利于高岭石胶体在柱内的衰减;而pH对蒙脱石胶体迁移的影响不明显。离子强度增强可促进蒙脱石胶体在石英砂上的沉降,而降低离子强度会引起胶体从石英砂面的解吸。胡俊栋等[5]研究了土壤水pH、离子强度、孔隙水流速和胶体粒径对天然土壤胶体在土壤介质中释放和沉积等迁移行为的影响,同样发现了高pH和低离子强度有利于土壤胶体的迁移;粒径能影响能量次井高度从而控制胶体颗粒的迁移。刘庆玲等[6]综述了胶体的表面性质(亲水或疏水)、稳定性、水溶液的化学组分、离子强度、pH值和流速等因素对胶体沉积、释放和迁移动力学产生的影响。除了水物理化学和多孔介质特征对胶体迁移的影响,污染物与胶体的共迁移是污染物迁移新的研究方向。孙慧敏等[7]研究了黏土矿物胶体对铅的迁移的影响,发现黏土胶体可以携带并促进铅的迁移。杨悦锁等[8]综述分析了在土壤和地下水环境中的胶体与污染物的共同迁移机理。这些研究,促进了对于黏土胶粒和其他工程纳米材料在多孔介质中迁移行为的理解。
镉与腐植酸是地下水环境中较常见的两种污染物质。镉是地球上危害最大的重金属元素之一[9-10],许多地区的地下水中都存在镉含量超标的现象;腐植酸是天然有机大分子的混合物,在地下水环境中广泛存在[11]。因此,在地下水环境中,黏土胶粒很可能与镉和腐植酸发生共迁移。理解这些物质对黏土胶粒迁移的影响,对于准确评价黏土胶粒的迁移行为以及对其他污染物质的携带迁移十分重要。但目前讨论重金属镉和腐植酸对黏土胶粒迁移影响的研究相对不足。针对这一现状,本文选择结构存在差异的蒙脱石和高岭石黏土胶粒作为研究对象,基于同步注射柱实验,研究镉和腐植酸对黏土胶粒在饱和多孔介质中的迁移影响。
1 材料与方法 1.1 石英砂石英砂(0.125~0.15 mm)(MACKLIN)用浓盐酸(12 mol·L-1)浸泡24 h去除表面的金属矿物质,然后用超纯水冲洗至pH中性,再在烘箱中105 ℃烘干24 h备用[12-13]。由于石英砂的等电点为2~3,在本实验pH条件下,石英砂表面带净负电荷。
1.2 背景注射溶液支持电解质溶液为10 mmol·L-1的NaCl溶液。溶液pH用Tris-HCl稳定到pH 7.1。所有需要过柱的液体均需在水浴超声(昆山市超声仪器有限公司,KQ2200E)条件下,使用真空泵(上海亚荣生化仪器厂,SHZ-Ⅲ型)抽真空除气30 min。
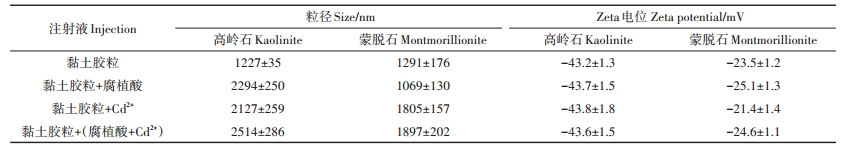
1.3 黏土胶粒黏土胶粒选用蒙脱石(源叶生物科技有限公司,上海)和高岭石(2.0 μm)(上海昊弗化工有限公司,上海)。将黏土胶粒分散到背景溶液中,获得80 mg·L-1蒙脱石和50 mg·L-1高岭石悬浮液。柱实验中柱端流出的黏土胶粒浓度用一台紫外可见光分光光度计在线测量(Hitachi,U-2910日本)。通过对两种黏土胶粒的全波扫描,确定浓度测量的波长为230 nm。同时,预实验结果显示在230 nm处,只有黏土胶粒的光信号明显,而腐植酸和镉离子的信号接近背景溶液值,因此,共注射实验中,腐植酸和镉离子不会干扰黏土胶粒的光信号。预实验结果显示在230 nm波长,紫外可见光分光光度计的测试下限为0.5 mg·L-1,小于注射浓度的1%,而测试上限超过了注射浓度。黏土胶粒的粒径和Zeta电位用马尔文激光粒度仪(Malvern,Nano ZS英国)测定(结果见表 1),溶液条件为pH 7.1,支持电解质溶液为10 mmol·L-1的NaCl溶液。
|
|
表 1 黏土胶粒的粒径与电势 Table 1 Particle size and potential of clay particles |
腐植酸(HA)从Sigma Aldrich公司订购,硝酸镉从MACKLIN订购。腐植酸溶液和镉离子溶液用背景溶液配制,浓度分别为0.5 mg·L-1腐植酸和0.01 mg· L-1 Cd2+。实验中未测量柱端流出液中两种物质的含量。
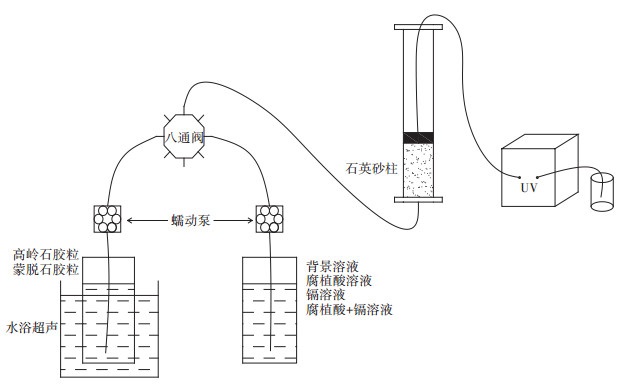
1.5 实验方法实验装置如图 1所示。石英砂柱在超声振动条件下通过湿灌法填实,以确保砂柱中没有气泡。砂柱直径为1 cm,长3 cm。在同步注射之前,用蠕动泵(保定雷弗流体科技有限公司,BT100F)按1 mL·min-1的流速注射背景液稳定实验系统30 min,使系统化学物理条件稳定。黏土胶粒进柱前均超声30 min,保证胶粒充分分散;注射实验过程中对注射黏土胶粒持续超声振动,确保粒径稳定。共注射时,每台泵的流速为0.5 mL·min-1(两台泵注射总流速为1 mL·min-1),分别同步注射黏土胶粒和腐植酸、Cd2+或腐植酸+Cd2+混合液15 min,然后继续注射背景液冲洗柱9 min结束。通过八通阀调节注射顺序。砂柱流出液中黏土胶粒浓度通过紫外可见光光度计在线连续测量。
|
图 1 柱实验装置图 Figure 1 Column experimental setup |
表 1汇总了高岭石和蒙脱石黏土胶粒在背景盐溶液、腐植酸溶液和Cd2+溶液中的粒径和Zeta电位。在背景溶液中,两种黏土胶粒粒径均在1200~1300 nm之间,粒径差小于5%。两种黏土胶粒表面总体显负电性,高岭石的Zeta电位绝对值为蒙脱石的两倍。蒙脱石和高岭石都具有阳离子交换能力,其表面带负电的点位能通过静电吸附作用吸附溶液中的钠离子和其他阳离子;相比而言,蒙脱石(2:1型层状硅酸盐矿物)的阳离子交换容量为90~150 cmol(+)·kg-1,远大于高岭石(1:1型层状硅酸盐矿物,3.3 cmol(+)·kg-1)[14]。因此,蒙脱石表面能吸附更多的钠离子,使Zeta电位绝对值低于高岭石。
黏土胶粒与腐植酸混合后粒径与Zeta电位均变化。高岭石粒径从1200 nm增长到约2300 nm,而蒙脱石粒径略有下降,表明腐植酸促使高岭石胶粒发生了聚凝。Zeta电位测量结果显示与腐植酸混合后,蒙脱石和高岭石的Zeta电位分别从-23.5 mV和-43.2 mV降到-25.1 mV和-43.7 mV,表明腐植酸带负电,并通过在黏土胶粒上的吸附,增加了黏土胶粒的负电性。腐植酸由于含有羧基,在中性pH条件下通常显负电性[15]。而高岭石和蒙脱石虽然总体显负电性,但其端面(Edge side)由于质子化(Protonation)可带正电[16-17],且这些端面对于黏土胶粒在环境界面上的吸附与迁移具有重要控制作用。因此,腐植酸有可能吸附在黏土胶粒端面。由于结构不同,高岭石的端面面积与平面面积之比大于蒙脱石[18],可促使更多的腐植酸吸附。这些有机聚合物可能通过键桥作用使高岭石发生聚凝;吸附在高岭石胶粒上的腐植酸还会改变高岭土的理化性质,使原本亲水的胶粒表面具有一定的疏水性,进一步促使高岭石聚凝[19]。
黏土胶粒与Cd2+混合也导致粒径与Zeta电位变化。高岭石和蒙脱石的粒径分别增长了约73%和40%,表明Cd2+能促使高岭石和蒙脱石聚凝。这是因为Cd2+为二价阳离子,可通过阳离子键桥作用连接黏土胶粒,引起其聚凝而粒径增大[20-21](粒径数据见表 1)。黏土胶粒与腐植酸和Cd2+混合后,粒径增长幅度大于与腐植酸或Cd2+单独混合:高岭石胶粒粒径增长105%,而蒙脱石粒径增长47%。这表明腐植酸和Cd2+对黏土胶粒聚凝的作用效果有一定的协同性。高岭石胶粒和蒙脱石胶粒与腐植酸和Cd2+的混合物共存时,Zeta电位的绝对值低于仅有腐植酸存在的情况(-43.6 mV vs -43.7 mV;-24.6 mV vs -25.1 mV),可能是由于Cd2+与腐植酸形成化学键,消耗了部分腐植酸,从而使腐植酸在黏土胶粒端面的吸附量减弱。
2.2 黏土胶粒与腐植酸和镉离子的共迁移图 2总结了高岭石胶粒(图 2a)和蒙脱石胶粒(图 2b)在背景溶液、Cd2+溶液、腐植酸溶液以及Cd2+与腐植酸的混合溶液中迁移的实验结果。穿透曲线展示了柱端流出的黏土胶粒浓度随时间的变化规律,流出浓度越高表明黏土胶粒在砂柱中的沉降速度越低,移动性越强。基于穿透曲线,可通过公式1[22]计算黏土胶粒的沉降速度。表 2汇总了计算结果。
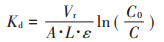
|
(1) |
|
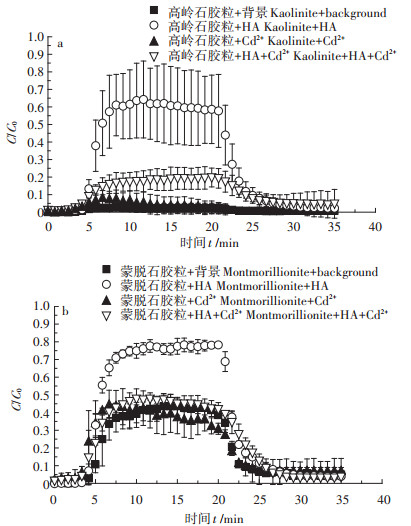
图 2 高岭石胶粒(a)和蒙脱石胶粒(b)在不同环境条件中迁移的穿透曲线 Figure 2 The breakthrough curves of kaolinite (a) and montmorillionite (b) colloids under different environmental conditions |
|
|
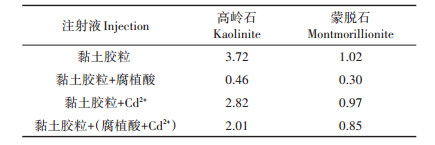
表 2 柱实验中黏土胶粒的沉降速度(min-1) Table 2 Sedimentation speed of clay particles in column experiment (min-1) |
式中:Kd为沉降速度,min-1;Vr为流体流速,mL·min-1;A为砂柱横截面积,cm2;L为砂柱长度,3 cm;ε为砂柱孔隙度,%;C/C0为穿透曲线拐点处的值,%。
由图 2a可见,高岭石胶粒的穿透曲线平台高度在无Cd2+或腐植酸的背景溶液中最低(0.03),在腐植酸溶液中最高(0.65),在Cd2+溶液中略高于在背景溶液中;而当腐植酸和Cd2+共存时,高岭石胶粒的穿透高度高于Cd2+单独存在的实验,而低于腐植酸溶液单独存在的实验。表 2计算结果显示,腐植酸与高岭石胶粒共迁移时黏土胶粒的沉降速度仅为黏土胶粒单独迁移时的12%(0.46/3.72),表明腐植酸显著提升了高岭石胶粒的移动性。Cd2+的存在,使高岭石胶粒的沉降速度从3.72 min-1降低到2.82 min-1,说明Cd2+对高岭石黏土胶粒的移动性也具有一定的促进作用,但不如腐植酸的效果显著。有趣的是,当Cd2+与腐植酸共存时,黏土胶粒的移动性介于这两种物质单独作用之间,沉降速度为2.01 min-1,表明移动性高于Cd2+单独作用,低于腐植酸单独作用。这说明Cd2+和腐植酸对于高岭石黏土胶粒的作用具有一定的拮抗性。
由图 2b可见,蒙脱石胶粒的穿透曲线平台在背景溶液中达到0.38左右,对应的沉降速度Kd为1.02 min-1,显著低于高岭石胶粒在背景溶液中的沉降速度(3.72 min-1),说明蒙脱石胶粒在石英砂柱中的迁移能力比高岭石胶粒更强。腐植酸的存在显著提高了蒙脱石穿透平台的高度,达到0.75左右,使沉降速度降到0.30 min-1,明显高于Cd2+对蒙脱石移动性的促进作用。后者使蒙脱石的沉降速度降低到0.97 min-1,与蒙脱石在背景溶液中的沉降速度接近。腐植酸与Cd2+共存时,蒙脱石胶粒的穿透曲线平台介于两种物质单独作用实验的曲线平台之间,表明Cd2+和腐植酸对于蒙脱石黏土胶粒的作用具有一定的拮抗性。这些结果表明腐植酸和Cd2+对蒙脱石和高岭石胶粒的迁移效果比较一致,可总结为:(1)腐植酸与Cd2+均能促进两种黏土胶粒的迁移,促进作用腐植酸最强而镉离子的作用较弱;(2)腐植酸和Cd2+之间存在拮抗作用,即二者的加合作用反而小于腐植酸单独作用。
虽然在实验条件(pH 7.1)下,高岭石和蒙脱石黏土胶粒与石英砂均显负电性(见表 1),但两种黏土胶粒均能在石英砂面沉降;此外,高岭石表面负电位高于蒙脱石,而高岭石沉积量显著(约97%),远大于蒙脱石(约75%)。这一现象无法用传统的DLVO理论解释。根据过滤理论,胶粒粒径也会影响其沉降速度:弥散是控制胶体沉降的主要机制并随粒径增大而减小[23],但在背景溶液中,两种胶粒粒径均在1250 nm左右,差别不显著,所以不是造成这一沉降差异的原因。Missand等[24]也发现DLVO理论不能描述黏土胶粒的界面行为,并指出这是由于电荷非均匀地分布在黏土胶粒层间和端面(Edge side),与DLVO理论的基本假设不一致造成的。在我们的实验中,虽然两种黏土胶粒总体都显负电性,但其端面由于质子化(Protonation)而带正电[16-17]。因此,黏土胶粒在石英砂面的吸附沉降应该是通过带正电的端面与带负电的石英砂面之间的静电吸附作用。高岭石的端面面积与平面面积之比大于蒙脱石[18, 25],因而能为其沉降提供更多吸附点位,导致高岭石比蒙脱石更容易在石英砂面吸附。前面的分析显示腐植酸带负电,并能吸附到黏土胶粒表面,增加其负电性。这与已发表的研究结果一致:腐植酸通过表面羧基的去质子而带负电[26],并通过静电吸附作用吸附在蒙脱石和高岭石端面[27]。由于蒙脱石和高岭石通过端面吸附在砂面上,因此,腐植酸对端面吸附点位的占据,降低了黏土胶粒的沉降速度。通过上节分析,Cd2+作为二价阳离子,可通过阳离子键桥作用连接黏土胶粒,引起其聚凝而粒径增大(粒径数据见表 1)。根据Elimelech等[23]研究,胶粒粒径增大导致沉降速度降低,胶粒移动性增强。此外,由于Cd2+与胶粒端面带同种电荷,因此难以像腐植酸那样吸附并改变胶粒端面的电性。由于端面是黏土胶粒在砂面吸附的主要点位,因此,Cd2+对蒙脱石和高岭石胶粒的移动性的促进效果并不显著。当Cd2+和腐植酸共存时对黏土胶粒迁移的促进作用小于腐植酸单独作用。基于上一节分析,可能是由于Cd2+与腐植酸络合,消耗了部分腐植酸,从而减弱了黏土胶粒端面的腐植酸吸附量。相关研究也证实了Cd2+会与一部分腐植酸发生络合反应[28-29]。
3 结论(1)虽然高岭石和蒙脱石胶粒总体显负电性,但两种黏土胶粒均能通过端面吸附在带负电的石英砂面。且高岭石胶粒由于端面/总面积之比大于蒙脱石而吸附性更强,所以迁移能力相对蒙脱石较弱。这一结果表明,对于电荷分布异质化的黏土胶粒等天然胶体材料,其端面与环境界面的交互作用对其迁移过程起主导作用。用胶粒表面总体电势和传统的DLVO理论来预测黏土胶粒的迁移行为,会导致高估它们的移动性。
(2)腐植酸和Cd2+均能促进黏土胶粒迁移,但通过不同的机理:腐植酸通过吸附在黏土胶粒的端面,并改变端面的电性来抑制黏土胶粒的沉降,而Cd2+通过阳离子键桥作用使黏土胶粒聚凝,粒径增大来降低其沉降。相比而言,腐植酸的效果明显强于Cd2+。
(3)当腐植酸与Cd2+共存时,腐植酸的促进效应被削弱,表明腐植酸和Cd2+的交互作用具有一定的拮抗性。
| [1] |
Davis C H, Mathias L J, Gilman J W, et al. Effects of melt-processing conditions on the quality of poly (ethylene terephthalate) montmorillonite clay nanocomposites[J]. Journal of Polymer Science Part B Polymer Physics, 2002, 40(23): 2661-2666. DOI:10.1002/(ISSN)1099-0488 |
| [2] |
滕飞, 李福春, 吴志强, 等. 高岭石和蒙脱石吸附胡敏酸的对比研究[J]. 中国地质, 2009, 36(4): 892-898. TENG Fei, LI Fu-chun, WU Zhi-qiang, et al. Comparative study on adsorption of humic acid by kaolinite and montmorillonite[J]. Geology in China, 2009, 36(4): 892-898. DOI:10.3969/j.issn.1000-3657.2009.04.017 |
| [3] |
孙慧敏, 殷宪强, 曹秀蓉. 离子强度对蒙脱石胶体在饱和多孔介质中运移与释放的影响[J]. 环境科学学报, 2012, 32(5): 1120-1125. SUN Hui-min, YIN Xian-qiang, CAO Xiu-rong. Effect of ionic strength on migration and release of montmorillonite in saturated porous media[J]. Acta Scientiae Circumstantiae, 2012, 32(5): 1120-1125. |
| [4] |
孙慧敏.黏土矿物对铅的环境行为影响研究[D].杨凌: 西北农林科技大学, 2010. SUN Hui-min. Effect of clay minerals on environmental behavior of study[D]. Yangling: Northwest A&F University, 2010. |
| [5] |
胡俊栋, 沈亚婷, 王学军. 土壤胶体在不同饱和度土壤介质中的释放与淋溶行为研究[J]. 农业环境科学学报, 2009, 28(9): 1829-1836. HU Jun-dong, SHEN Ya-ting, WANG Xue-jun. The study on the release and leaching behavior of soil colloids in different saturated soil media[J]. Journal of Agro-Environment Science, 2009, 28(9): 1829-1836. DOI:10.3321/j.issn:1672-2043.2009.09.010 |
| [6] |
刘庆玲, 徐绍辉. 地下环境中胶体促使下的污染物运移研究进展[J]. 土壤, 2005(2): 129-135. LIU Qing-ling, XU Shao-hui. The research progress of pollutant migration in underground environment[J]. Soils, 2005(2): 129-135. DOI:10.3321/j.issn:0253-9829.2005.02.003 |
| [7] |
孙慧敏, 殷宪强, 王益权. pH对黏土矿物胶体在饱和多孔介质中运移的影响[J]. 环境科学学报, 2012, 32(2): 419-424. SUN Hui-min, YIN Xian-qiang, WANG Yi-quan. The influence of pH on the migration of clay mineral colloids in saturated porous media[J]. Acta Sicentiae Circumstantiae, 2012, 32(2): 419-424. |
| [8] |
杨悦锁, 王园园, 宋晓明, 等. 土壤和地下水环境中胶体与污染物共迁移研究进展[J]. 化工学报, 2017, 68(1): 23-36. YANG Yue-suo, WANG Yuan-yuan, SONG Xiao-ming, et al. Advances in the study of colloid and pollutant in soil and groundwater environment[J]. CIESC Journal, 2017, 68(1): 23-36. |
| [9] |
Patricia M, Carolina M, Alejandro C C. Cd(Ⅱ) removal from aqueous solution by Eleocharis acicularis biomass, equilibrium and kinetic studies[J]. Bioresource Technology, 2010, 101(8): 2637-2642. DOI:10.1016/j.biortech.2009.10.067 |
| [10] |
李婧, 周艳文, 陈森, 等. 我国土壤镉污染现状、危害及其治理方法综述[J]. 安徽农学通报, 2015, 21(24): 104-107. LI Jing, ZHOU Yan-wen, CHEN Sen, et al. The present situation, harm and treatment of soil cadmium pollution in China are reviewed[J]. Anhui Agricultural Science Bulletin, 2015, 21(24): 104-107. DOI:10.3969/j.issn.1007-7731.2015.24.044 |
| [11] |
Duan J C, Tan J H, Hao J M, et al. Size distribution characteristics and sources of heavy metals in haze episod in Beijing[J]. Journl of Environmental Sciences, 2014, 26(1): 189-196. DOI:10.1016/S1001-0742(13)60397-6 |
| [12] |
Xu S P, Qian L, Saiers J E. Straining of non-spherical colloids in saturated porous media[J]. Environmental Science & Technology, 2008, 42(3): 771-778. |
| [13] |
Yang X, Yin Z, Chen F, et al. Organic matter induced mobilization of polymer-coated silver nanoparticles from water-saturated sand[J]. Science of the Total Environment, 2015, 529: 182-190. DOI:10.1016/j.scitotenv.2015.05.066 |
| [14] |
Aksu I, Bazilevskaya E, Karpyn Z T. Swelling of clay minerals in unconsolidated porous media and its impact on permeability[J]. Georesj, 2015, 7: 1-13. DOI:10.1016/j.grj.2015.02.003 |
| [15] |
Yang X, Flynn R, Kammer F V D, et al. Quantifying the influence of humic acid adsorption on colloidal microsphere deposition onto ironoxide-coated sand[J]. Environmental Pollution, 2010, 158(12): 3498-3506. DOI:10.1016/j.envpol.2010.03.011 |
| [16] |
Gao B, Saiers J E, Ryan J N. Deposition and mobilization of clay colloids in unsaturated porous media[J]. Water Resources Research, 2004, 40(8): 10-1029. |
| [17] |
Shen C, Wang H, Lazouskaya V, et al. Cotransport of bismerthiazol and montmorillonite colloids in saturated porous media[J]. Journal of Contaminant Hydrology, 2015, 177-178: 18. DOI:10.1016/j.jconhyd.2015.03.003 |
| [18] |
Cai P, Huang Q Y, Zhang X W. Interactions of DNA with clay minerals and soil colloidal particles and protection against degradation by DNase[J]. Environmental Science & Technology, 2006, 40(9): 2971. |
| [19] |
魏世勇, 谭文峰, 刘凡. 土壤腐殖质-矿物质交互作用的机制及研究进展[J]. 中国土壤与肥料, 2009(1): 1-6. WEI Shi -yong, TAN Wen-feng, LIU Fan. Mechanism and research progress of soil humus-mineral interaction[J]. Soil and Fertilizer Sciences, 2009(1): 1-6. DOI:10.3969/j.issn.1673-6257.2009.01.001 |
| [20] |
吴宏海, 刘佩红, 张秋云, 等. 高岭石对重金属离子的吸附机理及其溶液的pH条件[J]. 高校地质学报, 2005, 11(1): 85-91. WU Hong-hai, LIU Pei-hong, ZHANG Qiu-yun, et al. The adsorption mechanism of kaolinite on heavy metal ions and their pH conditions[J]. Geological Journal of China Universities, 2005, 11(1): 85-91. DOI:10.3969/j.issn.1006-7493.2005.01.007 |
| [21] |
Angove M J, Johnson B B, Wells J D. Adsorption of cadmium (Ⅱ) on kaolinite[J]. Colloids & Surfaces A Physicochemical & Engineering Aspects, 1997, 126(2): 137-147. |
| [22] |
Wang C, Bobba A D, Attinti R, et al. Retention and transport of silica nanoparticles in saturated porous media:Effect of concentration and particle size[J]. Environmental Science & Technology, 2012, 46(46): 7151-7158. |
| [23] |
Elimelech M, Gregory J, Jia X, et al. Particle deposition and aggregation[M]. 1995.
|
| [24] |
Missana T, Adell A. On the applicability of DLVO theory to the prediction of clay colloids stability[J]. J Colloid Interface Sci, 2000, 230(1): 150-156. DOI:10.1006/jcis.2000.7003 |
| [25] |
Tombácz E, Szekeres M. Surface charge heterogeneity of kaolinite in aqueous suspension in comparison with montmorillonite[J]. Applied Clay Science, 2006, 34(1): 105-124. |
| [26] |
朱晓婧, 何江涛. 腐植酸-高岭土复合体形成机制及对三氯乙烯的吸附[J]. 环境科学, 2015(1): 227-236. ZHU Xiao-jing, HE Jiang-tao. Formation mechanism of humic acidkaolin complex and adsorption of trichloroethylene[J]. Environmental Science, 2015(1): 227-236. |
| [27] |
李爱民.腐植酸在高岭石上的吸附及其对Cu (Ⅱ)在高岭石上吸附的影响[D].南京: 南京农业大学, 2006. LI Ai-min. Adsorption of humic acid on kaolinite and the Cu (Ⅱ) adsorbed on kaolinite[D]. Nanjing: Nanjing Agricultural University, 2006. |
| [28] |
滕飞.黏土矿物及黏土矿物-胡敏酸复合体对Cd2+吸附及对Cd2+和Pb2+的选择性[D].南京: 南京农业大学, 2009. TENG Fei. Clay minerals and clay mineral-humic acid complex on Cd adsorption and the selection of Cd and Pb[D]. Nanjing: Nanjing Agricultural University, 2009. |
| [29] |
何为红, 李福春, 吴志强, 等. 重金属离子在胡敏酸-高岭石复合体上的吸附[J]. 岩石矿物学杂志, 2007, 26(4): 67-73. HE Wei-hong, LI Fu-chun, WU Zhi-qiang, et al. Adsorption of heavy metal ions on the complex of humic acid-kaolinite[J]. ACTA Petrologica et Mineralogica, 2007, 26(4): 67-73. |
 2019, Vol. 38
2019, Vol. 38