2. 中国科学院水利部成都山地灾害与环境研究所, 山地表生过程与生态调控重点实验室, 成都 610000;
3. 重庆工商大学旅游与国土资源学院, 重庆 400067;
4. 生态环境空间信息数据挖掘与大数据集成重庆市重点实验室, 重庆 400067
2. Key Laboratory of Mountain Surface Biological Processes and Ecological Regulation, Institute of Mountain Hazards and Environment, China Acadmey of Sciences, Chengdu 610000, China;
3. College of Tourism and Land Resources, Chongqing Technology and Business University, Chongqing 400067, China;
4. Chongqing Key Laboratory of Spatial Data Mining and Big Data Integration for Ecology and Environment, Chongqing 400067, China
三峡库区位于坝址湖北宜昌至库尾重庆江津之间,地形总体以起伏山地为主,人口密度高,是长江上游最主要的生态脆弱和敏感区之一[1-2]。三峡库区消落带是因三峡水库调度在水库干流和支流回水区形成的水位反季节涨落的水陆交错带,其长度为660 km,最高水位落差达到30 m,最大出露面积约349 km2[3]。已有研究表明[4-6],库区生产生活活动排放的污染物以及水库上游来水和泥沙携带的污染物的沉降导致三峡库区消落带土壤重金属污染问题日益严重,尤以镉(Cd)污染极为突出。此外,库区蓄水期,长江干流的中层水体可以携带大量水溶态或颗粒物结合态重金属随干流倒灌进入支流上游[7],可能增加支流库湾消落带土壤对重金属的吸附和富集。2010年库区以最高水位(175 m)蓄水以来,干流和支流消落带土壤中Cd呈现富集的趋势,磷肥施用是Cd的主要来源,导致消落带土壤中Cd的最大潜在生态风险指数(Ei)高达819.23,具有最高生态风险[4-5]。而不同高程的消落带由于淹水时长和排干时长的不同,可能产生较大的理化性质差异,从而影响Cd在不同高程消落带土壤中的吸附和富集。
近年来,畜禽养殖业已成为库区农业的主要成分和农户的主要经济来源之一[8-9]。雨季畜禽粪便的不合理堆放或直接还田对库区坡耕地农业面源污染有重要贡献[10-11]。溶解性有机质(Dissolved organic matter,DOM)是猪粪有机质中最活跃的组分,含有羟基、羧基、羰基等多种活性官能团。这些官能团可能与重金属发生配位、络合、共吸附或沉降等反应,进而影响重金属在土壤表面的吸附[12-13]。
目前文献中并未见外源DOM对三峡库区消落带土壤中Cd吸附特征影响的报道。而仅有的相关文献仅探索了土壤自身性质如pH和土壤有机质(SOM)对消落带土壤吸附Cd的影响,并未考虑不同淹水时长的消落带土壤吸附Cd的差异[14-16]。因此,本文选取三峡库区消落带不同高程(151、160 m)土壤为对象,对比非消落带(> 175 m)土壤,研究淹水时长差异导致的消落带土壤内在理化性质变化对土壤吸附Cd的影响,同时探索外源(猪粪)DOM引入造成的土壤吸附Cd的差异及其机理,以期为“后三峡”时代不同来源(如畜禽粪便、生活污水/污泥)有机质存在情况下消落带土壤中重金属向库区水体迁移的研究提供参考。
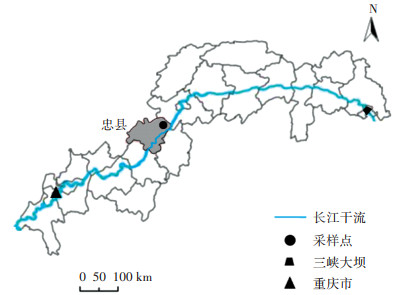
1 材料与方法 1.1 试验材料 1.1.1 土样的采集与处理忠县坪山小流域消落带,处于三峡库区腹地,是长江的支流库湾,属于典型的农业消落带与回水区消落带,见图 1。
|
图 1 采样点位置图 Figure 1 Location of the sampling site |
消落带内选择两个采样梯度,分别采集高程151 m(淹水时长约300 d·a-1)和160 m(淹水时长约220 d·a-1)[17]台地的土壤。每个高程随机选取5个采样点,采样深度为0~20 cm,混合样作为该台地的土壤样品;以相同方法采集非消落带(177 m,未经淹水)土壤。另外,再采集3个不同高程台地相应环刀(D:5 cm;H:5 cm)样品用于容重测试。土样保存于密封袋,在实验室经风干、剔除植物根、砂砾等杂物的处理,并研磨过筛(100目),保存于密封袋中备用。
1.1.2 猪粪DOM的采集与制备供试猪粪采自川中丘陵区绵阳市盐亭县林山乡养猪场。新鲜猪粪样品经30 min初级离心(4 000 r·min-1),分离获取的上清液经30 min二次超高速冷冻离心(15 000 r·min-1),最后分离得到的上清液立即用0.45 μm无菌微孔滤膜抽气过滤,滤液经冷冻干燥得到猪粪DOM样品,冷冻保存。
1.2 研究方法 1.2.1 土壤理化性质分析及猪粪源DOM组分分析测定供试土壤的pH、CEC、容重、孔隙度、有机质(SOM)及机械组成同Cui等[18]的研究,滤液中总Cd浓度通过电感耦合等离子体质谱(ICP - MS,NexlONTM300,USA)测定,此外,利用傅里叶变换红外光谱(FTIR,Nicolet iS50,USA)对猪粪源DOM进行组分分析。
1.2.2 吸附动力学试验为探索淹水时长对土壤吸附Cd动力学特征的影响,以177 m非消落带台地土壤为对照,消落带(151 m和160 m)土壤为试验组进行吸附动力学试验。各自称取1 g供试土壤,置于50 mL离心管中,按照水土比10:1,加入0.01 mol·L-1 CaCl2溶液和Cd2+浓度为30 mg·L-1的CdCl2溶液,将样品放置于25 ℃恒温振荡器中连续振荡(180 r·min-1),振荡时间分别为0.5、2、4、8、12、24 h和48 h。振荡后样品经离心(4 000 r·min-1,10 min)、过滤(0.45 μm PTFE滤膜),测定滤液中Cd含量。
1.2.3 等温吸附试验称取2 g供试土壤,置于50 mL离心管中,按照水土比10:1(V/m),加入0.01 mol·L-1CaCl2溶液和不同浓度的CdCl2溶液,CdCl2溶液中Cd2+的浓度梯度分别为5、15、30、50 mg·L-1和75 mg·L-1。将样品放置于25 ℃恒温振荡器(ZWF-200,上海智城分析仪器)中连续振荡(180 r·min-1)至吸附平衡(24 h,依据吸附动力学结果),振荡结束后的过滤、离心及Cd浓度测定方法同1.2.1。
1.2.4 猪粪源DOM对土壤吸附Cd的影响试验在以上两个试验基础上分别考虑猪粪DOM添加对土壤吸附Cd的影响。对于吸附动力学试验,猪粪DOM溶液(30 mg C·L-1,含0.1 g·L-1的NaN3以抑制微生物对DOM的降解)与CdCl2溶液一同加入CaCl2溶液中,其余步骤同1.2.2。对于等温吸附试验,猪粪DOM溶液与CdCl2溶液一同加入CaCl2溶液中,DOM添加浓度为30 mg C·L-1。此外,对比DOM不同初始添加浓度对土壤吸附Cd的影响,CdCl2溶液中Cd2+浓度为30 mg·L-1,DOM浓度梯度分别为10、30、50、70 mg C·L-1和100 mg C·L-1。其余步骤同1.2.3。
1.3 模型计算本研究采用文献中常用的重金属吸附动力学模型和等温吸附模型拟合试验结果。准一级动力学模型和Elovich动力学模型表达式分别为公式(1)和公式(2):
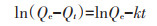
|
(1) |
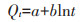
|
(2) |
式中:Qe和Qt分别为吸附平衡和t时刻土壤对Cd的吸附量,mg·kg-1;k为准一级动力学常数,a和b均为Elovich模型常数。
Langmuir模型和Freundlich模型的表达式分别为公式(3)和公式(4):
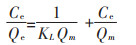
|
(3) |
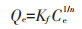
|
(4) |
式中:Ce为土壤对Cd的平衡吸附量,mg·kg-1;Qm为土壤对Cd的最大吸附量,mg·kg-1;KL表示Langmuir吸附系数。Freundlich吸附常数Kf代表吸附容量,其值越大,吸附速率越快;1/n反映吸附的非线性程度。其余参数同上。
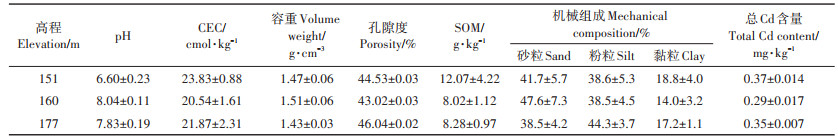
2 结果与讨论 2.1 土壤理化性质及猪粪源DOM的特性非消落带(177 m)土壤呈弱碱性,pH为7.83± 0.19,中部(160 m)土壤碱性有所增强(pH=8.04 ± 0.11),消落带下部(151 m)土壤呈中性(pH=6.60 ± 0.23)。已有研究[19]报道了淹水导致消落带土壤pH随高程降低(淹水时长增加)而增加,为厌氧环境下还原性碳酸铁、锰的积累所致。本研究中消落带下部土壤pH的降低可归因于长期淹水下土壤或植被残体中有机酸的积累。不同高程间土壤的阳离子交换量(CEC)、容重及孔隙度均不存在显著性差异(P > 0.05),但消落带土壤容重高于非消落带土壤,表明周期性淹水-排干的交替作用导致土壤总孔隙度减小。消落带下部SOM含量显著(P < 0.05)高于中部消落带或非消落带的土壤,主要原因为该高程长时间淹水厌氧环境下SOM分解缓慢。消落带和非消落带土壤均以砂粒和粉粒为主,但消落带土壤的砂粒含量稍高于非消落带土壤,可能由上层非消落带坡耕地表土侵蚀的泥沙堆积所致,不同高程间土壤黏粒含量没有显著性差异(P > 0.05),库区土壤中Cd含量均高于重庆市土壤Cd自然背景值(0.084 mg·kg-1)[20],表明人类活动影响导致土壤中Cd的富集。非消落带177 m和消落带160 m高程的土壤Cd含量均低于我国农用地土壤污染风险值(0.6 mg·kg-1,pH > 7.5),而消落带151 m高程土壤Cd含量(0.37±0.014 mg·kg-1)高于相应风险值(0.3 mg·kg-1,6.5 < pH≤7.5)[21]。
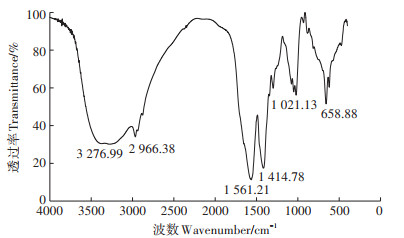
猪粪源DOM的FTIR分析结果如图 2所示。在3277、2966、1561、1415、1021 cm-1以及659 cm-1处,DOM出现不同的吸收峰。根据Bekiaris等[22]和Kim等[23]的图谱解析,3500~3250 cm-1宽吸收带表明DOM中富含-OH和-COOH官能团。2966 cm-1处的吸收峰表明DOM中脂肪族CH3和CH2的C-H对称伸缩振动的存在。1561 cm-1处吸收峰表明胺基-N-H振动的存在。1400~1420 cm-1区域内的吸收峰表明DOM中存在C=O伸缩振动。1020 cm-1附近的吸收峰表明DOM中存在C-O不对称伸缩振动。660 cm-1附近的吸收峰表明DOM羧基中-OH的弯曲变形振动。
|
图 2 猪粪源DOM的傅里叶红外图谱 Figure 2 FTIR spectra of manure-DOM |
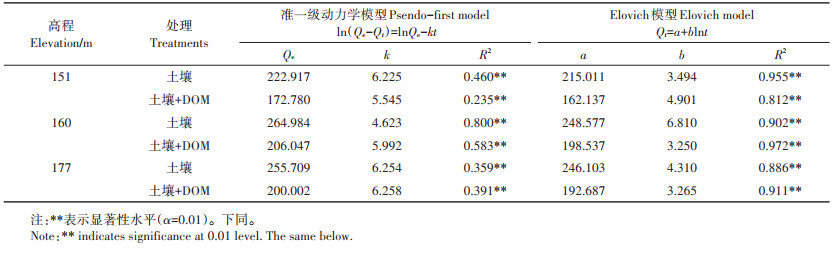
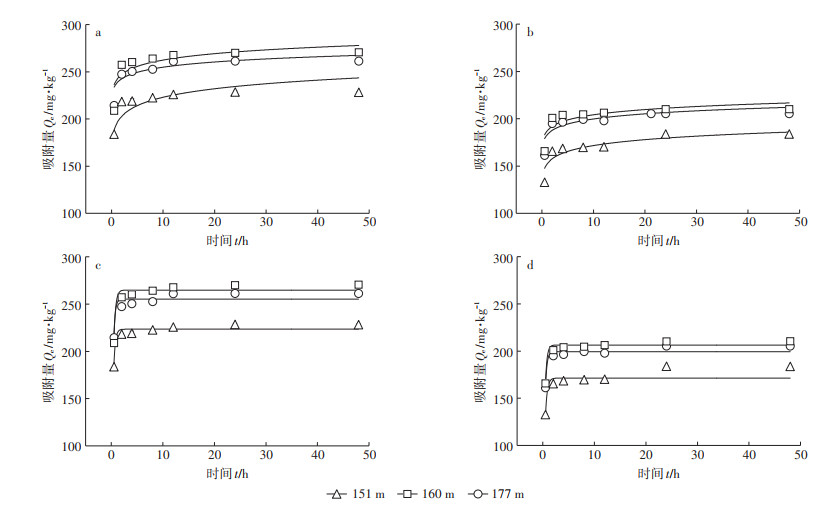
图 3(a)、图 3(c)分别展示了准一级动力学吸附模型和Elovich模型对库区土壤吸附Cd动力学的拟合结果。两种模型均能有效模拟土壤对Cd的动态吸附过程,但Elovich模型的拟合效果明显优于准一级动力学吸附模型,前者拟合优度(0.886 < R2 < 0.955)远高于后者(0.359 < R2 < 0.800)(表 2)。相关文献[24-25]同样报道了Elovich模型能较好地拟合Cd的吸附动力学特征。Elovich方程假定吸附剂表面的活性吸附点位是非均质的且适用于描述化学吸附行为[26]。因此,三峡库区消落带和非消落带土壤对Cd的吸附为非均质的化学吸附。吸附的非均质性同时还体现在Cd的阶段性吸附特征上。从图 3(a)、图 3(c)可以看出,3个高程土壤对Cd的吸附分为明显的快速吸附(0~2 h)和慢速吸附阶段,吸附平衡时间为24 h。短时间的快速吸附阶段主要归因于土壤表面大量存在的可利用的活性吸附点位。而慢速吸附至平衡阶段,吸附速率缓慢且吸附量没有显著变化。其他学者也报道了类似的现象[25, 27]。
|
a.未添加DOM条件下Cd2+的准一级动力学模型拟合;b.添加DOM条件下Cd2+的准一级动力学模型拟合;c.未添加DOM条件下Cd2+的Elovich模型拟合;d.添加DOM条件下Cd2+的Elovich模型拟合 a.Psendo-first model fitting of Cd2+ without DOM added; b.Pseudo-first model fitting of Cd2+ with DOM; c.Elovich model fitting of Cd2+ without DOM added; d.Elovich model fitting of Cd2+ with DOM 图 3 有无猪粪DOM添加下库区土壤对Cd的吸附动力学过程及其模型拟合 Figure 3 Sorption kinetics and curve fitting of Cd to soils in the presence and absence of manure-DOM |
|
|
表 2 3个高程土壤吸附Cd的动力学拟合结果 Table 2 Kinetic fitting results of Cd adsorption to soils from 3 altitudes |
从Elovich模型的斜率(b)和截距(a)以及准一级动力学模型的Qe(表 2)可以看出,梯度上库区土壤对Cd的平衡吸附量:消落带160 m > 非消落带177 m > 消落带151 m,与土壤pH的变化规律一致但与CEC和土壤有机质含量的变化相反。对于碱性土壤(如消落带160 m,pH=8.04±0.11),因H+浓度降低,金属氧化物(如铁铝氧化物)可能因去质子化而增加土壤矿物表面负电荷[28],进而提高碱性土壤对Cd2+的静电吸附能力。此外,碱性环境可能促进Cd2+水解形成CdOH+[14],而CdOH+相对于自由态Cd2+更容易在土壤表面形成金属络合物而被吸附固持。Wong等[29]与Li等[30]的控制试验证明了不同土壤对Cd的吸附能力随着pH的增加而增大,而Lair等[31]的研究也表明在不同土壤管理措施下,土壤pH是控制重金属(Cd、Cu及Zn)吸附的主要因素。虽有文献证实CEC可能通过阳离子交换作用[32]、黏粒或黏土矿物含量可能通过表面电化学性质促进土壤对Cd的吸附[33-34],但消落带和非消落带土壤CEC、黏粒(表 1)、黏土矿物[18]含量的差异不显著(P > 0.05),从而无法判断其是否为影响Cd吸附的有效因素。消落带下部(151 m)土壤中虽然SOM含量显著高于(P < 0.05)中部及非消落带土壤,但Elovich模型的斜率(b)和截距(a)以及准一级动力学模型的Qe值却相对最小。一方面,就重金属的吸附而言,SOM的组分或表面性质比SOM的含量更重要[35-36],151 m台地土壤中SOM可能缺乏能有效络合Cd2+的表面基团。另一方面,151 m台地土壤中性偏弱酸,增加的H+可能与Cd2+竞争SOM表面吸附点位,也可能导致SOM表面基团的质子化从而减少对Cd2+的吸附。因此,土壤pH是影响三峡库区消落带土壤吸附Cd2+的最重要内在因子。
|
|
表 1 坪山消落带土壤(0~20 cm)基本理化性质 Table 1 Physiochemical properties of soils at Pingshan site |
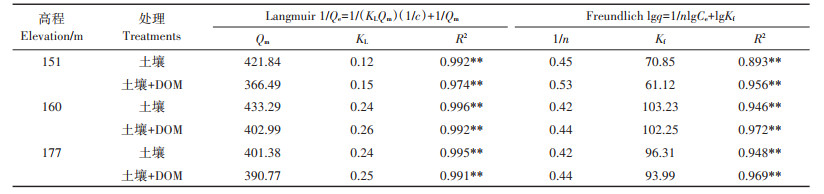
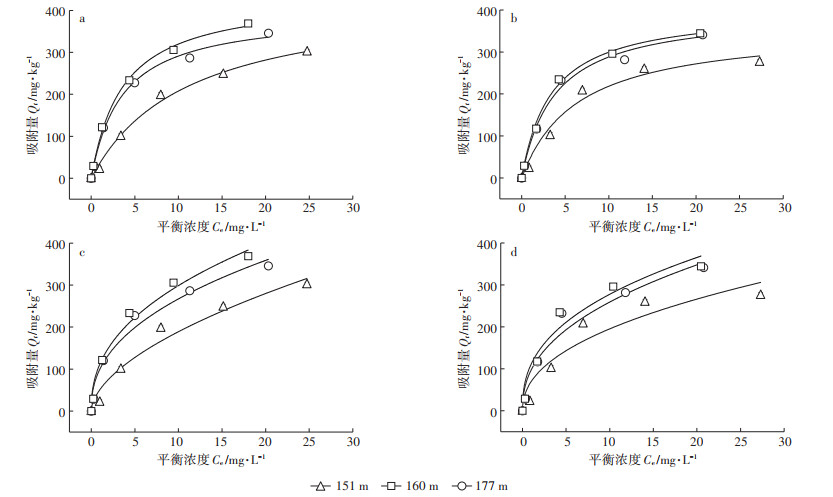
由图 4可以看出,随着平衡溶液中Cd2+浓度增加,土壤对Cd的吸附量非线性地增加且增加速率(斜率)逐渐减小。因此,库区土壤对Cd的吸附等温线为“L”型等温线,与Wong等[29]的研究结果类似。表 3列出了Langmuir模型和Freundlich模型对Cd吸附等温线的拟合结果。两个模型均能较好地拟合库区土壤对Cd的等温吸附情况(R2 > 0.89)。相比之下,Langmuir模型的拟合效果(0.992 < R2 < 0.996)稍好于Freun⁃ dlich模型(0.893 < R2 < 0.948),表明土壤对Cd的吸附可能为单层吸附[25]。
|
a.未添加DOM条件下Cd2+的Langmuir模型拟合;b.添加DOM条件下Cd2+的Langmuir模型拟合;c.未添加DOM条件下Cd2+的Freundlich模型拟合;d.添加DOM条件下Cd2+的Freundlich模型拟合 a.Langmuir model fitting of Cd2+ without DOM added; b.Langmuir model fitting of Cd2+ with DOM; c.Langmuir model fitting of Cd2+ without DOM added; d.Freundlich model fitting of Cd2+ with DOM 图 4 有无猪粪DOM添加下Cd的吸附等温模型 Figure 4 Sorption isotherms of Cd in the presence and absence of manure-DOM |
|
|
表 3 土壤Cd吸附的Langmuir及Freundlich方程的拟合结果 Table 3 Parameters of Langmuir and Freundlich equations for Cd sorption in the presence and absence of manure-DOM |
依据Langmuir模型,梯度上库区土壤对Cd的吸附亲和力(KL表征):消落带160 m(KL=0.244) > 非消落带177 m(KL=0.236) > 消落带151 m(KL=0.115),与吸附动力学的结果一致。而最大吸附量:消落带160 m(Qm=433.29 mg·kg-1) > 消落带151 m(Qm=421.84 mg· kg-1) > 非消落带177 m(Qm=401.38 mg·kg-1),与吸附动力学的结果不完全一致,可能原因为本研究中动力学吸附过程并未达到最大吸附。在Freundlich模型中,Kf与吸附容量正相关,由大到小为消落带160 m(Kf=103.23) > 非消落带177 m(Kf=96.31) > 消落带151 m(Kf=70.85),与KL及吸附动力学结果一致。因此,不同淹水时长引起的消落带土壤理化性质的差异导致消落带土壤对Cd的吸附容量具有较大的空间异质性。1/n是衡量Freundlich吸附等温线非线性的指标[31]。由表 3可知,不同土壤对Cd吸附的1/n值均远小于1,表明库区土壤对Cd的吸附呈强烈的非线性或表面异质性特征。可能的原因在于,在土壤吸附Cd的过程中,土壤表面能量较高的吸附点位优先吸附Cd,而能量较低的点位对Cd的吸附亲和力较小且吸附速率较低。其他学者也报道过类似的结果[28]。
2.4 猪粪源DOM对消落带土壤吸附Cd的影响猪粪源DOM的添加(30 mg C·L-1)极大提高了土壤平衡溶液中有机质的水平,177、160 m及151 m台地土壤平衡溶液中溶解性有机碳(DOC)的浓度分别增加了252%、366%及236%。猪粪源DOM的添加对库区土壤吸附Cd的动力学特征和吸附等温线的影响分别如图 3(b)、图 3(d)和图 4(b)、图 4(d)及表 2、表 3所示。猪粪DOM加入后,非消落带和消落带土壤对Cd的动态吸附过程如吸附速率和平衡时间并未产生显著影响,但准一级动力学模型的Qe值和Elovich模型的a值均大幅度降低,表明猪粪DOM的添加能有效减少Cd在库区土壤上的饱和吸附量。类似地,添加猪粪DOM后,177、160 m及151 m高程土壤对Cd的最大吸附量(Qm,表 3)分别减少2.6%、7.0%和13.1%。FTIR的结果表明猪粪源DOM富含羟基(-OH)、羧基(-COOH)及羰基(C=O)等具有较高反应活性的官能团,因此,猪粪源DOM加入消落带土壤后,平衡溶液中存在的自由态猪粪DOM分子中这些活性官能团可能与Cd2+发生络合或配位反应[37],形成含Cd的螯合物,从而减少Cd2+被土壤颗粒吸附。研究表明[38-39],重金属-DOM络合物的稳定性远高于重金属-土壤矿物络合物的稳定性。因而,在猪粪DOM存在的情况下,库区土壤对Cd的吸附量总体减少。类似地,其他研究证实不同来源或处理(如新鲜或堆肥处理后的猪粪、鸡粪、污泥)获取的DOM均能有效减少土壤或黏土矿物对Cd的吸附量[29-30, 40]。但与DOM存在情况下Qm的变化相反,177、160 m及151 m高程土壤与Cd的吸附亲和力(KL)却分别增加4.2%、8.3%及25.0%。可能原因为土壤表面原本对Cd不具有活性的吸附点位可能通过吸附DOM后改变其表面化学性质进而增强吸附剂对Cd的亲和力[23],但局部点位增强的吸附亲和力并未能抵消前述原因所致减少的Cd的吸附量从而使得Cd在土壤表面的最大吸附量呈现净减少的结果。对于Freundlich吸附等温线,添加猪粪DOM后,177、160 m及151 m高程土壤对Cd吸附的Kf值分别减少2.4%、0.9%和13.7%,与Qm相应的变化相似,表明猪粪DOM的添加能减少库区土壤尤其是消落带下部的土壤对Cd的吸附容量。对应的1/n值分别增加3.5%、6.2%及17.2%,表明猪粪DOM的引入造成Cd在库区土壤表面吸附的均质性有所增加,可能归因于DOM分子在土壤表面优先吸附后土壤表面剩余吸附点位的异质性降低或Cd在土壤-DOM结合物上的吸附均质性稍高于在土壤表面吸附的均质性。Wong等[29]与Li等[30]也发现外源DOM添加后,Cd在土壤表面吸附的Kf减小而1/n值增大。梯度上,加入猪粪DOM后,消落带151 m高程土壤吸附Cd的Qe、Qm及Kf值减小幅度均最大,即猪粪DOM对消落带下部土壤吸附Cd的抑制作用相对最大。因消落带下部土壤中Cd含量相对最高且环境风险最大,且总孔隙度高于消落带其余高程或非消落带土壤[41],所以外源DOM(不仅限于猪粪等畜禽粪便源,还可能包括污泥、生活污水等潜在源)进入消落带土壤后可能促进Cd向库区水体的释放和迁移。已有研究证实,在总孔隙度高、富含大孔隙或存在优先流通道的土壤中,DOM对Cd具有显著的辅助运移作用[42-43]。因此,在“后三峡”时代消落带监测与管理过程中应特别注意消落带下部土壤中Cd的动态。
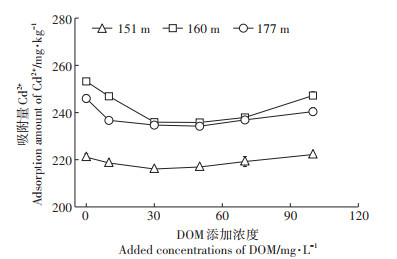
不同高程土壤吸附Cd2+的量对猪粪DOM初始添加浓度(30 mg·L-1)的响应一致(图 5)。在猪粪DOM添加量较低(0~30 mg C·L-1)时,3个高程土壤对Cd的吸附量随着DOM添加浓度的增加快速降低。DOM与Cd2+竞争土壤表面吸附点位以及溶液中DOM分子对Cd2+的络合作用是土壤对Cd2+吸附降低的主要原因。而随着猪粪DOM添加量继续增大(30~100 mg C·L-1),土壤对Cd的吸附量开始平稳缓慢地增加。对于非消落带177 m和消落带160 m高程土壤,较高浓度猪粪DOM(> 30 mg C·L-1)的引入使得土壤溶液pH由 < 7.10上升至7.20,是Cd的吸附量稍有增大的主要原因。不同的是,对于消落带151 m高程的酸性土壤(pH=6.60),猪粪DOM添加后土壤溶液pH稍微减小(pH=6.54~6.59)。研究证实,酸性环境中,pH降低导致土壤对外源DOM的吸附作用减弱[44],从而减小DOM与Cd2+对土壤表面吸附点位的竞争,间接促进Cd2+吸附的增加。其他学者的研究则发现,城市污泥源DOM初始添加浓度的增加(最高到800 mg C·L-1)会持续抑制不同酸碱性土壤对Cd的吸附且DOM浓度 < 250 mg C·L-1时抑制作用最强[29]。新鲜猪粪源DOM初始浓度梯度也存在类似效应,但猪粪堆肥后获取的DOM在浓度较高时(> 250 mg C·L-1)对污染土壤中Cd的吸附反而有促进作用[29]。因此,外源DOM的浓度梯度总体降低土壤对Cd的吸附,但DOM性质如熟化程度和土壤自身特性如pH可能导致在较高DOM浓度时促进土壤对Cd的吸附。
|
图 5 猪粪DOM添加浓度对库区土壤吸附Cd的影响 Figure 5 Effects of the initial addition concentrations of manureDOM on the sorption of Cd to soils |
(1)库区土壤对Cd的吸附为化学吸附,非线性极强,吸附强度(Qe、Qm、Kf)由高到低为消落带160 m > 非消落带177 m > 消落带151 m,土壤pH是最主要的内在影响因素。
(2)猪粪DOM的添加会抑制库区土壤尤其是消落带下部(151 m)土壤对Cd的吸附。
(3)猪粪DOM初始添加浓度 < 30 mg C·L-1时,库区土壤对Cd的吸附量随DOM浓度增加而持续降低;DOM初始添加浓度 > 30 mg C·L-1时,土壤对Cd的吸附量平稳缓慢增加。
| [1] |
于慧, 邓伟, 刘邵权, 等. 地势起伏度对三峡库区人口及经济发展水平的影响[J]. 长江流域资源与环境, 2013, 22(6): 686-690. YU Hui, DENG Wei, LIU Shao-quan, et al. Impact of relief amplitude on population and economic development in the Three Gorges Reservoir[J]. Resources and Environment in the Yangtze Basin, 2013, 22(6): 686-690. |
| [2] |
张信宝. 关于三峡水库消落带地貌变化之思考[J]. 水土保持通报, 2009, 29(3): 1-4, 9. ZHANG Xin-bao. Thinking about geomorphologic evolution of slopes in hydro-fluctuation belt of Three Gorges Reservoir[J]. Bulletin of Soil and Water Conservation, 2009, 29(3): 1-4, 9. |
| [3] |
Bao Y, Gao P, He X, et al. The water-level fluctuation zone of Three Gorges Reservoir:A unique geomorphological unit[J]. Earth-Science Reviews, 2015, 150: 14-24. DOI:10.1016/j.earscirev.2015.07.005 |
| [4] |
Pei S, Jian Z, Guo Q, et al. Temporal and spatial variation and risk assessment of soil heavy metal concentrations for water-level-fluctuating zones of the Three Gorges Reservoir[J]. Journal of Soils and Sediments, 2018, 18(9): 2924-2934. DOI:10.1007/s11368-018-1966-7 |
| [5] |
Wang T, Pan J, Liu X, et al. Characterization of heavy metal contamination in the soil and sediment of the Three Gorges Reservoir, China[J]. Journal of Environmental Science and Health, Part A, 2017, 52(3): 201-209. DOI:10.1080/10934529.2016.1246931 |
| [6] |
王金霞, 罗乐, 陈玉成, 等. 三峡库区库尾典型农用地土壤重金属污染特征及潜在风险[J]. 农业环境科学学报, 2018, 37(12): 2711-2717. WANG Jin-xia, LUO Le, CHEN Yu-cheng, et al. The characteristics and potential risk of heavy metals pollution in farmland soil of an agricultural land in the Three Gorges Reservoir area[J]. Journal of AgroEnvironment Science, 2018, 37(12): 2711-2717. DOI:10.11654/jaes.2018-0844 |
| [7] |
Holbach A, Norra S, Wang L, et al. Three Gorges Reservoir:Density pump amplification of pollutant transport into tributaries[J]. Environmental Science & Technology, 2014, 48(14): 7798-7806. |
| [8] |
刘安平, 孙晓楠, 杨东侠, 等. 三峡库区生态屏障区畜禽养殖场污染风险评估及其治理对策研究[J]. 环境工程, 2015, 33(增刊1): 682-685, 702. LIU An-ping, SUN Xiao-nan, YANG Dong-xia, et al. The pollution risk assessment and countermeasures research on livestock farms in ecological barrier zone of the Three Gorges Reservoir[J]. Environmental Engineering, 2015, 33(Suppl 1): 682-685, 702. |
| [9] |
黄美玲, 夏颖, 范先鹏, 等. 湖北省三峡库区畜禽养殖污染现状评价[J]. 生态学杂志, 2017, 36(3): 725-733. HUANG Mei-ling, XIA Ying, FAN Xian-peng, et al. Evaluation of livestock pollution status in the Three Gorges Reservoir area of Hubei Province[J]. Chinese Journal of Ecology, 2017, 36(3): 725-733. |
| [10] |
蔡金洲, 范先鹏, 黄敏, 等. 湖北省三峡库区农业面源污染解析[J]. 农业环境科学学报, 2012, 31(7): 1421-1430. CAI Jin-zhou, FAN Xian-peng, HUANG Min, et al. Sources analysis of agricultural non-point source pollution in the Three Gorges Reservoir area of Hubei Province, China[J]. Journal of Agro-Environment Science, 2012, 31(7): 1421-1430. |
| [11] |
胥焘, 王飞, 郭强, 等. 三峡库区香溪河消落带及库岸土壤重金属迁移特征及来源分析[J]. 环境科学, 2014, 35(4): 1502-1508. XU Tao, WANG Fei, GUO Qiang, et al. Transfer characteristic and source identification of soil heavy metals from Water-Level-Fluctuating zone along Xiangxi River, Three Gorges Reservoir area[J]. Environmental Science, 2014, 35(4): 1502-1508. |
| [12] |
王艮梅, 周立祥. 陆地生态系统中水溶性有机物动态及其环境学意义[J]. 应用生态学报, 2003, 14(11): 2019-2025. WANG Gen-mei, ZHOU Li-xiang. Dynamics of dissolved organic matter in terrestrials ecosystem and its environmental impact[J]. Chinese Journal of Applied Ecology, 2003, 14(11): 2019-2025. DOI:10.3321/j.issn:1001-9332.2003.11.048 |
| [13] |
Elliott H A, Denneny C M. Soil adsorption of cadmium from solutions containing organic ligands[J]. Journal of Environmental Quality, 1982, 11(4): 658-663. |
| [14] |
王林泉, 戴泽龙, 胥焘, 等. 香溪河水位消落带土壤在不同pH条件下对镉的吸附特性[J]. 三峡大学学报(自然科学版), 2017, 39(1): 108-112. WANG Lin-quan, DAI Ze-long, XU Tao, et al. Adsorption characteristics of cadmium at different values of n soil under water level fluctuating zone of Xiangxi River[J]. J of Three Gorges Univ(Natural Sciences), 2017, 39(1): 108-112. |
| [15] |
方卢秋. 环境激素Cd在三峡库区消落带土壤中的吸附-解吸特性[J]. 江西师范大学学报(自然科学版), 2010, 34(3): 232-236. FANG Lu-qiu. Properties of adsorption-desorption of environmental hormone Cd in soil of the Water-Level-Fluctuating region of Three Gorges Reservoir[J]. Journal of Jiangxi Normal University(Natural Science), 2010, 34(3): 232-236. DOI:10.3969/j.issn.1000-5862.2010.03.003 |
| [16] |
温华.三峡水库消落区土壤矿质胶体对Cd的吸持特征与胶体-Cd复合迁移研究[D].重庆: 西南农业大学, 2005. WEN Hua. Adsorption and desorption characteristics of cadmium by typical soil colloids from drawdown areas of the Three Gorges Reservoir and subsurface migration of cadmium facilitated by colloid[D]. Chongqing: Southwest Agricultural University, 2005. http://cdmd.cnki.com.cn/Article/CDMD-10625-2005089935.htm |
| [17] |
Lin J, Zhang S, Liu D, et al. Mobility and potential risk of sedimentassociated heavy metal fractions under continuous drought-rewetting cycles[J]. Science of the Total Environment, 2018, 625: 79-86. DOI:10.1016/j.scitotenv.2017.12.167 |
| [18] |
Cui J, Tang X, Zhang W, et al. The effects of timing of inundation on soil physical quality in the water-level fluctuation zone of the Three Gorges Reservoir region, China[J]. Vadose Zone Journal. DOI:10.2136/vzj2018.03.0043 |
| [19] |
常超, 谢宗强, 熊高明, 等. 三峡水库蓄水对消落带土壤理化性质的影响[J]. 自然资源学报, 2011, 26(7): 1236-1244. CHANG Chao, XIE Zong-qiang, XIONG Gao-ming, et al. The effect of flooding on soil physical and chemical properties of riparian zone in the Three Gorges Reservoir[J]. Journal of Natural Resources, 2011, 26(7): 1236-1244. |
| [20] |
Chen H, Teng Y, Lu S, et al. Contamination features and health risk of soil heavy metals in China[J]. Science of the Total Environment, 2015, 512: 143-153. |
| [21] |
生态环境部.土壤环境质量农用地土壤污染风险管控标准(试行) (GB 15618-2018)[S].北京: 中国标准出版社, 2018. Ministry of Ecology and Environment of the People's Republic of China. Environment soil environmental quality risk control standards for soil contamination agricultural land(trial)(GB 15618-2018)[S]. Beijing: Standards Press of China, 2018. |
| [22] |
Bekiaris G, Bruun S, Peltre C, et al. FTIR-PAS:A powerful tool for characterising the chemical composition and predicting the labile C fraction of various organic waste products[J]. Waste Management, 2015, 39: 45-56. DOI:10.1016/j.wasman.2015.02.029 |
| [23] |
Kim H C, Yu M J, Han I. Multi-method study of the characteristic chemical nature of aquatic humic substances isolated from the Han River, Korea[J]. Applied Geochemistry, 2006, 21(7): 1226-1239. DOI:10.1016/j.apgeochem.2006.03.011 |
| [24] |
Inyang H I, Onwawoma A, Bae S, et al. The Elovich equation as a predictor of lead and cadmium sorption rates on contaminant barrier minerals[J]. Soil and Tillage Research, 2016, 155: 124-132. DOI:10.1016/j.still.2015.07.013 |
| [25] |
Zhu W, Du W, Shen X, et al. Comparative adsorption of Pb2+, and Cd2+, by cow manure and its vermicompost[J]. Environmental Pollution, 2017, 227: 89-97. DOI:10.1016/j.envpol.2017.04.048 |
| [26] |
Li T, Liang C, Han X, et al. Mobilization of cadmium by dissolved organic matter in the rhizosphere of hyperaccumulator Sedum alfredii[J]. Chemosphere, 2013, 91(7): 970-976. DOI:10.1016/j.chemosphere.2013.01.100 |
| [27] |
Frišták V, Pipíška M, Lesný J, et al. Utilization of biochar sorbents for Cd2+, Zn2+, and Cu2+ ions separation from aqueous solutions:Comparative study[J]. Environmental Monitoring and Assessment, 2015, 187(1): 4093. |
| [28] |
Mustafa G, Singh B, Kookana R S. Cadmium adsorption and desorption behaviour on goethite at low equilibrium concentrations:Effects of pH and index cations[J]. Chemosphere, 2004, 57(10): 1325-1333. DOI:10.1016/j.chemosphere.2004.08.087 |
| [29] |
Wong J W C, Li K L, Zhou L X, et al. The sorption of Cd and Zn by different soils in the presence of dissolved organic matter from sludge[J]. Geoderma, 2007, 137(3/4): 310-317. |
| [30] |
Li Z, Bian C, Jie X, et al. Characteristic of Cd sorption in the copper tailings wasteland soil by amended dissolved organic matter from fresh manure and manure compost[J]. African Journal of Biotechnology, 2007, 6(3): 227-237. |
| [31] |
Lair G J, Gerzabek M H, Haberhauer G, et al. Response of the sorption behavior of Cu, Cd, and Zn to different soil management[J]. Journal of Plant Nutrition and Soil Science, 2006, 169(1): 60-68. DOI:10.1002/jpln.200521752 |
| [32] |
蒋田雨, 姜军, 徐仁扣, 等. 稻草生物质炭对3种可变电荷土壤吸附Cd(Ⅱ)的影响[J]. 农业环境科学学报, 2012, 31(6): 1111-1117. JIANG Tian-yu, JIANG Jun, XU Ren-kou, et al. Effect of biochar from rice straw on adsorption of Cd(Ⅱ)by variable charge soils[J]. Journal of Agro-Environment Science, 2012, 31(6): 1111-1117. |
| [33] |
吕焕哲, 张建新. 黏土矿物原位修复Cd污染土壤的研究进展[J]. 中国农学通报, 2014, 30(12): 24-27. LÜ Huan-zhe, ZHANG Jiang-xin. Research advances immobilization remediation of Cd contaminated soils using claying minerals[J]. Chinese Agricultural Science Bulletin, 2014, 30(12): 24-27. DOI:10.11924/j.issn.1000-6850.2013-2047 |
| [34] |
Kalbitz K, Wennrich R. Mobilization of heavy metals and arsenic in polluted wetland soils and its dependence on dissolved organic matter[J]. Sci Total Environ, 1998, 209(1): 27-39. DOI:10.1016/S0048-9697(97)00302-1 |
| [35] |
Bonten L T C, Groenenberg J E, Weng L, et al. Use of speciation and complexation models to estimate heavy metal sorption in soils[J]. Geoderma, 2008, 146(1/2): 303-310. |
| [36] |
Yuan G, Lavkulich L M. Sorption behavior of copper, zinc and cadmium in response to simulated changes in soil properties[J]. Commun. Soil Sci Plant Anal, 1997, 28(6/7/8): 571-587. |
| [37] |
Schindler P W, Stumm W. The surface chemistry of oxides, hydroxides, and oxide minerals[J]. Aquatic Surface Chemistry:Chemical Processes at the Particle-Water Interface, 1987(49): 83-110. |
| [38] |
周江敏, 代静玉, 潘根兴. 土壤中水溶性有机质的结构特征及环境意义[J]. 农业环境科学学报, 2003(6): 731-735. ZHOU Jiang-min, DAI Jing-yu, PAN Gen-xing. Characterization of dissolved organic matters in soil and its significance for environment[J]. Journal of Agro-Environment Science, 2003(6): 731-735. DOI:10.3321/j.issn:1672-2043.2003.06.023 |
| [39] |
Fan T T, Wang Y J, Li C B, et al. Effects of soil organic matter on sorption of metal ions on soil clay particles[J]. Soil Science Society of America Journal, 2015, 79(3): 794-802. |
| [40] |
Zhou W, Ren L, Zhu L, et al. Reducement of cadmium adsorption on clay minerals by the presence of dissolved organic matter from animal manure[J]. Environmental Pollution, 2017, 223: 247-254. DOI:10.1016/j.envpol.2017.01.019 |
| [41] |
Zhang S, Tang Q, Bao Y, et al. Effects of seasonal water-level fluctuation on soil pore structure in the Three Gorges Reservoir, China[J]. Journal of Mountain Science, 2018, 15(10): 2192-2206. DOI:10.1007/s11629-018-5013-3 |
| [42] |
Li Z, Zhou L. Cadmium transport mediated by soil colloid and dissolved organic matter:A field study[J]. Journal of Environmental Sciences, 2010, 22(1): 106-115. DOI:10.1016/S1001-0742(09)60081-4 |
| [43] |
Gerritse R G. Column-and catchment-scale transport of cadmium:Effect of dissolved organic matter[J]. Journal of Contaminant Hydrology, 1996, 22(3/4): 145-163. |
| [44] |
Shen Y H. Sorption of natural dissolved organic matter on soil[J]. Chemosphere, 1999, 38(7): 1505-1515. |
 2020, Vol. 39
2020, Vol. 39