2. 北京城市学院城市建设学部, 北京 101399;
3. 中国农业科学院农业环境与可持续发展研究所, 北京 100081
2. Urban Construction School, Beijing City University, Beijing 101399, China;
3. Institute of Environment and Sustainable Development in Agriculture, Chinese Academy of Agricultural Sciences, Beijing 100081, China
畜禽污水的贮存是重要的氨气(NH3)和温室气体(GHG)排放源[1]。在污水常规贮存中,25%~35%的N会以NH3-N的形式损失掉[2]。NH3大量排放后,会通过大气化学反应生成硝酸铵、硫酸铵等成为大气气溶胶细粒子PM2.5的重要组成部分,对灰霾的形成有重要影响[3]。除NH3以外,污水贮存中有机质分解排放的二氧化碳(CO2)、甲烷(CH4)和氧化亚氮(N2O)是重要的GHG。气体排放一方面造成污水农田利用中肥效的下降,同时也造成了环境的污染。因此,对养殖污水贮存中NH3和GHC进行减排具有重要意义。
当前污水贮存过程气体减排措施主要包括覆盖和酸化。采用人工覆盖塑料膜、秸秆等方法可以减少粪污贮存过程中69%~85% 的NH3排放[1]。但是覆盖技术存在难以回收的问题,此外秸秆等生物材料长久使用后会沉入水中,并进一步作为C源增加污水的CH4排放[4]。同时覆盖层上厌氧好氧兼性微环境的形成利于硝化反硝化细菌活性,导致N2O排放升高[2]。在污水贮存过程中加酸可以使NH3排放降低70% 以上[5-6],同时污水pH降低可抑制产甲烷菌活性,导致CH4排放量降低[7-9]。当前普遍采用的酸化剂为硫酸[10-12]。Petersen等[8]报道了采用浓硫酸酸化猪场污水至pH为5.5,不仅能使NH3排放量降低84%,同时能使CH4排放量降低90%。硫酸酸化相较其他酸成本较低,但是在国内由于硫酸的安全性问题使其推广应用受到限制[13],且直接加入硫酸可能会增加污水的H2S排放[9]。此外,也有部分研究探索了采用盐酸、乳酸、硫酸钾、硫酸铝的酸化NH3减排效果[5, 7, 14],但是使用成本一般都超过硫酸。因而需要探索一种较为安全、经济的酸化技术。
膨胀蛭石密度较低,可以悬浮于水面上形成覆盖层而减少气体排放[15]。同时蛭石具有较大的比表面积,吸附性能较强,因而部分研究将蛭石应用于吸附废水中的氨氮[16]。对蛭石进行酸改性处理可以增加蛭石的比表面积、加快蛭石的阳离子交换速度,提高蛭石对染料、重金属离子等的吸附能力[17-20]。此外酸改性后蛭石表面会呈现一定的酸性[21],可以进一步增加蛭石对NH3排放的抑制。在盐改性方面,研究认为采用金属氯化物改性蛭石可以在蛭石表面形成络合物,因而可以增加NH3的吸收[19-20, 22],当前这一技术主要应用于工业中的氨吸附式制冷技术[23]。
基于此,本研究推测若采用改性蛭石覆盖污水,一方面可以通过覆盖减少气体排放,同时改性之后蛭石吸附能力的提高可以进一步提高气体减排效果。考虑到酸改性蛭石在生产过程中可能存在的安全性问题,本研究拟采用两种典型的酸性金属盐溶液对蛭石进行改性,探索不同改性方法对蛭石覆盖污水后NH3、CH4、CO2和N2O排放的影响,实现污水贮存过程气体的高效减排。
1 材料与方法 1.1 沼液试验中所用的沼液取自北京市密云区某奶牛场,该牛场采用水冲粪的方式进行牛舍粪便管理,冲出的粪污总固体(TS)含量为8%~10%,直接进入全混合厌氧反应器(Continuous stirred tank reactor,CSTR)进行发酵。该CSTR反应器有效池容为6 000 m3,采取中温发酵,水力停留时间(HRT)为20~30 d。试验中所取沼液为该沼气工程的新鲜出水,在2 h内被运送到试验基地开展试验。
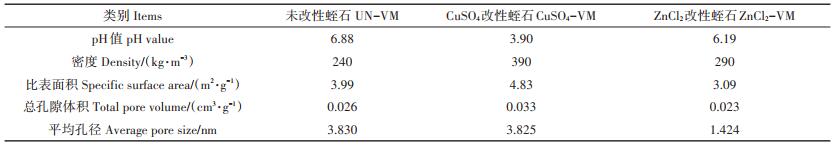
1.2 改性蛭石的制备试验中所用的膨胀蛭石产自河北灵寿县,成分为SiO2 46%、Al2O3 15.6%、Fe2O3 15.6%、MgO 10.0%、CaO 2.7%、K2O 5.3%、TiO2 3.9% 和Na2O 0.6%。所用膨胀蛭石直径为1~2 mm,密度为240 kg·m-3。设置2种浸渍材料,硫酸铜和氯化锌分别配制为质量浓度为15%的溶液,在15%的浓度下,这2种盐溶液pH分别为3.60和5.50。改性过程中按照每600 mL溶液中放入160 g蛭石的比例进行配比,搅拌器进行搅拌和浸泡4 h,将材料过滤后用105 ℃烘干完成改性。改性后两种蛭石pH相较未改性蛭石pH降低;同时由于改性蛭石吸附了部分溶质,密度上升(表 1)。
|
|
表 1 不同改性蛭石pH、密度、比表面积、总孔隙体积、平均孔径变化 Table 1 Changes of pH, density, specific surface area, total pore volume and average pore size for expanded vermiculite under different modifications |
试验中设置4个试验组,分别为硫酸铜改性蛭石覆盖组(CuSO4-VM)、氯化锌改性蛭石覆盖组(ZnCl2-VM)、未改性蛭石覆盖组(UN-VM)、对照组(不加覆盖组,CK),每个试验组设置3个重复。试验过程中所使用的贮存盒长、宽、高分别为0.24、0.15、0.14 m,实际容积为5 L。在试验中,将新鲜沼液量取2.5 L于每一贮存盒内。在CuSO4-VM、ZnCl2-VM和UN-VM组上分别均匀铺洒相应的覆盖材料,保证覆盖厚度均为2 cm。CK为污水的直接贮存,共计12个贮存盒。
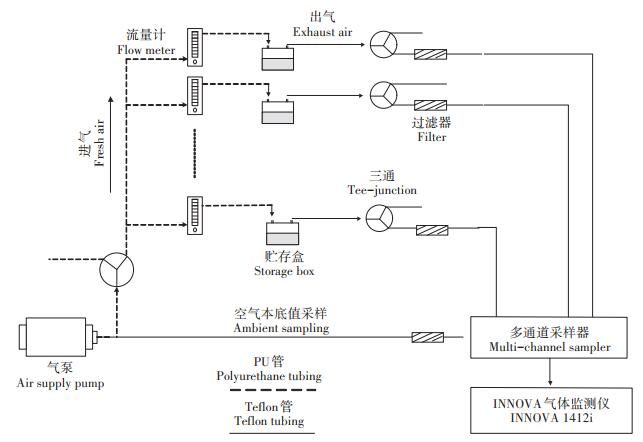
试验中采用动态箱法对污水表面的气体排放进行监测[2, 24]。采用空气真空泵进行供气,空气通过玻璃转子流量计平均分配到各个贮存盒中,设置进入贮存盒的气体流量值为1 L·min-1(图 1)。进气口高度保持在距离污水表面上5 cm,进气将带出污水表面挥发的各种气体从出气口排出。出气口通过特氟龙管路连接到多通道采样仪(Innova 1409,丹麦LumaSense公司)和红外光声谱气体监测仪(INNOVA 1412i型,丹麦LumaSense公司),实时监测污水存储过程中NH3、CO2、CH4和N2O的浓度。对每个处理标准一致的供气量设置可保证监测浓度的可比性。试验时间为2018年12月3日至2019年1月3日,存储时间32 d。
|
图 1 气体测试系统 Figure 1 Gas monitoring system |
使用多通道采样仪每10 min依次自动采集1~12号贮存盒和室外空气本底值的气样(每隔2 min一次,采集5次),采样后用多功能气体测定仪同步测定NH3、CO2、CH4和N2O 4种气体的浓度。为避免管路过长或者仪器内管路冲洗等造成的气体监测浓度误差,在计量过程中,只取第5次的监测浓度数据进行核算。INNOVA气体分析仪在使用前采用NH3、CO2、CH4和N2O标准气体(中国计量科学研究院购买)进行标定,确保数据准确性。气体监测为24 h连续运行,实现对各个贮存盒内污水排放的各目标气体的循环在线监测,每个贮存盒平均每日可以获得11~12组气体浓度数据。
1.4.2 液体样品采集与分析试验开始前采集初始阶段的新鲜沼液样品,试验结束后小心去除各贮存盒污水表面覆盖物后,分别对各贮存盒内的污水进行混匀采样。各水样分析其pH值、化学需氧量(COD)、总氨氮(TAN)、总氮(TN)、总固体含量(TS)、挥发性固体含量(VS)。在试验第1、4、8、12、17、23、32 d采用便携式pH计(LAQUAtwin-pH-22,日本HORIBA公司)测定贮存盒内污水pH值;同时在尽量不破坏覆盖物的前提下,第8、17、23 d利用注射器采集覆盖物下污水样品5 mL,用以检测COD、TAN和TN的变化。
COD、TAN和TN采用Hach试剂盒结合DR5000光谱仪(美国Hach公司)进行测试。根据HACH测试操作指导手册,COD采用消解法(Digestion method 8000,20~1 500 mg·L-1)测定;TN采用过硫酸盐消解法(Persulfate digestion method 10072,10~150 mg·L-1)测定;TAN采用水杨酸法(Salicylate method 10 031,0~50.0 mg·L-1)进行测定。TS和VS采用恒重法测试,使用仪器为烘箱(DN610,YAMATO,日本)、马弗炉(中国沈阳节能电炉厂)、万分之一天平(AL104,梅特勒-托利多仪器(上海)有限公司)。其中TS在105 ℃烘箱中烘烤24 h,冷却后测定;VS将称量后的样品在550 ℃马弗炉灼烧2 h,冷却后测定。
1.4.3 改性材料采集及分析采集2 g左右的2种改性蛭石和未改性蛭石,采用扫描电镜(SEM)(Phenom XL,荷兰Phenom公司)观察各类型蛭石表面结构形态。采用全自动气体吸附分析仪(Autosorb-iQ,美国Quantachrome仪器公司)结合多点Brunauer–Emmett–Teller(BET)法和Barrett–Joyner–Halenda(BJH)法测出各蛭石样品的比表面积、总孔隙体积和平均孔径。试验末期(第32 d),对表层覆盖物取样分析其pH值、COD、TAN、TN;具体做法是取1 g覆盖物,溶解于50 mL水中,经过超声波萃取30 min,采用1.4.2中所述的Hach试剂盒测试相应指标含量;同时采用如上方法测试未改性蛭石的COD、TAN、TN含量。
1.5 污水温度测试选取一个贮存盒,采用HoBo Pro T/RH(美国On⁃ set公司)监测贮存盒内污水温度,测试频率为每小时一次。
2 结果与讨论 2.1 改性蛭石表面结构变化采用扫描电镜将各组蛭石放大2 550倍后,发现改性后的蛭石其表面结构发生了明显的变化(图 2)。未改性蛭石表面呈现较立体的层状结构,而改性后的蛭石立体结构均被一定程度破坏,其中CuSO4-VM表面出现大量团簇状物质,而ZnCl2-VM片状结构保存相对较为完整,且表面未出现团簇状物质。15% 的CuSO4溶液相比ZnCl2溶液pH更低,溶液中H+浓度更高。经过酸性溶液改性后,蛭石层间域可交换的阳离子(Na+、K+、Ca2+、Mg2+)将被质子替换;若是酸浓度较高,蛭石内八面体结构也会发生部分解析,部分八面体阳离子(Al3+、Mg2+、Fe3+)也将溶出[21, 25]。除了CuSO4溶液更低的pH外,阴离子的尺寸对于矿物溶解性也有影响。相比氯离子,硫酸根离子和蛭石矿物的晶格尺寸及几何结构更为接近,因而蛭石在硫酸铜溶液中溶解性更大[17, 26]。由于蛭石晶体结构的破坏,立体结构坍塌,层状结构剥落,片状结构聚集[27]。矿物晶格内相关金属离子溶出,在蛭石表面堆积,形成了CuSO4-VM表面的团簇状颗粒[27-28]。此外,由于浸渍后未对改性蛭石进行清洗便进行烘干,残余在改性蛭石表面的CuSO4或者ZnCl2可能是导致改性后蛭石pH降低的主要原因[29]。

|
图 2 不同处理下蛭石扫描电镜图(×2 550倍) Figure 2 SEM micrographs of vermiculites under different modifications(×2 550 times) |
试验初期各蛭石覆盖组均在污水表面形成了较好的覆盖。贮存过程中两种改性蛭石表面出现了不同程度的裂缝,但是整体覆盖一直保持到了试验结束。而UN-VM组在第4 d出现裂缝随后便开始下沉,到第12 d全部沉没。主要是未改性蛭石具有很强的吸水性[30],吸水导致了膨胀蛭石后期的下沉。而蛭石经过改性后内部孔隙已经被相应的盐离子填充,吸水性降低,因而改性后的蛭石可以浮在污水表面。同时两种酸性盐溶液改性蛭石在覆盖养殖场污水后,对周边的污水产生酸化作用,导致污水缓冲体系内CO32-与H+结合产生CO2,以及溶解态的CO2转变成气体状态[31],初始阶段CO2大量产生。产生的CO2往上扩散进入改性蛭石层,在一定程度上加强了覆盖层在污水上的悬浮能力,导致改性蛭石层在污水上有更好的覆盖效果。
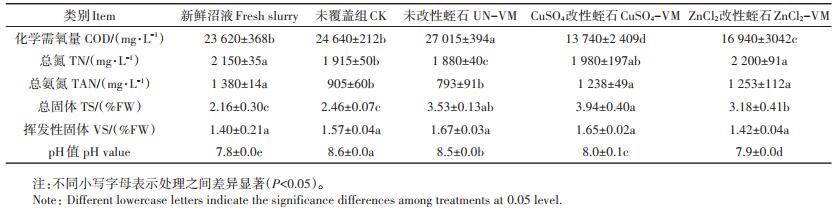
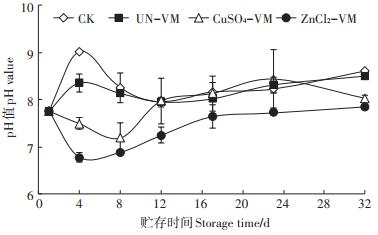
2.3 水质特性试验中初始沼液以及经过各蛭石组覆盖32 d后沼液的各项指标变化见表 2。pH是影响污水气体排放的关键因素,CK和UN-VM两组污水在贮存末期pH相似,均上升至8.5~8.6;而两种盐改性蛭石覆盖组污水最终pH相比初始新鲜沼液pH略有上升,为7.9~8.0。污水pH是污水内多重缓冲体系共同作用的结果[32]。一般情况下,随着贮存中CO2的不断排放,污水pH将随着贮存的进行逐步上升[2, 33-34]。观察本试验中整个贮存过程中pH的变化,发现CK和UN-VM组在第1~4 d pH值即出现上升,随后下降,并于后期保持缓慢上升趋势(图 3)。CK和UN-VM组贮存初期pH的升高可能是由于初始CO2的快速排放造成[32];在第5~10 d内,温度快速升高,NH3快速挥发,导致pH快速下降。而CuSO4-VM和ZnCl2-VM组贮存初期pH呈现下降趋势,随后逐步上升;ZnCl2-VM在整个贮存过程中始终保持最低的pH。酸性盐溶液改性的蛭石均具有一定的酸性(表 1),随着贮存的进行,上部改性蛭石内部的酸性盐逐渐被溶解出来[35],导致贮存的污水相较CK组pH较低,可以抑制NH3的排放。
|
|
表 2 各覆盖处理沼液贮存初期和末期水质指标 Table 2 Digested slurry characteristics at the start and end of storage period under different cover treatments |
|
图 3 不同覆盖处理下沼液pH变化情况 Figure 3 Changes of pH for biogas slurry stored under different cover treatments |
TAN对NH3排放有重要影响,CK和UN-VM组最终的TAN含量相比初始含量显著降低,下降幅度为34.4%~42.5%(表 2)。而CuSO4-VM和ZnCl2-VM覆盖的沼液TAN含量下降不显著。从TN来看,CK和UN-VM两组表现出较低的保N能力,这两组污水最终TN含量显著低于初始沼液;而CuSO4-VM覆盖的沼液TN含量下降幅度较低;ZnCl2-VM组最终TN含量甚至出现了升高。改性材料覆盖后较低的NH3挥发量,以及贮存过程中污水的不断蒸发导致ZnCl2-VM组TN含量升高。
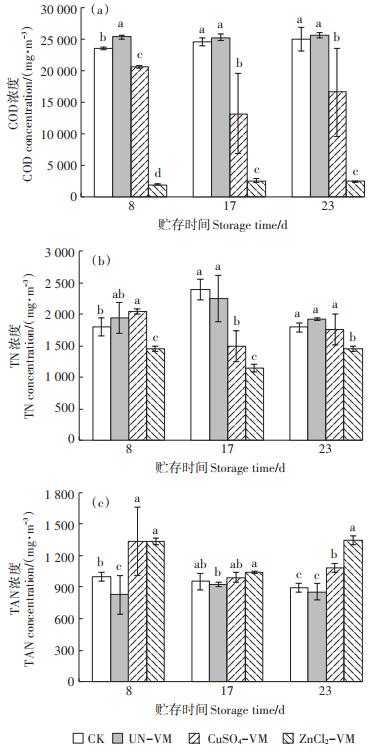
COD在一定程度上代表了污水中可以被微生物分解的有机物的含量。CK和UN-VM组COD含量上升的部分原因在于污水的蒸发速率高于COD的分解速度。但是对于盐改性组,可能是改性蛭石的絮凝作用造成了污水COD的大幅下降[36]。在污水贮存的第8、17、23 d对覆盖物下部的污水采用针头采样后测试,发现CuSO4-VM和ZnCl2-VM组污水COD含量,显著低于CK和UN-VM组。同时观察到ZnCl2-VM组所采集到的污水呈现极度澄清的状态,检测得到该污水第8、17、23 d COD含量在1 910~2 580 mg·L-1,明显低于初始阶段污水和最终混合污水的COD浓度(表 2),也低于同时间段内其他组的COD含量(图 4a)。研究认为,蛭石被硫酸盐或者氯盐改性后,蛭石层内主要的阳离子如Fe3+、Al3+等被大量溶出,与相应的阴离子结合形成AlCl3、FeCl3、Al2(SO4)3和Fe2(SO4)3等物质,而这些化合物都是典型的无机絮凝剂[31]。刘芳[36]报道采用硫酸改性蛭石制备的蛭石絮凝剂具有很好的絮凝效果,与聚合氯化铝(PAC)絮凝效果几乎相同。在絮凝作用下,水中悬浮颗粒发生凝聚沉淀,因而两种盐改性蛭石覆盖组取得的水样COD含量降低。同时由于金属氯化物可以在蛭石表面形成络合物[19-20],络合离子的生成能强烈吸附大分子胶体微粒,导致了ZnCl2-VM组污水澄清状态的出现以及COD含量的剧烈降低。同时TN中有一部分以有机氮的形式出现在悬浮的大分子物质内,因而絮凝作用对贮存过程中TN含量也有一定影响(图 4b)。但是对于溶解性的TAN,其并不以悬浮颗粒为载体,因而絮凝作用对其不存在影响,两组酸性盐溶液改性组中TAN含量始终保持最高(图 4c)。
|
不同小写字母表示处理之间差异显著(P < 0.05) Different lowercase letters indicate the significance differences among treatments at 0.05 level 图 4 不同处理组沼液第8、17、23 d时COD、TN、TAN含量 Figure 4 Changes in COD, TN, TAN of biogas slurry with different treatments at 8th, 17th and 23th day |
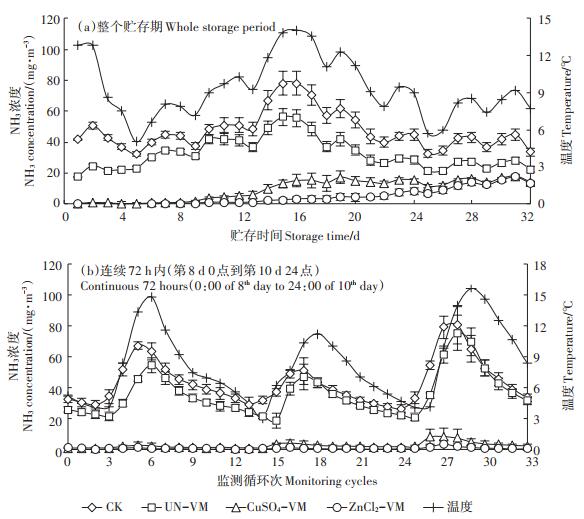
CK组沼液NH3日排放浓度明显高于覆盖的3个组别,显然蛭石覆盖沼液是NH3减排的有效方法(图 5a,表 3)。UN-VM对污水贮存NH3减排效率为34%。采用蛭石改性后再进行覆盖可使NH3减排效果明显加强。在各种处理组中,以ZnCl2改性蛭石对NH3的减排效果最佳,ZnCl2-VM组在第13 d开始出现微量NH3排放,整体NH3减排效率达到90%。CuSO4-VM组NH3减排效率为81%。由于ZnCl2、CuSO4改性蛭石显酸性,覆盖后酸性盐溶出,污水pH降低(图 3),进而导致NH3的产生量降低[37]。改性蛭石组获得了酸化和覆盖的双重减排效果,有效地保证了沼液中氨氮的含量,减少了氮损失。在72~95 d的贮存期内,利用硫酸酸化技术对于污水NH3减排效果为40%~84%[8-10];Balsari等[38]研究发现采用leca球对污水进行10 cm覆盖,7 d内污水NH3减排87%;Amon等[39]在污水上覆盖10 cm的秸秆,80 d内NH3排放甚至增加了24%。分析发现,相比leca球、秸秆等传统覆盖物,采用改性蛭石覆盖在较小的覆盖厚度下即可取得较好的NH3减排效果。在未来,需要在更长的覆盖时间下判断改性蛭石覆盖法的NH3减排效果,同时需要探索覆盖厚度与NH3减排效果间的关系以进一步降低技术的费效。检测得到由于改性后蛭石比表面积、孔径等指标相比未改性蛭石没有明显变化(表 1),因而蛭石对NH4+的吸附作用可能并不是造成这两种改性蛭石对NH3优势减排效果的主要原因。
|
图 5 不同覆盖物下沼液的NH3排放浓度变化 Figure 5 NH3 emission concentration of biogas slurry stored under different cover treatments |
|
|
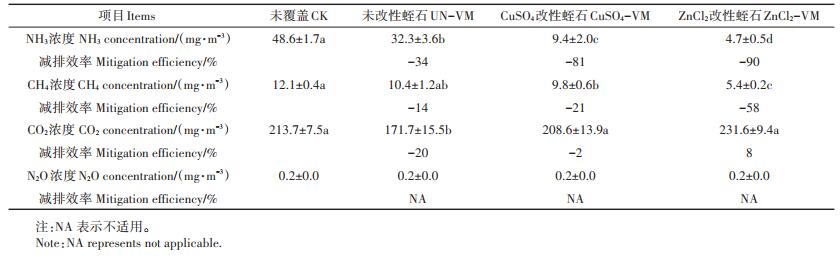
表 3 各处理组污水在整个贮存期内平均气体排放浓度统计及减排率 Table 3 The mean gas emission concentrations and mitigation efficiencies of slurry stored under different cover treatments during the whole storage period |
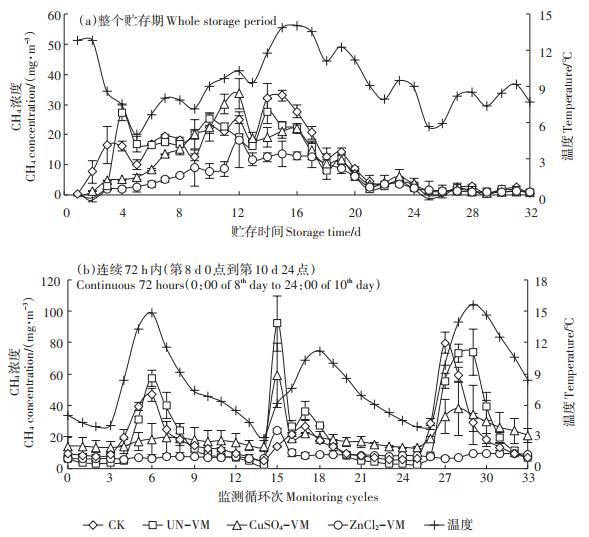
关于不同覆盖条件下污水贮存过程的CH4排放,各组没有非常明确的差异规律(图 6a)。除了各组初始前3 d排放浓度较低外,整体上各组CH4的排放与污水贮存期间温度变化状态相符。贮存初期极低的CH4排放现象在Wang等[2]的研究中同样被观察到,但是相关机制尚不清楚。从整体上看各蛭石覆盖组的CH4排放低于未覆盖的CK组,整个贮存期内UNVM、CuSO4-VM和ZnCl2-VM覆盖使污水CH4分别减排14%、21% 和58%。由于ZnCl2-VM覆盖组絮凝作用下污水内极低的COD含量及较低的pH环境,不利于产甲烷菌的活性[7-8],导致其CH4排放最低。Petersen等[8]和Wang等[9]发现硫酸酸化法可使污水CH4排放减少31%~99%。关于CH4的减排,污水直接酸化法对污水整个体系内甲烷菌活性都有一定的抑制,因而其对甲烷的减排效果相比改性蛭石覆盖法更好。采用酸性盐改性的蛭石覆盖污水可能相比传统的秸秆覆盖等技术可以获得更稳定的CH4减排效果。采用秸秆覆盖极有可能造成污水贮存CH4排放的升高[4, 29, 40];同时Berg等[29]发现采用珍珠岩覆盖也可能使CH4排放增加14%。
|
图 6 不同覆盖物下沼液的CH4排放浓度变化 Figure 6 CH4 emission concentration of biogas slurry stored under different cover treatments |
为了进一步明确温度对CH4排放的影响,对连续3 d(第8~10 d)各试验组贮存过程中连续72 h期间的气体排放进行了分析(图 6b),在此72 h内合计监测了33个循环的气体排放。研究发现,CK组和各蛭石覆盖组CH4排放在一定程度上与水温变化趋势相符,相关系数r分别为0.54(P < 0.001)和0.68(P < 0.001)。但是可以发现在此72 h内的第15次循环时,除了CK组,其他3个覆盖试验组均在日温度达到峰值前出现了一个极高的排放高峰;随后在温度达到峰值左右,再次出现一个较小的CH4排放峰值。可能原因是在第15个监测循环期内对污水进行了溶氧测试,溶氧探头较大,不可避免地对各覆盖表面造成了相对较大的破坏,此时被覆盖物抑制的CH4大量排出,造成了巨大的排放峰值;而NH3的排放却几乎不受采样操作影响(图 5b),表明改性蛭石覆盖对于NH3和CH4的减排机理并不相同。各类改性物质对于NH3挥发的抑制除了覆盖作用外,主要在于降低了污水pH导致NH3挥发减少的化学减排机制;而对于CH4的抑制则主要是絮凝作用对COD的消减,以及物理的覆盖抑制[15];同时改性蛭石降低污水pH,一定程度上也可以减少甲烷菌活性[8-9],因而两者针对人为扰动的反馈不同。由于整个贮存期定期的pH测试、采水样等操作对于覆盖物的破坏,造成了整个贮存过程各组不时的排放高峰;而即使同一平行组间,也存在采样的时间差距,造成整个32 d的贮存期内各组CH4排放标准差较大。
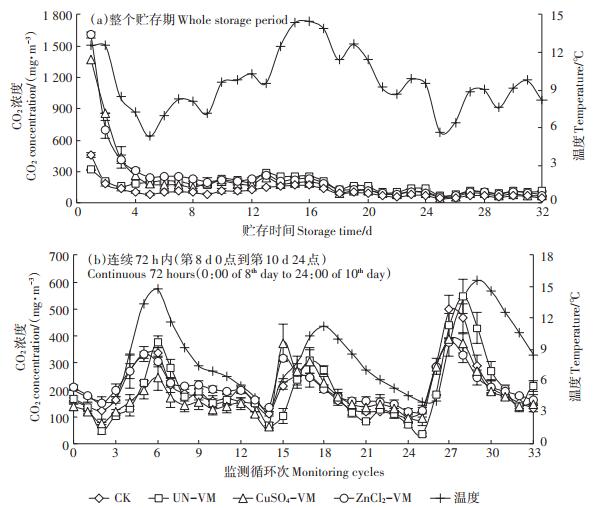
2.4.3 CO2的排放两种盐改性蛭石覆盖后的沼液,其CO2排放速率前3 d明显高于CK组和UN-VM组;随后各组CO2排放速率快速下降直至平稳(图 7a)。由于沼液中存在CO32-/HCO3-缓冲物质,而两种改性材料均为弱酸性,在沼液中释放H+后与CO32-/HCO3-结合产生了较多的CO2[32],所以改性材料覆盖处理时前期CO2排放速率较高。随后各试验组间CO2日排放速率无明显差异。
|
图 7 不同覆盖物下沼液的CO2排放浓度变化 Figure 7 CO2 emission concentration of biogas slurry stored under different cover treatments |
在第15个循环期,CuSO4-VM和ZnCl2-VM覆盖组同样因为采样测试等扰动出现瞬时的CO2排放高峰;而ZnCl2-VM和UN-VM组在温度达到日峰值左右时又再次出现一个CO2排放高峰(图 7b)。在一定程度上说明除了改性引入的H+增加了CO2的排放外,覆盖对于CO2的减排在一定程度上与CH4相似,即覆盖被扰动破坏后,容易出现排放峰值。Blanes-Vidal等[32]证明污水被扰动后,会出现瞬时的CO2排放峰值。但是从整体上来看,仍然是酸碱中和提高CO2排放的作用大于覆盖的抑制作用,因而ZnCl2-VM组使CO2排放增加了8%。Dai等[37]同样发现猪场污水添加强酸后能够使NH3排放量降低50%~77%,但同时贮存中CO2排放量增加了3~4倍。而UN-VM组由于在贮存初始阶段的覆盖抑制了CO2排放,整体CO2减排率达到20%。
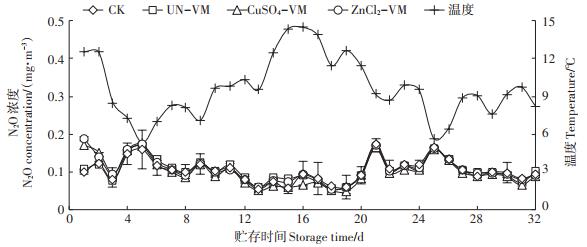
2.4.4 N2O的排放在污水贮存过程中N2O排放极低,气体排放浓度仅为0.1~0.2 mg·m-3(图 8)。Wang等[2]研究发现,只有污水温度超过15 ℃贮存过程才会出现N2O排放。但是在本试验整个存储过程中污水温度都不足15 ℃,导致本研究中极低的N2O排放量。因而不能判断改性蛭石覆盖对N2O排放的影响。
|
图 8 不同覆盖物下沼液的N2O排放浓度变化 Figure 8 N2O emission concentration of biogas slurry stored under different covers |
(1)酸性盐溶液改性极大增强了蛭石覆盖的NH3减排效果,减排率达到81%~90%;同时改性蛭石覆盖后也使CH4减排效果增加到21%~58%。改性蛭石对污水的酸化是产生NH3减排效果的主要因素,而改性蛭石对污水中有机物的絮凝作用是形成CH4减排效果的主要机制,同时优良覆盖效果的形成对于CH4的减排也有一定贡献。相比CuSO4-VM,ZnCl2-VM对污水有更强的酸化效果以及絮凝效果,对污水的NH3和CH4减排效果更高。
(2)未改性蛭石覆盖可使CO2排放下降20%;改性蛭石覆盖沼液后对CO2几乎没有减排效果,其中ZnCl2-VM组由于造成较强的酸化效果,使CO2排放增加了8%。研究中较低的日温造成N2O排放较低,不能判断改性对N2O排放的影响。
(3)基于本研究中对机理的初步分析,未来需要开展采用硫酸和盐酸直接对膨胀蛭石进行改性的研究,更强的酸化效果下可能可以获得更好的污水贮存气体减排效果。同时考虑到技术未来的实际应用,需要针对膨胀蛭石本身特性差异、所使用的改性溶液浓度、改性蛭石应用中的覆盖厚度等开展研究,以确定对于改性过程、覆盖效果有决定性作用的关键参数,减少技术的使用成本,并且进一步提高技术的气体综合减排效率。
| [1] |
Wang Y, Dong H M, Zhu Z P, et al. Mitigating greenhouse gas and ammonia emissions from swine manure management: A system analysis[J]. Environmental Science & Technology, 2017, 51: 4503-4511. |
| [2] |
Wang Y, Dong H M, Zhu Z P, et al. CH4, NH3, N2O and NO emissions from stored biogas digester effluent of pig manure at different temperatures[J]. Agriculture, Ecosystems and Environment, 2016, 217: 1-12. DOI:10.1016/j.agee.2015.10.020 |
| [3] |
Damme M, Clarisse L, Whitburn S, et al. Industrial and agricultural ammonia point sources exposed[J]. Nature, 2018, 564: 99-103. DOI:10.1038/s41586-018-0747-1 |
| [4] |
Guarino M, Fabbri C, Brambilla M. Evaluation of simplified covering systems to reduce gaseous emissions from livestock manure storage[J]. Transactions of the ASAE, 2006, 49(3): 737-747. DOI:10.13031/2013.20481 |
| [5] |
Regueiro I, Coutinho J, Fangueiro D. Alternatives to sulfuric acid for slurry acidification: Impact on slurry composition and ammonia emissions during storage[J]. Journal of Cleaner Production, 2016, 131: 296-307. DOI:10.1016/j.jclepro.2016.05.032 |
| [6] |
Kai P, Pedersen P, Jensen J, et al. A whole-farm assessment of the efficacy of slurry acidification in reducing ammonia emissions[J]. European Journal of Agronomy, 2008, 28(2): 148-154. DOI:10.1016/j.eja.2007.06.004 |
| [7] |
Petersen S O, Andersen A J, Eriksen J. Effects of cattle slurry acidification on ammonia and methane evolution during storage[J]. Journal of Environmental Quality, 2012, 41(1): 88-94. DOI:10.2134/jeq2011.0184 |
| [8] |
Petersen S, Hojberg O, Poulsen M, et al. Methanogenic community changes, and emissions of methane and other gases, during storage of acidified and untreated pig slurry[J]. Journal of Applied Microbiology, 2014, 117(1): 160-172. DOI:10.1111/jam.12498 |
| [9] |
Wang K, Huang D, Ying H, et al. Effects of acidification during storage on emissions of methane, ammonia, and hydrogen sulfide from digested pig slurry[J]. Biosystems Engineering, 2014, 122: 23-30. DOI:10.1016/j.biosystemseng.2014.03.002 |
| [10] |
Misselbrook T, Hunt J, Perazzolo F, et al. Greenhouse gas and ammonia emissions from slurry storage: Impacts of temperature and potential mitigation through covering(pig slurry) or acidification(cattle slurry)[J]. Journal of Environmental Quality, 2016, 45(5): 1520-1530. DOI:10.2134/jeq2015.12.0618 |
| [11] |
Park S H, Lee B R, Jung K H, et al. Acidification of pig slurry effects on ammonia and nitrous oxide emissions, nitrate leaching, and perennial ryegrass regrowth as estimated by 15N-urea flux[J]. Asian-Australasian Journal of Animal Sciences, 2018, 31(3): 457. DOI:10.5713/ajas.17.0556 |
| [12] |
Bicoku A, Provolo G, Riva E, et al. Assessments of mitigation techniques on ammonia emissions from animal slurries and digestate during storage[J]. Albanian Journal of Agricultural Sciences, 2018, 17(1): 84-90. |
| [13] |
Marszałek M, Kowalski Z, Makara A. Emission of greenhouse gases and odorants from pig slurry-effect on the environment and methods of its reduction[J]. Ecological Chemistry and Engineering S, 2018, 25(3): 383-394. DOI:10.1515/eces-2018-0026 |
| [14] |
Lefcourt A, Meisinger J. Effect of adding alum or zeolite to dairy slurry on ammonia volatilization and chemical composition[J]. Journal of Dairy Science, 2001, 84(8): 1814-1821. DOI:10.3168/jds.S0022-0302(01)74620-6 |
| [15] |
Qi X, Wu S, Wang Z, et al. Seasonal and daily emissions of methane and carbon dioxide from a pig wastewater storage system and the use of artificial vermiculite crusts[J]. Biosystems Engineering, 2015, 131: 15-22. DOI:10.1016/j.biosystemseng.2014.12.009 |
| [16] |
Wang M, Liao L, Zhang X, et al. Adsorption of low-concentration ammonium onto vermiculite from Hebei Province, China[J]. Clays and Clay Minerals, 2011, 59: 459-465. DOI:10.1346/CCMN.2011.0590503 |
| [17] |
Steudel A, Batenburg L F, Fischer H R, et al. Alteration of swelling clay minerals by acid activation[J]. Applied Clay Science, 2009, 44: 105-115. DOI:10.1016/j.clay.2009.02.002 |
| [18] |
Stawiński W, Węgrzyn A, Dańko T, et al. Acid-base treated vermiculite as high performance adsorbent: Insights into the mechanism of cationic dyes adsorption, regeneration, recyclability and stability studies[J]. Chemosphere, 2017, 173: 107-115. DOI:10.1016/j.chemosphere.2017.01.039 |
| [19] |
Veselovskaya J V, Tokarev M M, Aristov Y I. Novel ammonia sorbents "porous matrix modified by active salt"for adsorptive heat transformation: 1. Barium chloride in various matrices[J]. Applied Thermal Engineering, 2010, 30(6/7): 584-589. |
| [20] |
Grekova A D, Veselovskaya J V, Tokarev M M, et al. Ammonia sorption on the composites"(BaCl2+BaBr2) inside vermiculite pores"[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2014, 448: 169-174. |
| [21] |
苏小丽. 河北灵寿蛭石的结构与表面性质调控及其反应机理[D]. 广州: 中国科学院广州地球化学研究所, 2019. SU Xiao-li. Modification on structure and surface property of vermiculite from Lingshou Hebei and the mechanism involved[D]. Guangzhou: Guangzhou Institute of Geochemistry, Chinese Academy of Sciences, 2019. |
| [22] |
Zhong Y, Critoph R E, Thorpe R N, et al. Isothermal sorption characteristics of the BaCl2-NH3 pair in a vermiculite host matrix[J]. Applied Thermal Engineering, 2007, 27(14/15): 2455-2462. |
| [23] |
曾涛, 何兆红, 小林敬幸, 等. 氨吸附式制冷技术研究进展[J]. 新能源进展, 2017, 5(2): 146-150. ZENG Tao, HE Zhao-hong, KO-BAYASHI Noriyuki, et al. Research progress of adsorption refrigeration using ammonia as adsorbate[J]. Advanced in New and Renewable Energy, 2017, 5(2): 146-150. |
| [24] |
李路路, 董红敏, 朱志平, 等. 酸化处理对猪场原水和沼液存储过程中气体排放的影响[J]. 农业环境科学学报, 2016, 35(4): 774-784. LI Lu-lu, DONG Hong-min, ZHU Zhi-ping, et al. Effects of acidification on gas emissions from raw pig slurry and biogas liquid during storage[J]. Journal of Agro-Environment Science, 2016, 35(4): 774-784. |
| [25] |
Ijagbemi C O, Baek M H, Kim D S. Adsorptive performance of un-calcined sodium exchanged and acid modified montmorillonite for Ni2+ removal: Equilibrium, kinetics, thermodynamics and regeneration studies[J]. Journal of Hazardous Material, 2010, 174: 746-755. DOI:10.1016/j.jhazmat.2009.09.115 |
| [26] |
Pushpaletha P, Rugmini S, Lalithambika M. Correlation between surface properties and catalytic activity of clay catalysts[J]. Applied Clay Science, 2005, 30: 141-153. DOI:10.1016/j.clay.2005.03.011 |
| [27] |
Chmielarz L, Wojciechowska M, Rutkowska M, et al. Acid-activated vermiculites as catalysts of the DENOx process[J]. Catalysis Today, 2012, 191: 25-31. DOI:10.1016/j.cattod.2012.03.042 |
| [28] |
Hashem F S, Amin M S, El-Gamal S M A. Chemical activation of vermiculite to produce highly efficient material for Pb2+ and Cd2+ removal[J]. Applied Clay Science, 2015, 115: 189-200. DOI:10.1016/j.clay.2015.07.042 |
| [29] |
Berg W, Brunsch R, Pazsiczki I. Greenhouse gas emissions from covered slurry compared with uncovered during storage[J]. Agriculture Ecosystems & Environment, 2006, 112: 129-134. |
| [30] |
习永广, 彭同江. 膨胀蛭石表面疏水改性的实验研究[J]. 非金属矿, 2010, 33(5): 8-12. XI Yong-guang, PENG Tong-jiang. Experimental study on surface hydrophobic modification of expanded vermiculite[J]. Non-Metallic Mines, 2010, 33(5): 8-12. DOI:10.3969/j.issn.1000-8098.2010.05.003 |
| [31] |
Popovic O, Jensen L S. Storage temperature affects distribution of carbon, VFA, ammonia, phosphorus, copper and zinc in raw pig slurry and its separated liquid fraction[J]. Water Research, 2012, 46: 3849-3858. DOI:10.1016/j.watres.2012.04.020 |
| [32] |
Blanes-Vidal V, Guardia M, Dai X R, et al. Emissions of NH3, CO2 and H2S during swine wastewater management: Characterization of transient emissions after air-liquid interface disturbances[J]. Atmospheric Environment, 2012, 54: 408-418. DOI:10.1016/j.atmosenv.2012.02.046 |
| [33] |
Wang Y, Dong H M, Zhu Z P, et al. Comparison of air emissions from raw liquid pig manure and biogas digester effluent storages[J]. Transactions of the ASABE, 2014, 57(2): 635-645. |
| [34] |
Wang Y, Dong H M, Zhu Z P, et al. Ammonia and greenhouse gas emissions from biogas digester effluent stored at different depths[J]. Transactions of the ASABE, 2014, 57(5): 1483-1491. |
| [35] |
Kavanagh I, Burchill W, Healy M G, et al. Mitigation of ammonia and greenhouse gas emissions from stored cattle slurry using acidifiers and chemical amendments[J]. Journal of Cleaner Production, 2019, 237: 117822. DOI:10.1016/j.jclepro.2019.117822 |
| [36] |
刘芳. 无机矿物絮凝剂的开发与应用研究[D]. 天津: 天津科技大学, 2016. LIU Fang. Study on development and application of inorganic mineral materials flocculants[D]. Tianjin: Tianjin University of Science and Technology, 2016. |
| [37] |
Dai X R, Blanes-Vidal V. Emissions of ammonia, carbon dioxide, and hydrogen sulfide from swine wastewater during and after acidification treatment: Effect of pH, mixing and aeration[J]. Journal of Environmental Management, 2013, 115: 147-154. |
| [38] |
Balsari P, Dinuccio E, Gioelli F. A low cost solution for ammonia emission abatement from slurry storage[J]. International Congress Series, 2006, 1293: 323-326. DOI:10.1016/j.ics.2006.02.045 |
| [39] |
Amon B, Kryvoruchko V, Amon T, et al. Methane, nitrous oxide and ammonia emissions during storage and after application of dairy cattle slurry and influence of slurry treatment[J]. Agriculture Ecosystems & Environment, 2006, 112: 153-162. |
| [40] |
Petersen S O, Dorno N, Lindholst S, et al. Emissions of CH4, N2O, NH3 and odorants from pig slurry during winter and summer storage[J]. Nutrient Cycling in Agroecosystems, 2013, 95(1): 103-113. DOI:10.1007/s10705-013-9551-3 |
 2021, Vol. 40
2021, Vol. 40