2. 中国农业科学院研究生院,北京 100081
2. Graduate School of Chinese Academy of Agricultural Sciences, Beijing 100081, China
重金属含量作为茶叶质量安全的一类重要指标,是茶产业生产和出口的重点关注对象之一。镉(Cd)作为我国最严重且最易被植物吸收的土壤重金属污染物[1],在植物及土壤中的含量一般较低,但该元素进入土壤后易被茶树根系吸收并转移到地上部造成累积,且会通过食物链进入人体,从而威胁人类健康[2]。当镉累积浓度超过茶树自身防御反应的阈值时,茶树的基本生理过程,如光合、蒸腾、代谢、抗氧化等会受到影响,从而抑制茶树正常生长,影响茶叶的产量和品质[3-6]。为保证农副产品的质量安全,我国《土壤环境质量农用地土壤污染风险管控标准(试行)》(GB 15618—2018)中规定:pH≤6.5的农用地镉污染风险筛选值为≤0.3 mg·kg-1,风险管制值为≤1.5 mg·kg-1,其中镉为土壤总镉含量。但现在人们普遍认识到,镉的毒性和对植物的有效性很大程度上取决于其特定的化学形态和结合状态。有效态镉能更加准确地反映植物对重金属的吸收和利用程度,是进行土壤重金属污染评价的重要参数[7-8]。研究表明,用土壤总镉含量来判断茶叶镉污染状况具有一定的局限性,且与茶叶镉含量的相关性较差,而土壤有效态镉含量与茶叶镉含量的相关性极为显著。因此,土壤有效态镉和总镉含量结合可以更加全面准确地评估茶园土壤镉污染状况[9]。
目前,常用的有效态镉提取剂类型主要有稀酸溶液(如HCl、HNO3等)、络合剂(如DTPA、EDTA等)、中性盐溶液(如CaCl2、NH4NO3等)和缓冲溶液(如NH4OAc等)[10]。茶园有效态镉提取剂的选择尚不统一,主要有CaCl2、HCl、DTPA 3种[11-17]。但这3种提取剂是否适用于茶园土壤有效态镉的提取还有待验证。此外,提取剂浓度、提取时间、土液比、振荡频率等因素对有效态镉提取率的影响也尚未进行对比验证。筛选出高效的土壤有效态镉提取剂及提取方法,可为准确判断茶树镉吸收状况和确保茶叶产品质量安全提供技术支持。因此,本研究以不同地区茶园土壤和新梢为材料,选择5种不同提取剂进行有效态镉提取对比试验,以选出适用于茶园土壤有效态镉提取的最佳提取试剂和提取参数。
1 材料与方法 1.1 试验材料 1.1.1 样品采集与处理为使所选样品镉含量具有一定的浓度差异,选择未经镉处理的田间土壤样品和经过镉处理的盆栽土壤样品及其对应的茶叶新梢(一芽二叶)样品。采集地点分别为云南省普洱市(n=20),浙江省丽水市(n= 20),中国农业科学院茶叶研究所嵊州综合试验基地(n=22,包含13个盆栽样品,其中8个为人工添加Cd(NO3)2溶液至土壤镉含量为0.5 mg·kg-1,3个为人工添加Cd(NO3)2溶液至土壤镉含量为0.9 mg·kg-1,2个为空白对照)。采用土壤和新梢对应采样的方法,在样品点0~20 cm处选取3个采样点进行取土并混匀,代表该样点的土壤样品,新梢样品为土壤采集点对应的茶树新梢。采集的新梢样品用自来水和去离子水清洗3遍并晾干,用微波炉短时间杀青后置于80 ℃烘箱中烘干,粉碎后密封保存待测。土壤样品风干后除去砾石、植物残体,分别过20目筛用于土壤有效态镉含量和土壤基本理化性质的测定,过100目筛用于土壤总镉含量的测定。
1.1.2 供试提取剂的配制0.1 mol·L-1 CaCl2溶液[11]:称取CaCl2 11.1 g,溶解后加水稀释至1 L,备用。
0.1 mol· L-1 HCl溶液[12]:吸取HCl(优级纯)8.3 mL,加水稀释至1 L,备用。
1 mol·L-1 NH4OAc溶液[13]:称取NH4OAc 77.08 g,溶解后加水稀释至1 L,备用。
1 mol·L-1 MgCl2溶液[13]:称取MgCl2·6H2O 203.3 g,溶解后加水稀释至1 L,备用。
0.005 mol·L-1 DTPA溶液[14-15]:称取1.967 g DTPA溶于13.3 mL TEA(三乙醇胺)和少量水中,再称取1.11 g CaCl2溶于水中,一并转入1 L容量瓶,加水至约950 mL后用6 mol·L-1 HCl溶液调节pH至7.30(6 mol· L-1 HCl用量约为8.5 mL),最后加水定容至1 L,备用。
1.1.3 主要仪器微波消解仪(MARS6,美国CEM公司),石墨赶酸仪,高分辨电感耦合等离子体质谱仪(HR-ICP-MS,ELEMENTⅡ,美国热电),摇床,微量超细球磨机。
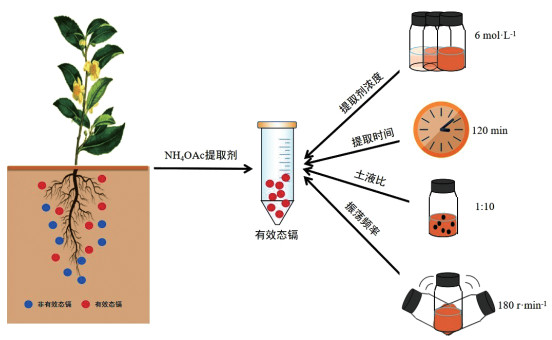
1.2 试验方法 1.2.1 有效态镉和总镉含量测定土壤有效态镉含量测定:称取过20目筛的土壤样品5 g于100 mL塑料瓶中,分别加入1.1.2中的5种提取剂各25.0 mL。后置于摇床,摇床参数设定为:温度25 ℃,振荡频率180 r·min-1,提取时间2 h。提取完成后先用双层滤纸过滤,再取少量滤液用亲水PTFE针式滤器(孔径0.22 μm)过滤,吸取0.5 mL二次过滤的滤液于15 mL刻度试管中,用超纯水稀释至10 mL,上ICP-MS进行测定。
植物样品总镉含量测定:称取0.2 g植物样品于聚四氟乙烯消解管中,加4 mL HNO3、4 mL HF,加盖后置于微波消解仪中消解(程序设定为25 min升温至180 ℃,并在该温度下保持20 min),待消解管冷却后置于赶酸仪(温度150 ℃,时间80 min)赶至消解管中仅剩约1 mL液体,用3% HNO3定容至50 mL容量瓶中,上ICP-MS进行测定。
土壤样品总镉含量测定:称取0.1 g土壤样品于聚四氟乙烯消解管中,加6 mL HNO3、1 mL HF、2 mL HCl,加盖后置于微波消解仪中消解(程序设定为30 min升温至190 ℃,并在该温度下保持30 min),待消解管冷却后置于赶酸仪(温度设定150 ℃,时间80 min)赶至消解管中仅剩约1 mL液体,用3% HNO3定容至50 mL容量瓶中,上ICP-MS进行测定。
1.2.2 提取条件优化根据1.2.1测定的土壤有效态镉含量与茶叶新梢镉含量的相关系数选出最佳提取剂后进行提取条件优化试验。本试验依次对提取剂浓度(0.5、1、2、4、6、7 mol·L-1),土液比(1∶2.5、1∶5、1∶10、1∶15),提取时间(30、60、120、180、240 min)、振荡频率(140、180、220、260、300、340 r·min-1)4个因素进行条件优化。采用单一变量法,每次仅改变一个提取条件,其他提取条件不变,以单一试验选择出的最佳提取条件作为下一个提取条件优化试验的参数依据,每个试验3次重复。
1.3 数据处理与分析数据处理和图表制作采用Microsoft Excel 2016和Prism。使用IBM SPSS Statistics 25进行相关性分析,确定不同提取剂测定的有效态镉与新梢镉的相关性,确定Pearson相关系数。
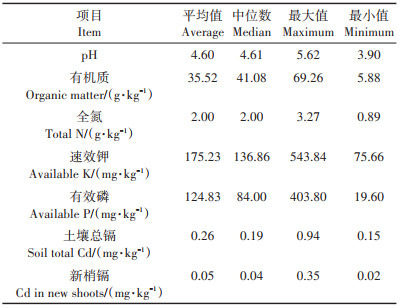
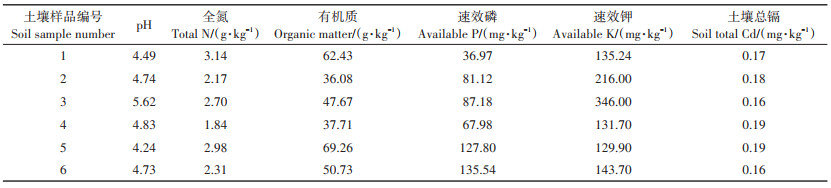
2 结果与讨论 2.1 土壤和新梢镉含量评价土壤样品的理化性质如表 1所示,土壤的pH值介于3.90~5.62,均为酸性土壤。按照有机质含量的高低选择6个土壤样品进行后续的提取方法优化试验,6个土壤样品的理化性质见表 2。
|
|
表 1 供试土壤基本性质和新梢镉含量 Table 1 Basic properties of tested soil and Cd content in new shoots |
|
|
表 2 优化试验土壤样品的基础性状 Table 2 Basic properties of optimized soil samples |
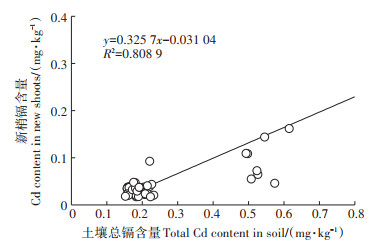
土壤总镉含量介于0.15~0.94 mg·kg-1,平均含量为0.26 mg·kg-1,其中有11个样品(0.49~0.94 mg·kg-1)超过《土壤环境质量农用地土壤污染风险管控标准(试行)》(GB 15618—2018)中的土壤污染风险筛选值(0.3 mg · kg-1)。新梢中镉含量介于0.02~0.35 mg · kg-1,平均值为0.05 mg·kg-1,所有样品均远低于《茶叶中铬、镉、汞、砷及氟化物限量》(NY 659—2003)中的限量标准(1 mg·kg-1)。如图 1所示,新梢镉含量随土壤总镉含量的增加而增加,呈现出显著的正相关关系(R2=0.808 9),该趋势表明茶园土壤镉具有一定的生物有效性[16]。
|
图 1 土壤总镉与新梢镉的相关关系 Figure 1 The correlation between total Cd in soil and Cd in new shoots |
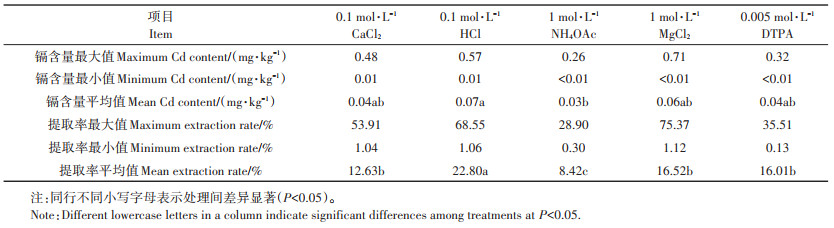
土壤样品相同情况下,提取剂类型不同,土壤有效态镉的提取率也不同。本研究所用的5种提取剂类型分别为稀酸溶液(0.1 mol · L-1 HCl)、络合剂(0.005 mol·L-1 DTPA)、中性盐溶液(0.1 mol·L-1 CaCl2、1 mol·L-1 MgCl2)和缓冲溶液(1 mol·L-1 NH4OAc)[17]。不同提取剂的提取率采用土壤有效态镉含量占土壤总镉含量的百分比来表征。由表 3可知,HCl的提取率最大,NH4OAc的提取率最小,HCl的平均提取率约为NH4OAc的3倍。提取率从高到低依次为0.1 mol· L-1 HCl>1 mol · L-1 MgCl2>0.005 mol · L-1 DTPA>0.1 mol·L-1 CaCl2>1 mol·L-1 NH4OAc。稀HCl由于自身pH较低、Cl-含量高、溶解能力强,易将土壤中碳酸盐结合态等非有效态镉提取出来,且HCl增加了酸性土壤中的H+含量,使其对金属阳离子的置换能力增强,因此提取率高,在某些文献中甚至存在提取率超过土壤总镉含量的情况[13, 18-19]。本研究中,0.1 mol·L-1 HCl的有效态镉提取率明显高于其他4种提取剂。中性盐溶液和缓冲溶液提取的土壤镉形态一般为可交换态和水溶态两种有效态,提取的镉含量较少,提取率相较其他类型提取液较低[20]。因此本研究中中性盐溶液和缓冲溶液的提取率最低。此外,Ca2+作为土壤溶液中的主要阳离子,离子强度与典型的土壤溶液相似,从土壤基质中解吸重金属的竞争能力强于一价阳离子NH4+[21]。这解释了本研究中中性盐提取剂CaCl2的提取率高于缓冲溶液NH4OAc的原因。
|
|
表 3 不同提取剂对土壤有效态镉的提取效果对比 Table 3 Comparison of extraction effects of different extractants on soil available cadmium |
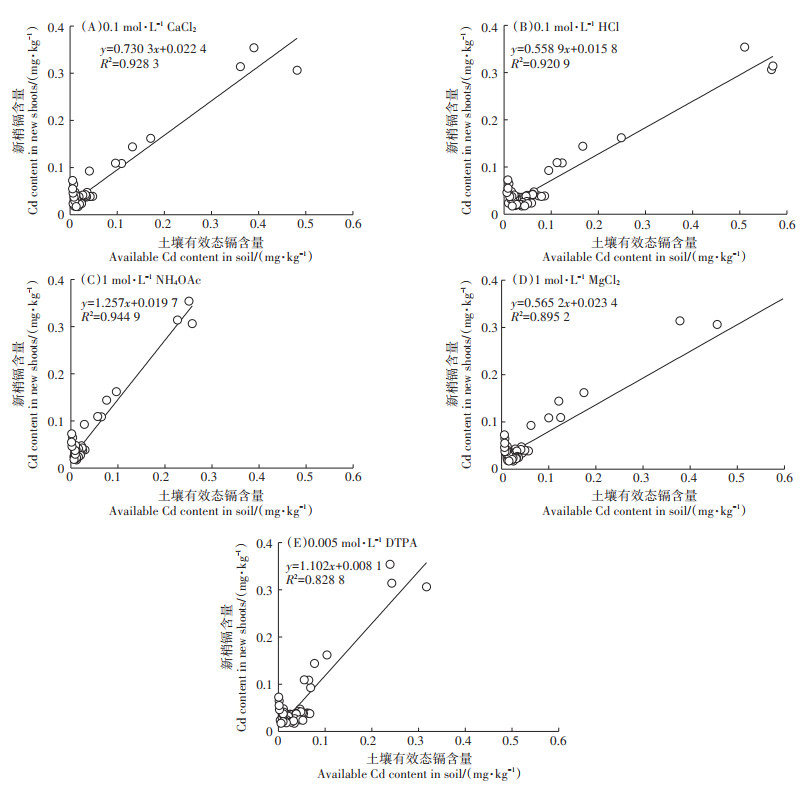
图 1和图 2表明,土壤中总镉和有效态镉含量的增加均会引起新梢镉含量的增加。如图 2所示,5种单一提取剂的土壤有效态镉与新梢镉含量的相关关系均达到极显著相关,相关系数大小依次为1 mol· L-1 NH4OAc>0.1 mol · L-1 CaCl2>0.1 mol · L-1 HCl>1 mol·L-1 MgCl2>0.005 mol·L-1 DTPA,有效态镉含量与新梢镉含量的相关系数均大于土壤总镉含量与新梢镉含量的相关系数,且缓冲溶液和中性盐溶液的相关系数优于稀酸溶液和络合剂。
|
图 2 土壤有效态镉与新梢镉含量的相关性分析 Figure 2 Correlation analysis of available Cd in soil with Cd content in new shoots |
虽然部分文献中使用DTPA溶液对茶园土壤有效态镉进行提取[9, 22],且国家标准GB/T 23739—2009中规定了以DTPA作为土壤有效态镉的测定试剂。但DTPA溶液提取有效态镉的适用范围是中性和碱性土壤,当应用于酸性土壤时可能会超过土壤溶液自身的缓冲能力,导致铁锰氧化物和碳酸盐吸附的重金属被释放,而该部分重金属为非有效态,因此不能很好地反映酸性土壤中有效态镉的含量状况[23]。HCl溶液属于强代换剂且pH较低,在进行提取时易将有机结合态和碳酸盐结合态两种非有效态镉提取出来,从而导致其提取的有效态镉含量偏高,准确性差[24]。MgCl2溶液中的Mg2+和Cl-分别具有较强的离子交换能力和较弱的络合能力,用于有效态镉提取时会造成土壤pH的降低,从而使碳酸盐和氧化锰部分溶解,导致可交换态镉含量被高估[25]。CaCl2溶液对于土壤pH和土壤结构的影响较小,接近土壤自然状态下对于重金属的溶解能力,适用范围广[26-27]。主要是由于中性盐提取剂对土壤pH、氢氧化物和硅酸盐的影响较小,并且对土壤颗粒吸附的金属离子置换能力较强,可提取出土壤中真实的有效态镉含量而非潜在的有效态镉含量[28-29]。NH4OAc中的NH4+可以促进交换位离子的置换,形成的金属络合物稳定性优于Cl-形成的金属络合物,有利于交换并减少已络合金属的再吸附和沉淀,且缓冲溶液相较于中性盐溶液对pH的敏感性更低[25, 30]。因此NH4OAc提取剂适用于茶园酸性土壤重金属有效态镉含量的提取研究。
根据5种提取剂的提取能力差异以及土壤有效态镉含量与新梢镉含量的相关系数,选择NH4OAc作为茶园土壤有效态镉含量的最佳提取剂,并进行后续的提取条件优化试验。NH4OAc作为酸性土壤有效态镉的提取剂目前已有相关文献报道[31]。如贺静等[32]发现6种不同提取剂中NH4OAc最适合作为酸性水稻田土壤中有效态镉的提取剂,其提取量的相对标准偏差稳定性强,有效态镉含量与土壤总镉含量和水稻籽粒中镉含量呈极显著相关。MENZIES等[17]的研究表明,NH4OAc可以较好地反映土壤镉的生物有效性。尹君等[33]的研究表明,以NH4OAc溶液作为提取剂,土液比为1∶5、浸提60 min可以较好地表征土壤有效态镉含量。因此,我们认为NH4OAc提取有效态镉适用于测定茶园土壤中镉的生物有效性。
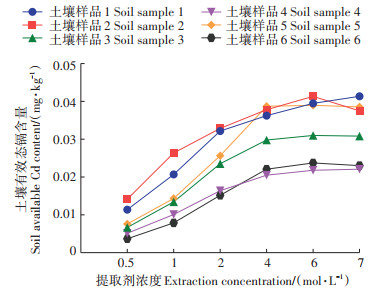
2.3 提取方法的优化 2.3.1 提取剂浓度的选择提取剂浓度是影响有效态镉提取率的重要因素之一。如图 3所示,随着提取剂浓度的增加,有效态镉提取率呈现明显增长趋势,但增长幅度随浓度增加逐渐减小。提取浓度从0.5 mol·L-1增加到4 mol·L-1时,有效态镉提取率增长幅度较大,平均相对偏差分别为94.81%、64.77%和29.36%(表 4)。由此可知,当提取剂浓度低于4 mol·L-1时,提取率较低,平均相对偏差变动较大。当提取剂浓度在4~6 mol·L-1之间时,提取率增长幅度较0.5~4 mol·L-1之间有所降低,平均相对偏差仅为6.13%。6~7 mol·L-1时提取率出现轻微下降,说明此时有效态镉的提取率几乎不再发生变化,增加提取剂浓度对提取率影响较小反而还会增加提取成本[30]。因此,选择6 mol·L-1作为最佳提取浓度并进行后续试验。
|
图 3 不同提取剂浓度的对比试验 Figure 3 Comparative experiment of different extractant concentrations |
|
|
表 4 不同提取剂浓度之间的平均相对偏差 Table 4 Average relative deviation between different extraction concentrations |
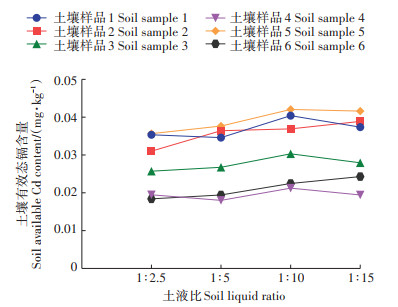
土液比是影响有效态镉提取率的因素之一。如图 4所示,当土液比从1∶2.5减小到1∶5时,提取率增加幅度较小,平均相对偏差仅为3.84%(表 5);从1∶5减小到1∶10时,提取率增长幅度较大,平均相对偏差为12.75%。从1∶10减小到1∶15时,有效态镉提取率出现轻微下降。因此,选择1∶10作为最佳土液比并进行后续试验。随着土液比减小,提取剂用量增加,土壤中固相状态的重金属离子解吸变成液相状态,溶液总体对于镉离子的交换和络合能力增强[33]。但当土液比过小时,重金属的质量分数在滤液中占比较低,不利于有效态镉含量的测定[34]。
|
图 4 不同土液比的对比试验 Figure 4 Comparative experiment of different soil liquid ratios |
|
|
表 5 不同土液比之间的平均相对偏差 Table 5 Average relative deviation between different soil liquid ratios |
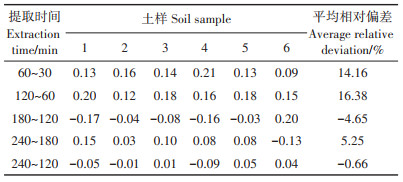
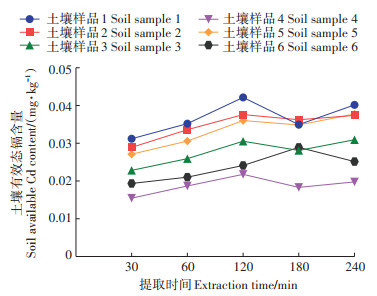
提取时间对于有效态镉的提取率也具有重要影响。如图 5所示,提取时间从30 min增加到120 min时,提取率明显增加,平均相对偏差分别为14.16%和16.38%(表 6)。从120 min增加到240 min时提取率出现轻微波动,对比120 min和240 min时的提取率,平均相对偏差仅为-0.66%,原因可能是当提取时间为120 min时,土壤中的有效态镉提取率已经或接近平衡状态,此时再增加提取时间对提取率的影响较小[34]。因此,在既保证测定准确性又提高工作效率的原则下选择120 min作为最佳提取时间并进行后续试验。
|
图 5 不同提取时间的对比试验 Figure 5 Comparative experiment of different extraction times |
|
|
表 6 不同提取时间之间的平均相对偏差 Table 6 Average relative deviation between different extraction times |
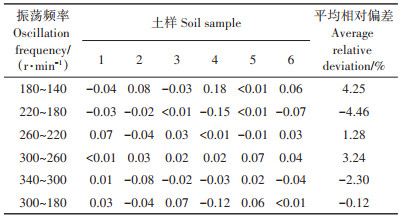
振荡频率是影响有效态镉含量提取的因素之一。如图 6所示,振荡频率对有效态镉的提取率影响较小。随着振荡频率的增加,提取率的增加幅度较小。振荡频率从140 r·min-1增加到180 r·min-1,以及从220 r·min-1增加到300 r·min-1时,有效态镉提取率出现轻微上升,平均相对偏差分别为4.25%、1.28% 和3.24%(表 7)。通过对比180 r·min-1与300 r·min-1有效态镉提取率发现,平均相对偏差仅为-0.12%,变化较小。在保证有效态镉含量测定结果准确的同时,选择较小的振荡频率可以减小对摇床的损耗[35],所以选择180 r·min-1作为有效态镉的最佳振荡频率。

|
图 6 不同振荡频率的对比试验 Figure 6 Comparative experiment of different oscillation frequency |
|
|
表 7 不同振荡频率之间的平均相对偏差 Table 7 Average relative deviation between different oscillation frequency |
(1)稀酸溶液和络合剂对茶园土壤的提取能力强,中性盐溶液和缓冲溶液对茶园土壤的提取能力弱。
(2)5种提取剂有效态镉与新梢镉含量的相关系数均大于土壤全镉,且缓冲溶液和中性盐溶液的相关系数优于稀酸溶液和络合剂。
(3)提取剂浓度和提取时间对有效态镉提取率的影响较大,土液比和振荡频率对有效态镉提取率的影响较小。
(4)茶园土壤以NH4OAc作为提取剂,提取条件设定为提取浓度6 mol·L-1,土液比1∶10,提取时间120 min,振荡频率180 r·min-1时的有效态镉提取效果最佳。
| [1] |
DUAN Q N, LEE J C, LIU Y S, et al. Distribution of heavy metal pollution in surface soil samples in China: A graphical review[J]. Bulletin of Environmental Contamination and Toxicology, 2016, 97(3): 303-309. DOI:10.1007/s00128-016-1857-9 |
| [2] |
CAO D J, YANG X, GENG G, et al. Absorption and subcellular distribution of cadmium in tea plant(Camellia sinensis cv."Shuchazao")[J]. Environmental Science and Pollution Research, 2018, 25(16): 15357-15367. DOI:10.1007/s11356-018-1671-5 |
| [3] |
王春梅, 唐茜, 张小琴, 等. 高浓度镉胁迫对茶树生理及吸收积累特性的影响[J]. 茶叶科学, 2012, 32(2): 107-114. WANG C M, TANG Q, ZHANG X Q, et al. Effect of high concentrations of Cd stress on the physiological characteristics, absorbtion and accumulation in tea plant[J]. Journal of Tea Science, 2012, 32(2): 107-114. DOI:10.3969/j.issn.1000-369X.2012.02.003 |
| [4] |
唐迪, 徐晓燕, 李树炎, 等. 重金属镉对茶树生理特性的影响[J]. 湖北农业科学, 2013, 52(12): 2839-2843. TANG D, XU X Y, LI S Y, et al. Effect of heavy metal cadmium on physiological characteristics of tea plant[J]. Hubei Agricultural Sciences, 2013, 52(12): 2839-2843. DOI:10.3969/j.issn.0439-8114.2013.12.028 |
| [5] |
唐迪, 李树炎, 徐晓燕, 等. 重金属镉处理对茶树鲜叶营养成分的影响[J]. 湖北农业科学, 2013, 52(18): 4407-4410. TANG D, LI S Y, XU X Y, et al. Effect of cadmium on the nutritional components in fresh leaves of Camellia sinensis[J]. Hubei Agricultural Sciences, 2013, 52(18): 4407-4410. DOI:10.3969/j.issn.0439-8114.2013.18.028 |
| [6] |
苏金为, 王湘平. 镉离子对茶叶光合机构及性能的影响[J]. 茶叶科学, 2004, 24(1): 65-69. SU J W, WANG X P. Effect of cadmium ions on photosynthetic structure and its functions of tea leaves[J]. Journal of Tea Science, 2004, 24(1): 65-69. DOI:10.3969/j.issn.1000-369X.2004.01.013 |
| [7] |
PARK H J, KIM S U, JUNG K Y, et al. Cadmium phytoavailability from 1976 through 2016:Changes in soil amended with phosphate fertilizer and compost[J]. Science of the Total Environment, 2021, 762: 143132. DOI:10.1016/j.scitotenv.2020.143132 |
| [8] |
黄迪, 杨燕群, 肖选虎, 等. 土壤重金属生物有效性评价技术进展[J]. 现代化工, 2019, 39(增刊1): 89-94. HUANG D, YANG Y Q, XIAO X H, et al. Technology for measuring bioavailability of heavy metals in soil[J]. Modern Chemical Industry, 2019, 39(Suppl 1): 89-94. |
| [9] |
向永生, 张军强, 李明伟, 等. 恩施州茶园土壤镉含量及其对茶叶质量安全的影响[J]. 湖北农业科学, 2010, 49(7): 1602-1604. XIANG Y S, ZHANG J Q, LI M W, et al. The cadmium contents in the soil of tea garden and its effect on quality and safety of tea in Enshi[J]. Hubei Agricultural Sciences, 2010, 49(7): 1602-1604. DOI:10.3969/j.issn.0439-8114.2010.07.020 |
| [10] |
陈飞霞, 魏世强. 土壤中有效态重金属的化学试剂提取法研究进展[J]. 干旱环境监测, 2006, 20(3): 153-158. CHEN F X, WEI S Q. Study of chemical extraction of heavy metals in soil[J]. Arid Environmental Monitoring, 2006, 20(3): 153-158. DOI:10.3969/j.issn.1007-1504.2006.03.008 |
| [11] |
王峰, 单睿阳, 陈玉真, 等. 闽中某县茶园土壤-茶树-茶汤中镉含量及健康风险评价研究[J]. 茶叶科学, 2018, 38(5): 537-546. WANG F, SHAN R Y, CHEN Y Z, et al. A case study of cadmium distribution in soil-tea plant-tea soup system in central Fujian Province and relative health risk assessment[J]. Journal of Tea Science, 2018, 38(5): 537-546. |
| [12] |
李云, 张进忠, 童华荣. 茶苗对重金属Pb Cu Cd和Cr的吸收累积规律[J]. 农业环境科学学报, 2009, 28(3): 454-459. LI Y, ZHANG J Z, TONG H R. Absorption and accumulation of Cr, Pb, Cu and Cd in young tea tree[J]. Journal of Agro-Environment Science, 2009, 28(3): 454-459. |
| [13] |
肖振林, 王果, 黄瑞卿, 等. 酸性土壤中有效态镉提取方法研究[J]. 农业环境科学学报, 2008, 27(2): 795-800. XIAO Z L, WANG G, HUANG R Q, et al. Extraction method for available cadmium in acid soils[J]. Journal of Agro-Environment Science, 2008, 27(2): 795-800. |
| [14] |
张斌. DTPA浸提-电感耦合等离子体质谱法测定土壤中的有效镉、有效铅[J]. 现代盐化工, 2021, 48(1): 11-13. ZHANG B. DTPA extraction - inductively coupled plasma mass spectrometry determine available cadmium and lead in soil[J]. Modern Salt and Chemical Industry, 2021, 48(1): 11-13. DOI:10.3969/j.issn.1005-880X.2021.01.005 |
| [15] |
刘铭, 刘凤枝, 刘保峰. 土壤中有效态铅和镉的测定[J]. 农业环境科学学报, 2007, 26(增刊1): 300-302. LIU M, LIU F Z, LIU B F. Determination of available lead and cadmium in soil[J]. Journal of Agro-Environment Science, 2007, 26(Suppl 1): 300-302. |
| [16] |
张秀芝, 王立平, 刘伟彬, 等. 北方碱性褐土有效镉提取方法筛选[J]. 地球与环境, 2021, 49(2): 207-215. ZHANG X Z, WANG L P, LIU W B, et al. Screening of effective cadmium extraction methods from northern alkaline cinnamon soil[J]. Earth and Environment, 2021, 49(2): 207-215. |
| [17] |
MENZIES N W, DONN M J, KOPITTKE P M. Evaluation of extractants for estimation of the phytoavailable trace metals in soils[J]. Environmental Pollution, 2007, 145(1): 121-130. DOI:10.1016/j.envpol.2006.03.021 |
| [18] |
颜世红, 吴春发, 胡友彪, 等. 典型土壤中有效态镉CaCl2提取条件优化研究[J]. 中国农学通报, 2013, 29(9): 99-104. YAN S H, WU C F, HU Y B, et al. Optimization of CaCl2 extraction of available cadmium in typical soils[J]. Chinese Agricultural Science Bulletin, 2013, 29(9): 99-104. DOI:10.3969/j.issn.1000-6850.2013.09.018 |
| [19] |
李发生, 韩梅, 熊代群, 等. 不同浸提剂对几种典型土壤中重金属有效态的浸提效率研究[J]. 农业环境科学学报, 2003, 22(6): 704-706. LI F S, HAN M, XIONG D Q, et al. Efficiency of some extractants for available heavy metals from several typical soils[J]. Journal of Agro-Environment, 2003, 22(6): 704-706. DOI:10.3321/j.issn:1672-2043.2003.06.016 |
| [20] |
熊婕, 朱奇宏, 黄道友, 等. 南方稻田土壤有效态镉提取方法研究[J]. 农业现代化研究, 2018, 39(1): 170-177. XIONG J, ZHU Q H, HUANG D Y, et al. Comparison of single extraction methods for assessing Cd availability in south China[J]. Research of Agricultural Modernization, 2018, 39(1): 170-177. |
| [21] |
MEERS E, LAING G D, UNAMUNO V, et al. Comparison of cadmium extractability from soils by commonly used single extraction protocols[J]. Geoderma, 2007, 141(3): 247-259. |
| [22] |
牟明辉, 石杨程, 张晓晴, 等. 恩施富硒茶园土壤重金属和氟含量及风险评价[J]. 河南农业科学, 2016, 45(5): 61-65. MOU M H, SHI Y C, ZHANG X Q, et al. Contents and risk assessment of heavy metal and fluorine in selenium enriched tea garden soils in Enshi area[J]. Journal of Henan Agricultural, 2016, 45(5): 61-65. |
| [23] |
FENG M H, SHAN X Q, ZHANG S Z, et al. A comparison of the rhizosphere-based method with DTPA, EDTA, CaCl2, and NaNO3 extraction methods for prediction of bioavailability of metals in soil to barley[J]. Environmental Pollution, 2005, 137(2): 231-240. DOI:10.1016/j.envpol.2005.02.003 |
| [24] |
贾双琳, 李长安. 土壤中重金属有效态分析技术研究进展[J]. 贵州地质, 2021, 38(1): 79-84. JIA S L, LI C A. Research progress on available state analysis technology of heavy metals in soil[J]. Guizhou Geology, 2021, 38(1): 79-84. DOI:10.3969/j.issn.1000-5943.2021.01.012 |
| [25] |
GLEYZES C, TELLIER S, ASTRUC M. Fractionation studies of trace elements in contaminated soils and sediments: A review of sequential extraction procedures[J]. Trends in Analytical Chemistry, 2002, 21(6): 451-467. |
| [26] |
许莉莉. 土壤中有效态重金属的化学试剂提取法研究进展[J]. 冶金与材料, 2019, 39(3): 32-33. XU L L. Research progress of chemical reagent extraction methods for available heavy metals in soil[J]. Metallurgy and Materials, 2019, 39(3): 32-33. DOI:10.3969/j.issn.1674-5183.2019.03.019 |
| [27] |
陈莹, 刘汉燚, 刘娜, 等. 农地土壤重金属Pb和Cd有效性测定方法的筛选与评价[J]. 环境科学, 2021, 42(7): 3494-3506. CHEN Y, LIU H Y, LIU N, et al. Screening and evaluation of methods for determining available lead(Pb)and cadmium(Cd)in farmland soil[J]. Environmental Science, 2021, 42(7): 3494-3506. |
| [28] |
周国华. 土壤重金属生物有效性研究进展[J]. 物探与化探, 2014, 38(6): 1097-1106. ZHOU G H. Recent progress in the study of heavy metal bioavailability in soil[J]. Geophysical and Geochemical Exploration, 2014, 38(6): 1097-1106. |
| [29] |
鄂倩, 赵玉杰, 刘潇威, 等. 不同土壤镉提取方法预测稻米富集镉性能评估[J]. 农业环境科学学报, 2020, 39(5): 1000-1009. E Q, ZHAO Y J, LIU X W, et al. Screening and evaluation of soil cadmium extraction methods for predicting cadmium accumulation in rice[J]. Journal of Agro-Environment Science, 2020, 39(5): 1000-1009. |
| [30] |
李利梅, 成永霞, 袁远, 等. 土壤重金属有效态单级提取方法研究[J]. 安徽农业科学, 2020, 48(12): 13-15. LI L M, CHENG Y X, YUAN Y, et al. Study on single-stage extraction method to heavy metals effective state in soil[J]. Journal of Anhui Agricultural Sciences, 2020, 48(12): 13-15. DOI:10.3969/j.issn.0517-6611.2020.12.004 |
| [31] |
章明奎, 方利平, 周翠. 污染土壤重金属的生物有效性和移动性评价: 四种方法比较[J]. 应用生态学报, 2006, 17(8): 1501-1504. ZHANG M K, FANG L P, ZHOU C. Evaluation of heavy metals bioavailability and mobility in polluted soils: A comparison of four methods[J]. Chinese Journal of Applied Ecology, 2006, 17(8): 1501-1504. DOI:10.3321/j.issn:1001-9332.2006.08.028 |
| [32] |
贺静, 林玉锁, 刘鹏, 等. 不同提取剂提取酸性土壤有效态Cu和Cd的方法研究[J]. 环境监测管理与技术, 2009, 21(5): 25-29. HE J, LIN Y S, LIU P, et al. The study of extraction method for available copper and cadmium in acidity soil with different extractants[J]. The Administration and Technique of Environmental Monitoring, 2009, 21(5): 25-29. DOI:10.3969/j.issn.1006-2009.2009.05.007 |
| [33] |
尹君, 刘文菊, 谢建治, 等. 土壤中有效态镉、汞浸提剂和浸提条件研究[J]. 河北农业大学学报, 2000, 23(2): 25-28. YIN J, LIU W J, XIE J B, et al. The study on extraction conditions and extractants of soil available Cd, Hg[J]. Journal of Agricultural University of Hebei, 2000, 23(2): 25-28. |
| [34] |
易磊, 张增强, 沈锋, 等. 浸提条件和浸提剂类型对土壤重金属浸提效率的影响[J]. 西北农业学报, 2012, 21(1): 156-160. YI L, ZHANG Z Q, SHEN F, et al. Impact of different extraction conditions and different extracts on heavy metals from several typical soils[J]. Acta Agriculturae Boreali-occidentalis Sinica, 2012, 21(1): 156-160. |
| [35] |
李源, 字雨姝, 刘朝, 等. 电感耦合等离子体质谱法测定土壤中有效态镉[J]. 化学分析计量, 2019, 28(5): 14-18. LI Y, ZI Y S, LIU C, et al. Determination of available cadmium in soil by inductively coupled plasma mass spectrometry[J]. Chemical Analysis and Meterage, 2019, 28(5): 14-18. DOI:10.3969/j.issn.1008-6145.2019.05.004 |
 2022, Vol. 41
2022, Vol. 41