2. 崇明生态研究院, 上海 200062
2. Institute of Eco-Chongming(IEC), Shanghai 200062, China
加拿大一枝黄花(Solidago canadensis L.)曾作为观赏性植物引入我国上海、南京等地区,80年代扩散蔓延为杂草,至今该物种仍存在进一步蔓延的趋势[1]。该外来入侵种使我国原生植物群落丰富性和多样性大幅降低[2],并对农田造成了严重的威胁。目前,人们广泛使用原地焚烧处理、本地物种播种以及在冬季进行土地治疗等措施控制其生长与蔓延[3],然而效果并不显著。并且,以简单焚烧为主的控制措施还会造成严重的空气污染。
作为一类低成本、高效率的新型吸附材料,生物炭已成为近年来全世界关注的焦点。目前,已有大量农业废弃物生产生物炭的研究和应用报道[4-7]。在有机污染物方面,玉米秸秆生物炭可吸附去除十二烷基苯磺酸、PAHs、双酚A等化工污染产物[8-9]。何琦等[10]通过比较6种不同挺水植物制得的生物炭对硫丹的吸附和催化水解效果发现,美人蕉、菖蒲、再力花衍生制得的生物炭对硫丹具有较优去除效果。在无机污染物方面,生物炭去除重金属污染的应用较为广泛。Shen等[11]通过静态吸附实验的方法发现,不同温度制备的水稻秸秆对Pb2+的吸附能力不同,在700 ℃热解温度下制得的生物炭有利于对Pb污染的修复,最大吸附效率可达171.34 mg·g-1。Chen等[12]对浒苔磁性生物炭进行了溶液中Cr(Ⅵ)吸附行为的研究,结果发现Cr(Ⅵ)的去除效率高达97.71%。Liu等[13]利用废弃椰壳生物炭对多金属污染的土壤进行修复,结果发现生物炭的添加显著降低了土壤中酸溶性Cd、Ni和Zn。Zhang等[14]研究发现由入侵种水葫芦制得的生物炭对Cd2+具有显著的吸附作用,最大吸附容量可达70.3 mg·g-1。然而同样作为入侵种,加拿大一枝黄花制备生物炭的报道较少。加拿大一枝黄花富含木质纤维素,且其分子链上含有大量的羟基、羰基等基团,对污染物具有一定的吸附去除作用。Zhang等[15]将加拿大一枝黄花研磨制成干粉,并用其对Cd进行吸附实验,结果发现加拿大一枝黄花本身对Cd具有一定的吸附能力。罗来盛等[16]研究发现,加拿大一枝黄花可作为优良的活性炭制备前驱体,活性炭的制备显著提升了其吸附容量,但是成本较高;利用其制备生物炭,可在保证高吸附率的同时,大幅降低制备成本。在直接利用加拿大一枝黄花生物炭吸附污染物方面,Zhang等[17]研究表明,加拿大一枝黄花生物炭对其原料产生的化感物质邻苯二甲酸二甲酯具有良好的吸附作用,然而在吸附重金属领域较少涉及。
重金属Cd因其毒性风险大、污染分布广和不可降解的特性,已被列为一级致癌物[18]。利用外来入侵种加拿大一枝黄花制备生物炭,并用于Cd2+的吸附,不仅可以作为管理入侵植物的一种经济高效的方法,而且可有效控制水环境中的重金属Cd污染。由于不同生长时期加拿大一枝黄花的茎叶比例不同,为提高其资源化利用效率,本研究分别以其茎、茎叶混合物为原料,以吸附水溶液中的Cd2+为目标,优化制备生物炭的最佳条件,并探索吸附特性和吸附机理,可为加拿大一枝黄花的高效利用提供一定的科学指导。
1 材料与方法 1.1 生物炭制备与基本理化性质本实验原料为加拿大一枝黄花(Solidago canadensis L.),采自上海市浦东新区临港新城环滴水湖河流滨岸带。将加拿大一枝黄花齐根剪下,剔除表面残留的石子、泥土等杂物,用去离子水清洗干净后,将其分为两组,一组剔除叶子,以茎秆作为生物炭原料,后续制得的生物炭标记为SBC;另一组不剔除叶子,以茎秆和叶子混合作为生物炭原料,后续制得的生物炭标记为SCBC。风干1周后,经研磨式粉碎机磨粉,过100目孔径筛后密封备用。采用TGA热重分析仪(Pyris 1 TGA,美国)对两种原料进行热重曲线的测定。
将两种原料分别称取一定质量样品于瓷坩埚中,放置于真空管式高温烧结炉(GSL-1600X,中国),持续通入氮气以充分营造缺氧条件,以10 ℃·min-1的速率分别升温至450、500、550 ℃炭化2 h,自然冷却至室温后取出。分别对不同制备条件下生物炭的基本性质进行表征:产率和灰分含量参考《木炭和木炭试验方法》(GB / T 17664—1999);利用元素分析仪(VARIO MICRO CUBE,德国)测定C、H、N等元素的含量;pH值测定方法参考文献[19],将0.5 g生物炭放入10 mL去离子水中,振荡30 min,静置10 min,使用pH计(ALALIS PH400,中国)测定溶液pH;通过傅里叶红外光谱仪(TENSOR 27,德国)对生物炭表面官能团进行定性分析;利用X射线衍射仪(Agilent 7890B,德国)测定生物炭的物相结构和结晶程度。
1.2 加拿大一枝黄花生物炭对Cd2+的吸附效果 1.2.1 生物炭的最优制备条件筛选分别称取0.5 g不同制备条件下制得的生物炭样品于1000 mL烧杯中,添加500 mL浓度为50.0 mg·L-1的Cd2+溶液,背景电解质为0.01 mol·L-1的NaNO3溶液。吸附反应于25 ℃恒温磁力搅拌器上以150 r· min-1的转速搅拌完成。自加入时刻起,分别于0、5、10、30 min及1、2、3、4、6、8、10、12、24 h时用一次性无菌注射器取样,然后过0.45 μm微孔滤膜,通过原子吸收光谱仪(ContrAA 700,德国)测定滤液中Cd2+浓度[20]。生物炭对Cd2+的吸附量(q)及吸附效率(R)计算公式如下:
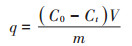
|
(1) |
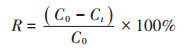
|
(2) |
式中:V为Cd2+溶液体积,L;m为添加生物炭的质量,g;C0和Ct分别为溶液中Cd2+的起始浓度和t时刻浓度,mg·L-1。
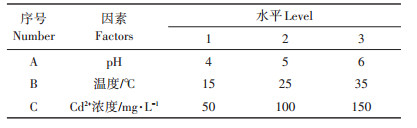
1.2.2 生物炭的最优吸附工艺条件筛选为探究溶液pH、温度和吸附质浓度对吸附作用的影响,设置3因素3水平L9(33)正交试验,分析各因素的影响效应并筛选最优吸附工艺组合。溶液pH通过0.1 mol·L-1NaOH和0.1 mol·L-1HNO3进行调节。称取0.1 g最优制备条件下制得的样品于250 mL具塞锥形瓶中,分别添加100 mL的Cd2+溶液,背景电解质为0.01 mol·L-1的NaNO3溶液,恒温振荡24 h,测定初始浓度和吸附后滤液中的Cd2+浓度,计算生物炭在不同工艺组合中对Cd2+的吸附效率,筛选吸附效果最优的工艺组合。正交设计如表 1所示。
|
|
表 1 正交实验设计表 Table 1 Orthogonal experimental design |
称取0.5 g最优制备条件下制得的生物炭于1000 mL烧杯中,添加500 mL浓度为50.0 mg·L-1的Cd2+溶液,在最优吸附工艺条件下进行吸附反应,分别于0、5、10、30 min及1、2、3、4、6、8、10、12、24 h时取样,测定滤液中Cd2+浓度,并分别利用一级动力学方程和二级动力学方程对Cd2+动力学吸附实验结果进行拟合,以描述加拿大一枝黄花生物炭吸附Cd2+的动力学过程。

|
(3) |
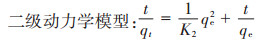
|
(4) |
式中:t为时间,min;qt为t时刻吸附量,mg·g-1;qe为吸附剂平衡吸附量,mg·g-1;K1为一级动力学吸附速率常数,min-1;K2为二级动力学吸附速率常数,g·mg-1· min-1。
称取0.5 g最优制备条件下制得的生物炭样品于1000 mL烧杯中,分别添加500 mL浓度为5.0、10.0、50.0、80.0、100.0、150.0、200.0 mg·L-1的Cd2+溶液,于最优吸附工艺条件下吸附24 h后取样,测定滤液中Cd2+浓度。根据测定Cd2+初始浓度和平衡浓度计算生物炭对Cd2+的吸附量,并代入等温吸附模型方程进行拟合。
Langmuir吸附模型:
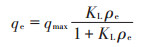
|
(5) |
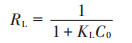
|
(6) |
式中:qe为吸附剂平衡吸附量,mg·g-1;ρe为吸附质平衡质量浓度,即溶液中残余吸附质的质量浓度,mg· L-1;qmax为最大理论吸附容量,mg·g-1;KL为吸附平衡常数,KL值越大,表明吸附剂的吸附性能越强。该模型的基本假设是:吸附剂表面只发生单分子层吸附,表面是均匀的,且被吸附的分子之间相互独立。RL为分离因子,可以对吸附剂有效吸附污染物的能力进行判断[21],0 < RL < 1,吸附过程为有利吸附;RL>1,吸附过程为不利吸附;RL=1,吸附过程为线性吸附;RL=0,吸附过程为不可逆吸附。
Freundlich吸附模型:
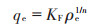
|
(7) |
式中:KF为吸附平衡常数,mg1-1/n·L1/n·g-1;1/n为浓度对吸附量的影响程度。Freundlich吸附模型适于描述非均匀表面发生的多层吸附过程,其特点是没有饱和吸附值。
1.3 加拿大一枝黄花生物炭对Cd2+的吸附机制为探究加拿大一枝黄花生物炭对Cd2+的吸附机制,对样品吸附前后的形貌和结构特性进行表征:利用X射线光电子能谱仪(Thermo ESCALAB 250 XI,英国)对生物炭表面化学特性进行全谱扫描以及C、O、Cd元素的精细谱扫描,测定数据采用XPS PEAK4.1进行谱图分析;利用傅里叶红外光谱仪(TENSOR 27,德国),采用KBr压片法,测定生物炭的FTIR图谱,表征其吸附前后表面官能团的变化情况;利用扫描电子显微镜(SU8100,日本)对Cd吸附前后的生物炭进行形貌表征,并对吸附颗粒进行EDS能谱测定。
1.4 数据统计分析所有实验均进行3次重复,取平均值作为最终结果。使用Microsoft Excel 2016软件进行数据的计算和处理;利用Origin 9.1软件进行作图分析;利用SPSS 23.0对数据进行方差分析,P < 0.05表示有显著差异。
2 结果与讨论 2.1 加拿大一枝黄花生物炭的基本性质两种不同原料加拿大一枝黄花在450、500、550 ℃下热解制得的生物炭的基本理化性质如表 2所示。随着热解温度的升高,生物炭产率逐渐减少,SCBC的产率均高于SBC,与原料热重分析结果一致。加拿大一枝黄花热解过程可以分为失水、热解及炭化3个阶段,两种原料均在400 ℃后进入炭化阶段,该阶段制得的生物炭基本稳定。两种原料相比较,茎叶混合组在热解阶段质量损失率较低,这与原料中木质纤维的含量以及叶中Ca、Mg等矿质元素对热解过程具有的催化作用有关[22]。此外,热解时发生了脱水、脱羧等反应,析出了大量的H2O、CO2、CO和CH4等,从而导致在热解过程中,SBC和SCBC的C含量逐渐增加,H、O含量逐渐减少。SBC和SCBC均在500 ℃时具有最小的O/C值,表明该温度下制得的生物炭具有较低的极性和亲水性[23],不利于污染物的吸附。H/C可表征生物炭的芳香性,随着热解温度的升高,H/C值降低,生物炭芳香性增强,结构更加稳定。
|
|
表 2 加拿大一枝黄花生物炭的基本性质 Table 2 Basic properties of prepared biochar |
两种不同原料生物炭相比较,SBC的C含量相对较高,稳定性较好,适用于土壤固碳;而SCBC的O含量相对较高,含氧官能团丰富,利于与重金属离子反应,发生吸附。此外,SCBC的N含量高于SBC,且热解后制得的生物炭中的N含量均高于原料中的N含量,说明在生物炭制备的热解过程中存在一定的固氮作用,且N元素的存在又可作为氨基等相关配位原子[24],增强了对金属离子的配位吸附作用。
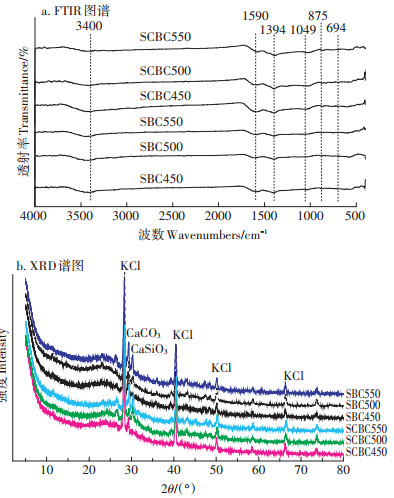
6种生物炭的FTIR图如图 1a所示。可以看出,生物炭表面均含有一定数量的表面官能团,且种类大致相同。3400 cm-1处较宽的羟基吸收峰、1590 cm-1和1394 cm-1处的羧基伸缩振动峰以及在875 cm-1和694 cm-1处CO32-的伸缩振动峰均明显存在于6种生物炭中,且随着热解温度的升高,峰强逐渐减弱。相较于SBC而言,SCBC在1049 cm-1处存在明显的P-O键伸缩振动,这与加拿大一枝黄花叶片中含有较高含量的磷有关。
|
图 1 加拿大一枝黄花生物炭的FTIR图谱和XRD图谱 Figure 1 FTIR and XRD analysis of Solidago canadensis-derived biochar |
图 1b为生物炭的XRD谱图。由图可以看出,6种生物炭中均富含KCl组分,并且检测到少量的CaCO3,与植物基生物炭的物相组成一致[25]。随着热解温度的升高,加拿大一枝黄花生物炭在2θ=25°处逐渐凸显出较宽的石墨结构(002)面的衍射峰,说明生物炭中存在不规则石墨结构的微晶,但石墨化程度较低,呈无定型碳结构。
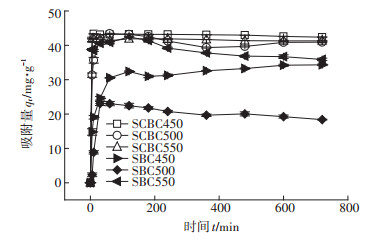
2.2 加拿大一枝黄花生物炭对Cd2+的吸附 2.2.1 生物炭的最优制备条件图 2为不同制备条件下制得的生物炭对Cd2+的吸附效果。不同生物炭对Cd2+的吸附过程相似,在最初的60 min内,生物炭对Cd2+的吸附量快速增加,300 min后基本达到吸附平衡。24 h后,6种生物炭吸附量大小顺序为:SCBC450>SCBC550>SCBC500>SBC550> SBC450>SBC500,SCBC450的吸附效果最佳,吸附量可达42.39 mg·g-1,SCBC550次之,为41.32 mg·g-1。SCBC和SBC两种加拿大一枝黄花生物炭对Cd2+的吸附效果存在较大的差异,3个温度下煅烧制得的SCBC对Cd2+的吸附量均明显大于SBC,这可能依赖于SCBC中N、O含量较高,官能团含量丰富,表面残余矿质元素多,有利于与Cd2+发生吸附反应,降低溶液中游离态Cd2+。因此,建议选择在每年10月花期前对加拿大一枝黄花进行全面清除,一方面此时的加拿大一枝黄花生物量大、茎叶比高,有利于高效率生物炭吸附剂的制备,另一方面有助于防止加拿大一枝黄花开花后种子的传播。
|
图 2 不同制备条件下生物炭对Cd2+的吸附效果 Figure 2 Adsorption of Cd2+ by biochar at different preparation conditions |
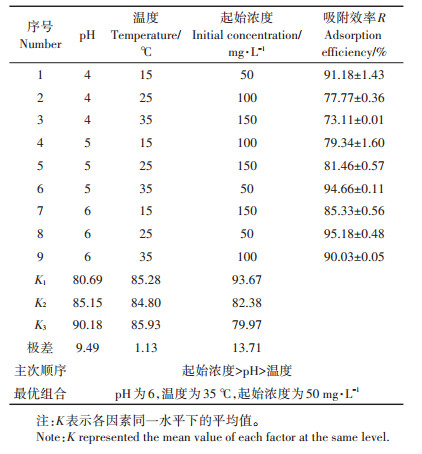
已有大量研究表明,溶液pH、温度和吸附质起始浓度均对生物炭吸附金属效果存在一定的影响,因此选择这3种因素对Cd2+吸附效果进行正交实验,结果如表 3所示。由表可知,随着pH的升高,SCBC450对Cd2+的吸附效率逐渐增加。pH通常可通过改变生物炭表面的电荷密度和金属离子的存在形式,进而影响吸附作用[26]。溶液温度对SCBC450吸附Cd2+的吸附效率影响不显著(P=0.885>0.05)。对于吸附质起始浓度而言,随着其增加,SCBC450对Cd2+的吸附量增加,且影响效果显著(P=0.011 < 0.05)。研究发现,起始浓度的增大直接增加了单位体积内生物炭和金属离子的接触吸附量,进而提高了对重金属的吸附量;然而随着起始浓度的增大,吸附效率却逐渐降低,这与Pellera等[27]的研究结果相似。
|
|
表 3 Cd2+吸附的最优工艺条件 Table 3 Optimal process for Cd2+ adsorption |
根据吸附效率进行最优工艺组合筛选可知,所选3种因素对SCBC450吸附Cd2+的影响程度由大到小分别为吸附质起始浓度>pH>温度,Cd2+吸附最优工艺组合为pH6、温度35 ℃、吸附质起始浓度50 mg·L-1,此时Cd2+的平均吸附效率可达(95.6±0.38)%。
2.2.3 吸附动力学和等温吸附拟合为了更好地评估吸附时的控速步骤及吸附机理,分别利用一级动力学和二级动力学对SCBC450在最优吸附工艺条件下吸附Cd2+的结果进行拟合,拟合参数如表 4所示。由表可知,SCBC450能较好地符合一级动力学模型和二级动力学模型,其中二级动力学方程拟合系数更优(R2=0.999 9),且得到的qe更接近实验真实值。结果表明,加拿大一枝黄花生物炭对Cd2+的吸附作用以化学吸附为主,与Kim等[28]利用芒草制得的生物炭吸附Cd的结果一致。
|
|
表 4 SCBC450对Cd2+的吸附动力学方程参数 Table 4 Kinetic parameters for the adsorption of Cd2+ on SCBC450 |
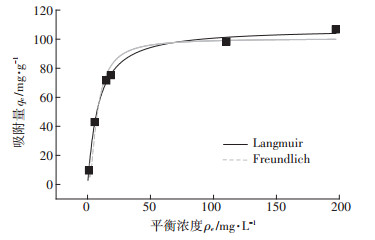
为进一步探究加拿大一枝黄花生物炭对Cd2+的吸附作用,用等温吸附曲线对吸附效果最佳的SCBC450进行拟合,拟合曲线如图 3所示,拟合参数如表 5所示。由表可知,Langmuir模型(R2=0.996 8)对SCBC450吸附Cd2+的吸附等温线拟合优于Freundlich模型(R2=0.882 5),表明SCBC450对Cd2+的吸附过程为单层均相吸附。且0 < RL < 1,表明SCBC450对Cd2+具有有效的吸附能力。由拟合参数得到,SCBC450最大理论吸附容量为107.03 mg·g-1。
|
图 3 SCBC450对Cd2+吸附的吸附等温线 Figure 3 Adsorption isotherms for Cd2+ by SCBC450 |
|
|
表 5 SCBC450对Cd2+的吸附等温线参数 Table 5 Parameters for the adsorption isotherms of Cd2+ on SCBC450 |
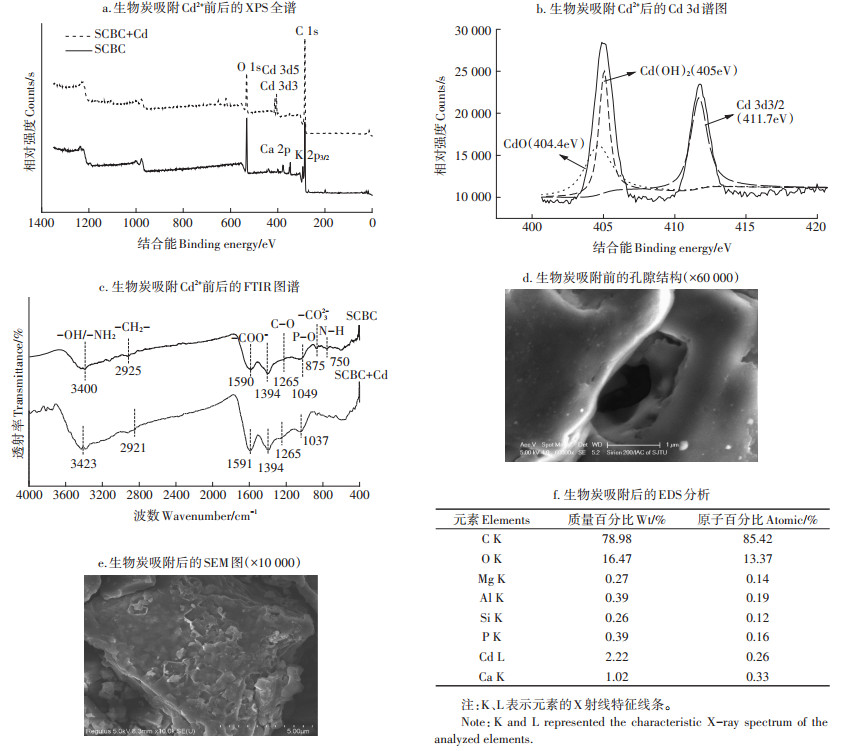
分析加拿大一枝黄花生物炭SCBC450吸附Cd2+前后的XPS图谱(图 4a)可知,SCBC450吸附前后具有相似的峰形结构,其元素组成主要有C、O、K、Ca,该结果与XRD基本物相分析结果一致。吸附后SCBC450的全谱扫描谱图在405.0 eV附近出现了明显清晰的Cd 3d的特征双峰,表明Cd2+被吸附到SCBC450上;同时可以发现,吸附后Ca 2p和K 2p3/2的峰强有所减弱,甚至消失,推测SCBC450可通过与K+、Ca2+发生离子交换吸附Cd2+。Chen等[29]通过对莲蓬生物炭吸附Cd2+前后进行表征发现,生物炭中K元素的分布和Cd元素的分布存在特殊的相关关系,研究表明Cd2+/K+离子交换在热力学上是有利的,且KCl矿物质有助于Cd的吸附和CdCO3的形成[30]。如图 4b所示,通过对Cd的精细谱分析发现,Cd 3d存在两种不同的化学位移,404.4 eV和405 eV处为Cd 3d5/2的特征峰,411.7 eV处对应为Cd 3d3/2的特征峰。Cd 3d5/2可通过沉淀和络合作用与表面官能团形成Cd-R键,主要以Cd(OH)2和CdO的形式存在[31]。结合对C、O元素谱图综合分析,推测生物炭表面大部分通过羟基、羰基与Cd2+发生化学反应而完成吸附。
|
图 4 加拿大一枝黄花生物炭吸附Cd2+前后的表征 Figure 4 Characterization of Solidago canadensis-derived biochar before and after Cd2+ adsorption |
为验证生物炭表面官能团的吸附机制,通过傅里叶红外光谱仪对SCBC450表面官能团变化进行分析,结果表明,吸附前后官能团峰的特征均发生了一定变化,主要表现在波数、振幅、峰强以及波峰宽度方面(图 4c)。在3400 cm-1处附近为羟基(-OH)伸缩振动峰与氨基(N-H)伸缩振动峰的叠加,在750 cm-1处为N-H面外弯曲振动峰,吸附Cd2+后波峰向左迁移,这可能和Cd2+与羟基、氨基在表面发生络合吸附作用有关,与XPS分析结果一致。在1590 cm-1处为羧酸盐(-COO-)反对称伸缩峰,吸附后波数增大、峰强增大,羧基易于与金属离子形成络合物而参与吸附反应[32]。1049 cm-1附近为磷酸根(PO43-)的不对称伸缩振动峰,吸附后红外光谱图P-O的峰减弱,推断重金属离子与生物炭表面的PO43-发生了共沉淀。夏广洁等[33]通过FTIR和XRD分析研究证明了生物炭在对Cd2+的吸附过程中会生成少量的Cd3(PO4)2,与本研究相一致。此外,结合-COO-、C-O以及875 cm-1处出现的CO32-面外变形振动峰分析可知,吸附后吸收峰减弱,推测可能与Cd2+和碳酸盐类反应生成CdCO3沉淀有关[34]。经SCBC450吸附后的SEM-EDS图分析发现(图 4e),生物炭表面有明显的晶体颗粒存在,经EDS点谱分析可知该颗粒中含有Cd、P、C、O等元素,表明Cd2+可通过形成Cd3(PO4)2或CdCO3沉淀而被吸附于表面。此外,对比分析吸附前后的SEM图发现,吸附前SCBC450表面光滑(图 4d),带有孔隙结构,该结构有利于金属离子进入生物炭的孔隙中,起到表面物理吸附的辅助作用。
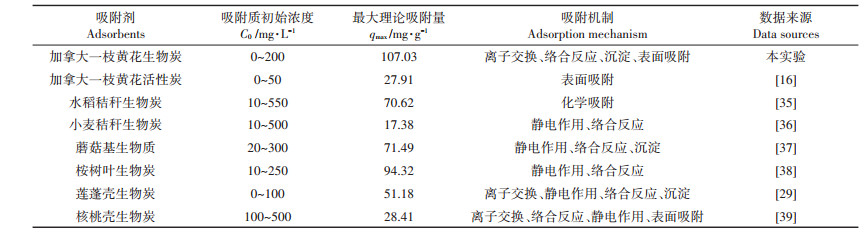
不同原料和不同制备方式生产的炭材料对Cd2+的吸附能力通常不同。对比表 6中不同农业废弃物来源的生物炭吸附剂对Cd2+的吸附性能可见,加拿大一枝黄花生物炭对Cd2+的理论吸附量最大,主要归因于其表面丰富的含氧官能团和矿物成分。对比核桃壳生物炭[39],加拿大一枝黄花生物炭作为植物基生物炭含有大量的灰分含量,包括KCl、CaCO3等矿物成分,有利于促进Cd2+的吸附,这与汪玉瑛等[40]对不同来源生物炭吸附水溶液中Cd2+的结果分析一致。并且,加拿大一枝黄花的茎叶成分复杂,富含酚类、萜类以及黄铜类化合物[41-42],低温炭化后生物炭表面仍存在大量的羟基、内酯和羰基,有助于与金属发生络合作用,从而起到对溶液中金属的去除作用。对比KOH微波活化制得的加拿大一枝黄花活性炭[16],本实验制得的加拿大一枝黄花生物炭对Cd2+的吸附能力明显更优。利用KOH微波活化有利于获得更高的比表面积,但是KOH作为强碱,易溶去吸附剂中的酸、碱等可溶性物质,破坏生物炭表面起主要化学吸附作用的含氧官能团,削减了吸附效率。此外,KOH腐蚀性极大,存在二次污染现象,且生产成本较高,不利于可持续发展。因此,作为一种具有较大应用潜能的Cd2+吸附剂,加拿大一枝黄花生物炭有望替代活性炭。
|
|
表 6 不同农业废弃物吸附剂对Cd2+的吸附性能对比 Table 6 Adsorption capacities of Cd2+ by different agricultural wastes derived-adsorbents |
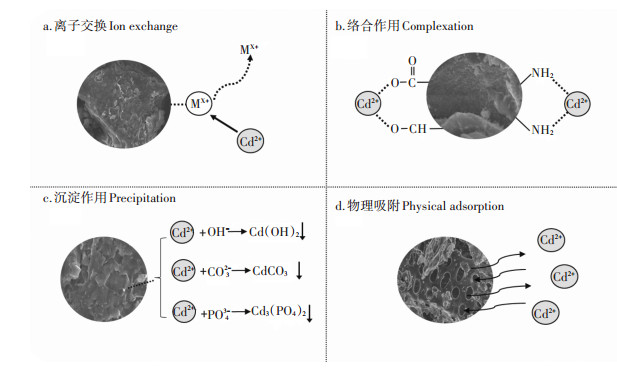
综上所述,加拿大一枝黄花生物炭对金属的吸附不仅与表面结构相关,而且与其表面官能团、矿物成分也相关。加拿大一枝黄花生物炭对Cd2+的吸附机制如图 5所示:(a)Cd2+与生物炭表面的可溶性K+、Ca2+等发生离子交换反应,从而使得Cd2+吸附于表面;(b)Cd2+与羟基、羧基、氨基通过配位络合作用发生表面吸附;(c)Cd2+与生物炭表面的可溶性OH-、PO43-及CO32-结合形成重金属类盐沉淀物,并固定于表面;(d)Cd2+与生物炭表面孔隙结构发生物理吸附,起到辅助作用。
|
图 5 SCBC450对Cd2+吸附机理图 Figure 5 SCBC450 adsorption mechanism for Cd2+ |
(1)原料和热解温度是影响生物炭基本性质的关键因素。随着炭化温度的升高,加拿大一枝黄花生物炭产率逐渐降低,灰分含量升高,pH碱性增强,芳香性增强;以茎叶混合作为原料制得的生物炭的产率和N、O含量均明显高于以纯茎秆作为原料制得的生物炭,且表面富含含氧官能团以及KCl、CaCO3等组分,石墨化程度较低。
(2)比较不同加拿大一枝黄花生物炭对Cd2+吸附的实验发现,在450 ℃下以茎叶混合作为原料热解制得的加拿大一枝黄花生物炭对Cd2+吸附能力最佳。通过最优解下加拿大一枝黄花生物炭对Cd2+的吸附工艺筛选可知,单因素对SCBC450吸附Cd2+的影响程度由大到小为吸附质起始浓度>pH>温度,最优工艺组合为pH=6、温度35 ℃、吸附质起始浓度50 mg·L-1,此时对Cd2+的吸附效率可达(95.6±0.38)%。在最优吸附工艺条件下,SCBC450对Cd2+的吸附过程符合二级动力学方程,以化学吸附为主;且符合Langmuir等温吸附模型,最大理论吸附量可达107.03 mg·g-1,具有极大的应用潜能。
(3)通过对加拿大一枝黄花生物炭吸附Cd2+前后的XPS、FTIR和SEM-EDS分析可知,其吸附机制为表层吸附,主要通过Cd2+与生物炭表面可溶性金属离子K+、Ca2+等发生交换反应,与可溶性OH-、PO43-及CO32-发生沉淀反应,与表面羟基、羧基、氨基等发生络合反应以及物理吸附作用达到金属离子的去除效果。
| [1] |
Wang C Y, Jiang K, Liu J, et al. Moderate and heavy Solidago canadensis L. invasion are associated with decreased taxonomic diversity but increased functional diversity of plant communities in East China[J]. Ecological Engineering, 2018, 112: 55-64. DOI:10.1016/j.ecoleng.2017.12.025 |
| [2] |
Dong L J, Yu H W, He W M. What determines positive, neutral, and negative impacts of Solidago canadensis invasion on native plant species richness?[J]. Scientific Reports, 2015, 17: 16804. |
| [3] |
Dodson E K, Fiedler C E. Impacts of restoration treatments on alien plant invasion in Pinus ponderosa forests, Montana, USA[J]. Journal of Applied Ecology, 2010, 43(5): 887-897. |
| [4] |
Qambrani N A, Rahman M M, Won S, et al. Biochar properties and eco-friendly applications for climate change mitigation, waste management, and wastewater treatment:A review[J]. Renewable & Sustainable Energy Reviews, 2017, 79: 255-273. |
| [5] |
Wei D N, Li B Y, Huang H L, et al. Biochar-based functional materials in the purification of agricultural wastewater:Fabrication, application and future research needs[J]. Chemosphere, 2018, 197: 165-180. DOI:10.1016/j.chemosphere.2017.12.193 |
| [6] |
Xu R K, Xiao S C, Yuan J H, et al. Adsorption of methyl violet from aqueous solutions by the biochars derived from crop residues[J]. Bioresource Technology, 2011, 102(22): 10293-10298. DOI:10.1016/j.biortech.2011.08.089 |
| [7] |
Oliveira F R, Patel A K, Jaisi D P, et al. Environmental application of biochar:Current status and perspectives[J]. Bioresource Technology, 2017, 246: 110-122. DOI:10.1016/j.biortech.2017.08.122 |
| [8] |
Zhao N, Yang X X, Zhang J, et al. Adsorption mechanisms of dodecylbenzene sulfonic acid by corn straw and poplar leaf biochars[J]. Materials, 2017, 10(10): 1119. DOI:10.3390/ma10101119 |
| [9] |
黄华, 王雅雄, 唐景春, 等. 不同烧制温度下玉米秸秆生物炭的性质及对萘的吸附性能[J]. 环境科学, 2014, 35(5): 1884-1890. HUANG Hua, WANG Ya-xiong, TANG Jing-chun, et al. Properties of maize stalk biochar produced under different pyrolysis temperatures and its sorption capability to naphthalene[J]. Environmental Science, 2014, 35(5): 1884-1890. |
| [10] |
何琦, 曹凤梅, 卢少勇, 等. 挺水植物生物炭对硫丹的吸附及催化水解作用[J]. 中国环境科学, 2018, 38(3): 1126-1132. HE Qi, CAO Feng-mei, LU Shao-yong, et al. Adsorption and catalytic hydrolysis of endosulfan on biochars derived from emergent plants[J]. China Environmental Science, 2018, 38(3): 1126-1132. DOI:10.3969/j.issn.1000-6923.2018.03.040 |
| [11] |
Shen Z T, Hou D Y, Jin F, et al. Effect of production temperature on lead removal mechanisms by rice straw biochars[J]. Science of the Total Environment, 2019, 655(10): 751-758. |
| [12] |
Chen Y Y, Wang B Y, Xin J, et al. Adsorption behavior and mechanism of Cr(Ⅵ)by modified biochar derived from Enteromorpha prolifera[J]. Ecotoxicology and Environmental Safety, 2018, 164(30): 440-447. |
| [13] |
Liu H K, Xu F, Xie Y L, et al. Effect of modified coconut shell biochar on availability of heavy metals and biochemical characteristics of soil in multiple heavy metals contaminated soil[J]. Science of the Total Environment, 2018, 654(15): 702-709. |
| [14] |
Zhang F, Wang X, Yin D X, et al. Efficiency and mechanisms of Cd removal from aqueous solution by biochar derived from water hyacinth (Eichornia crassipes)[J]. Journal of Environmental Management, 2015, 153(15): 68-73. |
| [15] |
Zhang J W, Bi F Z, Wang Q J, et al. Characteristics and influencing factors of cadmium biosorption by the stem powder of the invasive plant species Solidago Canadensis[J]. Ecological Engineering, 2018, 121(1): 12-18. |
| [16] |
罗来盛, 周美华. 微波活化制备加拿大一枝黄花活性炭及对Cd (Ⅱ)的吸附[J]. 环境工程学报, 2012, 6(5): 1543-1547. LUO Lai-sheng, ZHOU Mei-hua. Adsorption of Cd(Ⅱ)ions onto activated carbon prepared from Solidago canadensis by means of microwave activated[J]. Chinese Journal of Environmental Engineering, 2012, 6(5): 1543-1547. |
| [17] |
Zhang Z C, Chen L X, Wang J, et al. Biochar preparation from Solidago canadensis and its alleviation of the inhibition of tomato seed germination by allelochemicals[J]. Rsc Advances, 2018, 8(40): 22370-22375. DOI:10.1039/C8RA03284J |
| [18] |
Goswami R, Shim J, Deka S, et al. Characterization of cadmium removal from aqueous solution by biochar produced from Ipomoea fistulosa, at different pyrolytic temperatures[J]. Ecological Engineering, 2016, 97: 444-451. DOI:10.1016/j.ecoleng.2016.10.007 |
| [19] |
仇祯, 周欣彤, 韩卉, 等. 互花米草生物炭的理化特性及其对镉的吸附效应[J]. 农业环境科学学报, 2018, 37(1): 172-178. QIU Zhen, ZHOU Xin -tong, HAN Hui, et al. Properties of Spartina alterniflora Loisel. derived-biochar and its effect on cadmium adsorption[J]. Journal of Agro-Environment Science, 2018, 37(1): 172-178. |
| [20] |
Zhou Q W, Liao B H, Lin L, et al. Adsorption of Cu(Ⅱ)and Cd(Ⅱ) from aqueous solutions by ferromanganese binary oxide-biochar composites[J]. Science of the Total Environment, 2017, 615(15): 115-122. |
| [21] |
Zhao Y F, Zhang B, Zhang X, et al. Preparation of highly ordered cubic NaA zeolite from halloysite mineral for adsorption of ammonium ions[J]. Journal of Hazardous Materials, 2010, 178(1): 658-664. |
| [22] |
顾博文, 曹心德, 赵玲, 等. 生物质内源矿物对热解过程及生物炭稳定性的影响[J]. 农业环境科学学报, 2017, 36(3): 591-597. GU Bo-wen, CAO Xin-de, ZHAO Ling, et al. Influence of inherent minerals on biomass pyrolysis and carbon stability in biochar[J]. Journal of Agro-Environment Science, 2017, 36(3): 591-597. |
| [23] |
Jung K W, Kim K, Jeong T U, et al. Influence of pyrolysis temperature on characteristics and phosphate adsorption capability of biochar derived from waste-marine macroalgae(Undaria pinnatifida, roots)[J]. Bioresource Technology, 2016, 200: 1024-1028. DOI:10.1016/j.biortech.2015.10.016 |
| [24] |
Inyang M, Gao B, Yao Y, et al. Removal of heavy metals from aqueous solution by biochars derived from anaerobically digested biomass[J]. Bioresource Technology, 2012, 110(2): 50-56. |
| [25] |
Deng Y Y, Huang S, David A L, et al. Quantitative mechanisms of cadmium adsorption on rice straw and swine manure-derived biochars[J]. Environmental Science and Pollution Research, 2018, 25(1): 32418-32432. |
| [26] |
Chen T, Zhou Z Y, Han R, et al. Adsorption of cadmium by biochar derived from municipal sewage sludge:Impact factors and adsorption mechanism[J]. Chemosphere, 2015, 134: 286-293. DOI:10.1016/j.chemosphere.2015.04.052 |
| [27] |
Pellera F M, Giannis A, Kalderis D, et al. Adsorption of Cu(Ⅱ)ions from aqueous solutions on biochars prepared from agricultural by-products[J]. Journal of Environmental Management, 2012, 96(1): 35-42. |
| [28] |
Kim W K, Shim T, Kim Y S, et al. Characterization of cadmium removal from aqueous solution by biochar produced from a giant Miscanthus at different pyrolytic temperatures[J]. Bioresource Technology, 2013, 138(2): 266-270. |
| [29] |
Chen Z, Liu T, Tang J J, et al. Characteristics and mechanisms of cadmium adsorption from aqueous solution using lotus seedpod-derived biochar at two pyrolytic temperatures[J]. Environmental Science and Pollution Research, 2018, 25(12): 11854-11866. DOI:10.1007/s11356-018-1460-1 |
| [30] |
Tan G C, Xu N, Xu Y, et al. Sorption of mercury(Ⅱ)and atrazine by biochar, modified biochars and biochar based activated carbon in aqueous solution[J]. Bioresource Technology, 2016, 211: 727-735. DOI:10.1016/j.biortech.2016.03.147 |
| [31] |
Liang J, Li X M, Yu Z G, et al. Amorphous MnO2 modified biochar derived from aerobically composted swine manure for adsorption of Pb (Ⅱ) and Cd(Ⅱ)[J]. ACS Sustainable Chemistry & Engineering, 2017, 5(6): 5049-5058. |
| [32] |
Zhou L, Liu Y G, Liu S B, et al. Investigation of the adsorption-reduction mechanisms of hexavalent chromium by ramie biochars of different pyrolytic temperatures[J]. Bioresource Technology, 2016, 218: 351-359. DOI:10.1016/j.biortech.2016.06.102 |
| [33] |
夏广洁, 宋萍, 邱宇平. 牛粪源和木源生物炭对Pb (Ⅱ)和Cd (Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2014, 33(3): 569-575. XIA Guang-jie, SONG Ping, QIU Yu-ping. Sorption of Pb(Ⅱ)and Cd(Ⅱ)by manure-and wood-derived biochars[J]. Journal of AgroEnvironment Science, 2014, 33(3): 569-575. |
| [34] |
Xu X Y, Cao X D, Zhao L, et al. Removal of Cu, Zn, and Cd from aqueous solutions by the dairy manure-derived biochar[J]. Environmental Science & Pollution Research, 2013, 20(1): 358-368. |
| [35] |
Zhang H Y, Yue X P, Li F, et al. Preparation of rice straw-derived biochar for efficient cadmium removal by modification of oxygen-containing functional groups[J]. Science of the Total Environment, 2018, 631/632(1): 795-802. |
| [36] |
马锋锋, 赵保卫, 刁静茹. 小麦秸秆生物炭对水中Cd2+的吸附特性研究[J]. 中国环境科学, 2017, 37(2): 551-559. MA Feng-feng, ZHAO Bao-wei, DIAO Jing-ru. Adsorptive characteristics of cadmium onto biochar produced from pyrolysis of wheat straw in aqueous solution[J]. China Environmental Science, 2017, 37(2): 551-559. |
| [37] |
Xian Y, Wu J, Yang G, et al. Adsorption characteristics of Cd(Ⅱ)in aqueous solutions using spent mushroom substrate biochars produced at different pyrolysis temperatures[J]. Rsc Advances, 2018, 8: 28002-28012. DOI:10.1039/C8RA03958E |
| [38] |
郜礼阳, 邓金环, 唐国强, 等. 不同温度桉树叶生物炭对Cd2+的吸附特性及机制[J]. 中国环境科学, 2018, 38(3): 1001-1009. GAO Li-yang, DENG Jin-huan, TANG Guo-qiang, et al. Adsorption characteristics and mechanism of Cd2+on biochar with different pyrolysis temperatures produced from eucalyptus leaves[J]. China Environmental Science, 2018, 38(3): 1001-1009. DOI:10.3969/j.issn.1000-6923.2018.03.025 |
| [39] |
王立果, 钟金魁, 赵保卫, 等. 水中镉和芘在核桃壳生物炭上的吸附行为及其交互作用[J]. 农业环境科学学报, 2017, 36(9): 1868-1876. WANG Li-guo, ZHONG Jin-kui, ZHAO Bao-wei, et al. Adsorption and interaction of Cd(Ⅱ)and pyrene in water on walnut shell biochar[J]. Journal of Agro-Environment Science, 2017, 36(9): 1868-1876. |
| [40] |
汪玉瑛, 计海洋, 吕豪豪, 等. 羊栖菜生物炭对镉污染土壤性质及镉形态的影响[J]. 农业环境科学学报, 2018, 37(6): 1132-1140. WANG Yu-ying, JI Hai-yang, LÜ Hao-hao, et al. Effects of biochar derived from Sargassum fusiforme on the properties and cadmium forms of cadmium-contaminated soil[J]. Journal of Agro-Environment Science, 2018, 37(6): 1132-1140. |
| [41] |
Radusiene J, Marska M, Ivanauskas L, et al. Assessment of phenolic compound accumulation in two widespread goldenrods[J]. Industrial Crops and Products, 2015, 63: 158-166. DOI:10.1016/j.indcrop.2014.10.015 |
| [42] |
Deng Y, Zhao Y Y, Olga P Z, et al. Polyphenols, antioxidant and antimicrobial activities of leaf and bark extracts of Solidago canadensis L.[J]. Industrial Crops and Products, 2015, 74(15): 803-809. |
 2019, Vol. 38
2019, Vol. 38